Способ профилактики африканской чумы свиней
Иллюстрации
Показать всеИзобретение относится к области ветеринарии. Предложен способ профилактики африканской чумы свиней, включающий выявление животных с инфекционным заболеванием на начальной стадии развития, убой больных и дальнейшее обследование остальных животных. Остальных животных в очаге инфекционного заболевания африканской чумой свиней обследуют в течение суток методом полимеразной цепной реакции с флуоресцентной детекцией в режиме реального времени. Животных-носителей вируса и здоровых животных переводят в отдельные помещения и в их присутствии осуществляют санацию помещений озоно-воздушной смесью: в помещении с животными-носителями вируса - в течение месяца не менее 3-4 раз в неделю с концентрацией озона 4-6 г/м3 в течение 20-30 минут, в помещении со здоровыми животными - в течение не более двух недель 2-3 раза в неделю с концентрацией озона 3-4 г/м3 в течение 15-20 минут. Изобретение обеспечивает расширение функциональных возможностей способа профилактики африканской чумы свиней. 2 табл., 1 пр.
Реферат
Изобретение относится к области ветеринарии, в частности к способу профилактики африканской чумы свиней.
Известен способ санации животноводческих помещений в присутствии животных, в котором осуществляют обработку животноводческих помещений озоно-воздушной смесью, отличающийся тем, что обработку осуществляют озоно-воздушной смесью с концентрацией озона 1-3 мг/м3 с периодичностью 24 часа в течение 1,5-2 часа, которую готовят с помощью озонатора, установленного непосредственно в животноводческом помещении (RU №2542504).
Недостатком данного способа является невозможность его использования для проведения дезинфекции помещений в присутствии животных в случае их заражения вирусом африканской чумы свиней, т.к. для уничтожения данной инфекции необходима обработка озоно-воздушной смесью с более высокой концентрацией озона.
Известен способ оздоровления хозяйств от лейкоза крупного рогатого скота (ВЛКРС), включающий оздоровительные мероприятия, которые проводят по вариантам в зависимости от первоначальной инфицированности стада, определенной по результатам серологического исследования, изоляцию инфицированных ВЛКРС животных и немедленную сдачу на убой больных животных, отличающийся тем, что при первоначальной инфицированности стада до 2,5% инфицированных животных немедленно сдают на убой, а остальных животных исследуют каждые 3 месяца с обязательным удалением инфицированных животных; в хозяйствах, где выявлено 2,6-10,0% животных, инфицированных ВЛКРС, инфицированных животных собирают на отдельной ферме, откуда молодняк после откорма коров после отела и по мере прекращения лактации сдают на убой, оставшихся животных исследуют серологическим методом на ВЛКРС и вновь выявленных инфицированных животных немедленно переводят на указанную ферму; при первоначальной инфицированности стада 10,1-40,0% всех животных в хозяйстве делят на две группы: серопозитивные и серонегативные и содержат их изолированно друг от друга, инфицированных животных каждые 6 месяцев исследуют гематологическим методом и признанных больными сдают на убой, а коров и нетелей, не инфицированных ВЛКРС, исследуют серологическим методом с интервалом три месяца, при этом вновь выявленных серопозитивных животных переводят в группу инфицированных коров; при первоначальной инфицированности стада более 40,0% всех взрослых животных исследуют только гематологическим методом через каждые 6 месяцев и выявленных больных сдают на убой (RU №2268589).
Недостатком данного способа является продолжительность диагностирования лейкоза крупного рогатого скота серологическим методом, что в свою очередь способствует прогрессивному развитию заболевания, ведущему к массовой гибели животных.
Техническим результатом является расширение функциональных возможностей способа профилактики африканской чумы свиней.
Технический результат достигается тем, что в способе профилактики африканской чумы свиней, включающем выявление 2,5-3% от общего количества животных с инфекционным заболеванием на начальной стадии развития в очаге и 1-й угрожаемой зоне, убой больных и дальнейшее обследование остальных животных, согласно изобретению остальных животных в очаге инфекционного заболевания африканской чумы свиней обследуют в течение суток методом экспресс-диагностики, включающим отбор проб крови животных, выделение из нее ДНК генома вирусного заболевания, проведение полимеразной цепной реакции с флуоресцентной детекцией в режиме реального времени, по результатам которой выявляют животных-носителей вируса и здоровых животных, которых переводят в отдельные помещения и в их присутствии осуществляют санацию помещений озоно-воздушной смесью: в помещении с животными-носителями вируса - в течение месяца не менее 3-4 раз в неделю с концентрацией озона 4-6 г/м3 в течение 20-30 минут, в помещении со здоровыми животными - в течение не более двух недель 2-3 раза в неделю с концентрацией озона 3-4 г/м3 в течение 15-20 минут.
Новизна заявляемого способа профилактики африканской чумы свиней состоит в идентификации вируса в пробах патологического материала с помощью полимеразной цепной реакции (ПЦР) с флуоресцентной детекцией в режиме реального времени в течение суток, что в свою очередь позволяет выявить животных-носителей вируса африканской чумы свиней на начальной стадии их инфицирования, а также осуществление санации помещений, в которых отдельно друг от друга присутствуют животные-носители вируса и здоровые животные.
Признаки, отличающие заявляемое техническое решение от прототипа, направлены на достижение технического результата и не выявлены при изучении данной и смежной областей науки и техники и, следовательно, соответствуют критерию «изобретательский уровень».
Эти отличия позволяют сделать вывод о соответствии заявляемых технических решений критерию «новизна».
Заявляемый способ профилактики африканской чумы свиней рекомендовано использовать в специализированных ветеринарных, животноводческих, сельскохозяйственных предприятиях.
Способ профилактики африканской чумы свиней осуществляют следующим образом.
В стаде свиней ведут забор проб крови от каждого животного. Для получения сыворотки пробирки с кровью отстаивают при комнатной температуре до полного образования сгустка, затем центрифугируют. После сыворотку в количестве не менее 1 мл переносят одноразовыми наконечниками с фильтром в одноразовые пробирки объемом 1,5 мл. Для подготовки пробы к проведению полимеразной цепной реакции используют различные методики, с помощью которых осуществляют экстракцию ДНК из полученных образцов сыворотки крови животных и удаление или нейтрализацию посторонних примесей для получения препарата ДНК с чистотой, пригодной для проведения полимеразной цепной реакции.
Для подготовки образцов и проведения полимеразной цепной реакции используют специальный набор реагентов для выявления возбудителя африканской чумы свиней (инструкция по применению «ПЦР-АЧС-ФАКТОР», набора реагентов для выявления возбудителя африканской чумы свиней в клиническом материале методом полимеразной цепной реакции с флуоресцентным детектором в режиме реального времени компании «Фактор-мед», ссылка - http://faktor.ru/catalog/veterinarya/produkrsiya/ptsr_asf_faktor/).
Согласно данной инструкции в отдельной пробирке смешивают компоненты набора из расчета на каждую реакцию: 5 мкл ПНР СМЕСЬ, 10 мкл смеси ПНР БУФЕР, 0,5 мкл TAQ POLYMERASE, данную смесь перемешивают и сбрасывают капли кратковременным центрифугированием. Затем отбирают необходимое количество пробирок для амплификации ДНК исследуемых и контрольных проб, вносят по 15 мкл приготовленной реакционной смеси. Используя наконечники с фильтром, в подготовленные пробирки добавляют:
1) отрицательный контроль ПЦР (К-) - вносят в пробирку по 10 мкл ДНК буфера;
2) по 10 мкл ДНК из исследуемых образцов в соответствующие пробирки;
3) положительный контроль ПЦР (К+) - вносят в пробирку 10 мкл положительного контрольного образца.
Далее осуществляют полимеразную цепную реакцию с флуоресцентным детектором в режиме реального времени на амплификаторе Rotor-Gene 3000/6000. Прибор программируют, устанавливают параметры температурно-временного режима амплификации, детекцию флуоресцентного сигнала назначают после стации отжига праймеров, после чего начинают процесс амплификации с флуоресцентной детекцией в режиме реального времени. В его основе лежит принцип флуоресцентной детекции продуктов полимеразной цепной реакции непосредственно в ходе амплификации. Детекция продуктов амплификации проводится прямо в реакционной среде через стенки или крышку закрытой пробирки.
ПЦР с флуоресцентной детекцией в режиме реального времени имеет ряд значительных преимуществ:
- объединение этапов амплификации и детекции результатов. Появляется возможность оценить кинетику процесса, которая зависит от начального количества исследуемого материала;
- существенное снижение риска контаминации и ошибок при анализе результатов;
- высокая специфичность реакции за счет использования высокоспецифичных флуоресцентных зондов;
- высокая производительность;
- упрощение требований к организации ПЦР-лаборатории;
- возможность количественной оценки исходной ДНК матрицы;
- регистрация и учет данных в электронном формате.
ПНР в реальном времени характеризуется возможностью проведения качественного и количественного анализа. Регистрируемое в процессе амплификации нарастание сигнала от отделенного флуорофора прямо пропорционально увеличению концентрации синтезированных специфических продуктов и отражает концентрацию ДНК в исходной матрице.
Учет результатов полимеразной цепной реакции согласно указанной выше инструкции проводят по наличию или отсутствию пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией. Образец считают положительным (вирус АЧС присутствует), если наблюдают рост специфического сигнала, при этом значения контрольных образцов находятся в пределах нормы. Образец считают отрицательным (вирус АЧС отсутствует), если не наблюдают рост специфического сигнала, при этом значения контрольных образцов находятся в пределах нормы.
В результате проведения полимеразной цепной реакции с флуоресцентным детектором в режиме реального времени при выявлении первоначального инфицирования вирусом африканской чумы свиней 2,5-3% голов животных от общего количества в стаде инфицированных особей сдают на убой, после чего животных-носителей инфекции и здоровых особей переводят в отдельные помещения. Затем осуществляют санацию помещений в присутствии животных с помощью озоно-воздушной смеси, при этом в помещении с животными-носителями вируса ее проводят в течение месяца 3 раза в неделю с концентрацией озона 5 мг/м3 в течение 25 минут. В помещении со здоровыми животными санацию проводят в течение двух недель 2 раза в неделю с концентрацией озона 4 мг/м3 в течение 18 минут.
Результаты проведения опытов по санации помещений показывают, что санация помещения озоно-воздушной смесью с концентрацией озона 1-3 мг/м3 является малоэффективной при содержании общего микробного числа по результатам анализа санитарно-микробиологического контроля воздуха в животноводческом помещении более 400 тыс./м3, уровнем аммиака более 30 мг/м3 и сероводорода более 15 мг/м3, т.к. незначительно повлияла на снижение указанных показателей.
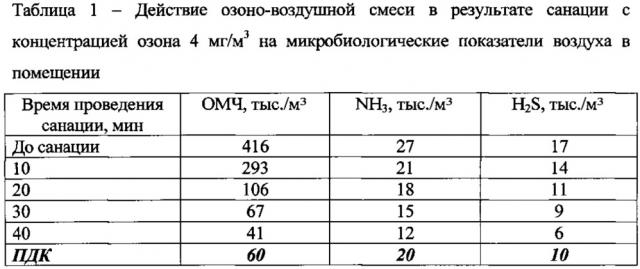
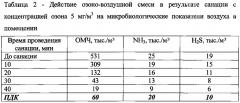
После санации помещений озоно-воздушной смесью с концентрацией озона 7-10 мг/м3 наблюдалось значительное снижение параметров ОМЧ, аммиака и сероводорода в воздухе, однако последствием такой дезинфекции являлось ухудшение общего самочувствия животных, снижение их активности и аппетита. Поэтому по итогам проведенных испытаний наиболее оптимальной признана санация с концентрациями озона 4 и 5 мг/м3, т.к. санация озоно-воздушной смесью с данными концентрациями озона не оказывала токсикологического побочного эффекта, а также снижала уровень содержания вредных веществ в животноводческих помещениях до регламентированных норм. Данные по содержанию вредных соединений в воздухе животноводческих помещений до и после санации в зависимости от концентрации озона в озоно-воздушной смеси представлены в таблицах 1 и 2.
По итогам санации видно, что обработка помещений озоно-воздушной смесью с концентрацией озона 4-5 мг/м3 в течение 15-25 минут снижает уровень загрязнения воздуха вредными соединениями до предельно допустимых значений, при этом не оказывая вредного токсикологического воздействия на состояние здоровья животных.
Результаты проведенных мероприятий в животноводческих помещениях в присутствии животных позволяют сделать вывод о том, что данный способ профилактики африканской чумы свиней эффективен в качестве улучшения и сохранения санитарного состояния на животноводческих предприятиях.
Способ профилактики африканской чумы свиней, включающий выявление 2,5-3% от общего количества животных с инфекционным заболеванием на начальной стадии развития в очаге и 1-й угрожаемой зоне, убой больных и дальнейшее обследование остальных животных, отличающийся тем, что остальных животных в очаге инфекционного заболевания африканской чумой свиней обследуют в течение суток методом экспресс-диагностики, включающим отбор проб крови животных, выделение из нее ДНК генома вирусного заболевания, проведение полимеразной цепной реакции с флуоресцентной детекцией в режиме реального времени, по результатам которой выявляют животных-носителей вируса и здоровых животных, которых переводят в отдельные помещения и в их присутствии осуществляют санацию помещений озоно-воздушной смесью: в помещении с животными-носителями вируса - в течение месяца не менее 3-4 раз в неделю с концентрацией озона 4-6 г/м3 в течение 20-30 минут, в помещении со здоровыми животными - в течение не более двух недель 2-3 раза в неделю с концентрацией озона 3-4 г/м3 в течение 15-20 минут.