Способ определения топирамата в плазме крови
Иллюстрации
Показать всеИзобретение относится к фармакологии и может быть использовано для проведения терапевтического лекарственного мониторинга топирамата у пациентов в условиях стационара. Для этого проводят количественное определение топирамата в плазме крови человека с использованием высокоселективного метода хроматомасс-спектрометрии. Анализ проводят с использованием матрицы раствора внутреннего стандарта - 2,3-4,5-бис-О-изопропилиден-бета-D-фруктопиранозы-N-(4-хлорбензоил)сульфамата и топирамата, полученного экстракцией из плазмы крови. Разделение продуктов экстракции проводят на колонке ХTerra MS C18. Элюирование со скоростью 0,8 мл/мин при температуре колонки 35°C проводят раствором А (10 мМ ацетат аммония) и раствором Б (смесь ацетонитрила и 10 мМ ацетата аммония в отношении 90:10) в соотношении раствор А : раствор Б = 40:60 (%). Топирамат детектируют по четырем дочерним ионам с m/z 95.9, 122.0, 161.9, 280.0, образующимся в результате фрагментации родительского молекулярного иона топирамата с m/z 338.2, а его концентрацию рассчитывают по формуле: С=15,06732079×AR, где С - концентрация топирамата (мкг/мл), AR - отношение площади хроматографического пика топирамата к площади пика внутреннего стандарта. Изобретение позволяет количественно и с высокой достоверностью определять топирамат в плазме крови пациентов. 1 табл., 4 ил.
Реферат
Изобретение относится к области медицины, а именно к фармакологии, и может быть использовано для количественного определения топирамата в плазме крови человека с целью проведения терапевтического лекарственного мониторинга данного препарата у пациентов в условиях стационара.
Топирамат - противоэпилептическое средство относится к классу сульфат-замещенных моносахаридов. Химическое название 2,3:4,5-Ди-O-изопропилиден-бета-D-фруктопиранозы сульфамат; брутто-формула C12H21NO8S.
В связи с появлением новых технологий в фармакокинетике, фармакогенетике и аналитической химии современная медицина выходит на качественно новый этап развития. Базисом рациональной терапии в современной медицине становится терапевтический лекарственный мониторинг - способ управления и контроля эффективности фармакотерапии в реальном времени. Как известно, главная цель рациональной терапии - максимальный лечебный эффект при минимальном побочном действии. Для достижения этой цели в клинике осуществляется разнонаправленный мониторинг больных, с целью получения исчерпывающей информации об их состоянии. Такого рода информацию можно получить различными способами, в том числе и терапевтический лекарственный мониторинг. Топирамат уменьшает частоту возникновения потенциалов действия, характерных для нейрона в состоянии стойкой деполяризации, что свидетельствует о зависимости блокирующего действия препарата на натриевые каналы от состояния нейрона. Топирамат потенцирует активность GABA в отношении некоторых подтипов GABA-рецепторов (в т.ч. GABAA-рецепторов), а также модулирует активность самих GABAA-рецепторов, препятствует активации каинатом чувствительности каинат/АМПК-рецепторов к глутамату, не влияет на активность N-метил-D-аспартата в отношении NMDA-рецепторов. Эти эффекты топирамата являются дозозависимыми при концентрации топирамата в плазме от 1 мкМ до 200 мкМ, с минимальной активностью в пределах от 1 мкМ до 10 мкМ. Кроме того, топирамат угнетает активность некоторых изоферментов карбоангидразы, однако этот эффект у топирамата более слабый, чем у ацетазоламида и, по-видимому, не является главным в противоэпилептической активности топирамата.
На сегодняшний день известен способ оптимизации режима дозирования противоэпилептических препаратов, в том числе и топирамата, путем забора биологического материала и проведения полимеразной цепной реакции по генам-кандидатам с последующим анализом их аллельных вариантов. Далее, путем сопоставления выявленного аллельного полиморфизма с данными о его влиянии на эффективную терапевтическую дозу и возникновении побочных эффектов, производится расчет эффективной терапевтической дозы противоэпилептического препарата и определение риска развития побочных эффектов. Предложенное изобретение позволяет с высокой точностью определять эффективную терапевтическую дозу и наличие риска развития побочных эффектов (RU 2574204, 10.02.2016). Это эффективный метод молекулярной биологии, но в то же время он довольно трудоемок и требует наличия опытных специалистов по проведению данной реакции. Необходимо отметить, что наличие фармакогенетической информации о пациенте действительно обладает определенной прогностической ценностью, однако фармакогенетический скриннинг сам по себе не отменяет необходимости измерения реальной концентрации антиконвульсантов в крови конкретного пациента в процессе индивидуализации лекарственной терапии.
Известен также способ определения топирамата в плазме крови путем жидкостной хроматографии - масс-спектрометрии, в котором в качестве внутреннего стандарта для определения топирамата используется дейтерированный топирамат (топирамат-d12), при этом детектирование проводится с использованием интерфейса мультимодального - электрораспыления по молекулярному иону топирамата с m/z 338.1. В качестве аналитического оборудования использовалось устройство LC (модель 1200, компания Agilent Technologies, Inc.) с бинарным насосом и автосемплером в сочетании с масс-селективным детектором (LOMSD SL, Agilent Technologies, Inc.). Точность варьировала в диапазоне от 0,075 до 7,5 мкг/мл. Определение известного значения в соответствии с предписанной концентрацией составляла от 96.93% и 97,68%.
Наиболее близким техническим решением является способ определения топирама в плазме крови с помощью хроматомасс-спектрометрии причем в качестве внутреннего стандарта для определения топирамата используется дейтерированный топирамат (топирамат-d12) (Kamal М. Matar Therapeutic drug monitoring of topiramate by liquid chromatography-tandem mass spectrometry. Clinica Chimica Acta, 2010, pp. 1-6, в статье Matar K., 2010). Применение в обоих этих способах в качестве внутреннего стандарта молекулы топирамата, в котором атомы водорода замещены дейтерием в целом оправдано и имеет ряд серьезных преимуществ: одинаковый с аналитом коэффициент экстракции, схожее хроматографическое поведение, одинаковый характер масс-фрагментации с анализируемым соединением. Однако дейтерированные аналоги имеют ряд серьезных недостатков, лимитирующих их широкое применение. Прежде всего это высокая цена и труднодоступность в сравнении с недейтерированными веществами. Вторая особенность связана с содержанием незамещенных дейтерием атомов водорода в молекуле. При их наличии приходится лимитировать верхнюю концентрацию внутреннего стандарта, дабы он не давал вклада в сигнал измеряемого вещества. Кроме того, при длительном нахождении в водных растворах в молекулах дейтерированных соединений может происходить самопроизвольный процесс замены дейтерия на наиболее распространенный изотоп водорода (протий), что может влиять на параметры количественного анализа, внося дополнительную погрешность в измерения. Это обуславливает их ограниченный срок годности в сравнении с недейтерированными соединениями. Также с этим связана необходимость создания особых условий хранения для этих соединений (-20°С).
Технический результат заявленного изобретения заключается в создании способа определения топирамата в плазме крови с высокой воспроизводимостью и точностью, наиболее адаптированного для решения задач экспериментальной и клинической фармакокинетики.
Технический результат достигается тем, что проводят количественное определение топирамата в плазме крови путем ее анализа на наличие топирамата высокоселективным методом хроматомасс-спектрометрии, при этом хроматомасс-спектрометрию осуществляют с использованием матрицы в виде плазмы крови с топираматом и внутреннего стандарта, вещества, близкого по строению молекулы к анализируемому веществу - 2,3-4,5-бис-О-изопропилиден-бета-D-фруктопиранозы-N-(4-хлорбензоил)сульфамата, разделение продуктов экстракции проводят на обращенно-фазной хроматографической колонке 4,6×150 мм, при этом в качестве элюента применяют 10 мМ ацетат аммония - раствор А и смесь ацетонетрила и 10 мМ ацетата аммония в отношении 90:10 - раствор Б, взятых в процентном соотношении раствора А к раствору Б 40:60 соответственно, с температурой разделения 35°С, и скоростью подачи элюента 0,8 мл/мин, детектирование топирамата проводят по четырем дочерним ионам с m/z 95.9, 122.0, 161.9, 280.0, образующихся в результате фрагментации родительского молекулярного иона топирамата с m/z 338.2, а его концентрацию рассчитывают по формуле: С=15,06732079×AR, где С - концентрация топирамата (мкг/мл), AR - отношение площади хроматографического пика топирамата к площади пика внутреннего стандарта.
Способ осуществляется следующим образом.
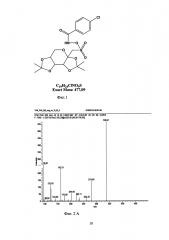
Все растворители имели квалификацию «Для хроматографии», реактивы - не ниже «ч.д.а.». Для приготовления растворов стандартных образцов использовали субстанции стандартов топирамата (производства Sigma-Aldrich, США) и 2,3-4,5-бис-O-изопропилиден-бета-D-фруктопиранозы (4-хлорбензоил)сульфамата (см. фиг. 1). На фигуре 1 показан стандарт топирамата - C19H24ClNO9S Exact Mass: 477,09. В качестве биологической матрицы использовали плазму крови.
Для выделения топирамата из плазмы крови и очистки экстракта используют метод жидкостной экстракции. К образцу плазмы крови объемом 500 мкл добавляют 50 мкл внутреннего стандарта (2,3-4,5-бис-О-изопропилиден-бета-D-фруктопиранозы-N-(4-хлорбензоил)сульфамата, 100 мкг/мл) и 500 мкл пересыщенного раствора бикарбоната натрия (NaHCO3, 1,14 моль/л) с целью повышения коэффициента извлечения топирамата. Затем приливают 5 мл органического экстрагента - этилацетата. Образовавшуюся смесь встряхивают в течение 5 минут на вортекс-миксере Heidolph Ultra, а затем центрифугируют на скорости 3500 об/мин для разделения органического и гидрофильного слоя. Надосадочную жидкость осторожно декантируют и упаривают в центрифужном вакуумном концентраторе Eppendorf Concentrator 5301 при температуре 60°С. Полученный сухой остаток перерастворяют в 500 мкл метанола. Образец переносят в хроматографическую виалу, которую помещают в автосамплер хроматографа для дальнейшего хромато-масс-спектрометрического анализа. Раствор инжектируют в петлю хроматографа в объеме 10 мкл.
В данных условиях коэффициент экстракции для топирамата составляет 88,97±1,25%, для внутреннего стандарта - 90,96±0,93%.
Для высокоэффективной жидкостной хромато-масс-спектрометрии используют хроматограф - «Finnigan Surveyor LC Pump Plus», детектор - масс-спектрометрический детектор «LCQ Fleet MS» (квадрупольная ионная ловушка) и аналитическую колонку - обращенно-фазную колонку XTerra MS С18 фирмы Waters, США (4,6×150 мм; 5 мкм).
Масс-спектрометрическое детектирование топирамата проводят, по четырем дочерним ионам с m/z 95.9, 122.0, 161.9, 280.0, образующимся в результате фрагментации родительского молекулярного иона топирамата с m/z 338.2 при нормализованной энергии соударений 23 eV. Масс-спектр второго порядка для топирамата представлен на фиг. 2А и для 2,3-4,5-бис-О-изопропилиден-бета-D-фруктопиранозы-N-(4-хлорбензоил)сульфамата на фиг. 2Б1 (по вертикали интенсивность (Intensity) по горизонтали масса заряда (m/z).
Внутренний стандарт детектируют по дочерним ионам с m/z 154.90, 234.00, 250.00, 262.00, 418.20, образующимся в результате распада молекулярного иона внутреннего стандарта с m/z 476.4. Масс-спектрометр работал в режиме регистрации ионов, отрицательно заряженных электроспреем (ESI), создаваемым напряжением в 5 кВ. Скорость потока газа-небулайзера (азота): 5 л/мин, давление на распылителе - 100 psi. Температура интерфейса капилляра составляла 350°С, температура нагревателя - 300°С. Амплитуда возбуждения на концевых электродах ловушки 0,1 В. В качестве демпфирующего газа в ионной ловушке использовался гелий. Данные обрабатывались с помощью Xcalibur 2.1 w/Foundation 1.0.1.
Разделение осуществляют на обращенно-фазной хроматографической колонке XTerra MS С18 фирмы Waters, США, 5 мкм, 4,6×150 мм. Подвижная фаза состоит из двух растворов: 10 мМ ацетата аммония, (раствор А) и смеси ацетонитрила и 10 мМ ацетата аммония в соотношении 90:10 соответственно (раствор Б). Растворы А и Б взяты в процентном соотношении 40А:60Б. Работа проводилась в изократическом режиме элюирования. Скорость потока подвижной фазы составляла 0,8 мл/мин. Объем пробы - 10 мкл. Температура разделения 35°С. Продолжительность хроматографирования - 10 минут. Время удерживания аналита - 3,22±0,05 минут. Время удерживания внутреннего стандарта (2,3-4,5-бис-O-изопропилиден-бета-D-фруктопиранозы-N-(4-хлорбензоил)сульфамата) - 2,75±0,05 минут.
Демонстрационная хроматограмма образца плазмы крови с концентрацией топирамата 10 мкг/мл представлена на фигуре 3, на которой видна хроматограмма экстрагированного образца плазмы крови с концентрацией топирамата 10 мкг/мл, верхний пик - пик аналита, нижний пик - пик внутреннего стандарта (по вертикали относительное содержание (Relative abundance), по горизонтали время (Time) в минутах).
Для приготовления калибровки готовили маточные растворы стандартов топирамата и внутреннего стандарта в метаноле с концентрациями 1 мг/мл. Раствор топирамата применяли для приготовления растворов рабочих стандартных образцов на плазме крови с концентрациями 0,156 мкг/мл; 0,313 мкг/мл; 0,625 мкг/мл; 1,25 мкг/мл; 2,5 мкг/мл; 5 мкг/мл; 10 мкг/мл; 20 мкг/мл. Раствор внутреннего стандарта с концентрацией 1 мг/мл разбавляли в 10 раз для получения рабочего раствора внутреннего стандарта с концентрацией 100 мкг/мл. Калибровочная кривая топирамата в плазме крови показана на фиг. 4.
Количественное определение осуществляли по градуировочной зависимости для топирамата в плазме крови и рассчитывали по формуле С=15,06732079×AR, где С - концентрация топирамата (мкг/мл), AR (Area Ratio) - отношение площадей пиков аналита и внутреннего стандарта. Коэффициент корреляции составил R2=0.9973, что соответствует надлежащей аналитической аппроксимации. Предел количественного определения - 0,625 мкг/мл.
Точность и воспроизводимость
Точность выражалась в виде коэффициента вариации (% C.V.) для каждой серии образцов согласно уравнению:
, где
SD - стандартное отклонение серии определений;
- среднее арифметическое значение полученных концентраций.
Воспроизводимость измерялась, как процент отклонения (% dev.) от теоретического значения по формуле , где
- среднее арифметическое значение полученных концентраций;
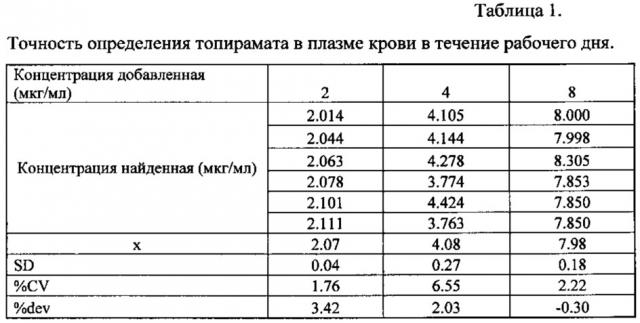
Для метрологической валидации полученной методики определяли точность в течение рабочего дня. Каждый из образцов, предназначенных для контроля качества, анализировали в течение 1 рабочего дня (6 определений). Результаты представлены в таблице 1.
Относительная ошибка определения топирамата не превышала 10%.
Таким образом, заявленный способ обладает высокой эффективностью в проведении анализа, не требует использования большого количества химических реактивов. Высокая точность и чувствительность данного метода количественного определения топирамата в плазме крови обеспечивает идентификацию вещества с установленными характеристиками погрешности, что позволяет ее использовать как в экспериментальной, так и клинической фармакокинетики препарата.
Способ количественного определения топирамата в плазме крови, включающий анализ крови на наличие топирамата высокоселективным методом хроматомасс-спектрометрии, отличающийся тем, что проводят хроматомасс-спектрометрию с использованием матрицы в виде плазмы крови с топираматом и внутреннего стандарта, вещества, близкого по строению молекулы к анализируемому веществу - 2,3-4,5-бис-О-изопропилиден-бета-D-фруктопиранозы-N-(4-хлорбензоил)сульфамата, разделение продуктов экстракции проводят на обращенно-фазной хроматографической колонке 4,6×150 мм, при этом в качестве элюента применяют 10 мМ ацетат аммония - раствор А и смесь ацетонитрила и 10 мМ ацетата аммония в отношении 90:10 - раствор Б, взятых в процентном соотношении раствора А к раствору Б 40:60 соответственно, с температурой разделения 35°C, и скоростью подачи элюента 0,8 мл/мин, детектирование топирамата проводят по четырем дочерним ионам с m/z 95.9, 122.0, 161.9, 280.0, образующимся в результате фрагментации родительского молекулярного иона топирамата с m/z 338.2, а его концентрацию рассчитывают по формуле С=15,06732079×AR, где С - концентрация топирамата (мкг/мл), AR - отношение площади хроматографического пика топирамата к площади пика внутреннего стандарта.