Способ получения антимикробного пептида цекропина р1 из экстракта трансгенных растений каланхоэ перистого
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности и касается разработки получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого. Способ получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого, включающий инкубацию листьев растений в темноте при 4-8°С в течение 7 сут, измельчение листьев, экстрагирование дистиллированной водой, взятой в равном количестве, отделение экстракта центрифугированием, выдерживание экстракта при 70°С 1 ч, стерилизацию экстракта через мембранный фильтр и добавление консерванта - 0,5% хлороформа для хранения экстракта, а для выделения пептида цекропина Р 1 высаливание его из экстракта 80%-ным сульфатом аммония, растворение осадка и его гельфильтрацию с последующей очисткой на колонке с носителем Superdex Peptide HR 10/30 и определением молекулярного веса элюируемого пика методом масс-спектрометрии и его антибиотической активности. Вышеописанный способ является эффективным для получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого, обладающего широким спектром антимикробного действия. 1 з.п. ф-лы, 6 ил., 6 пр.
Реферат
Способ получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого
Изобретение относится к фармацевтической промышленности и касается разработки способа получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого.
Лекарственные растения занимают существенное место в лечении и профилактике многих заболеваний. В нашей стране насчитывается около 3000 видов растений, которые обладают лекарственными свойствами. В некоторых странах до 50% лекарственных препаратов получают из природного сырья, преимущественно из растений. В настоящее время с повышением цен на многие препараты и ухудшением экологической ситуации актуально создание новых фармакологических фитопрепаратов. Кроме того, растительные препараты малотоксичны, что дает возможность применять их более длительное время.
Каланхоэ перистое (Kalanchoe pinnata) лекарственное растение, экстракт которого используют для лечения ожогов, артритов, ревматизма, кашля, лихорадки, кожных ран, язв и как биостимулятор при пересадке кожи. Установлено, что сок каланхоэ проявляет антигистаминное [Nassis C.Z., Haebisch Е.М.А.В., Giesbrecht A.M. Antihistamine activity of Bryophillum calycinum // Brazilian J. Med. Res. 1992. V. 25. P. 929-936], иммуносупрессивное [Moraes V.L.G., Santos L.F.M., Castro S.B. et al. Inhibition of lymphocyte activation by extracts and fractions of Kalanchoe, Alternanthera, Paullinea and Mikania species // Phytomedicine. 1994. V. 1. P. 199-204], противогрибковое [Misra S.B., Dixit S.N. Antifungal activity of leaf extracts of some higher plants // Acta Botanica Indica. 1979. V. 7. P. 147-150], пртиволейшманиозное [Da-Silva A.A.G., Costa S.S., Mendonca S.C.F. et al. Therapeutic effect of oral Kalanchoe pinnata leaf extract in murine leishmaniasis // Acta Tropica. 1995. V. 60. P. 201-210], инсектицидное [Supratman U., Fujita Т., Akiyama K., Hayashi H. Insecticidal compounds from Kalanchoe daigremontiana x tubiflora // Phytochem. 2001. V. 58. P. 311-314], противовоспалительное [Costa S.S., de Lourdes M., de Souza M. et al. Kalanchosine Dimalate, an Antiinflammatory Salt from Kalanchoe brasiliensis // J. Nat. Prod. 2006. V. 69. P. 815-818], противоопухолевое [Murakami A., Nakamura Y., Koshimizu K., Ohigasha H. Glyceroglycolipids from Citrus hystrix, a traditional herb in Thailand, potently inhibit the tumour-promoting activity of 12-tetradecanoylphorbol 13-acetate in mouse skin // J. Agric. Food Chem. 1995. V. 43. P. 2779-2783; Murakami A., Kumagai Т., Hada T. et al. effect of glycolipids from spinach on mammalian DNA polymerases // Biochem. Pharmacol. 2003. V. 65. P. 259-267] действие. Основными действующими компонентами препаратов, получаемых из сока каланхоэ, считают дубильные вещества, полисахариды, липиды, аминокислоты и фенольные соединения.
Экспрессия в растениях генов гетерологичных антимикробных пептидов (АМП) перспективна для повышения лечебных и бактерицидных свойств каланхоэ. В настоящее время антимикробные пептиды (АМП) рассматривают как эффективную альтернативу классическим антибиотикам, к которым, последнее время, развивается резистентность патогенных микроорганизмов. В настоящее время методы генетической инженерии позволяют синтезировать в клетках растений гетерологичные белки, в том числе терапевтического назначения. Трансгенные растения являются перспективными объектами для получения дешевых и безопасных рекомбинантных белков по сравнению с их традиционными продуцентами - бактериями и дрожжами. Они могут быть использованы в качестве "биофабрик" по производству целевых белков медицинского назначения [Magnuson N.S., Linzmaier P.М., Reeves R., An G., HayGlass K., Lee J.M. // Secretion of biologically active human interleukin-2 and interleukin-4 from genetically modified tobacco cells in suspension culture. Protein Expr. Purif. 1998. V. 13. P. 45-52]. Себестоимость АМП, выделенных из трансгенных растений, в 20-30 раз ниже по сравнению с другими методами их получения (твердофазный синтез, получение из других источников). Как продуценты фармакологической субстанции растения более безопасны, так как они свободны от патогенных вирусов животных и человека.
Цекропин Р1 нематод относится к группе линейных α-спиральных пептидов, не содержащих цистеина [Boman H.G., Hultmark D. Annu. Rev. Microbiol. 1987. V. 41. P. 103-126]. В отличие от цекропинов насекомых он состоит из одной положительно заряженной α-спирали, в образовании которой задействованы практически все аминокислотные остатки. Цекропин Р1 активен против патогенных грамположительных и грамотрицательных бактерий [Pillai A., Ueno S., Zhang Н., Lee J. М., Kato Y. Cecropin P1 and novel nematode cecropins: a bacteria-inducible antimicrobial peptide family in the nematode Ascaris suum II Biochem. J. 2005. V. 390. P. 207-214], грибов [Захарченко H.C., Рукавцова Е.Б., Гудков А.Т., Юхманова А.А., Школьная Л.А., Кадо К.И., Бурьянов Я.И. Эспрессия искусственного гена антимикробного пептида цекропина Р1 повышает устойчивость растений картофеля к фитофторозу и белой гнили // Доклады Академии наук. 2007. Т. 415. №1. С. 129-131] и некоторых опухолевых клеток [Shin S.Y., Kang J.H., Jang S.Y., Kim Y., Kim K.L., Hahm K-S. Effect of the hinge region of cecropin A (1-8)-magainin 2(1-12), a synthetic antimicrobial peptide, on liposomes, bacterial and tumor cells // Biochimica et biophysica Acta. 2000. V. 1463. P. 209-218]. Ранее получены трансгенные растения каланхоэ перистого (Kalanchoe pinnata L.), экспрессирующие ген антимикробного пептида цекропина Р1, и показали их повышенную устойчивость к фитопатогенным микроорганизмам [Захарченко Н.С., Лебедева А.А., Бурьянов Я.И. Способ получения генетически модифицированных растений каланхоэ, экспрессирующих ген цекропина Р1. Патент №2445768 (РФ) // БИ 2012, №9]. Биосинтез в растениях каланхоэ перистого цекропина Р1 актуален для его фармацевтического и медицинского использования.
В настоящее время из растений, животных и микроорганизмов были выделены множество белков с различной биологической активностью. Существуют различные способы выделения, очистки и анализа антимикробных препаратов из растений, в частности.
Известен способ выделения растительного пептида дефензина Lc-def из проростков чечевицы [Finkina E.I., Shramova E.I., Tagaev А.А., Ovchinnikova T.V. A novel defensin from the lentil Lens culinaris seeds // Biochem. Biophys. Res. Commun. 2008. Vol. 371 (4). P. 860-865]. В этом способе сначала получали суммарный белковый осадок. Для этого гомогенизировали проращенные семена в экстракционном буфере (10 мМ Na2HPO4, 15 мМ NaH2PO4, 100 мМ KCl, 2 мМ ЭДТА), содержащем поливинилполипирролидон и смесь ингибиторов протеаз, затем высаливали белки 75% сульфатом аммония. Первая стадия выделения включала гельфильтрацию на колонке с Сефадексом G-75, уравновешенной 200 мМ ацетатом аммония с 2 М мочевиной, рН 7,0. Затем фракции, содержащие белки С М.в. 3-6 и 7-10 кДа, объединяли и подвергали диализу с последующим разделением на катионообменной колонке Mono S HR 5/5, а затем на обращенно-фазовой колонке Luna С18.
Недостатком этого способа является дороговизна и трудоемкость процесса выделения.
Известен способ выделения АМП из зерновок пшеницы Triticum kiharae, включающий различные типы высокоэффективной жидкостной хроматографии (аффинную и обращенно-фазовую) в сочетании с секвенированием амикислотных последовательностей по Эдману и масс-спектрометрией [Egorov Т.А., Odintsova T.I., Pukhalsky V.A., Grishin E.V. Diversity of wheat antimicrobial peptides // Peptides. 2005. V. 26. P. 2064-2073]. Для этого семена пшеницы были гомогенизированы в миксере и мука обезжирена с петролейным эфиром (1:10) в течение 1 ч. Затем пептиды экстрагированы буфером, содержащим 1% трифторуксусной кислоты (ТФУ), 1 М HCl, 5% муравьиной кислоты и 1% NaCl в присутствии пепстатина А (1 мкг/мл) в соотношении 1:4. Экстракт концентрировали и обессоливали на катридже С8 Aquapore RP-300 catridge (10×30 mm), уравновешанным 0,1% ТФУ (растворитель А). Белки и пептиды были элюированы 70% растворителем В (80% ацетонитрил в растворителе А). Белки/петиды были фракционированы замораживанием и растворены в 150 мкл буфера, содержащего 150 мкл 10 мМ Трис-HCl (рН 7,5), центрифугировали 14 тыс. g 15 мин при 20°С и супернатант был помещен на 1 мл колонку HiTrap Heparin HP (Amersham). После этого пептиды фракционировали на колонке Superdex Peptide HR 10/30 и очищали высокоэффективной жидкостной хроматографией на колонке Vydac С18 в линейном градиенте растворителя В 1 ч. Пептиды были детектированы при длине волны 214 нм. В дальнейшем проводился масс-спектрометрический анализ выделенных пептидов.
Недостатком этого способа является длительность и дороговизна способа выделения.
Задачей настоящего изобретения является разработка нетрудоемкого способа получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого (Kalanchoe pinnata).
Известен способ получения экстракта (сока) каланхоэ перистого (Kalanchoe pinnata) [В.П. Широбоков, А.И. Евтушенко, В.Ф. Лапчик, Д.Н. Широбокова. Ингибитор вирусов. Авторское свидетельство изобретения №903380. 09.02.1982. Бюл. №5, (53) УДК 576.858(088.8]. В этом способе описывается ингибирующее действие сока каланхоэ на вирусы полиомиелита. Для этого вымытые в проточной воде листья измельчают в гомогенизаторе и полученный материал центрифугируют при 3 тыс. об/мин в течение 10 мин, затем надосадочную жидкость стерилизуют через мембранные фильтры. В работе для проведения инактивации к вирусосодержащему материалу добавляют сок в концентрации 0,4% и смесь выдерживают при 10-20°С в течение 10 и более минут. При этом проявляется вирулицидное действие. Недостатком этого способа является то, что при получении сока каланхоэ не добавляют консервант, способствующий длительному хранению экстракта.
Наиболее близким к предлагаемому является способ получения экстракта (сока) каланхоэ перистого (Kalanchoe pinnata) [Курищук К.В., Диденко Н.В. Способ получения сока каланхоэ. UA, 66418, С2]. В этом способе сорванные листья растений подвергались измельчению и центрифугированию экстракта. После этого отделенный сок выдерживали в темноте и прохладном месте (+4 - +8°С) 1-10 сут. При этом образовавшийся осадок удаляли стерилизацией через мембранный фильтр и добавляли, в качестве консерванта, этиловый спирт или хлороформ.
Недостатком этого способа является то, что экстракт не обладал высокой бактерицидной активностью.
Задачей настоящего изобретения является разработка способа получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого (Kalanchoe pinnata), обладающего высокой бактерицидной активность за счет синтеза цекропин Р1.
Технический эффект, который может быть получен, при использовании предлагаемого изобретения, заключается в том, что он обеспечивает получение значительно более дешевого антибиотического лекарственного средства нового поколения.
Поставленная задача решается путем получения экстракта каланхоэ и выделения цекропина Р1, содержащегося в нем. Для этого листья трансгенных растений каланхоэ перистого, после предварительной инкубации в темноте при пониженной температуре [В.П. Филатов. Биологические основы тканевой терапии. Известия АН СССР, сер. биол. №6, с. 23-59] измельчают в лабораторном гомогенизаторе и экстрагируют дистиллированной водой, консервацию проводят при температуре плюс 4-8°С в течение 3-10 суток, смесь после гомогенизации отжимают, центрифугируют и прогревают при 65-70°С 1-2 ч. Далее супернатант используют в двух вариантах: 1 - консервация экстракта и его расфасовка; 2 - выделение пептида цекропина Р1 из экстракта. 1) Для стерилизации экстракта полученный супернатант пропускают через мембранные фильтры TYPE HAWP 0,22 мкм, добавляют консервант 0,5-2% хлороформа, полученный концентрат подвергают биологическому тестированию и расфасовывают по флаконам. 2) Для выделения пептида супернатант осаждают 80% сульфатом аммония (NH4)2SO4, проводят гель-фильтрацию на колонке с Сефадексом G-50 и очистку на колонке с носителем Superdex Peptide (HR 10/30). Полученный препарат анализируют методом высокоэффективной жидкостной хроматографией (ВЭЖХ или HPLC (по англ)) и масс-спектрометрией.
Проверку качества экстракта и выделенного пептида цекропина Р1 проводят с помощью вестерн-блот анализа с антителами к цекропину Р1 и исследованием антибиотической активности пептида по отношению к патогенным бактериям.
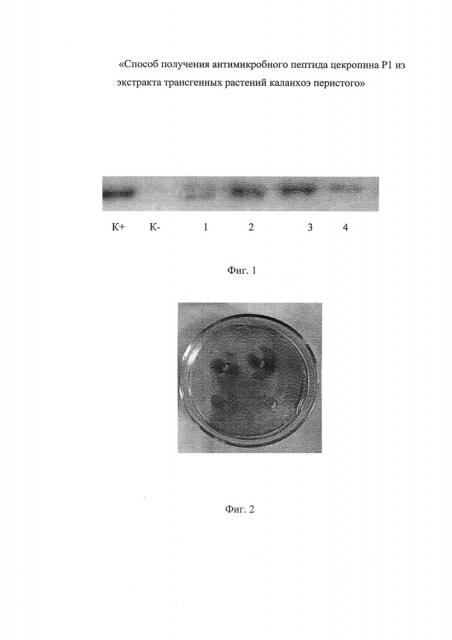
На Фиг. 1 результаты Вестерн-блот анализа экстрактов трансгенных растений K. pinnata. К(+) - синтетический цекропин Р1 мол. м. 3.4 кДа (30 нг); (К-) - нетрансформированное растение; 1, 4 - экстракты растений (линии 1, 2) до холодового стресса; 2-3 - экстракты растений после холодового стресса (линии 1, 2).
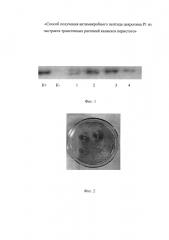
На Фиг. 2 результаты антибиотической активности экстрактов каланхоэ. 1 - экстракт каланхоэ линии 1, зона лизиса 5 мм; 2 - экстракт каланхоэ линии 2, зона лизиса 5 мм; 3 - синтетический цекропин Р1 (500 нг), добавленный в экстракт контрольного растения, зона лизиса 7 мм; 4 - экстракт каланхоэ контрольного нетрансформированного растения.
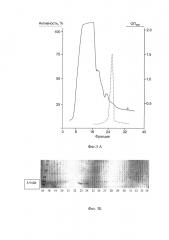
На Фиг. 3А результаты очистки и анализа пептида цекропина Р1 из каланхоэ перистого. Гель-хроматография сульфат-аммониевой фракции с цекропином Р1 на Sephadex G-50.
На Фиг. 3Б результаты очистки и анализа пептида цекропина Р1 из каланхоэ перистого. Электрофорез фракций 18-34 в 12,5%-ном SDS-ПААГ. М - маркер молекулярного веса.
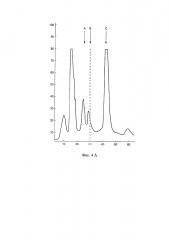
На Фиг. 4А результаты высокоэффективной гельфильтрации цекропина Р1 на носителе Superdex Peptide (HR 10/30). Сплошная линия - оптическое поглощение при 280 нм. Штриховая линия - детекция цекропина Р1 по антимикробной активности. А - цитохром С (12,4 кДа), В - цекропин Р1 (3,3 кДа), С - глицин (75 Да).
На Фиг. 4Б результаты электрофореза фракций 15-32 в 12,5%-ном SDS-ПААГ; М - маркер молекулярного веса. 16-32 - пробы белка после элюции.
На Фиг. 5 результаты анализа антимикробной активности фракций после очистки на Superdex Peptide (HR 10/30). 1 - фракция 28; 2 - фракция №29; 3 - фракция №30; 4 - фракция 31.
На Фиг. 6 результаты масс-спектрометрического анализа пептидов из трансгенных растений каланхоэ перистого.
Возможность осуществления предлагаемого способа подтверждается представленными примерами, но не ограничивается ими.
Пример 1. Подготовка растительного материала.
Трансформированные растения каланхоэ перистого, экспрессирующие ген антимикробного пептида цекропина Р1, выращивают в теплице при температуре 22-24°С, 16-часовом дне и освещенности 2 клк. Состав грунта: торф:песок в соотношении 1:1 с добавлением 20 г на 10 кг грунта коммерческого азотно-фосфорного минерального удобрения «нитрофоски» («Росагрохим»). Для получения экстракта и выделения пептида цекропина Р1 из него берут 3 кг листьев среднего яруса трансформированных молодых растений каланхоэ. Листья обрывают и помещают в темное, прохладное место - +4°С на 7 сут. После этого листья промывают водопроводной водой, подсушивают на бумажном полотенце и используют для анализа и выделения экстракта.
Пример 2. Получение экстракта каланхоэ перистого.
Для получения экстракта листья (3 кг) измельчают в лабораторном блендере МВ800 (Kinematica AG, Швейцария) до однородной массы, добавляя равное количество дистиллированной воды (3 л). Растительную массу отжимают через несколько слоев марли и центрифугируют (Beckman G-21, ротор G-10) при скорости 6000 g в течение 30 мин. Супернатант прогревают в термостате (VEF MLW PRUFGERATE-WERK MEDINGEN, Германия) при 70°С в течение 1 ч в стеклянных стаканах, стерилизуют через мембранный фильтр TYPE HAWP 0,22 мкм, добавляют 0,5% хлороформа в качестве консерванта и расфасовывают по 130 мл во флаконы объемом 250 мл.
Пример 3. Вестерн-блот анализ экстракта каланхоэ
Проводят сравнительный анализ содержания цекропина Р1 в трансгенных растениях до 7-дневной инкубации листьев в прохладном месте и после инкубации методом вестерн блот анализа. Для анализа используют равное количество биологического материала (белок из 50 мг листьев). Для вестерн-блот анализа 1 мл экстракта отбирают в чистые пробирки, концентрируют 5% ТХУ, осадок растворяют в 100 мкл 0,1 М NaOH. Для электрофореза берут по 10 мкл раствора белков. Перед нанесением пробы белок смешивают с равным объемом буфера для нанесения, содержащего в 20 мл 2.48 мл tris-HCl рН 6.8; 4 мл 20% SDS; 4 мл глицерин; 40 мг бромфенолового синего; 2 мл бета-меркаптоэтанола; 7.52 мл воды дистиллированной. Для электрофоретического разделения белков используют 12,5%-ный SDS-ПААГ. Для переноса белков используют PVDF-мембрану ("Porablot", Германия). Электроперенос проводят в течение ночи при 20 мА в буфере (25 М Трис-HCl рН 7,4; 250 мМ глицина) с добавлением 20% метанола. Мембрану инкубируют последовательно сначала с антителами к гену цекропина Р1, а затем с вторичными кроличьими поликлональными антителами, конъюгированными с пероксидазой хрена. Иммунодетекцию проводят с помощью набора хемилюминисцентной системы ECL ("Amersham", Великобритания). Синтетический пептид получают твердофазным синтезом.
На Фиг. 1 представлены результаты исследований экстрактов, полученных из листьев до обработки пониженной температурой и после обработки. Показали, что при пониженной температуре у растений каланхоэ происходит индукция пептида цекропина Р1, что видно из вестерн-блот анализа - полосы 3, 4, соответствующие растениям, подвергшихся холодовой обработке, более яркие, чем полосы 1, 2, соответствующие растениям без охлаждения. Эти данные показывают, что холодовая предобработка растений каланхоэ способствует накоплению цекропина Р1 в экстракте, что важно для использования растений как продуцента цекропина Р1.
Пример 4. Анализ антибиотической активности полученного экстракта по отношению к патогенному штамму Erwinia carotovora.
1 мл экстракта концентрируют 5%-ной трихлоруксусной кислотой (ТХУ) и осадок растворяют в 100 мкл 0,1М NaOH. Раствор препарата вносят в лунки, сделанные в агаре (30 мл 1,5% агара), на поверхность которого наносят патогенный штамм Е. carotovora. Чашки Петри инкубируют 8 ч при 4°С для диффузии экстрактов в агар, а затем инкубируют при 25°С в течение суток. Ингибирующее влияние экстрактов на рост клеток бактерий оценивают по радиусу чистой зоны вокруг лунки. Количественную оценку содержания цекропина Р1 в экстракте проводят с контрольными пробами, где в качестве стандарта используют известные концентрации синтетического цекропина P1 ("Sigma", США). На Фиг. 2 видно, что полученный экстракт из трансформированных растений каланхоэ линий 1, 2 имел повышенную антибиотическую активность, о чем свидетельствовали зоны лизиса вокруг лунок 1 и 2. Эксперименты с добавлением к экстрактам контрольных растений фиксированных количеств синтетического цекропина Р1 позволяют установить экспрессию пептида в трансгенных растениях на уровне 0,1-0.2% от общего растворимого белка. Из 3 кг листьев растений получают около 5 л экстракта, который помещают в 38 штуки культуральных флаконов объемом 250 мл, содержащих препарат экстракта по 130 мл.
Образующийся экстракт каланхоэ перистого, антимикробный пептид цекропин Р1 представляют собой устойчивый при хранении стерильный раствор с концентрацией пептида не менее 0,7 мкг/мл. По биологическим характеристикам препарат пригоден для наружного применения как ранозаживляющее средство.
Пример 5. Выделение пептида цекропина Р1 из экстракта растений каланхоэ перистого.
Для гомогенной очистки пептида цекропина Р1 методами хроматографии осаждают белки из экстракта методом высаливания сульфатом аммония (Х. Биссвангер. «Практическая энзимология». Изд-во: Бином. Лаборатория знаний. - М., 2010, 328 с.). Аликвоты экстракта каланхоэ (по 5 мл) исследуют на эффективность процентного насыщения сульфатом аммония (NH4)2SO4 для определения максимального осаждения цекропина Р1. Наибольший выход цекропина Р1 в осадке дает 80%-ное насыщение (NH4)2SO4. Для препаративного выделения постепенно добавляют сухой порошок NH4)2SO4 к экстракту при перемешивании на мешалке в холодной комнате (+4°С) Через 6 ч, после высаливания 80%-ным раствором (NH4)2SO4 суспензию осаждают центрифугированием 30 мин, 6000 g. Белковый осадок (содержащий цекропин Р1), растворяют в минимальном количестве (10 мл) 20 мМ трис-буфера (рН 7.5) и проводят диализ (диализные трубки «Sigma») против того же буфера.
Очищенный от пигментов и низкомолекулярных веществ препарат подвергают гель-фильтрации с сорбентом Sephadex G-50. на колонке 2,5×100 см, уравновешенной 20 мМ трис-буфера (рН 7.5). Элюцию проводят при скорости потока 10 мл/ч. В результате хроматографии собирают 60 образцов элюата по 10 мл каждый. Образцы (по 1 мл) осаждают 5% ТХУ, растворяют в 0,1 М NaОH и с ними проводят электрофорез. На фиг. 3А представлена хроматограмма элюции. На Фиг 3Б, показывающей электрофорез полученных фракций, отмечены яркие полосы во фракциях 23 и 24, которые обладали антибиотической активностью. Далее эти фракции №23, 24, содержащие белки с М.в. 3-5 кДа и обладающие антибактериальной активностью, объединяют (18 мл) и подвергают диализу против 50-кратного объема 5 мМ трис-буфера (рН 7.5) в течение ночи при 4°С при перемешивании с последующим разделением на колонке с носителм Superdex Peptide (HR 10/30), предварительно уравновешенным 20 мМ трис-буфером (рН 7.5) с 15 мМ NaCl. Элюцию проводят градиентом NaCl (0.15 М-1.5 М) в том же буфере со скоростью 0.4 мл/мин; собирают фракции по 0.8 мл. На Фиг. 4А представлена хроматограмма гельфильтрации, в результате которой собрали 60 фракций по 0,8 мл каждая (48 мл). Полученные фракции проверяют с помощью электрофореза в SDS-ПААГе. Для этого каждую фракцию 0,4 мл осаждают добавлением 5% ТХУ, через 10 мин выдерживания на холоду при +4°С, раствор центрифугируют при 10000 g в течение 15 мин и образовавшийся осадок растворяют в 100 мкл 0,1 М NaOH, для электрофореза берут по 10 мкл. На Фиг. 4Б показан анализ фракций после элюции. Из Фиг. 4Б видно, что фракция №30 содержит специфическую мажорную белковую полосу с молекулярной массой около 3,4 кДа. На Фиг. 5 показана антимикробная активность фракции №30 по отношению к фитопатогену Е. carotovora. Фракция 30 содержит максимальное количество пептида, что коррелирует с пиком максимальной антимикробной активности во фракции.
Пример 6. Масс-спектрометрический анализ выделенного пептида.
С полученным препаратом основного пика после колонки с носителм Superdex Peptide (HR 10/30) проводят масс-спектрометрический анализ (Bruker Autoflex Speed MALDI TOF/TOF (Bruker Daltonik GmbH, Bremen Germany) (Фиг. 6). Раствор фракции №30 концентрируют 5% ТХУ и растворяют в 100 мкл воды. К водному раствору полученного препарата добавляют равный объем α-циано-4-гидроксикоричной кислоты (матрица) в 0.1%-ной трифторуксусной кислоте (40%) (ТФУ) и в ацетонитриле (60%) (MeCN). HPLC анализ проводят на жидкостном хроматографе Waters HPLC (Waters Corporation, США), колонка Luna 5u С18(2), 250×4,6 mm, 100 (Phenomenex, USA). Элюент A - 0,1% ТФУ, В - MeCN, градиент 0-80% В (25 мин), скорость потока - 0,7 мл/мин. Детектор - 280 нм. Масс-спектры MALDI выделенных пептидов регистрируют на масс-спектрометре Bruker Autoflex Speed MALDI TOF/TOF (Bruker Daltonik GmbH, Bremen Germany).
Проведенный анализ подтвердил молекулярный вес синтезируемого цекропина Р1 3338 кДа. Методом аналитической гельфильтрации безклеточного экстракта, очищенного от пигментов и низкомолекулярных веществ, и методом масс-спектрометрии молекулярная масса цекропина Р1, синтезируемого в трансгенных растениях, определена равной 3,3 кДа, что соответствует молекулярной массе синтетического цекропина Р1.
Полученные фракции элюатов, соответствующие основным пикам на хроматограммах, высушивают с помощью вакуумного концентратора SpeedVac и хранят при температуре - 20°С.
Проводят расчет количества выделенного цекропина Р1 после очистки на Superdex Peptide: Зона лизиса фракции №30 составляет 8 мм, тогда как 1 мкг синтетического пептида дает зону лизиса 14 мм. Соответственно, в 1 мл экстракта (такое количество наносится в лунку, после осаждения 5%-ным ТХУ) находится 0,5 мкг. Следовательно, при учете всего объема экстракта (5 л) и неизбежных потерь при очистке составляет количество цекропина 0,5×5000 мл = 2500 мкг (2,5 мг).
По приведенной схеме выделения выход очищенного пептида антимикробного пептида цекропина Р1 из экстракта 3 кг листьев трансгенных растений каланхоэ перистого составляет около 3 мг. Экономическая целесообразность выделения цекропина Р1 из растений очевидна, поскольку цена коммерческого препарата за 1 мг составляет около 80 тыс. руб. (Sigma), в то время как из растений цена, как минимум в 20-30 раз, ниже.
На мировом рынке пока нет препаратов антимикробных пептидов, выделенных из трансгенных растений, в то же время, в нескольких странах уже ведутся их доклинические испытания и планируется прозводство этих перспективных лекарственных средств уже в 2017-2018 гг.
Полученная разработка может найти применение в фармацевтических компаниях по производству противоожоговых и ранозаживляющих средств.
1. Способ получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого, включающий инкубацию листьев растений в темноте при 4-8°С в течение 7 сут, измельчение листьев, экстрагирование дистиллированной водой, взятой в равном количестве, отделение экстракта центрифугированием, выдерживание экстракта при 70°С 1 ч, стерилизацию экстракта через мембранный фильтр и добавление консерванта - 0,5% хлороформа для хранения экстракта, а для выделения пептида цекропина Р 1 высаливание его из экстракта 80%-ным сульфатом аммония, растворение осадка и его гельфильтрацию с последующей очисткой на колонке с носителем Superdex Peptide HR 10/30 и определением молекулярного веса элюируемого пика методом масс-спектрометрии и его антибиотической активности.
2. Способ по п. 1, отличающийся тем, что при выделении пептида цекропина Р1 используют метод гельфильтрации с сорбентом Sephadex G-50.