Аналог оксистерола oxy133 индуцирует остеогенез и сигнальный путь hedgehog и ингибирует липогенез
Иллюстрации
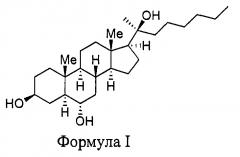
Показать всеИзобретение относится к соединению Оху133, имеющему формулу I,
.
Изобретение также относится к биоактивной композиции, к способам лечения и к способу индукции остеобластической дифференцировки и/или ингибирования дифференцировки адипоцитов мезенхимальных стволовых клеток млекопитающих. Технический результат: получено новое соединение, которое применимо для лечения заболевания кости, для увеличения остеоморфогенеза и/или остеопролиферации, для стимулирования костеобразования, для индукции остеобластической дифференцировки и/или ингибирования дифференцировки адипоцитов мезенхимальных стволовых клеток. 6 н. и 2 з.п. ф-лы, 15 ил., 2 табл., 4 пр.
Реферат
Область техники, к которой относится изобретение
Это изобретение касается синтетического соединения, Oxy133, имеющего структуру
или биоактивной или фармацевтической композиции, содержащей Oxy133 и фармацевтически приемлемый носитель, а также способов использования соединения или его биоактивной или фармацевтической композиции для лечения целого ряда заболеваний, включая заболевание костей, ожирение, сердечнососудистые заболевания и неврологические нарушения.
Уровень техники
Для оказания содействия росту костей, включая сращение перелома и хирургическое лечение заболеваний позвоночника (1-4), в медицине обычно применяются биологические препараты. Для решения проблем, связанных с дегенеративным заболеванием межпозвоночных дисков и артритом, затрагивающим поясничный и шейный отдел позвоночника, хирургом-ортопедом и нейрохирургом зачастую осуществляется спондилодез. Исторически сложилось так, что аутокостный трансплантат, обычно взятый из гребня подвздошной кости пациента, используется для увеличения сращения между уровнями позвонков. Однако, частота осложнений в донорском участке, увеличение времени операции и повышение кровопотери, связанной с получением аутокостного трансплантата (5-7), обусловливают поиск безопасной и эффективной альтернативы.
Для содействия формированию спондилодеза у людей обычно используется рекомбинантный человеческий костный морфогенетический белок-2 (rhBMP-2). Его применение было утверждено в 2002 г. Управлением по надзору за качеством пищевых продуктов и лекарственных веществ США (FDA) для одноуровневого переднего поясничного межтелового спондилодеза (S). С тех пор применение rhBMP-2 значительно увеличилось, а также были расширены показания для его применения с целью включения заднего поясничного спондилодеза, а также шейного спондилодеза. Несмотря на эффективность rhBMP-2, последние сообщения подвергают сомнению его безопасность при использовании во время хирургической операции спондилодеза. Описанные в литературе осложнения включают образование серомы, припухлость мягких тканей, остеолизис позвоночника, эктопическое костеобразование, ретроградную эякуляцию и канцерогенность (9-12). Более того, при его использовании в шейном отделе позвоночника наблюдался отек дыхательных путей, что побудило FDA к выпуску уведомления от системы здравоохранения, содержащего предупреждение о его применении при операциях в шейном отделе позвоночника. В настоящее время не существует подходящей альтернативы, которая имела бы сходную эффективность, вызывая сращение без побочных действий rhBMP-2 (12).
Оксистеролы образуют большое семейство окисленных производных холестерина, присутствующих в кровообращении, а также тканях человека и животных. Было обнаружено, что оксистеролы входят в состав атеросклеротических повреждений и играют роль в различных физиологических процессах, таких как клеточная дифференцировка, воспаление, апоптоз и выработка стероидных гормонов. Некоторые из настоящих изобретателей ранее сообщали, что отдельные оксистеролы природного происхождения обладают устойчивыми остеогенными свойствами (13). Наиболее эффективный остеогенный природный оксистерол, 20(S)-гидроксихолестерол ("20S") (14), является и остеогенным и антилипогенным при применении к мультипотентным мезенхимальным клеткам, способным дифференцироваться в остеобласты и адипоциты. Ранее были осуществлены структурные модификации 20S с целью синтеза более эффективных аналогов 20S, включая Oxy34 и Oxy49, которые, как было показано, вызывают остеогенную и ингибируют липогенную дифференцировку стромальных клеток костного мозга (MSC) посредством активации сигнального пути Hedgehog (Hh) (15). В дополнение к этому Oxy34 и Oxy49 стимулируют спондилодез in vivo на крысиной модели заднелатерального спондилодеза (15). Предшествующие молекулы оксистерола обладают колеблющимися в широких пределах и непредсказуемыми свойствами. Сохраняется потребность в новых, улучшенных оксистеролах по сравнению с rhBMP-2 и предшествующими оксистеролами для обеспечения повышенной активности и эффективности, облегчения синтеза и более низкой стоимости производства. Новый оксистерол может сделать более обоснованным клинический выбор врача при лечении, например, переломов длинных трубчатых костей, болезней позвоночника и остеопороза.
Краткое описание фигур
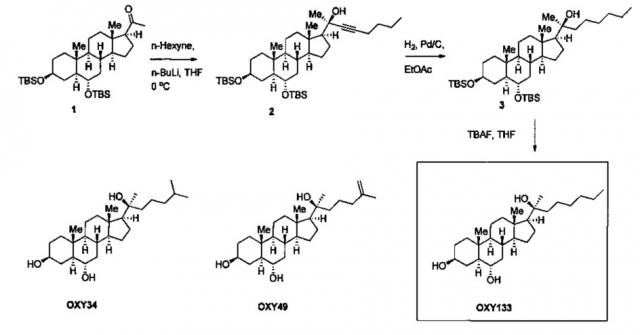
Фигура 1 показывает строение молекул остеогенных оксистеролов. Показано строение молекул 20(S)-гидроксихолестерола (20S), Oxy34, Oxy49 и Oxy133. Oxy34 отличается от 20S дополнительной ОН группой на С6, при этом двойная связь между С5 и С6 устраняется. Oxy49 имеет структуру, сходную с Oxy34, и включает двойную связь между С25 и С27. Oxy133 отличается от Oxy34 и 49 утратой С27 и увеличением длины боковой цепи на один атом углерода.
Фигура 2 показывает зависимое от дозы увеличение активности щелочной фосфатазы при воздействии оксистеролов. (Фиг. 2А) C3HT101/2 клетки или (фиг. 2В) М2-10 В4 клетки на этапе слияния обрабатывали разбавителем (контроль) или 0.125-10 мкм Oxy133. Для прямого сравнения с Oxy133 клетки C3H также обрабатывали Oxy34 и Oxy49 (фиг. 2А). Через 4 дня измеряли активность щелочной фосфатазы (ALP) в полных клеточных экстрактах. Результаты трех отдельных экспериментов приведены в виде среднего из трех определений +SD и нормированы по отношению к концентрации белка, (р<0.0001 для клеток, обработанных 0.25 мкМ или более высокими дозами всех оксистеролов по сравнению с контрольными клетками, обработанными разбавителем).
Фигура 3 показывает, что оху133 вызывает остеогенную дифференцировку. (Фиг. 3А) C3HT101/2 клетки на этапе слияния обрабатывали разбавителем (контроль) или 2.5 мкМ Oxy133 в остеогенной среде. Экспрессия остеогенных генов Runx2, ALP, BSP, OSX и OCN была измерена с помощью ПЦР в режиме реального времени через 48 часов, 4, 7 и 14 дней после обработки. Результаты типичного эксперимента представлены в виде среднего из трех определений ±SD (р<0.005 для контроля в сравнении с Oxy133 во всех временных точках ALP, BSP и OSX и через 4, 7 и 14 дней для Runx2 и OCN). (Фиг. 3В) C3H10T1/2 клетки обрабатывали разбавителем (контроль) или 2.5 мкМ Oxy133 в течение 3 недель. Для исследования внеклеточной минерализации проводили окрашивание по von Kossa, при этом минерализованный матрикс под световым микроскопом проявлялся в виде темного окрашивания (10Х). (Фиг. 3С) В параллельных культурах, описанных в (В), количественное определение минерализации осуществляли с помощью метода включения 45Са (р<0.005 для контроля против всех концентраций Oxy133). (Фиг. 3D) Первичные человеческие MSC обрабатывали в остеогенной среде разбавителем (контроль) или 5 мкМ Oxy133 в течение 4 недель. Экспрессия остеогенных генов OSX, BSP и OCN была измерена с помощью ПЦР в режиме реального времени. Результаты типичного эксперимента представлены в виде среднего из трех определений ±SD (р<0.05 для всех генов в контроле в сравнении с клетками, обработанными Oxy133). (Фиг. 3E) Первичные человеческие MSC обрабатывали в остеогенной среде с разбавителем (контроль) или 0.5, 1 и 5 мкМ Oxy133 в течение 5 недель. Для исследования внеклеточной минерализации проводили окрашивание по von Kossa, при этом минерализованный матрикс под световым микроскопом проявлялся в виде темного окрашивания (10Х).
Фигура 4 показывает роль сигнального пути Hedgehog в остеогенной дифференцировке, вызванной Oxy133. (Фиг. 4А) C3H10T1/2 клетки на этапе слияния обрабатывали в остеогенной среде разбавителем (контроль) или Oxy133 в присутствии или при отсутствии 4 мкМ циклопамина (Сус). Через 4 дня измеряли активность ALP и через 7 дней - экспрессию остеогенных генов ALP, BSP и OSX с помощью количественной ПЦР в режиме реального времени PCR (р<0.001 для контроля в сравнении с Oxy133, и для Oxy133 в сравнении с Oxy133+Сус в отношении активности ALP и экспрессии всех показанных генов). (Фиг. 4В) C3H10T1/2 клетки трансфицировали контрольной плазмидой (pGL3b) или плазмидой, содержащей 8X-Gli люциферазный репортер, и обрабатывали разбавителем (контроль) или Oxy133, причем люциферазную активность определяли через 48 часов. Результаты типичного эксперимента представлены в виде среднего из трех определений ±SD. (р<0.001 для контроля в сравнении с Oxy133 при 100 нМ, 250 нМ и 1 мкМ Oxy133). (Фиг. 4С) Количество YFP-Smo, захваченного 20S-гранулами, или контрольными гранулами сравнили в образцах, не содержащих конкурент или содержащих 50 мкМ свободного стерола-конкурента (20S, Oxy133 или Oxy16). Захваченный гранулами YFP-Smo измеряли методом вестерн-блоттинга (сверху) и наносили на график (внизу) относительно количества, захваченного в реакции связывания при отсутствии конкурента.
Фигура 5 показывает простые рентгенограммы масс сращения, образованных под воздействием ВМР2 и Oxy133. Показаны изображения (Faxitron) двух характерных животных из указанных групп через 8 недель после операции. Стрелки-указатели показывают отсутствие костеобразования; стрелки показывают костеобразование. Группа I (Контроль); пространство между поперечными отростками без костеобразования. Группа II (ВМР2); внедрение костной массы и билатеральное сращение между L4-L5. Группа III (Oxy133-20 мг); внедрение костной массы и билатеральное сращение между L4-L5. Группа IV (Oxy133-2 мг); внедрение костной массы и билатеральное сращение между L4-L5 у животных, показавших индукцию сращения с помощью Oxy133.
Фигура 6 показывает микро-СТ масс сращения, образованных под воздействием ВМР2 и Oxy133. Показаны микро-СТ двух характерных животных из указанных групп. Стрелки-указатели показывают отсутствие костеобразования; стрелки показывают костеобразование. Группа I (Контроль); пространство между поперечными отростками без костеобразования. Группа II (ВМР2); образование мостика из костной массы в пространстве между поперечными отростками и билатеральное сращение между L4-L5. Группа III (Oxy133-20 мг); образование мостика из костной массы в пространстве между поперечными отростками и билатеральное сращение между L4-L5. Группа IV (Oxy133-2 мг); образование мостика из костной массы в пространстве между поперечными отростками и билатеральное сращение между L4-L5 у животных, показавших индукцию сращения с помощью Oxy133. Группа V (Oxy133-0.2 мг); крайняя справа стрелка показывает небольшое количество костеобразования из L5 поперечного отростка.
Фигура 7 показывает гистологическое исследование эффекта Oxy133 на спондилодез. (Фиг. 7А) Показаны фронтальные гистологические срезы двух отдельных типичных животных из каждой группы (10Х). В группе I (Контроль) не наблюдается значительного костеобразования пространстве между поперечными отростками (стрелки-указатели). В группе II (ВМР2) происходит образование костного мостика L4-L5 (стрелки) с явным доказательством образования массы сращения трабекулярной и кортикальной кости. Образцы, полученные от группы III (Oxy133-20 мг) и группы IV (Oxy133-2 мг), демонстрируют значительное костеобразование в пространстве между поперечными отростками (стрелки) с трабекулярным и кортикальным костеобразованием, сравнимым с костеобразованием, индуцированным ВМР2. (Фиг. 7B) Фронтальные гистологические срезы, полученные от двух животных в каждой из групп группа II (ВМР2) и группа III (Oxy133-20 мг), показывают значительное образование адипоцитов в массе сращения у животных, обработанных ВМР2, и существенно меньшее количество адипоцитов в массе сращения у животных, обработанных оксистеролом (стрелки, увеличение 20Х).
Раскрытие изобретения
Изобретатели обнаружили остеогенный оксистерол, Oxy133, который вполне пригоден для целого ряда применений в клинической практике, и описали его способность оказывать содействие остеогенной дифференцировке in vitro и спондилодезу на крысиной модели in vivo. Среди большого количества синтезированных и исследованных аналогов оксистерола особенно эффективным и легким для синтеза неожиданно оказался Oxy133. Oxy133 вызывал значительную экспрессию остеогенных маркеров Runx2, osterix (OSX), щелочной фосфатазы (ALP), костного сиалопротеина (BSP) и остеокальцина (OCN) в фибробластах эмбриона мыши C3H10T1/2. Индуцированная Oxy133 активация 8X-Gli люциферазного репортера, его прямое связывание с Smoothened рецептором и ингибирование индуцированных Oxy133 остеогенных эффектов ингибитором пути Hedgehog (Hh), циклопамином, продемонстрировали роль пути Hh в опосредовании остеогенных ответов на Oxy133. В дополнение к этому, Oxy133 вызывал экспрессию OSX, BSP и OCN и стимулировал сильную минерализацию в первичных человеческих мезенхимальных стволовых клетках. In vivo, билатеральный спондилодез у животных, обработанных Oxy133 в месте сращения, наблюдался на рентгенограмме только через 4 недели и был подтвержден оценкой «вручную», микро-СТ и гистологическим исследованием через 8 недель, при одинаковой эффективности с костным морфогенетическим белком-2 (ВМР2). Однако, в отличие от ВМР2, Oxy133 не вызывал липогенез в массе сращения и приводил к образованию плотной костной ткани, о чем свидетельствует более высокое отношение BV/TV и меньшее трабекулярное отделение (trabecular separation). Таким образом, Oxy133 является пригодным для лечения состояний, которые могут получить пользу от локальной стимуляции костеобразования, включая, например, спондилодез, перелом кости, применение для костной регенерации/тканевой инженерии, увеличение плотности кости в челюсти для зубных имплантатов, остеопороз или тому подобное.
Изобретатели также продемонстрировали, что Oxy133 ингибирует липогенез плюрипотентных MSC клеток. Таким образом, Oxy133 является пригодным для лечения таких состояний, как, например, образование ксантом, локализованное скопление жировых «подушек» и ожирение.
Преимущества Oxy133 включают, например, более легкий синтез и сокращение времени до сращения по сравнению с другими остеогенными оксистеролами, исследованными изобретателями. Oxy133 является низкомолекулярным остеогенным оксистеролом, который может выступать в качестве члена следующего поколения костных анаболических терапевтических средств, а также в качестве средства, подходящего для лечения целого ряда других состояний, включая заболевания, которые могут получить пользу от стимулирования активности пути Hh.
Одним аспектом изобретения является соединение, называемое Oxy133 и имеющее формулу
или его фармацевтически приемлемая соль или сольват.
Другим аспектом изобретения является биоактивная или фармацевтическая композиция, содержащая Oxy133 или его фармацевтически приемлемую соль или сольват и фармацевтически приемлемый носитель. Термины "биоактивная" композиция или "фармацевтическая" композиция используются в описании взаимозаменяемым образом. Оба термина относятся к композициям, которые могут вводиться субъектам, используются для нанесения на устройство или присутствуют в медицинском устройстве, которое вводится субъекту, или т.п. Эти биоактивные или фармацевтические композиции иногда в описании называются "фармацевтическими композициями или биоактивными композициями изобретения". Фраза "введение Oxy133" используется в описании в отношении введения этого соединения субъекту (например, контактирование субъекта с соединением). Следует понимать, что соединение, предназначенное для такого использования, в большинстве случаев может иметь форму фармацевтической композиции или биоактивной композиции, содержащей Oxy133.
Другим аспектом изобретения является способ индуцирования (стимулирования, активизации) ответа, опосредованного путем (Hh), в клетке или ткани, включающий контактирование клетки или ткани с эффективным количеством (например, терапевтически эффективным количеством) Oxy133. Клетка или ткань может быть клеткой или тканью в культуре in vitro или может принадлежать субъекту, такому как млекопитающее (например, человек). В вариантах осуществления изобретения ответ, опосредованный путем (Hh), представляет собой стимулирование остеобластической дифференцировки, остеоморфогенез, и/или остеопролиферацию; или ответ представляет собой стимулирование роста волос и/или образования хряща (например, способ лечения субъекта с алопецией или остеоартритом, соответственно, включающий введение субъекту эффективного количества биологически активной композиции изобретения); или ответ представляет собой стимулирование неоваскулогенеза, например, ангиогенеза, и таким образом увеличение доставки крови к ишемическим тканям (например, способ лечения субъекта с сердечнососудистым заболеванием, артериосклерозом, инфарктом миокарда, стенокардией, болезнью периферических сосудов и/или инсультом, включающий введение субъекту эффективного количества биологически активной композиции изобретения); или ответ представляет собой ингибирование дифференцировки адипоцитов, морфогенеза адипоцитов и/или пролиферации адипоцитов (например, способ лечения субъекта, у которого наблюдается образование ксантом, локализованное скопление жировых «подушек» и/или ожирение, включающий введение субъекту эффективного количества биологически активной композиции изобретения); или ответ представляет собой стимуляцию клеток-предшественников с целью прохождения нейрогенеза (дифференцировки нейронов) (например, способ лечения субъекта с неврологической болезнью). Hh-опосредованный ответ может включать регенерацию любого из целого ряда типов тканей для использования в регенеративной медицине.
Другим аспектом изобретения является способ лечения субъекта с заболеванием костей, остеопенией, остеопорозом или переломом кости, включающий введение субъекту эффективного количества биоактивной композиции или фармацевтической композиции, содержащей Oxy133. Биоактивная композиция или фармацевтическая композиция может вводиться субъекту в терапевтически эффективной дозе в эффективной лекарственной форме с подобранным интервалом, например, с целью увеличения костной массы, улучшения симптомов остеопороза, уменьшения, устранения, предотвращения или лечения атеросклеротических повреждений или тому подобного. Биоактивная композиция или фармацевтическая композиция может вводиться субъекту в терапевтически эффективной дозе в эффективной лекарственной форме с подобранным интервалом с целью улучшения симптомов остеопороза. В одном варианте осуществления субъект подвергается лечению с целью стимулирования костеобразования путем сбора мезенхимальных стволовых клеток млекопитающего (например, от субъекта или от подходящего млекопитающего, или из ткани или банка клеток), обработки мезенхимальных клеток млекопитающего Oxy133 с целью вызвать остеобластическую дифференцировку клеток и введения дифференцированных клеток субъекту.
В любом из способов изобретения Oxy133 может быть введен в клетку, ткань или орган с помощью местного введения. Например, Oxy133 может применяться местно в виде крема или тому подобного, или он может быть введен (впрыснут) непосредственно в клетку, ткань или орган, или он может быть помещен в подходящее медицинское устройство (например, имплантат).
Другим аспектом изобретения является набор, предназначенный для осуществления одного или более описанных здесь способов. Набор может содержать эффективное количество (например, терапевтически эффективное количество) Oxy133, необязательно в контейнере.
Другим аспектом изобретения является имплантат, предназначенный для использования в организме субъекта (например, животного, такого как человек), содержащий имеющий поверхность субстрат. Поверхность или внутренняя сторона имплантата содержит биоактивную композицию или фармацевтическую композицию, включающую Oxy133 в количестве, достаточном для того, чтобы вызвать костеобразование в окружающей костной ткани.
В некоторых случаях биоактивная композиция, способ, набор или медицинское устройство изобретения может содержать одно или более других подходящих терапевтических средств, например, таких как паратиреоидный гормон, фторид натрия, инсулиноподобный фактор роста I (ILGF-I), инсулиноподобный фактор роста II (ILGF-II), трансформирующий ростовой фактор бета (TGF-β), ингибитор цитохрома Р450, остеогенный простаноид, BMP 2, BMP 4, BMP 7 и/или BMP 14.
Oxy133 имеет структуру
Химическое название данной структуры - (3S,5S,6S,8R,9S,10R,13S,14S,17S) 17-((S)-2-гидроксиоктан-2-ил)-10,13-диметилгексадекагидро-1Н-циклопента[а]фенантрен-3,6-диол.
Пример II описывает дизайн Oxy133 и метод синтеза данной молекулы.
В дополнение к соединению Oxy133 формулы I, другие варианты осуществления изобретения включают любые возможные отдельные стереоизомеры с любым из представленных формулой стереоцентров, включая диастереомеры, рацематы, энантиомеры и другие изомеры соединения. В некоторых вариантах осуществления изобретения "Oxy133" или "соединение, имеющее формулу I" или "Oxy133 или его фармацевтически приемлемая соль" может включать все полиморфы и сольваты соединения, например, образованные органическими растворителями, и гидраты. "Сольват" представляет собой комплекс или агрегат, образованный одной или более молекулами растворенного вещества, например, соединения или его фармацевтически приемлемой соли, и одной или более молекулами растворителя. Такие сольваты могут быть кристаллическими твердыми веществами, имеющими практически постоянное молярное отношение растворенного вещества и растворителя. Подходящие растворители известны специалистам в данной области техники, например, вода, этанол. Такие изомеры, полиморфы и сольваты можно получить с помощью известных в данной области методов, таких как региоспецифический и/или энантиоселективный синтез и разделение.
Пригодность для получения солей зависит от кислотности и основности соединения. Подходящие соли соединения включают, но не ограничиваются этим, соли присоединения кислоты, такие как соли, полученные при использовании хлористоводородной, бромистоводородной, йодистоводородной, хлорной, серной, азотной, фосфорной, уксусной, пропионовой, гликолевой, молочной, пировиноградной, малоновой, янтарной, малеиновой, фумаровой, яблочной, винной, лимонной, бензойной, угольной, коричной, миндальной, метансульфоновой, этансульфоновой, гидроксиэтансульфоновой, бензолсульфоновой, п-толуолсульфоновой, циклогексансульфаминовой, салициловой, п-аминосалициловой, 2-феноксибензойной и 2-ацетоксибензойной кислоты; соли, полученные при использовании сахарина; соли щелочных металлов, такие как соли натрия и калия; соли щелочно-земельных металлов, такие как соли кальция и магния; и соли, образованные с помощью органических или неорганических лигандов, таких как четвертичные аммониевые соли.
Дополнительные подходящие соли включают, но не ограничиваются этим, такие соли соединений, как ацетат, бензолсульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, эдетат кальция, камсилат, карбонат, хлорид, клавуланат, цитрат, дигидрохлорид, эдетат, эдизилат, эстолат, эзилат, фумарат, глюцептат, глюконат, глутамат, гликолиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, иодид, изотионат, лактат, лактобионат, лаурат, манат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, N-метилглюкамин аммонийная соль, олеат, памоат (эмбонат), пальмитат, пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, сульфат, субацетат, сукцинат, таннат, тартрат, теоклат, тозилат, триетиодид и валерат.
Понятно, что ссылки в описании на "Oxy133" включают его фармацевтически приемлемые соли или сольваты.
В любых из способов, композиций или наборов изобретения, в частности при использовании для лечения субъекта, композиция изобретения необязательно может предоставляться в сочетании с одним или более другими подходящими терапевтическими средствами. Может использоваться любое подходящее для лечения конкретного заболевания терапевтическое средство. Такие подходящие средства или лекарственные препараты известны специалисту в данной области техники. Например, для лечения заболеваний костей общепринятые терапевтические средства могут использоваться в комбинации с композицией изобретения. Некоторые такие средства включают, например, паратиреоидный гормон, фторид натрия, инсулиноподобный фактор роста I (ILGF-I), инсулиноподобный фактор роста II (ILGF-II), трансформирующий ростовой фактор бета (TGF-β), ингибитор цитохрома Р450, остеогенный простаноид, BMP 2, BMP 4, BMP 7 и/или BMP 14. Для лечения сердечнососудистого заболевания или нарушения липидного обмена может использоваться статин или средство для лечения кровяного давления в комбинации с композицией изобретения.
Композиция или соединение изобретения может быть создано в виде фармацевтической композиции, содержащей композицию изобретения и фармацевтически приемлемый носитель. "Фармацевтически приемлемый носитель" подразумевает вещество, которое не является биологически или другим образом нежелательным, т.е., данное вещество может быть введено субъекту и не вызовет каких-либо нежелательных биологических эффектов или не будет взаимодействовать вредоносным образом с каким-либо из других компонентов фармацевтической композиции, в которой оно содержится. Разумеется, носитель выбирают так, чтобы свести к минимуму любого рода деградацию активного ингредиента и любые вредные побочные эффекты у субъекта, что хорошо известно специалисту в данной области техники. Обсуждение фармацевтически приемлемых носителей и других компонентов фармацевтических композиций, смотри, например, в Remington’s Pharmaceutical Sciences, 18th ed., Mack Publishing Company, 1990. Некоторые подходящие фармацевтические носители известны квалифицированным специалистам и включают, например, воду (включая стерильную и/или деионизированную воду), подходящие буферы (такие как PBS), физиологический раствор, среду для культуры клеток (такую как DMEM), искусственную спинномозговую жидкость, диметилсульфоксид (DMSO), этанол и тому подобное.
Специалисту понятно, что конкретный состав изобретения будет зависеть, по меньшей мере, частично, от конкретного используемого средства или комбинации используемых средств и выбранного способа введения. Соответственно, существует большое разнообразие подходящих составов композиций настоящего изобретения. Некоторые типичные составы обсуждаются ниже. Другие будут очевидны для квалифицированного специалиста. В общем, Oxy133 вводится локально или непосредственно в клетку, ткань или орган, нуждающийся в лечении. Также может использоваться системное введение, если при этом достигаются желательные результаты в ткани или органе, нуждающемся в лечении.
Составы или композиции, подходящие для перорального введения, могут иметь вид жидких растворов, например, эффективное количество Oxy149 может быть растворено в разбавителях, таких как вода, физиологический раствор или фруктовый сок; могут иметь вид капсул, саше или таблеток, содержащих заранее установленное количество активного ингредиента в виде твердого вещества, гранул или лиофилизированных клеток; могут иметь вид растворов или суспензий в водосодержащей жидкости; и могут иметь вид эмульсий масло-в-воде или вода-в-масле. Таблетированные формы могут включать одно или более из числа лактозы, маннитола, кукурузного крахмала, картофельного крахмала, микрокристаллической целлюлозы, гуммиарабика, желатина, коллоидного диоксида кремния, кросскармеллозы натрия, талька, стеарата магния, стеариновой кислоты и других эксципиентов, красящих веществ, разбавителей, буферных веществ, увлажняющих веществ, консервирующих веществ, вкусовых веществ и фармацевтически совместимых носителей. Кроме того, подходящие для пероральной доставки композиции могут заключаться в микросферы из синтетических или природных материалов, или могут использоваться другие способы для защиты средств настоящего изобретения от разрушения в желудочно-кишечном тракте.
Подходящие для парентерального введения композиции (например, внутривенного) включают водосодержащие и безводные, изотонические стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостатические средства и растворенные вещества, приводящие композицию в изотоническое с кровью предполагаемого реципиента состояние, и водные и неводные стерильные суспензии, которые могут включать суспендирующие вещества, солюбилизаторы, загустители, стабилизирующие вещества и консервирующие вещества. Композиции могут помещаться в однодозовые и многодозовые контейнеры, такие как ампулы и флаконы, и могут храниться в высушенном сублимацией (т.е., лиофилизированном) состоянии, при этом для выполнения инъекции требуется только добавление стерильного жидкого носителя, например, воды, непосредственно перед применением. Растворы и суспензии для экстемпорального приготовления могут быть приготовлены из стерильных порошков, гранул или таблеток, описанных ранее.
Oxy133, отдельно или в комбинации с другими терапевтическими средствами, может входить в состав аэрозольных композиций, предназначенных для введения путем ингаляции. Эти аэрозольные составы могут быть помещены в находящиеся под давлением приемлемые пропелленты (распыляющие вещества), такие как дихлордифторметан, пропан, азот и т.п. Подходящие для местного введения композиции включают леденцы, содержащие активный ингредиент в ароматизирующем веществе, обычно сахарозе и гуммиарабике или трагакантовой камеди; пастилки, содержащие активный ингредиент в инертной основе, такой как желатин и глицерин, или сахароза и гуммиарабик; жидкости для полоскания рта, содержащие активный ингредиент в подходящем жидком носителе; или кремы, эмульсии, суспензии, растворы, гели, пасты, пены, смазки, спреи, суппозитории или тому подобное.
Другие подходящие композиции включают, например, гидрогели и полимеры, пригодные для регулируемого по времени высвобождения Oxy133, или наночастицы для доставки Oxy133 в низких дозах. Такие композиции хорошо известны специалистам в данной области техники.
Специалистам понятно, что подходящая или соответствующая композиция может быть выбрана, приспособлена или создана с учетом конкретного рассматриваемого применения. Кроме того, фармацевтические композиции настоящего изобретения могут быть приготовлены для введения с помощью целого ряда различных способов. Примеры локального или прямого введения включают, но не ограничиваются этим, внутрисуставное, внутричерепное, внутрикожное, внутрипеченочное, внутримышечное, внутриглазное, внутрибрюшинное, подоболочечное, внутривенное, подкожное, чрескожное введение или введение непосредственно в атеросклеротический участок кости, например, с помощью прямой инъекции, введение с помощью катетера или другого медицинского устройства, местное применение, направленное применение и/или введение путем имплантации устройства в артерию или другое место нужной ткани.
Oxy133 может быть заключен в состав или приспособлен для высвобождения хирургическим или медицинским устройством или имплантатом. В некоторых аспектах имплантат может быть покрыт или иным образом обработан Oxy133. Например, гидрогели или другие полимеры, такие как биосовместимые и/или биодеградируемые полимеры, могут использоваться для покрытия имплантата композициями настоящего изобретения (т.е. композиция может быть приспособлена для применения с помощью медицинского устройства с использованием гидрогеля или другого полимера). Полимеры и сополимеры, пригодные для нанесения средства на медицинское устройство, хорошо известны в данной области техники. Примеры имплантатов включают, но не ограничиваются этим, баллоны для ангиопластики, стенты, стенты с лекарственным покрытием, шовный материал, протезы, сосудистые катетеры, диализные катетеры, сосудистые трансплантаты, трансплантаты кости, искусственные клапаны сердца, электрокардиостимуляторы, имплантируемые кардиовертер-дефибрилляторы или IV иглы. Только в качестве примера, стент или стент-графт в большинстве случаев может включать участок стента из гибкого трубчатого материала, который обычно используется для укрепления или усиления слабого места во внутренних каналах организма, таких как кровеносный сосуд. Вставка стент-графта может осуществляться с помощью катетера. Размещение может облегчаться путем расширения с помощью баллона, например, во время или после процедуры баллонной ангиопластики, или альтернативно стент-графт может быть саморасправляющимся.
"Эффективное количество" Oxy133, при использовании в описании, относится к количеству, которое может вызывать, по меньшей мере, обнаружимый эффект. Использованный в описании термин "терапевтически эффективное количество" относится к количеству, которое может вызывать, по меньшей мере, обнаружимый терапевтический ответ у субъекта, подвергающегося лечению (например, улучшение одного или более симптомов) в течение целесообразного периода времени.
В вариантах осуществления изобретения Oxy133 может стимулировать или ингибировать терапевтический ответ, измеренный любым из целого ряда способов, примерно на 1%, 5%, 10%, 20%, 30%, 40%, 50% 150%, 200% или более по сравнению с контрольным необработанным образцом. Также включаются промежуточные значения этих пределов.
Дозировки Oxy133 могут содержаться в стандартных лекарственных формах, таких как таблетка или капсула. Использованный в описании термин "стандартная лекарственная форма" относится к физически раздельным единицам, подходящим в качестве однократных дозировок для субъектов (например, человека), при этом каждая единица содержит заранее установленное количество средства изобретения, отдельно или в комбинации с другими терапевтическими средствами, в количестве, достаточном для получения желательного эффекта, в сочетании с фармацевтически приемлемым разбавителем, носителем или средой.
Специалист в данной области может обычным путем определить подходящую дозу, режим и способ введения используемой композиции, имеющей определенный состав, для того, чтобы получить желательное эффективное количество или эффективную концентрацию средства у конкретного пациента. Специалист также может легко определить и использовать подходящий показатель "эффективной концентрации" соединений, например, Oxy133, полученный путем прямого или непрямого анализа соответствующего образца пациента (например, крови и/или тканей), в дополнение к анализу соответствующих клинических симптомов болезни, нарушения или состояния.
Точная доза Oxy133 или его композиции, которая вводится животному, например, человеку, в контексте настоящего изобретения будет варьировать в зависимости от вида, возраста, веса и общего состояния субъекта, тяжести или механизма нарушения, которое необходимо лечить, конкретного используемого средства или среды для лекарства, способа введения, применения дополнительной медикаментозной терапии и других факторов, обычно рассматриваемых лечащим врачом при установлении индивидуального режима и подходящего уровня дозировки для конкретного пациента, и тому подобного. Дозировка, используемая для получения желательной концентрации in vivo, будет определяться действенностью формы Oxy133, фармакодинамикой, связанной с Oxy133 у хозяина, наличием или отсутствием дополнительных средств, тяжестью болезненного состояния инфицированных индивидуумов, а также, в случае системного введения, весом тела и возрастом индивидуума. Величина дозировки также может определяться наличием каких-либо вредных побочных действий, которые могут сопутствовать конкретному используемому средству или его композиции. В общем, при наличии возможности, желательно удерживать вредные побочные действия на минимальном уровне.
Например, может быть введена доза в пределах примерно от 5 нг (нанограмм) до 1000 мг (миллиграмм), или примерно от 100 нг до 600 мг, или примерно от 1 мг до 500 мг, или примерно от 20 мг до 400 мг. Например, может быть выбрана доза для получения отношения по весу тела примерно от 0,0001 мг/кг до 1500 мг/кг, или примерно от 1 мг/кг до 1000 мг/кг, или примерно от 5 мг/кг до 150 мг/кг, или примерно от 20 мг/кг до 100 мг/кг. Например, единица дозирования может находиться в пределах примерно от 1 нг до 5000 мг, или примерно от 5 нг до 1000 мг, или примерно от 100 нг до 600 мг, или примерно от 1 мг до 500 мг, или примерно от 20 мг до 400 мг, или примерно от 40 мг до 200 мг Oxy133 или композиции, содержащей Oxy133. В одном варианте осуществления изобретения указанные выше количества Oxy133 (например, несколько грамм) вводятся локально, например, как в процедуре спондилодеза в качестве ча