Гидрогель для получения композиционных материалов с антибактериальной активностью для замещения костно-хрящевых дефектов методом 3d печати
Иллюстрации
Показать всеИзобретение относится к области медицины. Описан гидрогель, содержащий масс. %: альгинат натрия - 40-90; кальцийфосфатные наполнители - 10-60, полученный гидрогель охлаждают до t +37°C и при непрерывном перемешивании на оборотах от 500 до 1000 об/мин добавляют порошок ванкомицина в концентрациях 30, 50 и 70 масс. % по отношению к общей массе образца. При этом размеры частиц порошка или гранул изменяются от 20 до 100 мкм. Изготовленный каркас на основе гидрогеля обладает функциональными свойствами с антибактериальной активностью, что позволит заполнить костно-хрящевые дефекты различной формы и размера и восстановить их структуры и функции, а также снизить или полностью избежать частоту инфекционных осложнений. 4 ил., 5 табл.
Реферат
Изобретение относится к области медицины, а именно к разработке материалов, пригодных для 3D печати, и может быть использовано для получения персонализированных биомедицинских изделий на основе гидрогелей, содержащих альгинат натрия, фосфаты кальция (ФК) и антибактериальный агент – ванкомицин, для реконструктивно-восстановительной хирургии поврежденных костно-хрящевых тканей с целью снижения вероятности инфекционных осложнений.
Создание персонализированных биомедицинских изделий, предназначенных для регенерации утраченных тканей - восстановления их структуры и функций - является одной из важнейших и актуальных задач практической реконструктивно-восстановительной хирургии. В последние годы наибольших успехов в решении этой проблемы удалось достичь с помощью аддитивных технологий (3D печати), основанных на послойном синтезе твердых копий трехмерных компьютерных образов реальных объектов [Giannatsis J., Dedoussis V. Additive fabrication technologies applied to medicine and healthcare: areview. Int. J. Adv. Manuf. Technol., 2009, V. 40, P. 116-127]. При условии подбора полимера с требуемыми (для 3D печати) характеристиками возможно формирование с его участием пористых композиционных структур с соединениями кальция и антибактериальными агентами для замещения дефектов костно-хрящевой ткани с уменьшением вероятности инфекционных осложнений, частота которых достаточно высока, а сложности в их лечении общеизвестны. В этом аспекте особый интерес представляет биополимер альгинат, который характеризуется биосовместимостью и может выполнять каркасную функцию. В свою очередь материалы на основе ФК являются аналогами минеральной составляющей костной ткани и широко используются для изготовления остеопластических материалов и керамических матриксов для клеточных технологий [Dorozhkin S.V. Calcium orthophosphate - based bioceramics. Materials 2013, V. 6, P. 3840-2942]. Сочетание свойств минерал-полимерных систем на основе подхода 3D печати будет являться основой создания материалов с функциональными свойствами для замещения костно-хрящевых дефектов и как контейнеров для локальной доставки в область операционной раны антибактериального агента, что позволит снизить частоту инфекционных осложнений.
Известен способ формирования биологически совместимых материалов для регенерации тканей (US 20150039097 А1). Способ включает послойное нанесение полимерных слоев, из которых образуется изделие. В качестве полимеров используется полиуретан, полилактид, полигликолид, поли(е-капролактон), полидиоксанон, полиангидрид, триметиленкарбонат, поли(β-гидроксибутират), поли(г-этил глутамат), полицианоакрилат, полифосфазен, или их смеси. Раствор полимера наполняют частицами гидроксиапатита (ГА), трикальцийфосфата (ТКФ), композиционными ФК и карбоната кальция (КК), костными частицами из ксенографтов, костными частицами из аллотрансплантатов, костными частицами из аутотрансплантатов или их смеси. Способ получения биологически совместимых материалов включает формирование заданного количества слоев.
Однако известный способ, в отличие от заявляемого, не подразумевает использование альгината натрия в качестве каркаса, а армирующая составляющая включает в себя костные частицы, наночастицы ГА или полимерные нановолокна.
Наиболее близким по техническому решению является композиционный трехмерный каркас на основе альгината натрия и фосфатов кальция для замещения костно-хрящевых дефектов (RU 2015144535 А). В заявке описан способ получения композиционного трехмерного каркаса для замещения костно-хрящевых дефектов, включающий приготовление текучего гидрогеля, содержащего альгинат натрия и КФ наполнитель, нанесение гидрогеля на платформу, формирование трехмерного каркаса с последующей фиксацией структуры, при этом трехмерный каркас формируют методом 3D инъекционной печати послойным нанесением гидрогеля с фиксацией структуры на платформе, охлажденной до температуры -5±1°C до -30±1°C в процессе нанесения, при этом текучий гидрогель содержит, масс. %: альгината натрия - 40-90; наполнителя - 10-60. В качестве наполнителя в текучий гидрогель вводят порошки или гранулы ТКФ, брушита, монетита, октакальциевого фосфата, тетракальцийфосфата, гидроксиапатита, карбонатгидроксиапатита (КГА), фторгидроксиапатита или их другие модификации, при этом размеры частиц порошка или гранул изменяются от 20 до 500 мкм, а указанные наполнители могут быть смешаны в любом сочетании и в любом количестве между собой. Для получения трехмерного каркаса с пористостью от 40 до 95% по завершении печати каркас помещают в морозильную камеру и выдерживают в течение 1 ч при температуре -50°C, затем подвергают сублимационной сушке в рабочей камере при вакууме 6⋅10-5 атм, при температуре конденсирующей поверхности -50°C в течение 10-12 ч. Высушенный каркас сшивают 10% раствором хлорида кальция в шейкере-инкубаторе на протяжение 2 ч, далее полученный трехмерный каркас отмывают от остатка солей и вновь подвергают сублимационной сушке для сохранения структуры.
Полученный по известному способу композиционный материал - трехмерный каркас, не обладает антибактериальным свойством - при его использовании необходимы дополнительные процедуры и время по доставке антибактериального агента в область операционный раны.
Технический результат предлагаемого изобретения - получение композиционного трехмерного материала методом 3D инъекционной печати, обладающего функциональными свойствами с антибактериальной активностью для регенерации утраченных тканей - восстановления их структуры и функций.
Согласно изобретению, для достижения технического результата используется 3D инъекционная печать композиционных материалов на основе альгината натрия, ФК и ванкомицина по заданной программе, что обеспечивает требуемые геометрические и структурные характеристики композиционного материала.
Указанный технический результат при осуществлении изобретения достигается за счет того, что также как в известных технических решениях US 20150039097 и заявке на патент RU 2015144535, каркас получают из текучего гидрогеля, содержащего масс. %: альгинат натрия - 40-90 и кальцийфосфатные наполнители - 10-60: трикальцийфосфат, брушит, монетит, октакальцийфосфат, тетракальцийфосфат, гидроксиапатит, карбонатгидроксиапатит, фторгидроксиапатит или их смеси в виде порошков или гранул.
Особенность заявляемого изобретения заключается в том, что размеры частиц порошка или гранул изменяются от 20 до 100 мкм, далее полученный гидрогель охлаждают до t +37°С и при непрерывном перемешивании от 500 до 1000 об/мин добавляют порошок ванкомицина в концентрациях 30, 50 и 70 масс. % по отношению к общей массе образца, далее методом 3D печати из композиционных материалов получают образцы, обладающие антибактериальной активностью.
Изобретение поясняется подробным описанием способа, таблицами и иллюстрациями, на которых изображено:
Фиг. 1 - образец композиционного материала без наполнителя - ванкомицина.
Фиг. 2 - образец композиционного материала с ванкомицином; содержание ванкомицина в текучем гидрогеле составляет 30 масс. % по отношению к сухой общей массе образца на этапе его формирования.
Фиг. 3 - образец композиционного материала с ванкомицином; содержание ванкомицина в текучем гидрогели 50 масс. % по отношению к сухой общей массе образца на этапе его формирования.
Фиг. 4 - образец композиционного материала с ванкомицином; содержание ванкомицина в текучем гидрогели 70 масс. % по отношению к сухой общей массе образца на этапе его формирования.
Способ осуществляют следующим образом.
В сухой чистый стакан заливается дистиллированная вода, которая перемешивается стеклянной верхнеприводной мешалкой на высоких оборотах (от 2500 до 3000 об/мин) и нагревается до температуры 40°C, после чего в жидкую среду помещается порошок альгината натрия. После полного растворения альгината натрия при перемешивании добавляют кальцийфосфатный наполнитель в количестве до 60 масс. %. В качестве наполнителя вводят порошки или гранулы трикальцийфосфата, брушита, монетита, октакальцийфосфата, тетракальцийфосфат, гидроксиапатит, карбонатгидроксиапатит, фторгидроксиапатита или их другие модификации, при этом размеры частиц порошка или гранул изменяются от 20 до 100 мкм, а указанные наполнители могут быть смешаны в любом сочетании и в любом количестве между собой. Затем полученный гидрогель охлаждается до t +37°C и при непрерывном перемешивании стеклянной верхнеприводной мешалкой на оборотах от 500 до 1000 об/мин добавляют порошок ванкомицина в концентрациях 30, 50 и 70 масс. % по отношению к общей массе образца.
Методом 3D инъекционной печати из композиционных материалов получают образцы, соответствующие по форме и размерам костно-хрящевому дефекту. С целью получения этих данных о дефекте могут использоваться методы лучевой диагностики, такие как компьютерная томография, рентгенография и др. Полученную компьютерную модель дефекта преобразуют в файлы STL формата, разбивающие ее на слои определенной толщины, соответствующие характеристикам используемых исходных материалов. Программа, содержащая необходимый набор STL файлов, вводится в компьютер, управляющий 3D-принтером. Приготовленный гидрогель загружают в картридж 3D-принтера, и по заданной программе (модели) осуществляется послойное нанесение геля на платформу для печати, ступенчато охлаждаемую для фиксации трехмерного каркаса от -5±1°C до -30±1°C, в зависимости от количества наносимых слоев. После завершения процесса печати полученный трехмерный каркас извлекают из установки и помещают в морозильную камеру с температурой -50°C, время выдержки - 1 час. Далее трехмерный каркас подвергают сублимационной сушке в рабочей камере при вакууме 6⋅10-5 атм, при температуре конденсирующей поверхности -50°C в течение 10-12 часов. Высушенный трехмерный каркас сшивают 10% раствором хлорида кальция в шейкере-инкубаторе на протяжении 2 часов (трехмерный каркас/раствор = 100 г/80 мл). Полученный трехмерный каркас отмывают от остатка солей и вновь подвергают сублимационной сушке для сохранения структуры. В результате получают композиционный трехмерный каркас с пористостью от 40 до 95% в зависимости от состава.
При содержании ФК наполнителя больше 60 масс. % реализация 3D печати невозможна. Снижение содержания наполнителя до 5 масс. % и менее не позволяет получать трехмерный каркас с равномерным распределением компонентов по объему. При температуре заморозки менее -5±1°C фиксации заданной структуры не происходит, а при температуре менее -30°C материал замерзает в сопле принтера, что не дает возможности реализовать процесс печати. Добавка ванкомицина в диапазон 30-70 масс. % по отношению к общей массе образца не влияет на процесс печати.
Пример 1
Изготовление прототипа.
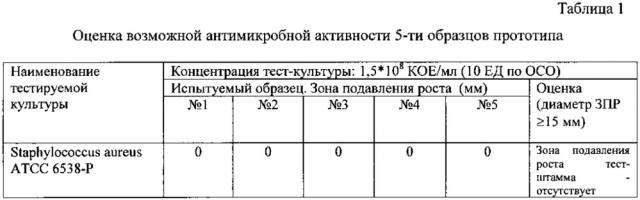
Готовый гидрогель альгината натрия с гранулами трикальцийфосфата 20-100 мкм (соотношение 70/30) поместили в картридж для печати 3D принтера. После чего данным гидрогелем осуществили печать трехмерного каркаса по заданной траектории на платформу для печати, которая охлаждается элементами Пельтье с градиентным изменением температуры послойно -5±1°C до -30±1°C, в зоне (слое) печати температура -5±1°C. За счет охлаждения платформы произошла кристаллизация воды, которая находиться в гидрогеле, таким образом была осуществлена фиксация структуры напечатанного образца трехмерной конструкции. Полученный трехмерный каркас извлекли из установки и поместили в морозильную камеру с температурой -50°C, время выдержки - 1 час. Далее образец подвергали сублимационной сушке при -50°C в течение 10-12 часов. Пористость материала - 90%, прочность - 5,5 МПа (Фиг. 1). В таблице 1 представлены данные по образцу (Фиг. 1) без наполнителя - ванкомицина.
Пример 2
В готовом гидрогеле альгината натрия с гранулами ТКФ 20-100 мкм (соотношение 70/30) растворили 30 масс. % порошка ванкомицина (по отношению к общей массе образца) и полученный композиционный материал поместили в картридж для печати 3D принтера. После чего, данным гелем осуществили печать образца по заданной траектории на подложку, которая охлаждается элементами Пельтье с температурой -5±1°C до -30±1°C, в зоне (слое) печати температура -5±1°C. За счет охлаждения подложки, произошла кристаллизация воды, которая находиться в гидрогеле, таким образом осуществлена фиксация структуры напечатанного образца. Далее заготовки подвергали сублимационной сушке -50°C в течение 10-12 часов. Пористость материалов достигает 88% и прочность - 5,3 Мпа (Фиг. 2). В таблице 2 представлены данные по изготовленному образцу, где содержание ванкомицина в текучем гидрогеле составляет 30 масс. % по отношению к сухой общей массе образца на этапе его формирования.
Пример 3
В готовом гидрогеле альгината натрия с гранулами ТКФ 20-100 мкм (соотношение 70/30) при 37°C растворили 50 масс. % (по отношению к общей массе образца) порошка ванкомицина и полученный композиционный материал поместили в картридж для печати 3D принтера. После чего данным гелем осуществили печать образца по заданной траектории на подложку, которая охлаждается элементами Пельтье с температурой -5±1°C до -30±1°C, в зоне (слое) печати температура -5±1°C. За счет охлаждения подложки произошла кристаллизация воды, которая находиться в гидрогеле, таким образом осуществлена фиксация структуры напечатанного образца. Далее заготовки подвергали сублимационной сушке -50°C в течение 10-12 часов. Пористость материалов достигает 95% и прочность - 4,4 МПа (Фиг. 3). В таблице 3 представлены данные по изготовленному образцу, где содержание ванкомицина в текучем гидрогеле составляет 50 масс. % по отношению к сухой общей массе образца на этапе его формирования.
Пример 4
В готовом гидрогеле альгината натрия с гранулами ТКФ 20-100 мкм (соотношение 70/30) растворили 70 масс. % (по отношению к общей массе образца) порошка ванкомицина и полученный композиционный материал поместили в картридж для печати 3D принтера. После чего данным гелем осуществили печать образца по заданной траектории на подложку, которая охлаждается элементами Пельтье с температурой -5±1°C до -30±1°C, в зоне (слое) печати температура -5±1°C. За счет охлаждения подложки произошла кристаллизация воды, которая находиться в гидрогеле, таким образом осуществлена фиксация структуры напечатанного образца. Далее заготовки подвергали сублимационной сушке -50°C в течение 10-12 часов. Пористость материалов достигает 95% и прочность - 3,7 МПа (Фиг. 4). Диаметр светлого кольца вокруг образца керамики соответствует области, в которой отсутствует (погибла) культура Staphylococcus aureus АТСС 6538-Р: чем больше диаметр светлого кольца, тем больше проявляются антибактериальные свойства. В таблице 4 представлены данные по изготовленному образцу, где содержание ванкомицина в текучем гидрогеле составляет 70 масс. % по отношению к сухой общей массе образца на этапе его формирования.
Полученный трехмерный каркас предложенного состава имеет высокую пластичность полимера, а в сочетании с заданной архитектурой и пористостью позволяет заполнять костно-хрящевые дефекты различной формы и размера.
В соответствии с примерами были определены их свойства в сравнении с прототипом (Таблица 5).
Изготовленный каркас на основе гидрогеля обладает функциональными свойствами с антибактериальной активностью, что позволит заполнить костно-хрящевые дефекты различной формы и размера и восстановить их структуры и функции, а также снизить или полностью избежать частоту инфекционных осложнений.
Гидрогель для получения композиционных материалов с антибактериальной активностью для замещения костно-хрящевых дефектов методом 3D печати, содержащий масс. %: альгинат натрия - 40-90 и кальцийфосфатные наполнители - 10-60: трикальцийфосфат, брушит, монетит, октакальцийфосфат, тетракальцийфосфат, гидроксиапатит, карбонатгидроксиапатит, фторгидроксиапатит или их смеси в виде порошков или гранул, отличающийся тем, что размеры частиц порошка или гранул изменяются от 20 до 100 мкм, далее полученный гидрогель охлаждают до t +37°С и при непрерывном перемешивании от 500 до 1000 оборотах в минуту добавляют порошок ванкомицина в концентрациях 30, 50 и 70 масс. % по отношению к общей массе образца, далее методом 3D печати из композиционных материалов получают образцы, обладающие антибактериальной активностью.