Дейтерированные диаминопиримидиновые соединения и фармацевтические композиции, содержащие такие соединения
Иллюстрации
Показать всеНастоящее изобретение относится к новым дейтерированным диаминопиримидинам общей формулы (I) и их фармацевтически приемлемым солям. Соединения обладают свойствами ингибирования ALK протеинкиназ и могут быть использованы для лечения и/или предупреждения онкологических заболеваний, нарушения пролиферации клеток, сердечнососудистых заболеваний, воспаления, инфекции, аутоиммунных заболеваний, трансплантации органов, вирусных заболеваний, сердечнососудистых заболеваний или метаболических заболеваний. В общей формуле (I)
R1a, R1b, R1c, R2a, R2b, R2c, R3, R4, R6, R7, R9, R10, R11, R12, R13a, R13b, R13c, R14a, R14b, R14c, R15a, R15b, R15c, R16, R17a, R17b, R18a, R18b, R19a, R19b, R20a и R20b независимо представляют собой водород или дейтерий; R5 представляет собой водород, дейтерий или галоген, R8 представляет собой галоген; при условии, что по меньшей мере четыре из R1a, R1b, R1c, R2a, R2b, R2c, R3, R12, R13a, R13b, R13c, R14a, R14b, R14c, R19a, R19b, R20a или R20b являются дейтерием. Изобретение также относится к способу получения соединений общей формулы (I) путем взаимодействия соединения А6 с соединением XV и к промежуточным соединениям А6 и XV.
.
При этом в соединении А6 R10, R11, R12, R13a, R13b, R13c, R14a, R14b, R14c, R15a, R15b, R15c, R16, R17a, R17b, R18a, R18b, R19a, R19b, R20a или R20b независимо выбраны из дейтерия или водорода и по меньшей мере один из них представляет собой дейтерий; в соединении XV R1a, R1b, R1c, R2a, R2b, R2c, R3, R4, R6, R7, R9 независимо выбраны из водорода или дейтерия и по меньшей мере один из них представляет собой дейтерий; и R5 представляет собой водород, дейтерий или галоген; и R8 представляет собой галоген; X2 выбран из F, Cl, Br, I. 7 н. и 11 з.п. ф-лы, 4 ил., 1 табл.
Реферат
Область техники
Настоящее изобретение относится к области фармацевтики. В частности, настоящее изобретение относится к новому соединению дейтерированного диаминопиримидина и фармацевтическим композициям, содержащим указанное соединение.
Предшествующий уровень техники
Киназа анапластической лимфомы (ALK) представляет собой член суперсемейства инсулиновых тирозинкиназных рецепторов, слитый белок ALK, мутация и сверхэкспрессия которого связаны с разными заболеваниями. ALK впервые была открыта в линиях клеток анапластической крупноклеточной лимфомы (ALCL), причем ген слитого белка, образованный транслокацией t2;5, содержит 3'-концевой участок гена ALK (включая внутриклеточный домен и протеинкиназный домен) и ген ядрышкового фосфопротеина (ген нуклеофозмина, NPM). Открыли более двадцати типов слитых белков ALK, образованных в результате разных хромосомных перестроек. Они участвуют в патогенезе заболеваний, включающих анапластическую крупноклеточную лимфому, диффузную B-крупноклеточную лимфому, воспалительную миофибробластическую опухоль, нейробластому и т.д. Слитый белок EML4-ALK и четыре других слитых белка ALK играют фундаментальную роль в развитии примерно 5% случаев немелкоклеточного рака легкого. Последующие сигнальные пути, включающие слитые белки ALK, включают модуль пролиферации Ras/Raf/MEK/ERK1/2 и путь клеточного выживания JAK/STAT, и данная внутренняя сеть сигнальной трансдукции влияет на клеточную пролиферацию, дифференциацию и апоптоз. Ингибитор киназы ALK можно использовать для лечения рака, аутоиммунных заболеваний и тому подобное. В августе 2011 селективный двойной ингибитор ALK и c-Met кризотиниб компании Pfizer (торговая марка Ксалкори) был одобрен Администрацией США по пищевым продуктам и лекарственным веществам для лечения мелкоклеточного рака легкого на поздних стадиях. Во время клинического применения Кризотиниба возникает устойчивость к лекарственному средству, стимулируя, таким образом, разработку лекарственных средств - ингибиторов киназ ALK второго поколения для лечения немелкоклеточного рака легкого и других заболеваний.
Соединения диаминопиримидинов и их производных представляют собой класс ингибиторов для протеинкиназ, таких как киназа AKL. Ряд диаминопиримидиновых производных, имеющих двойные 2,4-заместители на пиримидиновом кольце, были описаны в WO 2008073687 и WO 2012106540. В этих документах соединение LDK378 (Церитиниб), химическим названием которого является 5-хлор-N2-(2-изопропокси-5-метил-4-(пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин, представляет собой селективный ингибитор киназы ALK, и его можно использовать в лечении рака и заболеваний, связанных с нарушением пролиферации клеток, и других родственных заболеваний. В настоящее время соединение находится на Стадии II клинических испытаний лечения заболеваний, связанных с нарушением пролиферации клеток (таких как немелкоклеточный рак легкого).
Несмотря на то, что направленное ингибирование различных протеинкиназ является благоприятным для лечения разных заболеваний, связанных с киназами, открытие новых соединений, которые специфично ингибируют какую-либо протеинкиназу и обладают хорошей доступностью лекарственного средства, такой как пероральная биодоступность, все еще является актуальным. Кроме того, у некоторых доступных в настоящее время ингибиторов протеинкиназ существуют некоторые побочные эффекты и проблемы устойчивости к лекарственным средствам.
Таким образом, в данной области все еще существует потребность в разработке соединений, обладающих ингибиторной активностью в отношении киназ (например, киназ ALK) или лучшими фармакодинамическими/фармакокинетическими свойствами.
Краткое описание изобретения
Целью настоящего изобретения является предложение типа новых соединений, обладающих ингибирующей активностью в отношении киназ ALK и/или лучшими фармакодинамическими/фармакокинетическими свойствами, и способов их применения.
В первом аспекте настоящего изобретения предложено соединение дейтерированного диаминопиримидина формулы (I) или его кристаллическая форма, фармацевтически приемлемая соль, гидрат или сольват:
,
где R1a, R1b, R1c, R2a, R2b, R2c, R3, R4, R5, R6, R7, R9, R10, R11, R12, R13a, R13b, R13c, R14a, R14b, R14c, R15a, R15b, R15c, R16, R17a, R17b, R18a, R18b, R19a, R19b, R20a и R20b независимо представляют собой водород, дейтерий или галоген;
R8 представляет собой водород, дейтерий, галоген, циано, недейтерированный C1-C6 алкил или C1-C6 алкокси, однократно или многократно дейтерированный или пердейтерированный C1-C6 алкил или C1-C6 алкокси или однократно или многократно галогенированный или пергалогенированный C1-C6 алкил или C1-C6 алкокси;
при условии, что по меньшей мере один из R1a, R1b, R1c, R2a, R2b, R2c, R3, R4, R5, R6, R7, R9, R10, R11, R12, R13a, R13b, R13c, R14a, R14b, R14c, R15a, R15b, R15c, R16, R17a, R17b, R18a, R18b, R19a, R19b, R20a или R20b является дейтерированным или дейтерием.
В другом предпочтительным воплощении содержание изотопа дейтерий в замещенном дейтерием положении по меньшей мере выше, чем природное содержание изотопа дейтерий (примерно 0,015%), предпочтительно выше чем 30%, более предпочтительно выше чем 50%, более предпочтительно выше чем 75%, более предпочтительно выше чем 95%, более предпочтительно выше чем 99%.
В другом предпочтительном воплощении соединение формулы (I) содержит по меньшей мере один атом дейтерия, более предпочтительно два атома дейтерия, более предпочтительно четыре атома дейтерия, более предпочтительно 6 атомов дейтерия.
В другом предпочтительном воплощении R1a, R1b, R1c, R2a, R2b, R2c и R3 независимо представляют собой водород или дейтерий.
В другом предпочтительном воплощении R12, R13a, R13b, R13c, R14a, R14b и R14c независимо представляют собой водород или дейтерий.
В другом предпочтительном воплощении R15a, R15b и R15c независимо представляют собой водород или дейтерий.
В другом предпочтительном воплощении R16, R17a, R17b, R18a, R18b, R19a, R19b, R20a и R20b независимо представляют собой водород или дейтерий.
В другом предпочтительном воплощении каждый R8 независимо выбран из: галогена, циано, однократно или многократно дейтерированного или пердейтерированного метила или метоксила, или трифторметила.
В другом предпочтительном воплощении R3 представляет собой дейтерий;
В другом предпочтительном воплощении R8 представляет собой хлор;
В другом предпочтительном воплощении R12 представляет собой дейтерий;
В другом предпочтительном воплощении R15a, R15b и R15c представляют собой дейтерий;
В другом предпочтительном воплощении R19a, R19b, R20a и R20b представляют собой дейтерий;
В другом предпочтительном воплощении соединение представляет собой одно из следующих соединений или его фармацевтически приемлемую соль:
5-хлор-N2-(2-изопропокси-5-метил-4-(пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-изопропокси-5-метил-4-(пиперидин-4-ил)фенил)-N4-(2-((d7-изопропил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-((2-d-проп-2-илокси)-5-метил-4-(пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(d7-изопропокси)-5-метил-4-(пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-изопропокси-5-(d3-метил)-4-(пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-изопропокси-5-метил-4-(4-d-пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-изопропокси-5-метил-4-(2,2,6,6-d4-пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-изопропокси-5-метил-4-(2,2,4,6,6-d5-пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-((2-d-проп-2-илокси)-5-метил-4-(пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(d7-изопропокси)-5-метил-4-(2,2,6,6-d4-пиперидин-4-ил)фенил)-N4-(2-((d7-изопропил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-((2-d-проп-2-илокси)-5-метил-4-(4-d-пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-((2-d-проп-2-илокси)-5-(d3-метил)-4-(4-d-пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(2-d-проп-2-илокси)-5-метил-4-(2,2,6,6-d4-пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(2-d-проп-2-илокси)-5-метил-4-(2,2,4,6,6-d5-пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(2-d-проп-2-илокси)-5-(d3-метил)-4-(2,2,4,6,6-d5-пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(2-d-проп-2-илокси)-5-метил-4-(2,2,6,6-d4-пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(2-d-проп-2-илокси)-5-(d3-метил)-4-(2,2,6,6-d4-пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(2-d-проп-2-илокси)-5-(d3-метил)-4-(2,2,4,6,6-d5-пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(2-d-проп-2-илокси)-5-(d3-метил)-4-(2,2,6,6-d4-пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-(d7-изопропокси)-5-(d3-метил)-4-(2,2,4,6,6-d5-пиперидин-4-ил)фенил)-N4-(2-((d7-изопропил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-изопропокси-5-метил-4-(2,2,4,6,6-d5-пиперидин-4-ил)фенил)-N4-(2-((2-d-проп-2-ил)сульфонил)фенил)пиримидин-2,4-диамин;
5-хлор-N2-(2-изопропокси-5-метил-4-(2,2,4,6,6-d5-пиперидин-4-ил)фенил)-N4-(4-фтор-2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин;
В другом предпочтительном воплощении соединение представляет собой ; которое имеет следующие характеристики:
МС (масс-спектр) расчетный: 561; МС обнаруженный: 562 (M+H)+, 584 (M+Na)+.
В другом предпочтительном воплощении соединение представляет собой ; которое имеет следующие характеристики:
МС расчетный: 562; МС обнаруженный: 563 (M+H)+, 585 (M+Na)+.
В другом предпочтительном воплощении соединение представляет собой ; которое имеет следующие характеристики:
МС расчетный: 563; МС обнаруженный: 564 (M+H)+, 586 (M+Na)+.
В другом предпочтительном воплощении соединение представляет собой ; которое имеет следующие характеристики:
МС расчетный: 566; МС обнаруженный: 567 (M+H)+, 589 (M+Na)+.
В другом предпочтительном воплощении соединение представляет собой ; которое имеет следующие характеристики:
МС расчетный: 562; МС обнаруженный: 563 (M+H)+, 585 (M+Na)+.
В другом предпочтительном воплощении недейтерированные соединения не включены в соединение.
В другом предпочтительном воплощении недейтерированное соединение представляет собой 5-хлор-N2-(2-изопропокси-5-метил-4-(пиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиримидин-2,4-диамин.
В другом предпочтительном воплощении соединение получают способом, описанным в примерах 1-16.
Во втором аспекте настоящего изобретения предложен способ получения фармацевтической композиции, который включает следующую стадию: смешивание соединений согласно первому аспекту настоящего изобретения или их кристаллической формы, фармацевтически приемлемой соли, гидрата или сольвата с фармацевтически приемлемым носителем с получением фармацевтической композиции.
В третьем аспекте настоящего изобретения предложена фармацевтическая композиция, которая содержит фармацевтически приемлемый носитель и соединение согласно первому аспекту настоящего изобретения или его кристаллическую форму, фармацевтически приемлемую соль, гидрат или сольват.
В другом предпочтительном воплощении фармацевтическая композиция представляет собой инъекцию, капсулу, таблетку, пилюлю, порошок или гранулу.
В другом предпочтительном воплощении фармацевтическая композиция содержит другие терапевтические средства, и другие терапевтические средства представляют собой терапевтические средства для лечения онкологических заболеваний, нарушений пролиферации клеток, сердечнососудистых заболеваний, воспалений, инфекций, аутоиммунных заболеваний, вирусных заболеваний или нарушений метаболизма.
Более предпочтительно, другое терапевтическое средство включает: 5-фторурацил, фолфокс, Avastin™ (авастин, бевацизумаб), бексаротен, бортезомиб, кальцитриол, канертиниб, капецитабин, гемцитабин, карбоплатин, целекоксиб, цетуксимаб, цисплатин, дазатиниб, дигоксин, энзастаурин, эрлотиниб, этопозид, эверолимус, фулвестрант, гефинитиб, генистеин, иматиниб, иринотекан, лапатиниб, леналидомид, летрозол, лейковорин, матузумаб, оксалиплатин, Таксол (паклитаксел), доцетаксел, панитумумаб, пегилированный гранулоцитарный колониестимулирующий фактор (пэгфилграстин), пегилированный альфа-интерферон, пеметрексед, Полифенон®Е, сатраплатин, сиролимус, сунитиниб (сутент, сунитиниб), сулиндаковая кислота (сулиндак), Таксотер (таксотер), темозоломид (темодар, темозомоломид), Торизел, темсиролимус, типифарниб, транстузумаб, вальпроевая кислота, винфлунин, Волоциксимаб, Вориностат, сорафениб, Кризотиниб, Лкотиниб, лапатиниб, Тофацитиниб, PD-0332991 (Палбоциклиб), амбризентан, CD40 и/или CD154-специфичные антитела, слитые белки, ингибиторы NF-kB (ядерного фактора «каппа-би»), нестероидное противовоспалительное лекарственное средство, ингибиторы фактора свертывания крови FXa (например, ривароксабан и т.д.), антитела против ФНО (фактора некроза опухоли), антибиотики, такие как калихимицин, актиномицин, Адриамицин (доксорубицин) и другие терапевтические средства на основе простагландинов или монтелукаст (но не ограничивается ими).
В четвертом аспекте настоящего изобретения предложено применение соединения первого аспекта настоящего изобретения или его кристаллической формы, фармацевтически приемлемой соли, гидрата или сольвата в получении фармацевтических композиций, которые ингибируют протеинкиназы (например, киназы ALK).
В другом предпочтительном воплощении фармацевтическую композицию согласно изобретению можно применять для лечения следующих заболеваний: онкологические заболевания, нарушения пролиферации клеток, воспаления, инфекции, аутоиммунные соединения, трансплантации органов, вирусные заболевания, сердечнососудистые заболевания или нарушения метаболизма.
В другом предпочтительном воплощении онкологические заболевания включают: рак легкого, рак головы и шеи, рак молочной железы, рак предстательной железы, рак пищевода, рак толстой и прямой кишки, рак толстой кишки, рак носоглотки, рак матки, рак поджелудочной железы, лимфому, лейкоз, остеосаркому, меланому, рак почки, рак желудка, рак печени, рак мочевого пузыря, рак щитовидной железы или рак толстой кишки (но не ограничиваются ими).
В другом предпочтительном воплощении иммунные заболевания или воспаление включают: ревматоидный артрит, остеоартрит, ревматоидный спондилит, подагру, астму, бронхит, ринит, хроническую обструктивную болезнь легких, заболевание муковисцидоз (но не ограничиваются ими).
В другом предпочтительном воплощении нарушения пролиферации клеток включают: рак легкого, рак головы и шеи, рак молочной железы, рак предстательной железы, рак пищевода, рак толстой и прямой кишки, рак толстой кишки, рак носоглотки, рак матки, рак поджелудочной железы, лимфому, лейкоз, остеосаркому, меланому, рак почки, рак желудка, рак печени, рак мочевого пузыря, рак щитовидной железы или рак толстой кишки (но не ограничиваются ими).
В другом предпочтительном воплощении онкологическое заболевание представляет собой немелкоклеточный рак легкого.
В пятом аспекте настоящего изобретения предложен способ ингибирования протеинкиназы (например, киназ ALK) или способ лечения заболеваний (таких как рак, нарушения пролиферации клеток, воспаление, инфекция, иммунопатологические заболевания, трансплантация органов, вирусное заболевание, сердечнососудистые заболевания или метаболическое заболевание), включающий следующие стадии: введение соединения первого аспекта настоящего изобретения или его кристаллической формы, фармацевтически приемлемой соли, гидрата или сольвата, или введение фармацевтической композиции третьего аспекта настоящего изобретения нуждающемуся в этом субъекту.
Следует понимать, что в настоящем изобретении каждый из технических признаков, более конкретно описанных выше и ниже (например, технические признаки в разделе Примеры), можно объединять один с другим, образуя, таким образом, новые или предпочтительные технические решения, которые нет необходимости снова подробно описывать в данном документе.
Описание графических материалов:
Фиг. 1 представляет собой кривую время - концентрация соединения в плазме у самцов крыс, которым, соответственно, вводили 5 мг/кг контрольного соединения Церитиниб и соединения согласно Примеру 1 посредством зондового кормления.
Фиг. 2 представляет собой кривую время - концентрация соединения в плазме у самцов крыс, которым, соответственно, вводили 5 мг/кг контрольного соединения Церитиниб и соединения согласно Примеру 2 посредством зондового кормления.
Фиг. 3 представляет собой кривую время - концентрация соединения в плазме у самцов крыс, которым, соответственно, вводили 5 мг/кг контрольного соединения Церитиниб и соединения согласно Примеру 3 посредством зондового кормления.
Фиг. 4 представляет собой кривую время - концентрация соединения в плазме у самцов крыс, которым, соответственно, вводили 5 мг/кг контрольного соединения Церитиниб и соединения согласно Примеру 13 посредством зондового кормления.
Воплощения для осуществления изобретения
При проведении исследования автор изобретения неожиданно обнаружил, что соединение дейтерированного диаминопиримидина или его фармацевтически приемлемые соли явно превосходят недейтерированное соединение по фармакокинетическим и/или фармакодинамическим свойствам, которые, вследствие этого, больше подходят для применения в качестве соединений ингибиторов киназ ALK и более подходят для применения в получении лекарственных средств для лечения рака и заболеваний, связанных с киназами ALK. Настоящее изобретение осуществлено, исходя из этого.
Определения
В том виде, как он используется в данном документе, термин «галоген» относится к F, Cl, Br и I. Более предпочтительно, галоген выбран из F, Cl и Br.
В том виде, как он используется в данном документе, термин «C1-C6 алкил» относится к прямому или разветвленному алкилу, который содержит от 1 до 6 атомов углерода, такому как метил, этил, пропил, изопропил, бутил, изобутил, mpem-бутил и тому подобное.
В том виде, как он используется в данном документе, термин «C1-C6 алкокси» относится к прямому из разветвленному алкокси, который содержит от 1 до 6 атомов углерода, такому как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, трет-бутокси и тому подобное.
В том виде, как он используется в данном документе, термин «дейтерированный» означает, что один или более чем один водород в соединении или группе замещен дейтерием. «Дейтерированный» может быть однозамещенным, двузамещенным, многократно замещенным или полностью замещенным. Термин «однократно или многократно дейтерированный» и «дейтерированный один или более чем один раз» можно использовать взаимозаменяемо.
В том виде, как он используется в данном документе, «недейтерированное соединение» относится к соединению, доля атомов дейтерия которого составляет не больше чем природное содержание изотопа дейтерий (0,015%).
В другом предпочтительном воплощении содержание изотопа дейтерий в замещенном дейтерием положении выше чем природное содержание изотопа дейтерий (0,015%), более предпочтительно выше чем 50%, более предпочтительно выше чем 75%, более предпочтительно выше чем 95%, более предпочтительно выше чем 97%, более предпочтительно выше чем 99%, более предпочтительно выше чем 99,5%.
В другом предпочтительном воплощении соединение формулы (I) содержит по меньшей мере два атома дейтерия, более предпочтительно четыре атома дейтерия, более предпочтительно шесть атомов дейтерия, более предпочтительно восемь атомов дейтерия.
В соединении формулы (I) N может представлять собой 14N и/или 15N; O может представлять собой 16O и/или 18O.
Предпочтительно, в соединении формулы (I) N представляет собой 14N и/или O представляет собой 16O.
В другом предпочтительном воплощении в соединении содержание изотопа 14N в положении атома азота составляет ≥95%, предпочтительно ≥99%.
В другом предпочтительном воплощении в соединении содержание изотопа 16O в положении атома кислорода составляет ≥95%, предпочтительно ≥99%.
Активные ингредиенты
В том виде, как он используется в данном документе, термин «соединение согласно настоящему изобретению» относится к соединению формулы (I). Термин также включает кристаллические формы, фармацевтически приемлемые соли, гидраты или сольваты соединения формулы (I).
Среди которых термин «фармацевтически приемлемая соль» относится к соли, образованной соединением согласно настоящему изобретению и кислотой или основанием, которая подходит для лекарственного средства. Фармацевтически приемлемые соли включают неорганические и органические соли. Предпочтительным типом солей являются соли, образованные соединениями согласно настоящему изобретению и кислотой. Подходящие солеобразующие кислоты включают: неорганические кислоты, такие как соляная кислота, бромоводородная кислота, фтороводородная кислота, серная кислота, азотная кислота, фосфорная кислота и тому подобное; органические кислоты, такие как муравьиная кислота, уксусная кислота, трифторуксусная кислота, пропионовая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, яблочная кислота, винная кислота, лимонная кислота, пикриновая кислота, бензойная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, бензолсульфоновая кислота, нафталинсульфоновая кислота и тому подобное; и аминокислоты, такие как пролин, фенилаланин, аспарагиновая кислота, глутаминовая кислота и тому подобное, но не ограничиваются ими. Другим предпочтительным типом солей являются соли, образованные соединениями согласно настоящему изобретению и основаниями, например, соли щелочных металлов (например, соли натрия или калия), соли щелочно-земельных металлов (например, соли кальция или магния), аммонийные соли (например, аммонийные соли низших алканолов или другие фармацевтически приемлемые соли амина), например, соль метиламина, соль этиламина, соль пропиламина, соль диметиламина, соли триметиламина, соли диэтиламина, соли триэтиламина, соли трет-бутиламина, соли этилендиамина, соли гидроксиэтиламина, соли дигидроксиэтиламина, соли тригидроксиэтиламина и соли амина, образованные морфолином, пиперазином и лизином.
Термин «сольват» относится к комплексу определенного соотношения, образованному в результате образования координационных связей между соединением согласно настоящему изобретению и молекулами растворителя. Термин «гидрат» относится к комплексу, образованному в результате образования координационных связей между соединением согласно настоящему изобретению и водой.
Кроме того, соединения согласно настоящему изобретению дополнительно содержат пролекарства соединений диаминопиримидина формулы (I). Термин «пролекарство» включает тип соединений, которые обладают биологической активностью или неактивностью, и будут превращаться в соединение формулы (I) в результате метаболизма или химических реакций в организме человека при введении соответствующим способом или соль или сольват, образованные соединением формулы (I). Пролекарство включает сложный эфир карбоновой кислоты, сложный эфир угольной кислоты, фосфат, нитрат, сульфат, сложный эфир сульфоновой кислоты, сложные эфиры сульфоксида, аминосоединения, карбаматы, азосоединения, фосфорамиды, глюкозид, простой эфир, ацеталь соединения и т.д. (но не ограничивается ими).
Способ получения
Ниже в данном документе будет подробно описано получение соединений формулы (I), но такие конкретные способы не накладывают какого-либо ограничения настоящего изобретения. Соединения согласно изобретению можно также легко получать, возможно, путем комбинирования разных способов синтеза, описанных в данном описании или известных в данной области, такую комбинацию может легко осуществить средний специалист в данной области, к которой принадлежит настоящее изобретение.
Известны способы, используемые в настоящем изобретении для получения соединений недейтерированных диаминопиримидинов и их физиологически совместимых солей. Получение соответствующих соединений дейтерированных диаминопиримидинов можно проводить с использованием соответствующего исходного дейтерированного соединения посредством того же пути синтеза. Например, соединение формулы (I) согласно настоящему изобретению можно получать способом, описанным в WO 2008073687, за исключением того, что вместо недейтерированных веществ используют дейтерированные вещества.
Как правило, в способе получения каждую реакцию обычно проводят в инертном растворителе, при температуре от комнатной до температуры кипения (например, 0°C~80°C, предпочтительно от 0°C~50°C). Время реакции обычно составляет от 0,1 часа до 60 часов, предпочтительно от 0,5 до 48 часов.
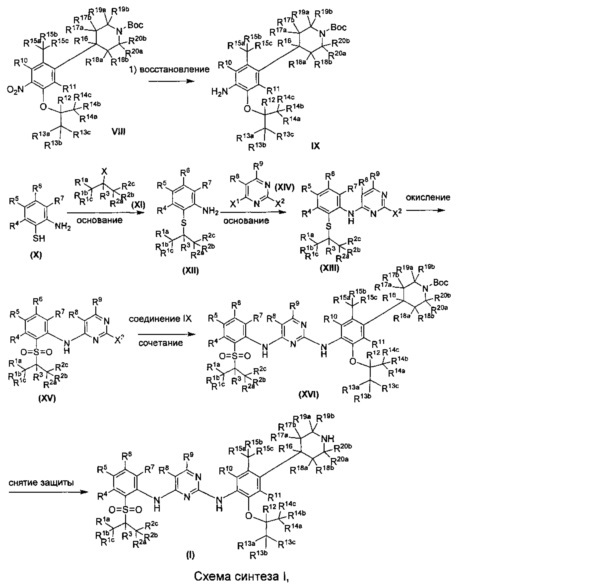
В синтезе соединений формулы (I) согласно настоящему изобретению можно использовать следующий общий путь получения.
где X, X1, X2 выбраны из F, Cl, Br, I, OTs, OMs, OTf; и R1a, R1b, R1c, R2a, R2b, R2c, R3, R4, R5, R6, R7, R9, R10, R11, R12, R13a, R13b, R13c, R14a, R14b, R14c, R15a, R15b, R15c, R16, R17a, R17b, R18a, R18b, R19a, R19b, R20a или R20b представляют собой такие, как определено выше.
Как показано в Схеме синтеза I, соединение II нитробензол взаимодействует с алканольным соединением III в щелочных условиях с получением соединения IV. 4-Хлор-пиперидиновое соединение V защищают группой Вос(трет-бутоксикарбонил) с получением соединения VI и в результате реакции с бораном получают соединение бора VII. Соединение IV и соединение бора VII сочетают с получением соединения VIII в результате сочетания Сузуки, и затем путем восстановления получают анилиновое соединение IX. В основных условиях посредством реакции замещения из тиофенольного соединения X и алкилгалидного соединения XI получают бензолсульфидное соединение XII, затем соединение XII и 2,4-дигалогенированное соединение пиримидина XIV подвергают реакции замещения в основных условиях с получением 2-галозамещенного соединения пиримидина XIII, и затем посредством реакции окисления получают соединение XV. Соединение XV и анилиновое соединение IX используют для получения соединения XVI посредством сочетания; и соединение I согласно настоящему изобретению получают из соединения XVI посредством реакции снятия защитной группы Вое. Приведенные выше реакции проводят в инертном растворителе, таком как дихлорметан, дихлорэтан, ацетонитрил, н-гексан, толуол, тетрагидрофуран, N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, изопропанол, н-бутанол, трет-бутанол, диоксан и т.д, при температуре 0-200°C. Основание выбрано из карбоната калия, карбоната цезия, гидроксида натрия, гидроксида калия, н-бутиллития, трет-бутиллития, изо-бутиллития, диизопропиламинолития, фосфата калия, бис(триметилсилил)аминолития, бис(триметилсилил)аминокалия, трет-бутоксида калия, трет-бутоксида натрия, этоксида натрия, 4-диметиламинопиридина, пиридина, триэтиламина, диизопропилэтиламина и тому подобное.
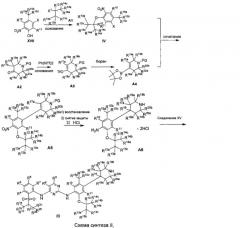
где X, X1, X2 выбраны из F, Cl, Br, I, OTs, OMs, OTf; и R1a, R1b, R1c, R2a, R2b, R2c, R3, R4, R5, R6, R7, R9, R10, R11, R12, R13a, R13b, R13c, R14a, R14b, R14c, R15a, R15b, R15c, R16, R17a, R17b, R18a, R18b, R19a, R19b, R20a или R20b представляют собой такие, как определено выше. PG представляет собой защитную группу аминогруппы, такую как трет-бутоксикарбонильная группа, бензильная группа, бензилоксикарбонильная группа, п-метоксибензильная группа и тому подобное.
Как показано в Схеме синтеза II, соединение XVII о-нитрофенол взаимодействует с соединением A1 в основных условиях с образованием соединения IV. В щелочных условиях соединение A2 4-пиперидон взаимодействует с N-фенил-бис(трифторметилсульфонил)имидом с получением соединения A3, затем оно взаимодействует с бис(пинаколато)дибораном с получением соединения A4. Соединение A5 получают из соединения IV и соединения A4 посредством реакции сочетания Сузуки; соединение гидрохлорид анилина A6 получают из соединения A5 путем восстановления водородом или газом дейтерия, снятия защиты и солеобразования с использованием гидрохлорида; и соединение A6 и соединение XV конденсируют с получением соединения I согласно настоящему изобретению. Приведенные выше реакции проводят в инертном растворителе, таком как дихлорметан, дихлорэтан, ацетонитрил, н-гексан, толуол, тетрагидрофуран, N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, изопропанол, н-бутанол, трет-бутанол, диоксан и т.д, при температуре 0-200°C. Основание выбрано из карбоната калия, карбоната цезия, гидроксида натрия, гидроксида калия, н-бутиллития, трет-бутиллития, изо-бутиллития, диизопропиламинолития, фосфата калия, бис(триметилсилил)аминолития, бис(триметилсилил)аминокалия, трет-бутоксида калия, трет-бутоксида натрия, этоксида натрия, 4-диметиламинопиридина, пиридина, триэтиламина, диизопропилэтиламина и тому подобное.
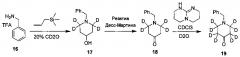
Дейтерированное соединение A2 может быть получено следующими путями:
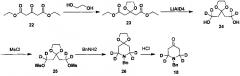
Ссылаясь на журнал Labelled Compounds and Radiopharmaceuticals 2007, 50, 131-137, бензиламина трифторацетат 16 взаимодействует с аллил-триметилсилиловым эфиром и дейтерированным формальдегидом с получением соединения 17, и затем соединение 18 получают путем окисления по методу Десс-Мартина. Соединение 18 подвергают обмену водорода на дейтерий с помощью дейтерированного хлороформа/тяжелой воды в условиях 1,5,7-триазабицикло(4.4.0)дец-5-ена с получением соединения 19.
Соединение 20 подвергают замене водорода на дейтерий с помощью дейтерированного хлороформа/тяжелой воды в условиях 1,5,7-триазабицикло(4.4.0)дец-5-ена с получением соединения 21.
Соединение 22 защищают этиленгликолем с получением кетального соединения 23, которое затем восстанавливают LiAlD4 с получением соединения 24; соединение 24 защищают мезилом с образованием соединения 25, и соединение 25 взаимодействует с бензиламином с получением соединения 26, с которого снимают защиту соляной кислотой с получением соединения 18.
Дейтерированное соединение A8 и A10 можно получать следующими путями:
,
где R1a, R1b, R1c, R2a, R2b, R2c, R3 представляют собой такие, как определено выше.
Ссылаясь на Organic Letters, 2008, pp. 4351-4353, соединение A7 нагревают микроволновым излучением в концентрированной соляной кислоте и тяжелой воде с получением соединения A8.
,
где R12, R13a, R13b, R13c, R14a, R14b, R14c, R15a, R15b, R15c, R16, R17a, R17b, R18a, R18b, R19a, R19b, R20a или R20b представляют собой такие, как определено выше.
Ссылаясь на Organic Letters, 2008, pp. 4351-4353, соединение A9 нагревают микроволновым облучением в концентрированной соляной кислоте и тяжелой воде с получением соединения A10.
Фармацевтическая композиция и ее введение
Соединения согласно настоящему изобретению обладают выдающейся активностью ингибирования протеинкиназы, такой как киназы ALK. Вследствие этого соединение согласно настоящему изобретению и его кристаллические формы, фармацевтически приемлемые неорганические или органические соли, гидраты или сольваты, и фармацевтическую композицию, содержащую соединение согласно настоящему изобретению в качестве основного активного ингредиента, можно использовать для лечения, предупреждения и облегчения заболеваний, опосредованных протеинкиназой (например, киназы ALK). На основе предшествующего уровня техники соединения согласно изобретению можно использовать для лечения следующих заболеваний: онкологические заболевания, нарушения пролиферации клеток, сердечнососудистые соединения, воспаления, инфекции, аутоиммунные соединения, трансплантации органов, вирусные заболевания, сердечнососудистые заболевания или метаболические заболевания.
Фармацевтическая композиция согласно изобретению содержит соединение согласно настоящему изобретению или его фармацевтически приемлемые соли в диапазоне безопасных и эффективных доз и фармацевтически приемлемые вспомогательные вещества или носители. При этом, термин «безопасная и эффективная доза» относится к количеству соединения, которого достаточно для улучшения состояния пациента без какого-либо серьезного побочного эффекта. Как правило, фармацевтическая композиция содержит 1-2000 мг соединения согласно изобретению на дозу, предпочтительно 10-1000 мг соединений согласно изобретению на дозу. Предпочтительно, «на дозу» означает одну капсулу или таблетку.
«Фармацевтически приемлемый носитель» означает один или более чем один совместимый твердый или жидкий наполнитель или гелевое вещество, которые подходят для человека и должны иметь достаточную чи