Способ предимплантационного хранения биологических протезов для сердечно-сосудистой хирургии
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к сердечно-сосудистой хирургии, и предназначено для хранения биологических протезов для сердечно-сосудистой хирургии до момента имплантации. Способ включает отмывку предварительно консервированного биологического протеза в растворе стерильного 0,9% раствора хлорида натрия и помещение в стерилизующий агент на фосфатном буфере. При этом в качестве стерилизующего агента используют смесь бактерицидных препаратов, состоящую из этилпарабена, метилпарабена, пропилпарабена и феноксиэтанола, приготовленную на 0,05-2,0 М фосфатном буфере и содержащую 5-20% этанола при рН 4,0-8,0 в концентрации 0,2-2,0% и температуре 5-40°C. Использование изобретения обеспечивает стерилизующий эффект при хранении, увеличивает прочность биоматериала при хранении и уменьшает время отмывки биопротезов перед имплантацией. 2 з.п. ф-лы, 2 табл., 2 пр.
Реферат
Изобретение относится к медицине, а именно к предимплантационной обработке биологических протезов для сердечно-сосудистой хирургии, и может быть использовано при хранении биологических протезов клапанов сердца, сосудов и т.п. до момента имплантации.
Известен способ стерилизации и хранения ксенопротезов в 0,5% растворе глутарового альдегида (Методические указания по стерилизации ксенобиопротезов раствором глутарового альдегида. Минздрав СССР. N 28-6/26 от 19.09.1986 г.).
Недостатком данного способа является длительная отмывка биопротеза от стерилизующего раствора - в течение 90 минут при интенсивном помешивании в 500 мл 0,9% стерильного раствора хлорида натрия со сменой раствора каждые 15 минут. Помимо этого, консервация и хранение биопротезов для сердечно-сосудистой хирургии в растворе глутарового альдегида провоцирует образование фосфата кальция в биоткани, что может приводить к дисфункции биопротеза после имплантации.
Известен способ консервации и стерилизации биологических протезов клапанов сердца и сосудов в буферном растворе диглицидилового эфира этиленгликоля (ДЭЭ) (пат. №2008767, Рос. Федерация: МПК A01N 1/00. Способ консервации биоткани для протезирования клапанов сердца и сосудов [Текст] / Барбарш Л.С., Новикова С.П., Журавлева И.Ю. и др.; патентообладатель Барбараш Л.С. (RU). - №5024513/14; заявл. 23.01.92; опубл. 15.03.94 г., бюл. №5). Консервация и стерилизация биологического материала достигается путем обработки 2-5% раствором ДЭЭ. До момента имплантации изделия хранят в этом же растворе. Предимплантационная обработка включает отмывку биопротезов от консерванта в 500 мл стерильного 0,9% раствора натрия хлорида в течение 1 часа с троекратной сменой раствора. Недостатком данного способа является длительность режима отмывки, что приводит к увеличению времени операции.
Известен способ стерилизации и предимплантационного хранения биологических протезов клапанов сердца и сосудов в 0,01-2,0% растворе 2-бром-2-нитропропан-1,3-диола на фосфатном буфере (пат. №2357766, Рос. Федерация, МПК A61N 1/02, A61L 27/00. Способ стерилизации и предимплантационного хранения биологических протезов для сердечно-сосудистой хирургии; правообладатель Журавлева И.Ю. (RU). - №2007125732/15; заяв. 06.07.07, опубл. 10.06.09), при котором предварительно консервированные биологические протезы помещают в 0,01-2,0% раствор 2-бром-2-нитропропан-1,3-диола, приготовленного на фосфатном буфере, и хранят в этом растворе до момента имплантации.
К недостаткам данного способа следует отнести тот факт, что препарат 2-бром-2-нитропропан-1,3-диол не обладает спороцидным действием, вследствие чего не может обеспечить стерилизующий эффект. Помимо этого длительное хранение (более 30 суток) биоматериала в растворе 2-бром-2-нитропропан-1,3-диола приводит к изменению цвета биоткани с белого до темно-желтого и придает ей ригидность.
Известен способ стерилизации и предимплантационного хранения биопротезов клапана сердца или сосудов, изготовленных из химически стабилизированной ксеногенной ткани, при котором изделия помещают для стерилизации и хранения до момента имплантации в раствор 2-3-бис(гидроксиметил)-хиноксалин-1,4-диоксида при температуре от 16 до 40°C (пат. №2457867, Рос. Федерация: МКП A61L 2/16, A61L 27/00, А61К 31/498. Способ стерилизации и предимплантационного хранения биологических протезов из ксеногенной и аллогенной ткани для сердечнососудистой хирурги [Текст] / Костава В.Т., Бакулева Н.П., Лютова И.Г. и др.; патентообладатель: Учреждение Российской академии медицинских наук Научный центр сердечно-сосудистой хирургии им. А.Н. Бакулева РАМН (RU). №2011117782/15; заявл. 05.05.2011; опубл. 10.08.2012 г., бюл. №22). Перед имплантацией биопротез помещают в 500 мл стерильного 0,9% раствора хлорида натрия не менее чем на 30 секунд. Препарат 2-3-бис(гидроксиметил)-хиноксалин-1,4-диоксид обладает мощным антибактериальным и бактериостатическим действием, действует на штаммы бактерий, устойчивых к другим химиопрепаратам, включая антибиотики.
К недостаткам данного способа можно отнести высокую токсичность 2-3-бис (гидроксиметил)-хиноксалин-1,4-диоксида, также данный препарат обладает тератогенным, эмбриотоксическим и мутагенным действием, категорически противопоказан к применению у детей. Для хранения бипротезов используется водный раствор 2-3-бис (гидроксиметил)-хиноксалин-1,4-диоксида, который имеет осмолярность раствора гораздо более низкую, нежели плазма крови, в которой он будет эксплуатироваться после имплантации. Низкая осмолярность раствора для хранения биопротезов может приводить к отеку биокани, которая может стать причиной дисфункции протеза после имплантации.
Наиболее близким к заявленному методу является способ хранения биологических протезов в растворе, содержащем метил- и пропилпарабены (US 5188834, кл. A61L 27/36, A61L 27/00; A61F 002/02 Method of preparing a biological implantation material. Inventors.: Grimm; Michael (AT), Eybl; Elisabeth (AT), Griesmacher; Andrea (AT), Grabenwoger; Martin (AT), Muller; Mathias M. (AT), Wolner; Ernst (AT); Assignee: Sorin Biomedica S.p.A. (IT), Filed 30.05.90, Date of patent 23.02.93). Суть этого метода заключается в том, что для хранения биопротезов используют раствор, содержащий 0,02% пропилпарабена и 0,18% метилпарабена, растворенные в фосфатном буфере.
К недостаткам данного способа можно отнести низкие концентрации парабенов, которые могут не оказывать достаточный антибактериальный, бактериостатический и фунгицидный эффект, поскольку данные вещества частично теряют свою активность при растворении в воде и при контакте с белками. Помимо этого фосфатный буфер имеет низкую осмолярность, что может приводить к отеку биоткани при хранении биопротезов и, как следствие, провоцировать дисфункцию изделий после имплантации.
Техническим результатом изобретения является усиление стерилизующего эффекта при хранении и сокращение времени отмывки биопротезов от консервирующего раствора перед имплантацией, за счет применения смеси бактерицидных препаратов, приготовленной на 0,05-0,2 М фосфатном буфере с добавлением этилового спирта.
Предложен способ стерилизации и предимплантационного хранения биологических протезов, включающий отмывку предварительно консервированного биологического протеза в растворе стерильного 0,9% раствора хлорида натрия и помещение в стерилизующий агент на фосфатном буфере с добавлением этилового спирта.
Отличием является то, что в качестве стерилизующего агента применяется смесь бактерицидных препаратов: этилпарабен, метилпарабен, пропилпарабен и феноксиэтанол, приготовленная на 0,05-2,0 М фосфатном буфере, содержащая 5-20% этанола при рН 4,0-8,0 в концентрации 0,2-2,0% и температуре 5-40°C.
Предложенный способ позволяет получить раствор для стерилизации и хранения биологических протезов, обладающий высокой антибактериальной, бактериостатической, фунгицидной и противоспоровой активностью, не оказывающий негативного воздействия на структуру и свойства предварительно консервированного биоматериала. Добавление этилового спирта в раствор для хранения биопротезов позволяет повысить осмолярность раствора до значений плазмы крови, улучшает растворимость используемых препаратов и дополняет стерилизующий эффект.
Используемые стерилизующие агенты относятся к химически синтезированным веществам и являются эффективными бактерицидными средствами против грамположительных и грамотрицательных бактерий, также активны против различной грибковой флоры и плесневых грибов, обладают сильными антисептическими свойствами. В сочетании друг с другом они усиливают свой антибактериальный эффект и обладают низкой токсичностью. В косметологической промышленности данные препараты и их смеси широко применяют в качестве консерванта при изготовлении очищающих средств для детей, средств для снятия макияжа, жидкости для полоскания рта, раствор стабилен при длительном хранении.
Отмывку одного биопротеза перед имплантацией можно проводить трехкратно в 500 мл 0,9% раствора NaCl по одной минуте, таким образом, общее время отмывки составит 3 минуты.
Предварительный этап консервации биологических протезов может быть осуществлен любым консервантом.
Ниже приведен пример осуществления предлагаемого способа.
Пример 1. Подготовленную по существующим методикам отбора нативную ткань промывают 0,9% раствором натрия хлорида, затем помещают в 2-5% раствор ДЭЭ (патент №2008767). Через 21 сутки консервации биологический протез отмывают в 0,9% растворе натрия хлорида в течение 1 часа с трехкратной сменой раствора и перекладывают на хранение в 1% раствор смеси стерилизующих агентов, содержащий 4 г метилпарабена, 2 г этилпарабена, 2 г пропилпарабена, 2 г феноксиэтанола, 100 г 95% этилового спирта (10% к массовой доли раствора) и 890 г 0,1 М фосфатного буфера.
Пример 2. Подготовленную по существующим методикам отбора нативную ткань промывают 0,9% раствором натрия хлорида, затем помещают в 2-5% раствор ДЭЭ (патент №2008767). Через 21 сутки консервации биологический протез отмывают в 0,9% растворе натрия хлорида в течение 1 часа с трехкратной сменой раствора и перекладывают на хранение в 0,5% раствор смеси стерилизующих агентов, содержащий 3,5 г метилпарабена, 1,5 г этилпарабена, 150 г 95% этилового спирта (15% к массовой доли раствора) и 845 г 0,1 М фосфатного буфера.
Для оценки стерилизующего эффекта были проведены бактериологические испытания - образцы биоматериала, контаминированные в течение 24 часов St.aureus, E.coli, Ent.faecalis, Kl. pheumoniae, Acin. baumani и грибами p. Candida albicans, были помещены в 0,5% и 1% растворы смесей метилпарабен/этилпарабен и метилпарабен/этилпарабен/пропилпарабен/феноксиэтанол на 48 часов, после чего провели исследования на стерильность (см. таблицу 1).
Результаты испытаний показывают, что предложенный способ оказывает хороший стерилизующий эффект 0,5-1,0% растворов смеси и этилпарабена/метилпарабена и раствор смеси этилпарабена/метилпарабена/пропилпарабена/феноксиэтанола при температуре 5-40°C подавляет рост всех микроорганизмов и грибов.
Для изучения влияния предлагаемого способа стерилизации на структуру биоматериала было проведено гистологическое исследование образцов ксеноперикарда и внутренней грудной артерии крупного рогатого скота, после хранения в опытных растворах в течение 30 суток. Хранение биоматериала, обработанного предложенным способом, не оказывает негативного воздействия на биоматериал - коллагеновые волокна извиты, расположены компактно.
Предлагаемый способ стерилизации и хранения биологических протезов не провоцирует кальций-связывающую активность биоматериала. Через 60 суток после имплантации образцов, обработанных предложенным способом, под кожу крысам линии Vistar, количество кальция в биоматериале равно метаболическому и не превышало 1,25±0,21 ммк/мг сухой ткани.
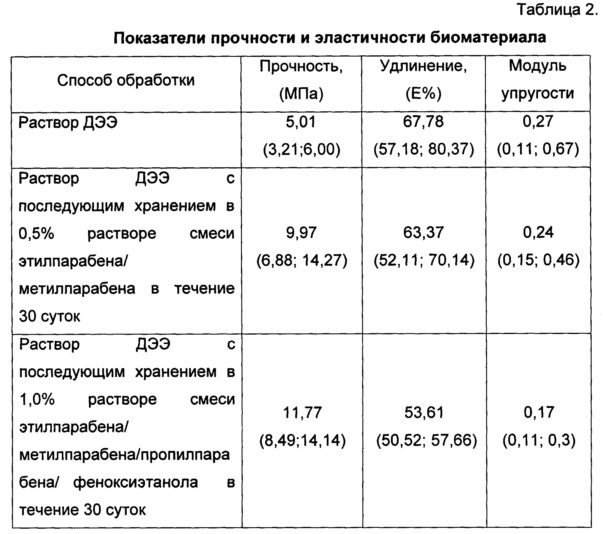
Предложенный способ увеличивает прочность биоматериала, предварительно консервированного раствором ДЭЭ (см. таблицу 2).
Применение смесей этилпарабена, метилпарабена, пропилпарабена и феноксиэтанола в пределах 0,2-2,0% обусловлено тем, что концентрация ниже 0,2% не оказывает необходимого стерилизующего эффекта, а использование свыше 2% - нетехнологично.
Использование раствора с рН 4,0-8,0 температурой 5-40°C позволяет сохранять стабильную концентрацию стерилизующего раствора в течение длительного периода хранения. При длительном хранении (30 суток и выше) биоматериал сохраняет стерильность, структуру коллагеновой матрицы, повышается прочность биоматериала, внешний вид не изменяется.
Преимуществом предложенного способа является усиление стерилизующего эффекта при хранении, увеличение прочности биоматериала и уменьшение времени отмывки биопротезов перед имплантацией, что сокращает время операции. Отмывать биопротез от стерилизующего раствора смесей этилпарабена/метилпарабена или этилпарабена/метилпарабена/пропилпарабена/феноксиэтанола необходимо в 500 мл стерильного 0,9% раствора натрия хлорида в течение 3 мин с двукратной сменой раствора через 1 мин.
1. Способ предимплантационного хранения биологических протезов для сердечно-сосудистой хирургии, включающий отмывку нативной ткани, ее консервацию в сшивающем и стерилизующем агенте с последующей отмывкой и хранением до имплантации в стерилизующем растворе пропилпарабена и метилпарабена, приготовленном на фосфатном буфере, отличающийся тем, что в стерилизующий раствор парабенов дополнительно по отношению к массе раствора вводят этилпарабен в массовой доле 0,02-0,4%, феноксиэтанол в массовой доле 0,02-0,4%, а также этиловый спирт в массовой доле 5-20%, при этом раствор готовят на 0,05-2,0 М фосфатном буфере при рН 4,0-8,0 до концентрации 0,2-2,0% и температуре 5-40°C.
2. Способ предимплантационного хранения биологических протезов по п. 1, отличающийся тем, что содержание пропилпарабена по отношению к массе раствора составляет 0,04-0,4%.
3. Способ предимплантационного хранения биологических протезов по п. 1, отличающийся тем, что содержание метилпарабена по отношению к массе раствора составляет 0,08-0,8%.