Способ получения n-арил-о-алкилкарбаматов
Иллюстрации
Показать всеИзобретение относится к способу получения N-арил-О-алкилкарбаматов общей формулы I, где R означает арильные группы, а R1 означает алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4. Способ заключается в том, что осуществляют взаимодействие спирта R1OH и симметричной дизамещенной мочевины II, где R означает арильные группы, a R1 означает алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4, в непрерывном режиме при атмосферном давлении в среде карбамата I при соотношении реагентов мочевина:алифатический спирт=1:(10÷60) мольн. и температуре от 140 до 250°C. Предлагаемый способ позволяет повысить выход N-арил-О-алкилкарбаматов формулы I и исключить использование растворителей. 5 пр.
Реферат
Изобретение относится к химии N-арил-О-алкилкарбаматов общей формулы I:
где R означают арильные группы, R1 означают алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4.
Изобретение относится к способам получения соединений формулы I.
Уретаны общей формулы I находят применение в качестве лекарственных препаратов, средств защиты растений, а также могут быть использованы как полупродукты при синтезе лекарственных препаратов и исходные вещества для получения изоцианатов.
Известны карбаматы общей формулы I, где R1 означает изопропильную, R-фенильную, о-хлорфенильную, м-хлорфенильную, п-хлорфенильную, ди- или полихлорфенилзамещенные группы, получаемые взаимодействием изопропилхлорформиата с соответствующим анилином, которые проявляют гербицидную активность [Патент США 273491, опубликован 14.02.1956.].
Известны эфиры общей формулы II, где R1 означает алкильную, бензильную, 2 - фенилэтильную, 3 - фенилпропильную группы, R2 и R3 - метильная или этильная группы обладают антиконвульсантной активностью [Tanaka М., Horisaka K., Yamagami С. et al. Quantitative Structure-Activity Relationships of Anticonvulsant Aralkyl and Alkyl Carbamates. // Chem. Pharm. Bull. - 1985. - V. 33, №6. - P. 2403-2410]. Синтез эфиров общей формулы II осуществлен из алифатических изоцианатов.
Таким образом, алифатические эфиры N-замещенной карбаминовой кислоты являются биологически активными веществами, а также применяются как полупродукты в органической химии.
Известны несколько способов синтеза N-арил-О-алкилкарбаматов. Основной промышленный способ использует в качестве исходных соединений ароматические изоцианаты [Arnold R.G., Nelson J.A., Verbanc J.J. Recent Advances in Isocyanate Chemistry. // Chem. Rev. - 1957. - V. 57, №1. - P. 47-76] или алкилхлорформиаты [Matzner M., Kurkjy P., Cotter R.J. The chemistry of Chlorformates. // Chem. Rev. - 1964. - Vol. 64. - P. 645-687]. Применение данных реагентов обеспечивает высокие выходы целевых уретанов.
Основным недостатком является использование фосгена для промышленного получения изоцианатов и хлорформиатов, которое приводит к увеличению затрат на охрану труда и окружающей среды. Кроме того, непроизводительный расход хлора обуславливает образование большого количества отходов, загрязненных токсичным фосгеном.
Наиболее известный бесфосгенный способ синтеза арилкарбаматов состоит в окислительном карбонилировании [Franz R.A., Applegaht F., Morriss F., Breed L. A new synthesis of ureas. V. The prepation of methyl-N-phenylurethane from carbon monooxide, sulfur, aniline and methanol // J. Org. Chem. - 1963. - V. 28. - №2. - P. 585-586; Kondo K., Sonoda N., Tsutsumi S. A new synthesis of carbamates. The reaction of carbon monooxide with amine and alcohol in the co-presence of selenium and trimethylamine // Chem. Lett. - 1972. - №5. - P. 373-374]. Процесс проводят при температуре 160-170°С и общем давлении СО и О2 ~ 10-500 атм, каталитическая система содержит селен, серу или соли благородных металлов.
Основным недостатком такой схемы производства является высокая токсичность оксида углерода (II), отсутствие способа регенерации гомогенных катализаторов на основе благородных металлов или селена, а также сложность аппаратурного оформления при проведении взаимодействия при высоких температурах и давлениях.
Заявлен способ получения N-алкил-О-алкилкарбаматов общей формулы I алкоголизом симметричных диалкилмочевин в непрерывном режиме в присутствии оловоорганических катализаторов [Патент РФ RU 2359958 C 2, заяв. 03.07.2007]. Данный способ позволяет получать целевые продукты с выходом 50-60% в расчете на загруженную мочевину.
Недостатком этого способа является необходимость использования катализатора, сложность его регенерации и трудность очистки целевых продуктов.
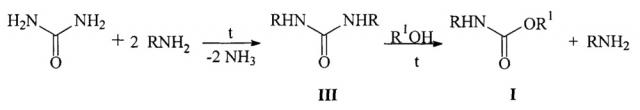
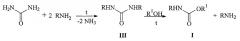
Наиболее близким по технической сущности и достигаемому результату способом синтеза заявленных N-арил-О-алкилкарбаматов является непрерывный алкоголиз симметричных диалкилмочевин с получением соответствующих N-алкил-О-алкилкарбаматов. В указанном патенте [патент США №2677698, 260-482, опубл. 04.05.1954] взаимодействием карбамида и алкиламина в непрерывном режиме получают 1,3-диалкилмочевину III, которую затем направляют в колонну, где она взаимодействует со спиртом с образованием уретана I.
В данном патенте представлена блочная технологическая схема производства разнообразных N-алкил-О-алкилкарбаматов и, в частности, N, O-диметилуретана, обеспечивающая утилизацию аммиака и регенерацию исходных компонентов. При этом основные реакционные узлы работают при температуре от 100°С до 200-250°С и давлении от атмосферного до автогенного. В работе не представлены примеры получения и характеристики целевых карбаматов.
Воспроизведение условий, описанных в данном патенте, при синтезе N-арилкарбаматов дает низкий выход целевых продуктов общей формулы I (не более 5%), что не пригодно для получения данных соединений в промышленных масштабах.
Задачей данного изобретения является повышение выхода N-арил-О-алкилкарбаматов общей формулы I, подбор оптимальных условий проведения процесса с целью избегания накопления побочных продуктов, исключение применения инертных растворителей, что обеспечивается осуществлением взаимодействия в среде расплавленного продукта реакции. Это упрощает очистку и выделение целевого карбамата и снижает энергозатраты, требуемые на регенерацию инертных растворителей.
Поставленная задача решается способом получения N-арил-О-алкилкарбаматов общей формулы I, где R означают арильные группы, R1 означают алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4, заключающегося в том, что осуществляют взаимодействие спирта R1OH и симметричной дизамещенной мочевины III, где R означают арильные группы, R1 означают алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4, в непрерывном режиме при атмосферном давлении в среде карбамата I при соотношении реагентов мочевина:алифатический спирт 1:(10÷60) мольн. и температуре от 140 до 250°С.
Отличие настоящего способа от известного заключается в проведении процесса при соотношениях реагентов мочевина:алифатический спирт 1:(10÷60) при 140-250°С. В качестве растворителя предлагается использовать продукт реакции - N-арил-О-алкилкарбамат.
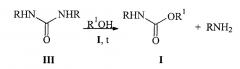
Таким образом, предлагается получать N-арил-О-алкилкарбаматы общей формулы I в колонне с насадкой и рубашкой для обогрева, работающей непрерывно. При этом сверху колонны предложено подавать питающий раствор диарилмочевины III, растворенной в расплавленном продукте реакции - N-арил-О-алкилкарбамате. Снизу колонны подаются пары спирта. В процессе взаимодействия избыток спирта уходит сверху колонны, а образующийся карбамат с растворенной в нем непрореагировавшей диарилмочевиной - снизу колонны. После охлаждения реакционной массы до температуры, превышающей температуру плавления карбамата на 15-20°С, непрореагировавшая диарилмочевина выпадает в осадок и ее отделяют от целевого продукта фильтрацией. Благодаря отсутствию побочных продуктов реакции и простоте отделения исходной диарилмочевины удается получить чистый N-арил-О-алкилкарбамат, не требующий дополнительный очистки. Таким способом целевые уретаны образуются с выходом 40-65% в расчете на загруженную мочевину и легко выделяются. При этом помимо продуктов взаимодействия реакционная масса содержит только непрореагировавшие исходные вещества, которые могут быть использованы повторно. При регенерации непрореагировавшей мочевины и возвращении ее в рецикл выход конечных карбаматов может быть увеличен до 90-98%.
Согласно настоящему изобретению, N-арил-О-алкилкарбаматы общей формулы I получают взаимодействием N,N'-диарилмочевины III с алифатическими спиртами в различных соотношениях мочевина: спирт 1:(10÷60), при температуре от 140 до 250°С.
В приведенной схеме R означают арильные группы, R1 означают алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4,
Изобретение может быть проиллюстрировано следующими примерами:
Пример 1. N-фенил-О-метилкарбамат
Процесс алкоголиза осуществляют в обогреваемой проточной колонне при температуре 220°С. Сверху колонны подают предварительно подогретый до 140°С раствор дифенилмочевины в N-фенил-О-метилкарбамате, в массовом соотношении 1 к 15-ти, соответственно. Снизу колонны, из испарителя подают пары метанола с такой скоростью, чтобы поддерживать его 30-кратный мольный избыток в колонне по отношению к дифенилмочевине. После прохождения раствора через колонну, его собирают снизу колонны и охлаждают до температуры 60°С. Отфильтровывают непрореагировавшую дифенилмочевину и фильтрат, представляющий собой практически чистый продукт, кристаллизуют путем охлаждения. Выход N-фенил-О-метилкарбамата в пересчете на загруженную дифенилмочевину составляет 65%. Т пл=43-44°С. ЯМР 1Н спектр (δ, м.д.; J, Гц) (400 МГц в CDCl3): 3.76 (3Н; s; СН3-О); 6.79 (1Н; s; -NH-); 7.06 (1H; t; 8.5 Гц; p-H-Ph); 7.30 (2Н; dd; 8.5 Гц, 7.9 Гц; m-H-Ph); 7.38 (2Н; d; 7.9 Гц; o-H-Ph).
Пример 2. N-фенил-О-метилкарбамат
Процесс алкоголиза осуществляют в обогреваемой проточной колонне при температуре 140°С. Сверху колонны подают предварительно подогретый до 140°С раствор дифенилмочевины в N-фенил-О-метилкарбамате, в массовом соотношении 1 к 1, соответственно. Снизу колонны, из испарителя подают пары метанола с такой скоростью, чтобы поддерживать его 40-кратный мольный избыток в колонне по отношению к дифенилмочевине. После прохождения раствора через колонну, его собирают снизу колонны и охлаждают до температуры 60°С. Отфильтровывают непрореагировавшую дифенилмочевину и фильтрат, представляющий собой практически чистый продукт, кристаллизуют путем охлаждения. Выход N-фенил-О-метилкарбамата в пересчете на загруженную дифенилмочевину составляет 35%. Т пл=43-44°С. ЯМР 1Н спектр (δ, м.д.; J, Гц) (400 МГц в CDCl3): 3.76 (3Н; s; СН3-О); 6.79 (1Н; s; -NH-); 7.06 (1H; t; 8.5 Гц; p-H-Ph); 7.30 (2H; dd; 8.5 Гц, 7.9 Гц; m-H-Ph); 7.38 (2H; d; 7.9 Гц; o-H-Ph).
Пример 3. N-фенил-О-этилкарбамат
Процесс алкоголиза осуществляют в обогреваемой проточной колонне при температуре 200°С. Сверху колонны подают предварительно подогретый до 160°С раствор дифенилмочевины в N-фенил-О-этилкарбамате, в массовом соотношении 1 к 10-ти, соответственно. Снизу колонны, из испарителя подают пары этанола с такой скоростью, чтобы поддерживать его 20-кратный мольный избыток в колонне по отношению к дифенилмочевине. После прохождения раствора через колонну, его собирают снизу колонны и охлаждают до температуры 70°С. Отфильтровывают непрореагировавшую дифенилмочевину и фильтрат, представляющий собой практически чистый продукт, кристаллизуют путем охлаждения. Выход N-фенил- О-этилкарбамата в пересчете на загруженную дифенилмочевину составляет 52%. Т пл=49-51°С. ЯМР 1Н спектр (δ, м.д.; J, Гц) (400 МГц в CDCl3): 1.29 (3Н; t; 7.1 Гц, CH3-(Et)); 4.21 (2Н; q; 7.1 Гц, CH2-O); 6.74 (1Н; s; -NH-); 7.02-7.46 (5H; m; Harom).
Пример 4. N-(3-хлорфенил)-О-изопропилкарбамат
Процесс алкоголиза осуществляют в обогреваемой проточной колонне при температуре 250°С. Сверху колонны подают предварительно подогретый до 200°С раствор ди-(3-хлорфенил)-мочевины в М-(3-хлорфенил)-O-изопропилкарбамате, в массовом соотношении 1 к 20-ти, соответственно. Снизу колонны, из испарителя подают пары изопропанола с такой скоростью, чтобы поддерживать его 60-кратный мольный избыток в колонне по отношению к ди-(3-хлорфенил)-мочевине. После прохождения раствора через колонну его собирают снизу колонны и охлаждают до температуры 60°С. Отфильтровывают непрореагировавшую ди-(3-хлорфенил)-мочевину и фильтрат, представляющий собой практически чистый продукт, кристаллизуют путем охлаждения. Выход N-(3-хлорфенил)-O-изопропилкарбамата в пересчете на загруженную дифенилмочевину составляет 35%. Т пл=40-41°С. ЯМР 1Н спектр (δ, м.д.; J, Гц) (400 МГц в CDCl3): 1.30 (6Н; d; 6.2 Гц, CH3-(iPr)); 5.02 (1Н; sep; 6.2 Гц, CH-O); 6.62 (1Н; s; -NH-); 7.02 (1H; d; 4.4 Гц, H4arom); 7.20 (2Н, m, Н5,6arom); 7.51 (1H, s, Н2-arom).
Пример 5. N-(4-хлорфенил)-O-бутилкарбамат
Процесс алкоголиза осуществляют в обогреваемой проточной колонне при температуре 250°С. Сверху колонны подают предварительно подогретый до 250°С раствор ди-(4-дихлорфенил)мочевины в N-(4-хлорфенил)-O-бутилкарбамате, в массовом соотношении 1 к 20-ти, соответственно. Снизу колонны, из испарителя подают пары бутанола с такой скоростью, чтобы поддерживать его 10-кратный мольный избыток в колонне по отношению к ди-(4-дихлорфенил)мочевине. После прохождения раствора через колонну, его собирают снизу колонны и охлаждают до температуры 80°С. Отфильтровывают непрореагировавшую ди-(4-дихлорфенил)мочевину и фильтрат, представляющий собой практически чистый продукт, кристаллизуют путем охлаждения. Выход М-(4-хлорфенил)-О-бутилкарбамата в пересчете на загруженную дифенилмочевину составляет 42%. Т пл=71-73°С. ЯМР 1Н спектр (δ, м.д.; J, Гц) (400 МГц в CDCl3): 0.95 (3Н, t, 7.6 Гц), 1.46-1.36 (2Н, m), 1.69-1.61 (2Н, m), 4.16 (2Н, t, 6.8 Гц), 6.61 (1Н, br. s), 7.26 (2Н, d, 8.8 Гц), 7.33 (2Н, d, 8.0 Гц)
Таким образом, разработан экологически безопасный, малоотходный и пригодный для промышленности эффективный способ получения N-арил-О-алкилкарбаматов общей формулы I алкоголизом симметричных диарилмочевин с выходом 35-65%) на загруженную мочевину без учета ее рецикла.
Способ получения N-арил-О-алкилкарбаматов общей формулы I
,
где R означает арильные группы, R1 означает алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4, заключающийся в том, что осуществляют взаимодействие спирта R1OH и симметричной дизамещенной мочевины II, где R означает арильные группы, a R1 означает алкильные группы нормального или разветвленного строения с числом атомов углерода от 1 до 4, в непрерывном режиме при атмосферном давлении в среде карбамата I при соотношении реагентов мочевина:алифатический спирт=1:(10÷60) мольн. и температуре от 140 до 250°C.