Катетерный баллон
Иллюстрации
Показать всеИзобретение относится к катетерному баллону, покрытие которого состоит из паклитаксела и по меньшей мере одного адъюванта, выбранного из группы, включающей трибутилцитрат, триэтилцитрат и их ацетилированные производные. Изобретение обеспечивает немедленное высвобождение антипролиферативного агента в течение короткого интервала времени, составляющего от 30 до 60 секунд. 2 з.п. ф-лы, 10 ил., 4 табл., 24 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к медицинскому оборудованию, в частности к катетерным баллонам, в том числе с насаженными на них стентами, по меньшей мере, с одним слоем, который содержит антипролиферативные, иммунодепрессантные, противовоспалительные, фунгицидные и/или антитромботические агенты, а также к способу изготовления указанного медицинского оборудования и к их применению для предотвращения рестеноза.
Уровень техники
В организме человека кровь соприкасается с внутренней поверхностью кровеносных сосудов и только в случае травмы контактирует с другими поверхностями. Система свертывания крови активируется во всех случаях, когда кровь контактирует с чужеродными поверхностями, чтобы остановить кровотечение и предотвратить угрожающую жизни кровопотерю. Поскольку имплант тоже представляет собой чужеродную поверхность, всем пациентам с введенным имплантом, который длительное время контактирует с кровью, вводят так называемые антикоагулянты, которые препятствуют свертыванию крови, при этом часто возникают побочные эффекты.
Одним из факторов риска при использовании вставки в сосуд, - так называемого стента, - является описанный риск возникновения тромбоза в кровеносных сосудах. Стент предназначен для поддержания сосуда в открытом состоянии при возникновении сужений и закупорки сосудов, например, вследствие атеросклеротических бляшек, прежде всего, коронарных сосудов сердца. Как правило, стент получают из высококачественной медицинской стали, сплавов Ni-Ti или сплавов Со-Cr, тогда как стенты на основе полимерных материалов находятся на стадии разработки. Уже при введении катетера может развиться так называемый ранний тромбоз, который составляет менее одного процента случаев, и от двух до пяти процентов случаев ранний тромбоз развивается во время пребывания в больнице. Приблизительно в пяти процентах случаев повреждения сосудов возникают из-за перекрытия артерий, а также существует рискформирования псевдоаневризмы сосудов, причиной которой является расширение сосуда.
Таким образом, введение чужеродного тела при проведении баллонной ангиопластики (PTKA) провоцирует активацию механизмов свертывания крови. Так как в указанном случае имплант вводят на короткое время, основная проблема заключается в степени дилатации сосуда, необходимой для устранения сужения или закупорки сосуда. Другим, наиболее часто возникающим осложнением, является рестеноз - повторная закупорка сосуда. Несмотря на то, что стенты снижают риск повторной закупорки сосуда, до настоящего времени не удается полностью предотвратить развитие рестеноза, а также гиперплазию неоинтимы.
Повторное сужение сосуда (рестеноз) после имплантации стента или использования катетерного баллона при наиболее тяжелых формах заболеваний возникает в 30% случаев, что является основной причиной повторной госпитализации пациента. Так как повторная закупорка сосуда после баллонной ангиопластики (ПТКА) происходит значительно чаще по сравнению с имплантацией стента, то при лечении пациентов с тяжелой формой стеноза или рестеноза, как правило, применяют стент.
Точные причины развития рестеноза в специальной литературе не описаны. Чаще всего для морфологического определения рестеноза используют рестеноз после успешной ЧТА (чрескожная транслюминальная ангиопластика), когда уменьшение диаметра сосуда составляет менее 50% от нормы. При этом речь идет об эмпирически принятой величине, которая определена без учета гемодинамики и взаимосвязи клинической симптоматики с прочной научной базой. На практике в большинстве случаев ухудшение состояния пациента рассматривается как признак рестеноза обработанного участка сосуда.
Повреждения сосудов, возникающие во время имплантации стента или при перерастяжении сосудов вследствие использования катетерного баллона, приводят к возникновению воспалительных реакций, которые в первые семь дней играют решающую роль для процесса выздоровления. Протекающие при этом процессы сопровождаются высвобождением факторов роста, начинается усиленная пролиферация клеток гладкой мускулатуры, что уже в короткий срок приводит к рестенозу, повторной закупорке сосуда из-за неконтролируемого роста клеток.
Если стент в ткани сосуда через несколько недель полностью покрывается гладкомышечными клетками сосуда, существует большой риск рубцевания (гиперплазия неоинтимы), что может привести к тому, что гладкомышечными клетками покрывается не только поверхность стента, но и закупоривается его внутренняя полость.
Было предпринято несколько неудачных попыток решить проблему рестеноза за счет создания микропористых, высвобождающих гепарин баллонов катетеров, а также стентов с покрытием, содержащим гепарин (J.Whorle и др., European Heart Journal, 2001, 22:1808-16). Это связано с тем, что гепарин проявляет свойства антикоагулянта только в растворе. Указанную проблему можно почти полностью устранить медикаментозным способом с использованием антикоагулянтов. В качестве другого подхода для решения указанной проблемы в настоящее время был исследован метод, основанный на локальном подавлении роста гладкомышечных клеток.
Были исследованы стенты, содержащие радиоактивные агенты, или стенты, содержащие фармацевтически активные вещества, которые оказывают антипролиферативное действие. Наиболее эффективным средством является химиотерапевтический препарат, паклитаксел, который останавливает клетки в фазе митоза за счет необратимого связывания с формирующимся митотическим веретеном, таким образом подавляя деление клеток. Клетки остаются в переходной фазе и погибают.
Известно, что применение стентов, содержащих паклитаксел, в отличие от стентов без покрытия приводит впоследствии к повышению интенсивности тромбоза, т.е. к отрицательному действию паклитаксела. Необратимое связывание и стабилизация тубулина во время деления клетки приводит к тому, что клетки не могут выполнять другие свои функции и погибают.
Предполагали, что можно использовать паклитаксел для контроля процесса ранозаживления, однако при его введении происходит образование нежизнеспособных клеток и, следовательно, наблюдается нежелательная воспалительная реакция и усиление иммунного ответа.
Контроль дозировки паклитаксела связан с множеством проблем при использовании паклитаксела для подавления процессов ранозаживления. Высокие дозы указанного соединения вызывают воспалительные процессы, а малые дозы не эффективны. В связи с тем, что необходимо учитывать два указанных условия, требуемый слой эндотелия на стенте не образуется даже в течение полугода.
Либо стент находится в незакрепленном состоянии, что сопряжено с высоким риском возникновения тромбоза у пациентов даже через несколько месяцев после имплантации (поздний острый тромбоз) и, как следствие, к летальному исходу, либо на стенте образуется слой из гладкомышечных клеток, моноцитов и т.д., что через некоторое время может привести к закупорке сосуда.
Наиболее эффективным средством для профилактики рестеноза является рапамицин (сиролимус), гидрофильный макролид-антибиотик. Указанный препарат применяют, прежде всего, в трансплантации в качестве иммунодепрессанта, причем рапамицин, в отличие от других иммунодепрессантов, ингибирует опухоль. После трансплантации у пациента повышается риск развития опухоли. Введение рапамицина является предпочтительным, так как другие иммунодепрессанты, например циклоспорин A, как известно, могут вызывать развитие опухоли.
К настоящему моменту действие рапамицина подробно не изучено, но установлено, что рапамицин образует комплекс с белком mTOR (мишень рапамицина млекопитающих), фосфатидилинозит-3-киназой с ММ 282 кДа. Белок mTOR участвует в различных цитокин-опосредованных путях передачи сигнала, в том числе сигнальных путях деления клетки и обладает кроме иммунодепрессантных свойств, противовоспалительными, антипролиферативными и фунгицидными свойствами.
Название согласно номенклатуре ИЮПАК - моногидрат [3S-[3R*[E(1S*,3S*,4S*)])4S*,5R*,8S*,9E,12R*,14R*,15S*,16R*,18S*,19S*,26aR*]]-5,6,8,11,12,13,14,15,16,17,18,19,24,25,26,26a-гексадекагидро-5,19-дигидрокси-3-[2-(4-гидрокси-3-метоксициклогексилН-метилэтинил3-М.Тб-диметокси-4,10,12,18-тетраметил-8-(2-пропенил)-15,19-эпокси-3H-пиридо[2,1-c][1,4]оксаазациклотрикозин-1,7,20,21 (4Н,23Н)тетрона.
Пролиферация клеток прекращается вследствие нарушения синтеза рибосомальноых белков в поздней фазе G1. Следует, прежде всего, отметить, что по сравнению с другими антипролиферативными препаратами, рапамицин оказывает действие, аналогичное действию сильно гидрофобного паклитаксела. Кроме того, предпочтительное преимущество рапамицина заключается в том, что он проявляет иммунодепрессантное и противовоспалительное действие, что способствует снижению воспалительных реакций и общего иммунного ответа, прежде всего, в начальный период после имплантации стента.
Таким образом, рапамицин удовлетворяет всем необходимым требованиям для предотвращения стеноза и рестеноза.
Другое преимущество рапамицина по сравнению с паклитакселом заключается в его ограниченной стабильности, т.е. рапамицин на поверхности или в составе имплантанта проявляет требуемую активность в течение первых недель после имплантации стента. В результате на поверхности стента образуется сплошной слой клеток эндотелия, таким образом, процесс ранозаживления завершается внедрением стента в структуру сосуда. Известные производные рапамицина (биолимус, эверолимус), содержащие функциональные группы, которые не влияют на связывание с mTOR, характеризуются аналогичным механизмом действия.
В ходе различных клинических испытаний (RAVEL, SIRIUS, SIROCCO) было установлено, что по сравнению с другими лекарственными средствами, например дексаметазоном, такролимусом, батимастатом и сильно гидрофобным паклитакселом, рапамицин является наиболее эффективным средством для предотвращения рестеноза в связи с другими физическими свойствами.
Само по себе применение активного агента не всегда обеспечивает эффективность профилактики рестеноза. Стент, высвобождающий активные агенты, должен удовлетворять ряду требований. Кроме того, что стент должен обеспечивать дозировку активного агента, он должен обеспечивать замедленное и контролируемое высвобождение. Время и скорость высвобождения активного агента зависят не только от физических и химических свойств активного агента, но и от свойств используемого полимера, а также от взаимодействия полимера с активным агентом. Материал стента, свойства стента и его конструкция являются важными факторами, которые следует учитывать при изготовлении медицинского изделия с улучшенными характеристиками.
В патенте EP 0950386 B1 описан стент с распорками (ячейками сетчатой структуры), в которых рапамицин содержится под полимерным слоем, контролирующим диффузию рапамицина. В патенте EP 1407726 A1 (первая заявка подана в 1998 г.) описан стент, высвобождающий рапамицин из полимерной матрицы (Cypher™ Stent, коммерчески доступный с 2002). Указанное медицинское изделие представляет собой стент, на который нанесено покрытие из парилена С и смеси двух биостабильных полимеров, полиэтиленвинилацетата (ПЭВА) и поли-н-бутилметилметакрилата (ПБМА) и рапамицина, при этом верхний слой из ПБМА обеспечивает контролируемое высвобождение лекарственного средства посредством диффузии. При испытаниях указанного стента было установлено, что после имплантации стента возникают значительные проблемы: развиваются аллергические реакции, воспалительные процессы, а также поздние тромбозы (работа проф. Renu Virmani, 2002). Кроме этого, было установлено, что после набухания наружный слой из ПБМА разрушается, что приводит к неконтролируемому высвобождению рапамицина (см. фиг.1).
Более того, при применении рапамицина возникает еще одна проблема. Рапамицин является гидрофильным соединением и быстро переходит в раствор, поэтому трудно контролировать его биодоступность. Как только разрушается наружный слой, контролирующий диффузию, высвобождение рапамицина становится быстрым и неконтролируемым.
Так как ПМБА является недостаточно эластичным материалом, существует риск отслаивания больших полимерных фрагментов, а в связи с тем, что ПМБА характеризуется высокой биостабильностью (см. фиг.2), возможно нарушение кровотока.
В патенте EP 0568310 B1 описана комбинация активных агентов, которая включает гепарин и рапамицин, предназначенная для лечения гиперпролиферативных сосудистых заболеваний. В указанном патенте коротко описан сосудистый стент, пропитанный указанной комбинацией активных агентов. Однако примеры осуществления изобретения не представлены и обсуждаются только общие представления об изделии. Патент опубликован в 1992 году, однако до настоящего времени выпускается только стент, описанный в EP 1407726 A1, т.е. стент Cypher™ (фирмы Cordis Corp). Таким образом, не описано получение экономически выгодного продукта, т.е. стентов, пропитанных рапамицином и гепарином, и цель, поставленная в указанных патентах, в действительности не достигнута.
В патенте EP 0551182 В1 описаны стенты, которые пропитаны рапамицином, предназначенные для профилактики или предотвращения гиперпролиферативных заболеваний, возникающих вследствие механических повреждений. В указанном патенте также описан пропитанный рапамицином стент, который предназначен для введения рапамицина в сосуд, однако подробное описание не представлено. Пропитанный рапамицином стент представляет собой чистый слой активного агента, нанесенный на каркас стента, без использования дополнительного носителя. Так как рапамицин на воздухе быстро гидролизуется и теряет свои свойства из-за расщепления лактоновых связей, прежде всего, в присутствии воды, указанный вариант осуществления изобретения сложно реализовать на практике.
Кроме этого, при введении баллона катетера, покрытого слоем рапамицина, или баллона со стентом, покрытым рапамицином, активный агент быстро высвобождается в кровоток и, следовательно, невозможно обеспечить требуемый уровень высвобождения рапамицина из медицинского изделия (баллона или стента). В качестве недостатка слоя, содержащего только активный агент без дополнительного носителя, следует отметить, что при дилатации активный агент полностью высвобождается в течение короткого периода времени, так как отсутствует слой, высвобождающий активный агент, в форме системы с замедленным высвобождением, поэтому происходит спонтанное высвобождение активного агента и невозможно воспользоваться преимуществами кинетики высвобождения.
Таким образом, настоящее изобретение не относится к получению стентов или баллонов катетеров с покрытием, содержащим рапамицин, а также к применению рапамицина для профилактики или предотвращения рестеноза, которые уже известны в предшествующем уровне техники. Настоящее изобретение относится к оптимизированной системе носителя для чувствительного рапамицина.
Как указано выше, не каждый активный агент будет проявлять эффективность при профилактике рестеноза. Независимо от типа имплант без специального покрытия для его длительного, эффективного использования и обеспечения безопасности пациента, имплант должен отвечать ряду требований. При этом следует учитывать физико-химические свойства используемых активных агентов, растворителя и носителя, а также взаимное влияние указанных факторов друг на друга.
При оптимизации указанных параметров можно эффективно контролировать дозу и скорость высвобождения лекарственного средства, что обеспечивает безопасность и выздоровление пациента.
Настоящее изобретение относится к получению стентов и баллонов катетеров, высвобождающих рапамицин, применение которых обеспечивает контролируемый и стабильный процесс лечения, позволяет полностью восстановить эндотелий стенки сосуда, без вышеописанных осложнений.
Таким образом, целью настоящего изобретения является получение оптимальной системы носителя для рапамицина, которую можно наносить на стент, то есть на опору сосуда или баллон катетера, а также стент и баллон катетера, на который установлен стент, и указанная система носителя характеризуется удовлетворительной адгезией и обеспечивает стабильное высвобождение рапамицина и требуемую кинетику высвобождения активного агента, что значительно повышает эффективность профилактики и предотвращения рестеноза.
При этом вследствие антипролиферативного, иммунодепрессантного и противовоспалительного действия рапамицина, его производных/аналогов и/или метаболитов, характеризующихся аналогичной активностью, подавление клеточных реакций предпочтительно происходит в первые дни и недели после имплантации. Дальнейшее ранозаживление или соответственно эффективность процесса ранозаживления достигается за счет оптимизации режима высвобождения активного агента и/или комбинации, содержащей активные агенты.
Указанная цель достигается согласно техническому решению, как определено в независимых пунктах формулы настоящего изобретения. Другие предпочтительные признаки изобретения определены в зависимых пунктах формулы изобретения, а также в описании и примерах.
Раскрытие изобретения
Катетерные баллоны или стенты по настоящему изобретению содержат один, два или более слоя, причем по меньшей мере один слой, содержащий рапамицин или активную комбинацию рапамицина и других совместимых с рапамицином и/или синергетически действующих агентов, наносят без полимерного носителя.
Рапамицин или активная комбинация рапамицина присоединены к расположенному снизу слою или к внешней поверхности стента или катетерного баллона ковалентно и/или с помощью адгезива включены в слой таким образом, чтобы обеспечивать непрерывное высвобождение активного соединения в незначительных дозах и в то же время обеспечить прорастание клеток в поверхность стента и при этом исключить избыточное прорастание. Комбинация обоих признаков придает стенту по изобретению способность быстро врастать в стенки сосуда и позволяет снизить риск развития рестеноза и тромбоза. Контролируемое высвобождение рапамицина происходит за период от 1 до 12 месяцев, предпочтительно в течение 1-2 месяцев после имплантации.
В вариантах осуществления настоящего изобретения рапамицин используют также в комбинации с другими активными агентами. В качестве антипролиферативных средств, средств против миграции клеток, антиангиогенных, противовоспалительных, цитостатических, цитотоксических и/или антитромботических активных агентов, которые усиливают действие рапамицина и/или его химических, а также биологических производных, можно использовать следующие средства: соматостатин, такролимус, рокситромицин, даунамицин, аскомицин, бафиломицин, эритромицин, мидекамицин, джозамицин, конканамицин, кларитромицин, тролеандомицин, фолимицин, церивастатин, симвастатин, ловастатин, флувастатин, розувастатин, аторвастатин, правастатин, питавастатин, винбластин, винкристин, виндезин, винорелбин, этопозид, тенипозид, нимустин, кармустин, ломустин, циклофосфамид, 4-гидроксиоксициклофосфамид, эстрамустин, мелфалан, ифосфамид, трофосфамид, хлорамбуцил, бендамустин, дакарбазин, бусулфан, прокарбазин, треосульфан, тремозоломид, тиотепа, даунорубицин, доксорубицин, акларубицин, эпирубицин, митоксантрон, идарубицин, блеомицин, митомицин, дактиномицин, метотрексат, флударабин, флударабин-5'-дигидрофосфат, кладрибин, меркаптопурин, тиогуанин, цитарабин, фторурацил, гемцитабин, капецитабин, доцетаксел, карбоплатин, цисплатин, оксалиплатин, амсакрин, иринотекан, топотекан, гидроксикарбамид, милтефозин, пентостатин, алдеслейкин, третиноин, аспарагиназа, пегаспараза, анастрозол, экземестан, летрозол, форместан, аминоглутетимид, адриамицин, азитромицин, спирамицин, цифарантин, 8-а-эрголин, диметилэрголин, агроклавин, 1-аллилсурид, 1-аллилтергурид, бромергурид, бромокриптин (2-бром-12'-гидрокси-2'-(1 -метилэтил)-5'-(2-метил пропил)-(5'альфа)-эрготаман-3',6',18-трион), элимоклавин, эргокристин (12'-гидрокси-2'-(1-метил этил)-5'-(фенил метил)-(5'альфа)-эрготаман-3', 6', 18-трион), эргокристинин, эргокорнин (12'-гидрокси-2',5'-бис(1-метилэтил)-(5'альфа)-эрготаман-3',6',18-трион), эргокорнинин, эргокриптин (12'-гидрокси-2'-(1-метилэтил)-5'-(2-метилпропил)-, (5'альфа)-эрготаман-З',6',18-трион, (9Cl)), эргокриптинин, эргометрин, эргоновин (эргобазин, МНН: эргометрин, (8бета(8))-9,10-дидегидро-N-(2-гидрокси-1-метилэтил)-6-метилэрголин-8-карбоксамид), эргозин, эргозинин, эрготметринин, эрготамин(12'-гидрокси-2'-метил-5'-(фенилметил)-(5'альфа)-эрготаман-3',6',18-трион, (9Cl)), эрготаминин, эрговалин (12'-гидрокси-2'-метил-5'-(1-метилэтил)-(5'альфа)-эрготаман-3',6',18-трион), лерготрил, лизурид (номер по каталогу 18016-80-3, 3-(9,10-дидегидро-6-метилэрголин-8альфа-ил)-1,1-диэтилмочевина), лизергол, лизергиновая кислота (D-лизергиновая кислота), амид лизергиновой кислоты (LSD, амид D-лизергиновой кислоты), диэтиламидлизергиновой кислоты (LSA, диэтиламид D-лизергиновой кислоты, МНН: лизергамид, (8бета)-9,10-дидегидро-N,N-диэтил-6-метилэрголин-8-карбоксамид), изолизергиновая кислота (D-изолизергиновая кислота), амид изолизергиновой кислоты (амид D-изолизергиновой кислоты), диэтиламид изолизергиновой кислоты (диэтиламид D-изолизергиновой кислоты), мезулергин, метерголин, метергин (МНН: метилергометрин, (8бета(5))-9,10-дидегидро-N-(1-(гидроксиметил)пропил)-6-метилэрголин-8-карбоксамид), метилэргометрин, метисергид (МНН: метисергид, (8бета)-9,10-дидегидро-N-(1-(гидроксиметил)пропил)-1,6-диметилэрголин-8-карбоксамид), перголид((8бета)-8-((метилтио)метил)-6-пропилэрголин), протергурид и тергурид, целекоксиб, талидомид, фасудил, циклоспорин, SMC пролиферативный ингибитор-2w, эпотилон A и B, митоксантрон, азатиоприн, микофенолатмофетил, антисенсибилизатор c-myc, антисенсибилизатор b-myc, бетулиновая кислота, камфотецин, PI-88 (сульфатированный олигосахарид), меланоцитостимулирующий гормон (α-MSH), активированный белок C, IL1-β-ингибитор, тимозин α-1, фумаровая кислота и ее эфиры, кальципотриол, такальцитол, лапахол, β-лапахон, подофиллотоксин, бетулин, 2-этилгидразид подофилловой кислоты, молграмостин (rhuGM-CSF), пэгинтерферон α-2b, ланограстим (r-HuG-CSF), филграстим, макрогол, дакарбазин, базиликсимаб, даклизумаб, селектин (антагонист цитокина), ингибитор СЕТР, кадхерин, ингибиторы цитокининов, ингибитор COX-2, NFkB, ангиопептин, ципрофлоксацин, камфотецин, флуробластин, моноклональные антитела, которые ингибируют пролиферацию мышечных клеток, антагонисты bFGF, пробукол, простагландины, 1,11-диметоксикантин-6-он, 1-гидрокси-11-метоксикантин-6-он, скополектин, колхицин, доноры N0, такие как пентаэритритолтетранитрат и сиднонимины, S-нитрозопроизводные, тамоксифен, стауроспорин, β-эстрадиол, α-эстрадиол, эстриол, эстрон, этинилэстрадиол, фосфестрол, медроксипрогестерон, эстрадиолципионат, бензоаты эстрадиола, траниласт, камебакаурин и другие терпеноиды, которые используют при лечении рака, верапамил, ингибиторы тирозинкиназы (тирфостины), циклоспорин A, паклитаксел и его производные, такие как 6-α-гидроксипаклитаксел, баккатин, таксотер, синтетические макроцикл ические олигомеры субоксидов углерода (MCS) и его производные, полученные из природных материалов, мофебутазон, ацеметацин, диклофенак, лоназолак, дапсон, орто-карбамоилфеноксиуксусная кислота, лидокаин, кетопрофен, мефенамовая кислота, пироксикам, мелоксикам, фосфат хлорохина, фенициламин, тумстатин, авастин, D-24851, SC-58125, гидроксихлорохин, ауранофин, ауротиомалат натрия, оксацепрол, целекоксиб, β-ситостерин, адеметионин, миртекаин, полидоканол, нонивамид, левоментол, бензокаин, аэсцин, эллиптицин, D-24851 (Calbiochem), колцемид, цитохалазин A-E, инданоцин, нокадазол, белок S 100, бацитрацин, антагонисты рецептора витронектина, азеластин, стимулятор гуанидилциклазы, тканевой ингибитор металпротеиназы-1 и -2, свободные нуклеиновые кислоты, нуклеиновые кислоты, включенные в вирусные векторы, фрагменты ДНКи РНК, ингибитор-1 плазминогенного активатора, ингибитор-2 плазминогенного активатора, антисмысловые олигонуклеотиды, ингибиторы VEGF, IGF-1, активные агенты из группы антибиотиков, такие как цефадроксил, цефазолин, цефаклор, цефотиксин, тобрамицин, гентамицин, пенициллины, такие как диклоксациллин, оксациллин, сульфонамид, метронидазол, антитромботические средства, такие какаргатробан, аспирин, абсиксимаб, синтетический антитромбин, бивалирудин, коумадин, эноксопарин, десульфатированный и N-реацетилированный гепарин, тканевой активатор плазминогена, рецептор GpIIb/IIIa мембраны тромбоцитов, антитела против ингибитора фактора Xa, ингибитор интерлейкина, гепарин, гирудин, r-гирудин, РРАСК, протамин, натриевая соль 2-метилтиазолидин-2,4-дикарбоновой кислоты, проурокиназа, стрептокиназа, варфарин, урокиназа, сосудорасширяющие средства, такие как дипирамидол, трапидил, нитропруссиды, антагонисты PDGF, такие кактриазолопиримидин и серамин, ингибиторы АКФ, такие как каптоприл, цилазаприл, лизиноприл, эналаприл, лосартан, ингибиторы тиопротеазы, простациклин, вапипрост, интерферон α, β и γ, антагонисты гистамина, блокаторы серотонина, ингибиторы апоптоза, регуляторы апоптоза, такие как р65, антисмысловые олигонуклеотиды NF-kB или Bcl-xL, галофугинон, нифедипин, токоферол, витамин В1, В2, В6 и В12, фолиевая кислота, траниласт, молсидомин, полифенолы из чая, эпикатехингаллат, эпигаллокатехингаллат, босвеллиновая кислота и ее производные, лефлуномид, анакинра, этанерцепт, сульфасалазин, этопозид, диклоксациллин, тетрациклин, триамцинолон, мутамицин, прокаинимид, D24851, SC-58125, ретиноловая кислота, хинидин, дизопиримид, флекаинид, пропафенон, сотолол, амидорон, природные и синтетические стероиды, такие как бриофиллин A, инотодиол, маквирозид A, галакинозид, мансонин, стреблозид, гидрокортизон, бетаметазон, дексаметазон, нестероидные противовоспалительные препараты (НПВП), такие как фенопрофен, ибупрофен, индометацин, напроксен, фенилбутазон и другие противовирусные агенты, такие как ацикловир, ганцикловир и зидовудин, противогрибковые агенты, такие какклотримазол.флуцитозин, гризеофулвин, кетоконазол, миконазол, нистатин, тербинафин, антипротозойные агенты, такие какхлорохин, мефлохин, хинин, а также природные терпеноиды, такие как гиппоцискулин, баррингтогенол-С21-ангелат, 14-дегидроагростистахин, агроскерин, агростистахин, 17-гидроксиагростистахин, оватодиолиды,4,7-оксициклоанизомеловая кислота, бакхариноиды В1, В2, B3 и В7, тубеимозид, бруцеанол A, B и C, бруцеантинозид С, яданзиозиды N и Р, изодеоксиэлефантопин, томенфантопин A и B, коронарин A, B, C и D, урсоловая кислота, гиптатовая кислота А, зеорин, изоиридогерманал, мэйтенфолиол, эффусантин A, эксцисанин A и B, лонгикаурин В, скулпонеатин C, камебаунин, лейкаменин A и B , 13,18-дегидро-6-α-сенециоилоксихапаррин, таксамаирин A и B, регенилол, триптолид, цимарин, апоцимарин, аристолоховая кислота, аноптерин, гидроксианоптерин, анемонин, протоанемонин, берберин, хлорид хелибурина, циктоксин, синококулин, бомбрестатин A и B, кудраизофлавон A, куркумин, дигидронитидин, нитидинхлорид, 12-бета-гидроксипрегнадиен-3,20-дион, билобол, гинкгол, гинкголевая кислота, хеленалин, индицин, индицин-N-оксид, лазиокарпин, инотодиол, гликозид 1a, подофиллотоксин, джастицидин A и B, ларреатин, маллотерин, маллотохроманол, изобутирилмаллотохроманол, маквирозидА, мархантин A, мэйтанзин, ликоридицин, маргетин, панкратистатин, лириоденин, оксоушинзунин, аристолактам-AII, биспартенолидин, периплокозид A, галакинозид, урсоловая кислота, деоксипсороспермин, психорубин, рицин A, сангуинарин, кислоты из пшеницы, метилсорбифолин, спателиахромен, стизофиллин, мансонин, стреблозид, акагерин, дигидроусамбарензин, дигидроксиусамбарин, стрихнопентамин, стрихнофиллин, усамбарин, усамбарензин, берберин, лириоденин, оксоушинсунин, дафноретин, ларицирезинол, метоксиларицирезинол, сирингарезинол, умбеллиферон, афромозон, ацетилвисмион B, дезацетилвисмион A, висмион A и B, и сера-содержащие аминокислоты, такие как цистеин, а также соли, гидраты, сольваты, энантиомеры, рацематы, энантиомерные смеси, диастереомерные смеси, метаболиты и смеси указанных выше активных агентов.
Активные агенты используют в отдельности или в смеси в равной или различной концентрации. Прежде всего, предпочтительно используют активные агенты, которые кроме антипролиферативной активности проявляют другие свойства. Кроме того, предпочтительной является комбинация со следующими активными агентами: такролимус, паклитаксел и его производные, фазудил, антагонисты рецептора витронектина, талидомид, циклоспосрин A, тергурид, лизурид, целекоксиб, соединения R-лизина и их производные/аналоги, а также активные метаболиты. Прежде всего, предпочтительной является комбинация рапамицина с тергуридом или рапамицина с лизуридом или рапамицина с паклитакселом или рапамицина с иммунодепрессантом, таким как циклоспорин A. Прежде всего, предпочтительной является комбинация рапамицина с паклитакселом, производными паклитаксела, прежде всего гидрофильными производными паклитаксела, эпотилона, тергурида или лизурида.
Предпочтительная фармацевтически активная концентрация активного агента составляет от 0,001 до 10 мг/см2 внешней поверхности стента. Другие активные агенты могут содержаться в аналогичной концентрации в одном и том же слое или в других слоях, причем предпочтительно, чтобы другие активные агенты содержались в других слоях в отличие от слоя с рапамицином.
Полимеры
Если активный агент или комбинацию активных агентов наносят не напрямую на поверхность стента или не напрямую включают в стент, то кроме обработки поверхности стента пригодными синтетическими, полусинтетическими и/или природными гемосовместимыми соединениями, в качестве носителя или матрицы можно использовать биостабильные и/или биодеградабельные полимеры или полисахариды.
В качестве биологически стабильных полимеров, с замедленной биоразлагаемостью можно упомянуть следующие полимеры: полиакриловая кислота и полиакрилаты, такие как полиметилметакрилат, полибутилметакрилат, полиакриламид, полиакрилонитрилы, полиамиды, простые эфиры полиамидов полиэтиленамин, полиимиды, поликарбонаты, поликарбоуретаны, поливинилкетоны, поливинилгалогениды, поливинилиденгалогениды, поливиниловые простые эфиры, поливиниловые ароматические соединения, поливиниловые сложные эфиры, поливинилпироллидоны, полиоксиметилены, полиэтилен, полипропилен, политетрафторэтилен, полиуретаны, полиолефинэластомеры, полиизобутилены, этиленпропилендиеновые смолы (EPDM), фторсиликоны, карбоксиметилхитозан, полиэтилентерефталат, поливалераты, карбоксиметилцеллюлоза, целлюлоза, вискоза, триацетаты вискозы, нитраты целлюлозы, ацетаты целлюлозы, гидроксиэтилцеллюлоза, бутираты целлюлозы, ацетатбутираты целлюлозы, сополимеры этилвинилацетатов, полисульфоны, поли(сложные эфиры)сульфоны, эпоксидные смолы, смолы АБС, смолы EPDM, силиконовые форполимеры, силиконы, такие как полисилоксаны, поливинилгалогениды и сополимеры, простые эфиры целлюлозы, триацетаты целлюлозы, хитозан и производные хитозана, полимеризуемые масла, такие как льняное масло и сополимеры и/или смеси указанных соединений.
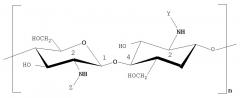
В качестве биоразлагаемых или рассасывающихся полимеров можно использовать, например, следующие полимеры: поливалеролактоны, поли-е-декалактоны, полилактиды, полигликолиды, сополимеры полилактидов и полигликолидов, поли-ε-капролактон, полигидроксибутановая кислота, полигидроксибутираты, полигидроксивалераты, сополимеры полигидроксибутирата и валерата, поли(1,4-диоксан-2,3-дионы), поли(1,3-диоксан-2-он), поли-пара-диоксаноны, полиангидриды, такие как полималеиновые ангидриды, полигидроксиметакрилаты, фибрин, полицианоакрилаты, поликапролактондиметилакрилаты, поли-b-малеиновая кислота, поликапролактонбутилакрилаты, многоблочные полимеры, такие как полимеры, полученные изолигокапролактондиолов и олигодиоксанондиолов, многоблочные полимеры, полученные из сложных и простых эфиров, такие как ПЭГ и поли(бутилентерефталаты), полипивотолактоны, триметилкарбонаты полигликолевой кислоты, поликапролактонгликолиды, поли(g-этилглутамат), поли(ОТН-иминокарбонат), поли(сополимер DTE и DT-карбоната), поли(бифенол-A-иминокарбонат), полиортоэфиры, триметилкарбонаты полигликолевой кислоты, политриметилкарбонаты, полииминокарбонаты, поли(N-винил)пирролидон, поливиниловые спирты, полиэфирамиды, гликолированные полиэфиры, полифосфоэфиры, полифосфазены, поли[пара-карбоксифенокси)пропан], полигидроксипентановая кислота, полиэтиленоксидпропиленоксид, мягкие полиуретаны, полиуретаны, содержащие остаток аминокислоты в основной цепи молекулы, сложные эфиры полиэфиров, такие как полиэтиленоксид, полиалкеноксалаты, полиортоэфиры, а также их сополимеры, каррагенаны, фибриноген, крахмал, коллаген, полимеры на основе белков, полиаминокислоты, синтетические полиаминокислоты, зеин, модифицированный зеин, полигидроксиалканоаты, пектиновая кислота, актиновая кислота, модифицированный и немодифицированные фибрин и казеин, карбоксиметилсульфат, альбумин, гиалуроновая кислота, гепарансульфаты, гепарин, хондроитинсульфат, декстран, b-циклодекстрины, сополимры ПЭГ и полипропиленгликоля, аравийская камедь, гуар, желатин, коллаген, коллаген-N-гидроксисукцинимид, липиды и липоиды, способные к полимеризации масла с низкой степенью сшивки, модификации и сополимеры и/или смеси указанных выше соединений
Предпочтительными полимерами в качестве переносчиков рапамицина или полимерами, пригодными для включения рапамицина, являются полиактиды, полигликолиды, сополимеры полиактидов и полигликолидов, полигидроксибутираты, полигидроксиметакрилаты, полиортоэфиры, гликолированные полиэфиры, поливиниловыеспирты, поливинилпиррол идон, сополимеры акриламида и акриловой кислоты, гиалуроновая кислота, гепарансульфат, гепарин, хондроитинсульфат, декстран, β-циклодекстрины, гидрофильные сшитые декстрины, альгинаты, фосфолипиды, карбомеры, сшитые пептиды и белки, силиконы, полиэтиленгликоль (ПЭГ), полипропиленгликоль (ППГ), сополимеры ПЭГ и ППГ, коллаген, способные к полимеризации масла и воски, а также их смеси и сополимеры.
Кроме того, предпочтительными являются полиэфир, полиактид, а также сополимеры диолов и сложных эфиров или диолов и лактидов. Например, в качестве диолов используются этан-1,2-диол, пропан-1,3-диол или бутан-1,4-диол.
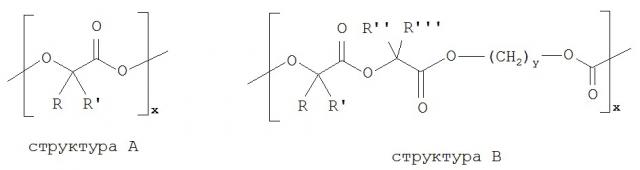
Согласно настоящему изобретению для полимерного слоя используют прежде всего полиэфиры. Предпочтительными полимерами из группы полиэфиров являются полимеры, содержащие следующие звенья
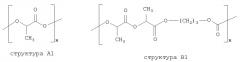
В указанных формулах R, R', R'' и R''' означают алкильный остаток, содержащий от 1 до 5 атомов углерода, предпочтительно метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, изо-бутил, н-пентил или циклопентил, предпочтительно метил или этил. Индекс у равен целому числу от 1 до 9, а x означает степень полимеризации. Особенно предпочтительными являются полимеры, содержащие следующие звенья:
В качестве примеров рассасывающихся полимеров типа Resomer® можно упомянуть следующие продукты: поли(1.-лактид)ы, характеризующиеся общей формулой -(C6H8O4)n-, такие как L 210, L 210 S, L 207 S, L 209 S, поли(сополимер L-лактида и D.L-лактида), характеризующийся общей формулой -(C6H8O4)n-, такие как LR 706, LR 708, LR 214 S, LR 704, поли(сополимер L-лактида и триметилкарбоната), характеризующийся общей формулой -[(C6H8O4)x-(C4H6O3)y]n-, такие как LТ 706 поли(сополимер L-лактида и гликолида), характеризующийся общей формулой -[(C6H8O4)х-(C4H4O4)y]n-, такие как LG 824, LG857, поли(сополимер L-лактида и ε-капролактона), характеризующийся общей формулой -[(C6H8O4)х-(C6H10O2)y]n-, такие как LC 703, поли(сополимер D.L-лактида и гликолида), характеризующийся общей формулой -[(C6H8O4)х-(C4H4O4)y]n-, такие как RG 509 S, RG 502 H, RG 503 Н, RG 504 Н, RG 502, RG 503, RG 504, поли(D,L-лактид)ы общей формулой -(C6H8O4)n-, такие как R 202 S, R 202 Н, R 203 S, R 203 Н. Resom