Способ молекулярной диагностики митохондриальных патологий на основе технологии пиросеквенирования
Иллюстрации
Показать всеИзобретение относится к области медицины и предназначено для выявления патогенных мутаций митохондриальной ДНК. Проводят реакцию просеквенирования с системой, состоящей из прямого праймера, обратного праймера, меченного биотином, и секвенирующего праймера. Всего разработаны четыре системы праймеров для четырех типов мутаций мтДНК m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G, ассоциированных с наследственными митохондриальными заболеваниями, представленные в виде лиофилизированных веществ. Изобретение обеспечивает молекулярно-генетическую детекцию патогенных мутаций митохондриальной ДНК, ассоциированных с наследственными митохондриальными патологиями, и определение уровня гетероплазмии по данным мутациям. 1 з. п. ф-лы, 2 ил., 1 табл.
Реферат
Область техники
Изобретение относится к области медицины, диагностике митохондриальных патологий и молекулярной биологии и может быть использовано для малоинвазивной диагностики митохондриальных мутаций (m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G).
Уровень техники
На сегодняшний день синдромы, обусловленные митохондральными патологиями, становятся актуальной проблемой института здравоохранения во всем мире по причине улучшения уровня медицинской диагностики, а также демографическими факторами замкнутых популяций. Показано, что различный уровень той или иной мутации или же сочетание нескольких мутаций формируют разные синдромы. Низкий уровень чувствительности методов диагностики и нехватка статистических данных о частоте встречаемости определенных мутаций при развитии конкретной патологии препятствуют эффективному диагностированию населения, что не позволяет адекватно оказывать медицинскую помощь.
В соответствии с современным состоянием научно-технической проблемы для ее решения применяются такие методы, как клонирование, флуоресцентная ПЦР, денатурирующая высокоразрешающая жидкостная хроматография. Пиросеквенирование на платформе Pyromark отличается простотой выполнения, низкой стоимостью реагентов, позволяет установить низкие значения уровня гетероплазмии патогенных мутаций мтДНК.
Известно изобретение «Способ генетической диагностики предрасположенности к атеросклерозу» (заявка на изобретение РФ №2010133468, 2010 г. C12N 15/00). Способ генетической диагностики атеросклероза и предрасположенности к развитию атеросклероза, отличающийся тем, что проводится количественное определение процента копий митохондриальной ДНК, содержащих мутацию 652delG в пробах ДНК, выделенных из циркулирующих лейкоцитов крови человека, при этом отсутствие данной мутации расценивается как отсутствие генетической предрасположенности к атеросклерозу, наличие данной мутации в 1-9% копий ДНК расценивается как неявная генетическая предрасположенность к атеросклерозу, и наличие данной мутации более чем в 9% копий ДНК расценивается как выраженная генетическая предрасположенность к атеросклерозу.
Недостатком описанного изобретения является то, что данная технология предназначена только для детекции делеции 652delG в пробах митохондриальной ДНК, что не подходит для поставленных нами задач.
Известно изобретение «Способ генетической диагностики доклинического атеросклероза» (заявка на изобретение РФ №2013119178, 2013 г. G01N 33/48). Данная технология подразумевает использование секвенирования на платформе Roche 454 и анализа высоты пиков на пирограмме.
Недостатком описанного изобретения является то, что изобретение утратило актуальность в силу снятия с производства платформы Roche 454 и дальнейшего отсутствия поддержки со стороны производителя систем.
Известно изобретение Method and kit for detecting polymorphism of mitochondrial ND1 gene mononucleotide, and application of kit (патент КНР № CN 101775435, 2009 г. C12N 15/11; C12Q 1/68. Метод базируется на использовании аллель-специфичных праймеров и флуоресцентного красителя и анализе кривых плавления после амплификации.
Недостатком описанного изобретения является использование анализа кривых плавления, что подразумевает низкую разрешающую способность метода и отсутствие возможности детектировать уровень гетероплазмии до 1%.
Известно изобретение «Quick detection method of primary mutation G3635A of Leber hereditary optic nerve pathological mitochondrial DNA» (заявка на изобретение КНР № CN 101781683, 2010 г. C12Q 1/68). Рассматривается способ детекции мутации G3635A, ассоциированной с наследственной оптической нейропатией Лебера, основанный на использовании пары аллель-специфичных праймеров с последующим разделением продуктов амплификации в агарозном геле.
Недостатком описанного изобретения является крайне низкая разрешающая способность и невозможность детектировать уровень гетероплазмии до 1%.
Известно изобретение «Screening method of mitochondrial disease gene» (заявка на изобретение КНР № CN 103305619, 2013 г. C12Q 1/68). Метод представляет собой обогащение геномной ДНК, включающей гены, кодирующие белки биогенеза митохондрий.
Недостатком описанного изобретения является то, что метод не подходит для работы с митохондриальной ДНК.
Известно изобретение «Kit for detecting mutations of A-G at 1555th site and C-T at 1494th site of mitochondrial gene» (заявка на изобретение КНР № CN 103540676, 2013 г. C12Q 1/68). Метод основан на модификации полимеразной цепной реакции.
Недостатком описанного изобретения является то, что метод не дает возможности детектировать уровень гетероплазмии до 1%.
Известно изобретение «Method, polynucleotide probe, dna chip and kit for identifying mutation of human mitochondrial DNA» (патент на изобретение Республики Корея № KR 100892253, 2006 г. C12Q 1/68; G01N 33/50; G01N 33/53). Метод обогащения гипервариабельного сегмента митохондриальной ДНК для установления митохондриальной гаплогруппы.
Недостатком описанного изобретения является то, что метод не обеспечивает детекцию уровня гетероплазмии основных патогенных мутаций митохондриальной ДНК.
Известно изобретение «Mitochondrial mutations and rearrangements as a diagnostic tool for the detection of sun exposure, prostate cancer and other cancers» (заявка на изобретение Новой Зеландии № NZ 587665, 2006 г. А61Р 35/00). Метод базируется на технологии выявления мутаций с помощью микрочипов.
Недостатком описанного изобретения является то, что метод не обеспечивает детекцию уровня гетероплазмии патогенных мутаций митохондриальной ДНК.
Известно изобретение «Detection of mitochondrial DNA mutation 14459 associated with dystonia and/or Leber's hereditary optic neuropathy» (заявка на изобретение США № US 5670320, 1994 г. C12Q 1/68). Технология детекции мутации 14459 митохондриальной ДНК, ассоциированной с наследственной оптической атрофией Лебера и дистонией, основана на капиллярном секвенировании.
Недостатком описанного изобретения является то, что метод имеет разрешающую способность до 10%, что является недостаточным уровнем чувствительности для молекулярной диагностики митохондриальных патологий.
Известно изобретение «Methods and compositions for presymptomatic or post-symptomatic diagnosis of Alzheimer's disease and other neurodegenerative disorders» (заявка на изобретение США № US 2009111093, 2004 г. C12Q 1/68). Рассматривается технология секвенирования гипервариабельного участка митохондриальной ДНК на наличие мутаций, ассоциированных с болезнью Альцгеймера и других нейродегенеративных патологий, основанная на капиллярном секвенировании.
Недостатком описанного изобретения является то, что метод имеет разрешающую способность до 10%, что является неадекватным для наших исследований.
Из данных отечественной и зарубежной литературы, патентов и патентных заявок авторы исследования заключили, что подход пиросеквенирования митохондриальной ДНК на платформе Pyromark Q24 ранее не был реализован. Подобная технология позволит выявлять до 1% патогенных мутаций в митохондриальной ДНК по четырем основным мутациям (m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G), ассоциированным с митохондриальной патологией.
Наиболее близким по технической сущности заявляемому устройству, (или выбранному в качестве прототипа) является «Способ количественной оценки мутантного аллеля митохондриального генома в лейкоцитах крови человека» (заявка на изобретение РФ №2009146012, 2009 г. C12Q 1/00). Данная технология подразумевает использование секвенирования на платформе Roche 454 и анализа высоты пиков на пирограмме.
Недостатком описанного изобретения является то, что изобретение утратило актуальность в силу снятия с производства платформы Roche 454 и дальнейшего отсутствия поддержки со стороны производителя систем.
Раскрытие изобретения
Основанием для проведения молекулярно-генетического типирования патогенных мутаций является феномен, который заключается в зависимости клинических проявлений заболеваний ассоциируемых с дефектами биогенеза митохондрий от уровня гетероплазмии. Поскольку уровень гетероплазмии во многом определяет фенотипическое проявление мутации, в процессе молекулярного анализа необходимо проводить количественную оценку мутантных мтДНК. Следует заметить, что оценка уровня гетероплазмии уже включает детекцию мутации, в то время как методы детекции мутации не всегда учитывают уровень ее гетероплазмии. В соответствии с современным состоянием научно-технической проблемы для ее решения применяются такие методы, как клонирование, флуоресцентная ПЦР, денатурирующая высокоразрешающая жидкостная хроматография. Пиросеквенирование на платформе Pyromark Q24 позволяет установить низкие значения уровня гетероплазмии патогенных мутаций мтДНК и является финансово более предпочтительным. Подготовка библиотеки для проведения пиросеквенирования просто в исполнении и не требует дорогостоящих реагентов. Проверка эффективности работы системы детекции уровня гетероплазмии на основе пиросеквенирования требует наличия стандартов, которые представляют собой плазмидные векторы, несущие патогенную мутацию мтДНК. Независимым применением разрабатываемой технологии является использование ее для оценки эффективности системы редактирования мтДНК. В частности, оценка уровня гетероплазмии до использования системы редактирования и после ее использования, покажет эффективность процесса элиминации мутантные варианты митохондриального генома.
Отличительным признаком заявляемого изобретения является использование стандартов, имитирующих разную степень гетероплазмии для четырех типов мутаций, ассоциированных с наследственными митохондриальными заболеваниями. Новизну представляют собой нуклеотидные последовательности синтетических олигонуклеотидов, предназначенных для проведения реакции пиросеквенирования.
Задачей, на решение которой направлено заявляемое изобретение, является молекулярно-генетическая детекция митохондриальной ДНК, содержащей патогенные мутации, ассоциированные с наследственными митохондриальными патологиями, и определение уровня героплазмии по данным мутациям.
Для решения поставленной задачи был разработан способ малоинвазивной диагностики и одновременной количественной оценки уровня гетероплазмии митохондриальной ДНК по четырем мутациям (m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G) с использованием метода пиросеквенирования, реализуемый в виде тест-системы.
Описание изобретения
Предложен способ малоинвазивной диагностики митохондриальных мутаций (m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G) с использованием метода пиросеквенирования.
Технический результат достигается за счет того, что в заявляемом изобретении для детекции одной мутации используются три синтетических олигонуклеотида, часть из которых модифицирована биотином. В качестве положительного контроля и количественной оценки используются плазмидные векторы, в которые клонирован фрагмент митохондриальной ДНК, содержащий одну из четырех патогенных мутаций.
Изобретение включает в себя четыре системы олигонуклеотидов, состоящих из праймеров прямого и обратного, меченного биотином, а также секвенирующего праймера. А также четыре системы смесей плазмид, содержащих вставки последовательностей мтДНК, соответствующих нормальной и мутантной последовательности по локусам m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G в соотношениях от 0 до 100% каждой из плазмид с шагом в 10% и от 10 до 1% с шагом в 1%. Все компоненты тест-системы представлены в виде лиофилизированных веществ.
Реализация изобретения
Образцы венозной крови, желательно, забирать в пробирки с ЭДТА. Процедуру экстракции нуклеиновых кислот, желательно, начинать не позднее чем через 2 часа с момента забора крови. Для получения плазмы пробирки с кровью центрифугируют (например, при 400 g в течение 20 мин или сопоставимо). После центрифугирования верхнюю фракцию, желательно, перенести в новую пробирку и вновь центрифугировать при тех же условиях.
Для определения уровня гетероплазмии по митохондриальным мутациям (m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G) используется метод пиросеквенирования. Пара праймеров, из которых обратный содержит на 5' конце биотин, используются для проведения первого этапа ПЦР, в результате которого получаем ампликонсодержащий биотин только на одном из концов. Биотин обеспечивает соединение с шариками сефарозы, покрытыми стрептавидином, через взаимодействие биотин-стрептавидин. Далее осуществляется очистка связавшихся с сефарозой ампликонов от неспецифических продуктов ПЦР и праймеров путем фильтрации смеси с использованием станции вакуумной пробоподготовки. Далее полученный раствор, содержащий ампликон и находящийся в станции пробоподготовки, подвергается денатурации, в результате получаем одноцепочечный фрагмент. К раствору добавляется секвенирующий праймер, полученный раствор приносится в пиросеквенатор Pyromark Q24 для проведения реакции пиросеквенирования в соответствии с технологией производителя. В качестве положительного контроля при количественной оценке уровня гетероплазмии используется набор разведений плазмид. Плазмиды содержат последовательности, соответствующие участкам нормальной и мутантной мтДНК. Для каждого типа мутаций разработаны системы контролей, представляющие лиофилизированные смеси плазмид двух типов (со вставками нормальной и мутантной последовательностей по локусам m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G), в соотношениях от 0 до 100% каждой из плазмид с шагом в 10% и от 10 до 1% с шагом в 1%. По результатам исследования с контрольными системами для прибора Pyromark Q24 показана чувствительность до 1%. Протокол проведения исследования на Pyromark Q24 полностью соответствует предлагаемому производителем.
Для оценки уровня гетероплазмии по каждому типу митохондриальных мутаций пирограммы, полученные для образцов, соотносятся с пирограммами, полученными для системы смесей плазмид.
Оценка эффективности
Разработка тест-системы включала подбор и оптимизацию простых и биотинилированных праймеров, совместимых с коммерческими реагентами для пиросеквенирования на платформе PyroMark Q24. Дизайн праймеров осуществляли с помощью программного обеспечения PyroMark Assay Design SW 2.0 (QIAGEN). В основе реакции пиросеквенирования лежит использование трех праймеров, один из которых является биотинилированным.
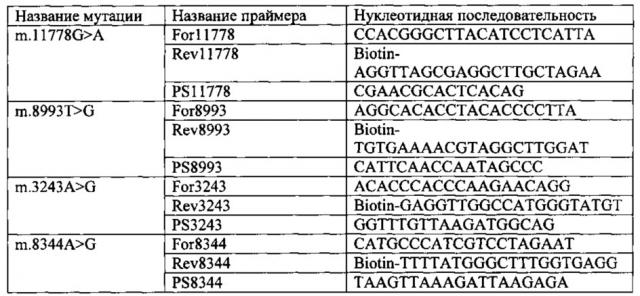
В ходе оптимизации процесса были выбраны следующие праймеры, представленные в таблице:
Используя разработанные на предыдущем этапе реагенты для построения калибровочных кривых, имитирующие гетероплазмию патогенных мутаций мтДНК с шагом 10%, были получены следующие результаты (Фиг. 1). Аналогичные данные нами были получены для всех четырех мутаций мтДНК.
Далее, мы изменили соотношения генетических конструкций таким образом, чтобы получить имитацию гетероплазмии с шагом 1%. На хроматограмме (Фиг. 2) представлены данные, подтверждающие, что чувствительность метода составляет 1% наличия мутантной мтДНК в пуле мтДНК дикого типа.
Оптимизация метода пиросеквенирования позволила добиться стабильной работы тест-системы с количеством геномной ДНК 10 нг. Набор для определения абсолютного количества мутантных вариантов мтДНК включает определение четырех патогенных мутаций m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G не менее чем для десяти пациентов.
Краткое описание чертежей
На Фиг. 1 представлены хроматограммы с прибора PyroMark Q24 по детекции мутации m.11778G>A, где в качестве матрицы использовались генетические конструкции, имитирующие гетероплазмию с шагом 10%.
На Фиг. 2 представлены хроматограммы с прибора PyroMark Q24 по детекции мутации m.11778G>A, где в качестве матрицы использовались генетические конструкции, имитирующие гетероплазмию с шагом 1%.
Использование заявленного изобретения позволяет осуществлять молекулярно-генетическую детекцию митохондриальной ДНК, содержащую патогенные мутации, ассоциированные с наследственными митохондриальными патологиями, и определять уровень героплазмии по данным мутациям, то есть осуществлять молекулярно-генетическую диагностику наследственных митохондриальных патологий.
1. Способ молекулярной диагностики митохондриальных патологий на основе технологии пиросеквенирования для выявления патогенных мутаций митохондриальной ДНК, который реализуют при использовании мтДНК выделенной периферической крови путем проведения реакции просеквенирования с системой, состоящей из прямого праймера, обратного праймера, меченного биотином, и секвенирующего праймера, причем всего разработано четыре системы праймеров для четырех типов мутаций мтДНК m.11778G>A, m.8993T>G, m.3243A>G, m.8344A>G, ассоциированных с наследственными митохондриальными заболеваниями: для выявления мутации m.11778G>A система, состоящая из праймеров For11778 SEQ ID N1, Rev11778 SEQ ID N2 и PS11778 SEQ ID N3; для выявления мутации m.8993T>G система, состоящая из праймеров For8993 SEQ ID N4, Rev8993 SEQ ID N5 и PS8993 SEQ ID N6; для выявления мутации m.3243A>G система, состоящая из праймеров For3243 SEQ ID N7, Rev3243 SEQ ID N8 и PS3243 SEQ ID N9, для выявления мутации m.8344A>G система, состоящая из праймеров For8344 SEQ ID N10, Rev8344 SEQ ID N11 и PS8344 SEQ ID N12, представленные в виде лиофилизированных веществ.
2. Способ по п. 1, отличающийся тем, что для положительного контроля и количественной оценки используют четыре системы смесей плазмид, содержащих вставки последовательностей мтДНК, соответствующих нормальной и мутантной последовательности по локусам m.11778G>A (11778G SEQ ID N20, 11778A SEQ ID N19), m.8993T>G (8993T SEQ ID N18, 8993G SEQ ID N17), m.3243A>G (3243A SEQ ID N13, 3243G SEQ ID N14), m.8344A>G (8344A SEQ ID N15, 8344G SEQ ID N16) в соотношениях от 0 до 100% каждой из плазмид с шагом в 10% и от 10 до 1% с шагом в 1% в виде лиофилизированных веществ, причем указанные системы смесей плазмид используют в качестве матрицы для проведения реакции пиросеквенирования с использованием вышеописанных систем праймеров в соответствии с типом мутации.