Композиции сложных эфиров омега-3 жирных кислот
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности и представляет собой способ лечения сердечно-сосудистого заболевания или состояния у пациента, включающий введение указанному пациенту, перорально или парентерально, фармацевтической композиции, которая самостоятельно образует мицеллы при контакте с водной средой с образованием сферических мицелл, которые имеют средний диаметр от 1 мкм до 10 мкм и обеспечивают абсорбцию сложных эфиров омега-3 жирных кислот практически независимо от любого влияния пищи, или стабильных мицелл, предварительно сформировавшихся из указанной композиции, в количестве, терапевтически эффективном для обеспечения снижения одного или более симптомов указанного сердечно-сосудистого заболевания или состояния, при этом указанная фармацевтическая композиция содержит: (a) от 60% (вес/вес) до 85% (вес/вес) по меньшей мере одного сложного эфира омега-3 жирной кислоты, выбранного из группы, состоящей из сложного эфира (все-Z омега-3)-5,8,11,14,17-эйкозапентаеновых кислот (ЕРА), сложного эфира (все-Z омега-3)-4,7,10,13,16,19-докозагексаеновых кислот (DHA), гексадекатриеновой кислоты ("НТА" или 16:3 (n-3) или все-Z-7,10,13-гексадекатриеновой кислоты), α-линоленовой кислоты ("ALA" или 18:3 (n-3) или все-Z-9,12,15-октадекатриеновой кислоты), стеаридоновой кислоты ("SDA" или 18:4 (n-3) или все-Z-6,9,12,15-октадекатетраеновой кислоты), эйкозатриеновой кислоты ("ЕТЕ" или 20:3 (n-3) или все-Z-11,14,17-эйкозатриеновой кислоты), эйкозатетраеновой кислоты ("ЕТА" или 20:4 (n-3)), генэйкозапентаеновой кислоты ("НРА" или 21:5 (n-3) или все-Z-6,9,12,15,18-генэйкозапентаеновой кислоты), докозапентаеновой кислоты ("DPA", или клупанодоновой кислоты или 22:5 (n-3), или все-Z-7,10,13,16,19-докозапентеновой кислоты); тетракозапентаеновой кислоты (24:5 (n-3) или все-Z-9,12,15,18,21-тетракозапентаеновой кислоты) и тетракозагексаеновой кислоты (низиновой кислоты или 24:6 (n-3) или все-Z-6,9,12,15,18,21-тетракозагексаеновой кислоты); и (b) поверхностно-активное вещество, которое содержит, в комбинации, по меньшей мере один неионный алкиловый эфир полиоксиэтиленгликоля и сорбитана (полисорбат), выбранный из группы, состоящей из полиоксиэтилен(20)сорбитанмонолаурата (полисорбат 20), полиоксиэтилен(20)сорбитанмонопальмитата (полисорбат 40), полиоксиэтилен(20)сорбитанмоностеарата (полисорбат 60) и полиоксиэтилен(20)сорбитанмоноолеата (полисорбат 80); и блок-сополимер полиэтиленгликоля и полипропиленгликоля, имеющий формулу [(НО(C2H4O)64(C3H6O)37(C2H4O)64Н] (Poloxamer 237); где указанный полисорбат присутствует в количестве от 15% (вес/вес) до 31% (вес/вес) от указанной композиции; и где указанный Poloxamer 237 присутствует в количестве от 0,5% (вес/вес) до 5% (вес/вес) от указанной композиции; при этом указанная комбинация поверхностно-активных веществ является эффективной для образования указанных стабильных мицелл при контакте с указанной водной средой, и где указанная композиция для перорального или парентерального введения, которая самостоятельно образует мицеллы, при введении человеку в равной дозировке обеспечивает по существу одинаковую биодоступность при введении с пищей или без пищи указанному человеку, нуждающемуся в таком введении; при этом указанная композиция, которая самостоятельно образует мицеллы, самостоятельно образует мицеллы в водной среде, таким образом формируя сферические мицеллы, имеющие средний диаметр от 1 мкм до 10 мкм, которые обеспечивают абсорбцию указанных сложных эфиров омега-3 жирных кислот практически независимо от любого влияния пищи; и где указанную фармацевтическую композицию вводят перорально или парентерально в количестве, терапевтически эффективном для обеспечения снижения одного или более симптомов указанного сердечно-сосудистого заболевания или состояния. Изобретение обеспечивает композиции, которые менее подвержены влиянию пищи, имеют высокую эффективность при низких дозах, минимизируют и устраняют неприятный запах, привкус или отрыжку у пациента. 12 н. и 77 з.п. ф-лы, 5 пр., 5 табл., 4 ил.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка заявляет преимущество приоритета предварительной заявки на патент США №61/618161, поданной 30 марта 2012 г.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002] Согласно информационному бюллетеню Всемирной организации здравоохранения (WHO) по сердечно-сосудистым заболеваниям (CVD), CVD являются главной причиной смерти во всем мире (информационный бюллетень №317, сентябрь 2012, доступный по адресу (http://www.who.int/mediacentre/factsheets/fs317/en/index.html от 31 января 2013 г.). По оценкам WHO приблизительно 17,3 миллиона человек умерли от CVD в 2008 г., что составило 30% всех случаев смерти в мире. Из данных смертей приблизительно 7,3 миллиона произошли вследствие ишемической болезни сердца (CHD) и 6,2 миллиона вследствие инсульта. Также по оценкам WHO к 2030 году почти 25 миллионов человек умрет от CVD, в основном от заболеваний сердца и инсульта. По оценкам Исследования глобального бремени заболеваний (Global Burden of Disease Study) на долю развивающихся стран пришлось 3,5 миллиона из 6,2 миллионов случаев смерти от CHD в мире в 1990 году. (Murray CJL and Lopez AD. The Global Burden of Disease A Comprehensive Assessment of Mortality and Disability from Disease, Injuries and Risk Factors in 1990 and Projected to 2020. Boston, Ma Harvard University Press; 1996). По оценке предполагаемых показателей на данные страны будет приходиться 7,8 миллиона из 11,1 миллиона смертей вследствие CHD в 2020 году. Развитые страны не застрахованы от CHD. Например, в США и Европе CHD остается самой распространенной единой причиной смерти и инвалидности. В 2005 году CHD стала причиной приблизительно 1 из каждых 5 смертей в США (Heron MP, et. al. Deaths preliminary data for 2006. Natl. Vital. Stat. Rep. 2008; 56: 1-52.). По данным Центров по контролю и профилактике заболеваний (Centers for Disease Control and Prevention) она является ведущей причиной смерти в Америке. Приблизительно 37% людей, у которых развивается коронарный приступ в определенном году, умрет от него. В то время как в Европе достигнуто наиболее значимое снижение смертности, связанной с CVD, на CVD по-прежнему приходится 54% всех смертей среди женщин и 43% всех смертей среди мужчин.
[0003] CVD связаны с многими факторами риска. Из данных факторов риска гиперлипидемия (например, гипертриглицеридемия) и гиперхолестеринемия являются важными индикаторами CVD. Поэтому в настоящее время пищевые добавки, нутрицевтики и отпускаемые по рецепту лекарственные средства, содержащие сложные эфиры омега-3 жирных кислот, такие как сложные этиловые эфиры ЕРА и DHA, применяются для лечения CVD и, в частности, для снижения повышенного уровня триглицеридов.
[0004] Однако, введение пищевых добавок, нутрицевтиков и отпускаемых по рецепту лекарственных средств, содержащих сложные эфиры омега-3 жирных кислот, представляет значительные трудности. Например, в настоящее время пищевые добавки, нутрицевтики и отпускаемые по рецепту лекарственные средства, содержащие сложные эфиры омега-3 жирных кислот, характеризуются различной абсорбцией и эффективностью при пероральном введении. В частности, существующие в настоящее время композиции подвергаются выраженному "влиянию пищи" со слабой абсорбцией при приеме натощак или с едой с низким содержанием жиров. При приеме с жирной пищей абсорбция сложных эфиров омега-3 жирных кислот улучшается частично благодаря присутствию выделяющихся в желудок солей желчных кислот, которые способствуют абсорбции сложных эфиров омега-3 жирных кислот.
[0005] Для преодоления низкой абсорбции пациентам можно давать дозы композиций, содержащие большие количества сложных эфиров омега-3 жирных кислот, но существуют практические ограничения для данного подхода в связи с побочными эффектами, которые обычно связаны с такими композициями. Окислительный распад сложных эфиров омега-3 жирных кислот, который происходит с течением времени, может привести к неприятному привкусу после введения, особенно при употреблении в больших количествах. Отрыжка и расстройство желудка являются дополнительными побочными эффектами, связанными с употреблением сложных эфиров омега-3 жирных кислот. После употребления сложные эфиры омега-3 жирных кислот, как правило, плавают на поверхности жидкого содержимого в желудке, образуя слой, который препятствует прохождению мелких пузырьков газа. При накоплении количества газа, достаточного для преодоления поверхностного натяжения масляного слоя, человек отрыгивает. Отрыжка обычно имеет рыбный привкус и запах.
[0006] Соответственно, побочные эффекты, связанные с введением существующих в настоящее время композиций, содержащих сложные эфиры омега-3 жирных кислот (например, подверженность влиянию пищи, большие дозы для достижения эффективности и получаемый привкус, неприятный запах и отрыжка), как известно, значительно снижают соблюдение пациентом режима и схемы лечения.
[0007] В то время как ведение здорового образа жизни может снизить заболеваемость CVD, новые терапевтические подходы для контроля CVD являются оправданными. Такие новые подходы могут включать поиск новых лекарственных средств или улучшение существующих в настоящее время лекарственных средств, применяемых для лечения CVD. Поиск новых лекарственных средств, однако, является дорогостоящим, без уверенности в конечном успехе. Соответственно, следует разрабатывать новые или более эффективные способы доставки существующих в настоящее время лекарственных средств с доказанным профилем безопасности и эффективности. Таким образом, существует потребность в улучшенных композициях, содержащих сложные эфиры омега-3 жирных кислот, такие как сложные этиловые эфиры ЕРА и DHA, которые менее подвержены влиянию пищи и которые имеют высокую эффективность при низких дозах. В идеальном случае такие улучшенные композиции могли бы минимизировать или устранить неприятный запах, и/или неприятный привкус, и/или отрыжку у пациента. Такая улучшенная композиция с уменьшенными побочными эффектами могла бы улучшить соблюдение пациентом режима и схемы лечения и более эффективно бороться с факторами риска, связанными с сердечно-сосудистыми заболеваниями.
КРАТКОЕ ОПИСАНИЕ
[0008] Во всех вариантах осуществления, предусматриваемых в данном документе, все композиции не содержат свободные омега-3 жирные кислоты. В определенных вариантах осуществления в данном документе предусмотрены композиции, содержащие сложные эфиры ЕРА и DHA в комбинации по меньшей мере с одним поверхностно-активным веществом. В определенных вариантах осуществления соотношение сложного эфира ЕРА и сложного эфира DHA составляет от более чем 2:1 до не более чем 3,4:1. Определенные варианты осуществления предусматривают соотношение сложного эфира ЕРА и сложного эфира DHA от приблизительно 2:1 до приблизительно 3,4:1. В определенных вариантах осуществления в данном документе предусматриваются композиции, содержащие по меньшей мере один сложный эфир омега-3 жирной кислоты и по меньшей мере одно поверхностно-активное вещество. В определенных вариантах осуществления сложный эфир омега-3 жирной кислоты выбран из группы, состоящей из гексадекатриеновой кислоты, α-линоленовой кислоты, стеаридоновой кислоты, эйкозатриеновой кислоты, эйкозапентаеновой кислоты, генэйкозапентаеновой кислоты, докозапентаеновой кислоты, докозагексаеновой кислоты, тетракозапентаеновой кислоты, тетракозагексаеновой кислоты или их комбинации. Определенные варианты осуществления предусматривают композиции, содержащие сложный этиловый эфир - производное указанного сложного эфира омега-3 жирной кислоты, необязательно в комбинации по меньшей мере с одним поверхностно-активным веществом, по меньшей мере одним терпеном, по меньшей мере одним антиоксидантом или их комбинациями. Определенные варианты осуществления также предусматривают комбинации различных сложных эфиров омега-3 жирных кислот в соотношениях от приблизительно 2:1 до приблизительно 3,4:1. Другие варианты осуществления предполагают соотношение от более чем 2:1 до не более чем 3,4:1. Как правило, соотношение составляет приблизительно 2,4:1. Определенные варианты осуществления предусматривают способ лечения различных состояний или нарушений, которые можно лечить путем введения указанных сложных эфиров омега-3 жирных кислот в композициях, описанных в данном документе, которые характеризуются описанными соотношениями, необязательно по меньшей мере с одним поверхностно-активным веществом, по меньшей мере одним терпеном, по меньшей мере одним антиоксидантом или их комбинациями. Композиции, описанные в данном документе, минимизируют несколько побочных эффектов, обнаруживаемых у зарегистрированных в настоящее время для продажи композиций, содержащих сложные эфиры омега-3 жирных кислот, которые могут удерживать субъекта-человека от выполнения схемы дозирования, необходимой для лечения состояния или нарушения, поддающегося лечению путем введения сложных эфиров омега-3 жирных кислот. В определенных вариантах осуществления биодоступность указанных сложных эфиров омега-3 жирных кислот при введении в виде определенных композиций, описанных в данном документе, практически остается одинаковой при введении с пищей или без пищи субъекту-человеку, нуждающемуся в таком введении, т.е. практически не зависит от влияния пищи.
[0009] Таким образом, определенные варианты осуществления предусматривают фармацевтические композиции, содержащие по меньшей мере один сложный эфир омега-3 жирной кислоты и по меньшей мере одно поверхностно-активное вещество, где указанный по меньшей мере один сложный эфир омега-3 жирной кислоты составляет по меньшей мере приблизительно 40% (вес/вес) композиции.
[0010] Определенные варианты осуществления предусматривают фармацевтические композиции, содержащие первый сложный эфир омега-3 жирной кислоты, выбранный из группы, состоящей из гексадекатриеновой кислоты, α-линоленовой кислоты, стеаридоновой кислоты, эйкозатриеновой кислоты, эйкозапентаеновой кислоты, генэйкозапентаеновой кислоты, докозапентаеновой кислоты, докозагексаеновой кислоты, тетракозапентаеновой кислоты, тетракозагексаеновой кислоты, и второй сложный эфир омега-3 жирной кислоты, выбранный из группы, состоящей из гексадекатриеновой кислоты, α-линоленовой кислоты, стеаридоновой кислоты, эйкозатриеновой кислоты, эйкозапентаеновой кислоты, генэйкозапентаеновой кислоты, докозапентаеновой кислоты, докозагексаеновой кислоты, тетракозапентаеновой кислоты, тетракозагексаеновой кислоты, таким образом, что выбранные первый и второй сложные эфиры омега-3 жирных кислот отличаются друг от друга, и соотношение первого и второго сложных эфиров омега-3 жирных кислот составляет от более чем 2:1 до не более чем 3,4:1 (первый сложный эфир омега-3 жирной кислоты: второй сложный эфир омега-3 жирной кислоты); где первый и второй сложные эфиры омега-3 жирных кислот в сумме составляют по меньшей мере приблизительно 40% (вес/вес) композиции, и где указанная композиция практически не содержит активные ингредиенты кроме указанных сложных эфиров омега-3 жирных кислот.
[0011] Определенные варианты осуществления предусматривают применение по меньшей мере одного сложного эфира омега-3 жирной кислоты. Как правило, сложный эфир омега-3 жирной кислоты является сложным этиловым эфиром.
[0012] Определенные варианты осуществления предусматривают фармацевтические композиции, содержащие по меньшей мере один сложный эфир омега-3 жирной кислоты и по меньшей мере один терпен, где указанный по меньшей мере один сложный эфир омега-3 жирной кислоты составляет по меньшей мере приблизительно 40% (вес/вес) композиции, которые практически не содержат активные ингредиенты кроме сложных эфиров омега-3 жирных кислот. В определенных вариантах осуществления по меньшей мере один сложный эфир омега-3 жирной кислоты составляет приблизительно 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%. Терпен, как правило, но не обязательно, представляет собой d-лимонен. В определенных других вариантах осуществления такие композиции содержат натуральное апельсиновое масло.
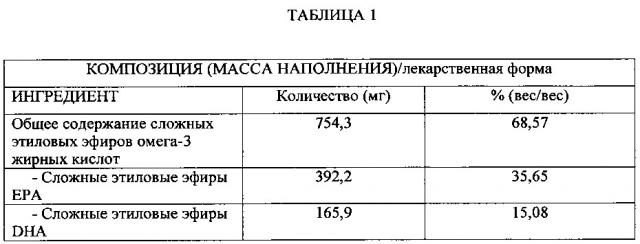
[0013] Определенные варианты осуществления предусматривают композиции, содержащие сложные этиловые эфиры ЕРА и сложные этиловые эфиры DHA и по меньшей мере один терпен, где соотношение EPA:DHA составляет приблизительно 2,4:1, и где указанные этиловые эфиры ЕРА и DHA в сумме составляют от приблизительно 40% (вес/вес) до приблизительно 95% (вес/вес) указанной композиции. В определенных вариантах осуществления сложные этиловые эфиры ЕРА и DHA в сумме составляют приблизительно 40% (вес/вес) указанной композиции. Терпен, как правило, но не обязательно, представляет собой d-лимонен. В определенных других вариантах осуществления такие композиции содержат натуральное апельсиновое масло.
[0014] В вариантах осуществления, включающих практически чистый d-лимонен, d-лимонен характеризуется от приблизительно 95% до приблизительно 98% чистоты. В определенных вариантах осуществления практически чистый d-лимонен характеризуется по меньшей мере 95%, 96%, 97% или 98% чистоты.
[0015] В определенных вариантах осуществления сложный эфир омега-3 жирной кислоты выбран из группы, которая состоит по меньшей мере из одного сложного эфира ЕРА, по меньшей мере одного сложного эфира DHA или их комбинации, и включает по меньшей мере одно поверхностно-активное вещество. В определенных вариантах осуществления по меньшей мере один сложный эфир ЕРА и по меньшей мере один сложный эфир DHA являются практически чистыми. Определенные варианты осуществления также предусматривают композиции, содержащие по меньшей мере один сложный эфир ЕРА и по меньшей мере один сложный эфир DHA в соотношениях от приблизительно 2:1 до приблизительно 3,4:1, которые практически не содержат активные ингредиенты кроме сложных эфиров омега-3 жирных кислот. Также описаны композиции, характеризующиеся другими соотношениями. Определенные композиции также могут не содержать натуральное апельсиновое масло или d-лимонен. В определенных вариантах осуществления сложные эфиры омега-3 жирных кислот составляют по меньшей мере 40% композиции. Как правило, сложные эфиры омега-3 ЕРА и DHA являются сложными этиловыми эфирами. Определенные композиции, описанные в данном документе, образуют мицеллы в водной среде и не зависят от влияния пищи. Определенные композиции при введении с пищей или без пищи, практически не зависят от влияния пищи. Также в данном документе предусмотрены способы лечения сердечно-сосудистых состояний или нарушений с использованием описанных композиций. Композиции, описанные в данном документе, минимизируют или устраняют побочные эффекты по сравнению с введением композиций предшествующего уровня техники. Также предусмотрены упакованные композиции или наборы сложных эфиров омега-3 жирных кислот, содержащие одну или несколько единичных лекарственных форм вместе с инструкциями по применению композиций.
[0016] Соответственно, по меньшей мере в одном варианте осуществления предусмотрена фармацевтическая композиция, содержащая по меньшей мере один сложный эфир ЕРА, и по меньшей мере один сложный эфир DHA в соотношении веса к весу от более чем приблизительно 2:1 до не более чем приблизительно 3,4:1 (EPA:DHA), и по меньшей мере одно поверхностно-активное вещество, где указанные сложные эфиры ЕРА и DHA в сумме составляют от приблизительно 40% до приблизительно 85% по весу композиции. В определенных таких вариантах осуществления сложные этиловые эфиры ЕРА и DHA в сумме составляют приблизительно 50% (вес/вес) указанной композиции.
[0017] По меньшей мере в одном другом варианте осуществления предусмотрена фармацевтическая композиция, содержащая по меньшей мере один сложный эфир ЕРА, и по меньшей мере один сложный эфир DHA в соотношении веса к весу от приблизительно 2:1 до приблизительно 3,4:1 (EPA:DHA), и по меньшей мере одно поверхностно-активное вещество, где указанные сложные эфиры ЕРА и DHA в сумме составляют от приблизительно 40% до приблизительно 85% по весу композиции. В определенных таких вариантах осуществления сложные этиловые эфиры ЕРА и DHA в сумме составляют приблизительно 50% (вес/вес) указанной композиции.
[0018] По меньшей мере в одном другом варианте осуществления предусмотрена фармацевтическая композиция, содержащая по меньшей мере один сложный эфир ЕРА, и по меньшей мере один сложный эфир DHA в соотношении веса к весу от более чем 2:1 до не более чем 3,4:1 (EPA:DHA), и по меньшей мере одно поверхностно-активное вещество, где указанные сложные эфиры ЕРА и DHA в сумме составляют от приблизительно 40% до приблизительно 85% по весу композиции. В определенных таких вариантах осуществления сложные этиловые эфиры ЕРА и DHA в сумме составляют приблизительно 50% (вес/вес) указанной композиции.
[0019] По меньшей мере в еще одном варианте осуществления предусмотрена фармацевтическая композиция, содержащая по меньшей мере один сложный эфир EPA, и по меньшей мере один сложный эфир DHA в соотношении веса к весу от более чем 2:1 до не более чем 3,4:1 (EPA:DHA), и по меньшей мере одно поверхностно-активное вещество, где указанные сложные эфиры ЕРА и DHA в сумме составляют от приблизительно 40% до приблизительно 85% по весу композиции, и где композиция при введении с пищей или без пищи субъекту-человеку, нуждающемуся в таком введении, практически не зависит от влияния пищи. В таких определенных вариантах осуществления сложные этиловые эфиры ЕРА и DHA в сумме составляют приблизительно 50% (вес/вес) указанной композиции.
[0020] По меньшей мере в одном варианте осуществления композиции, описанные в данном документе, содержат практически чистый по меньшей мере один сложный эфир ЕРА и/или по меньшей мере один сложный эфир DHA.
[0021] По меньшей мере в одном варианте осуществления композиции, описанные в данном документе, по сути, включают по меньшей мере один сложный эфир ЕРА и/или по меньшей мере один сложный эфир DHA.
[0022] В определенных вариантах осуществления любой или каждый из сложных эфиров ЕРА и DHA, составляющих композицию, является сложным этиловым эфиром.
[0023] В определенных вариантах осуществления композиции, описанные в данном документе, содержат практически чистый сложный этиловый эфир ЕРА и/или практически чистый сложный этиловый эфир DHA.
[0024] В определенных вариантах осуществления композиции, описанные в данном документе, по сути, включают практически чистый сложный этиловый эфир ЕРА и/или практически чистый сложный этиловый эфир DHA.
[0025] В определенных вариантах осуществления соотношение сложных эфиров ЕРА и DHA, составляющих композицию, составляет приблизительно 2,4:1 (сложный эфир ЕРА:сложный эфир DHA).
[0026] Определенные варианты осуществления предусматривают композиции, содержащие также натуральное апельсиновое масло, составляющее от приблизительно 0,1% до приблизительно 5% (вес/вес) указанной композиции. В вариантах осуществления, включающих натуральное апельсиновое масло, натуральное апельсиновое масло присутствует в количестве приблизительно 1,6% (вес/вес) композиции. Определенные другие варианты осуществления включают практически чистый d-лимонен, составляющий от приблизительно 0,1% до приблизительно 5%. В вариантах осуществления, включающих практически чистый d-лимонен, d-лимонен присутствует в количестве приблизительно 1,5% (вес/вес) композиции.
[0027] В определенных вариантах осуществления фармакологический эффект композиций, описанных в данном документе, практически не зависит от влияния пищи при введении субъекту.
[0028] По меньшей мере в одном варианте осуществления предусмотрена фармацевтическая композиция смешанных жирных кислот, в которой а) по меньшей мере 80% по весу композиции составляет комбинация (все-Z омега-3)-5,8,11,14,17-эйкозапентаеновых кислот (ЕРА) и (все-Z омега-3)-4,7,10,13,16,19-докозагексаеновых кислот (DHA) в весовом соотношении EPA:DHA от приблизительно 1:2 до приблизительно 2:1; b) (все-Z омега-3)-6,9,12,15,18-генэйкозапентаеновая кислота присутствует в количестве по меньшей мере одного процента по весу; и с) присутствует по меньшей мере одно поверхностно-активное вещество. Данные композиции могут необязательно дополнительно содержать натуральное апельсиновое масло в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) или практически чистый d-лимонен в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) композиции. Натуральное апельсиновое масло, как правило, присутствует в количестве приблизительно 1,6% (вес/вес) указанной композиции, и d-лимонен, как правило, присутствует в количестве приблизительно 1,5% (вес/вес) композиции.
[0029] По меньшей мере в одном варианте осуществления предусмотрена фармацевтическая композиция смешанных жирных кислот для лечения или профилактики по меньшей мере одного из множества факторов риска CVD, в которой а) по меньшей мере 80% по весу композиции составляют омега-3 жирные кислоты; b) по меньшей мере 80% по весу от общего содержания жирных кислот в композиции составляет комбинация (все-Z омега-3)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА) и (все-Z омега-3)-4,7,10,13,16,19-докозагексаеновой кислоты (DHA) в весовом соотношении EPA:DHA от 1:2 до 2:1, с) омега-3 жирные кислоты, кроме ЕРА и DHA, присутствуют в количестве по меньшей мере 1,5% по весу от общего содержания жирных кислот; и с) присутствует по меньшей мере одно поверхностно-активное вещество. Такие композиции могут необязательно дополнительно содержать натуральное апельсиновое масло в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) или практически чистый d-лимонен в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) композиции. Натуральное апельсиновое масло, как правило, присутствует в количестве приблизительно 1,6% (вес/вес) указанной композиции, и d-лимонен, как правило, присутствует в количестве приблизительно 1,5% (вес/вес) композиции.
[0030] По меньшей мере в одном варианте осуществления предусмотрена фармацевтическая композиция смешанных жирных кислот, в которой а) по меньшей мере 80% по весу композиции составляет комбинация (все-Z омега-3)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА) и (все-Z омега-3)-4,7,10,13,16,19-докозагексаеновой кислоты (DHA) в весовом соотношении EPA:DHA от 1:2 до 2:1, b) по меньшей мере 3% по весу композиции составляют омега-3 жирные кислоты, кроме ЕРА и DHA, которые содержат 18, 20, 21 или 22 атома углерода, и с) присутствует по меньшей мере одно поверхностно-активное вещество. Такие композиции могут необязательно дополнительно содержать натуральное апельсиновое масло в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) или практически чистый d-лимонен в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) композиции. Натуральное апельсиновое масло, как правило, присутствует в количестве приблизительно 1,6% (вес/вес) указанной композиции, и d-лимонен, как правило, присутствует в количестве приблизительно 1,5% (вес/вес) композиции.
[0031] По меньшей мере в одном варианте осуществления предусмотрена фармацевтическая композиция смешанных жирных кислот, в которой а) по меньшей мере 90% по весу композиции составляют длинноцепочечные полиненасыщенные омега-3 жирные кислоты; b) по меньшей мере 80% по весу композиции составляет комбинация (все-Z омега-3)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА) и (все-Z омега-3)-4,7,10,13,16,19-докозагексаеновой кислоты (DHA) в весовом соотношении EPA:DHA от 1:1 до 2:1, причем ЕРА составляет от 40 до 60% по весу композиции, и DHA составляет от 25 до 45% по весу композиции; с) по меньшей мере 4,5% по весу композиции составляют омега-3 жирные кислоты, кроме ЕРА и DHA, которые содержат 18, 20, 21 или 22 атома углерода; d) от 1 до 4% по весу композиции составляет (все-Z омега-3)-6,9,12,15,18-генэйкозапентаеновая кислота; е) присутствует по меньшей мере одно поверхностно-активное вещество; и f) композиция представлена в лекарственной форме для перорального применения и включает эффективное количество фармацевтически приемлемого антиоксиданта. Такие композиции могут необязательно дополнительно содержать натуральное апельсиновое масло в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) или практически чистый d-лимонен в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) композиции. Натуральное апельсиновое масло, как правило, присутствует в количестве приблизительно 1,6% (вес/вес) указанной композиции, и d-лимонен, как правило, присутствует в количестве приблизительно 1,5% (вес/вес) композиции.
[0032] Следует отметить, что во всех вариантах осуществления, включающих композиции, описанные в данном документе, общее количество всех ингредиентов, входящих в состав композиции, не превышает 100%.
[0033] В определенных вариантах осуществления предусмотрена фармацевтическая или лекарственная композиция, содержащая ЕРА и DHA в соотношении веса к весу от приблизительно 3,5:1 до приблизительно 5:1 и по меньшей мере одно поверхностно-активное вещество, и где композиция более чем на 84% по весу состоит из комбинированных ЕРА и DHA. Такие композиции могут необязательно дополнительно содержать натуральное апельсиновое масло в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) или практически чистый d-лимонен в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) композиции. Натуральное апельсиновое масло, как правило, присутствует в количестве приблизительно 1,6% (вес/вес) указанной композиции, и d-лимонен, как правило, присутствует в количестве приблизительно 1,5% (вес/вес) композиции.
[0034] Определенные варианты осуществления предусматривают определенные композиции, которые содержат по меньшей мере приблизительно 96% по весу этилэйкозапентаеноата (этил-ЕРА), по меньшей мере одно поверхностно-активное вещество, практически не содержат докозагексаеновую кислоту (DHA) или ее сложные эфиры. Такие композиции могут необязательно дополнительно содержать натуральное апельсиновое масло в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) или практически чистый d-лимонен в количестве от приблизительно 0,1% до приблизительно 5% (вес/вес) композиции. Натуральное апельсиновое масло, как правило, присутствует в количестве приблизительно 1,6% (вес/вес) указанной композиции, и d-лимонен, как правило, присутствует в количестве приблизительно 1,5% (вес/вес) композиции.
[0035] По меньшей мере в одном варианте осуществления предусмотрен способ лечения следующих нарушений: метаболического синдрома, дегенерации желтого пятна, дефицита омега-3, когнитивного нарушения, в том числе в результате хирургического вмешательства или травматического повреждения головного мозга (такого как, например, в результате сотрясения мозга), большой депрессии, суицидального поведения, послеродовой депрессии, воспаления, первичного склерозирующего холангита, пограничного расстройства личности у женщин, рака молочной железы, неалкогольной жировой болезни печени, и улучшения когнитивной деятельности и поведения у детей. Данные состояния или нарушения можно лечить путем введения композиций, описанных в данном документе, субъекту, как правило, человеку, нуждающемуся в таком введении.
[0036] По меньшей мере в одном варианте осуществления предусмотрен способ лечения по меньшей мере одного сердечно-сосудистого состояния или нарушения у субъекта, нуждающегося в таком лечении, причем указанный способ включает введение субъекту по меньшей мере одной композиции, описанной в данном документе, которая содержит терапевтически эффективное количество сложных эфиров омега-3 жирных кислот и по меньшей мере одно поверхностно-активное вещество.
[0037] По меньшей мере в одном варианте осуществления предусмотрен способ лечения по меньшей мере одного сердечно-сосудистого состояния или нарушения, например и без ограничений, нарушений в сердце и сосудистой системе, включая, например, гипертензию, гиперлипидемию, гипертриглицеридемию, атеросклероз, транзиторную ишемическую атаку, систолическую дисфункцию, диастолическую дисфункцию, аневризму, расслоение аорты, ишемию миокарда, острый инфаркт миокарда (AMI), острый инфаркт миокарда с подъемом сегмента ST (STEMI), острый инфаркт миокарда без подъема сегмента ST (NSTEMI), стенокардию, нестабильную стенокардию (UA) и стабильную стенокардию (SA), инфаркт миокарда, застойную сердечную недостаточность, дилатационную застойную кардиомиопатию, гипертрофическую кардиомиопатию, рестриктивную кардиомиопатию, легочное сердце, аритмию, порок клапанов сердца, эндокардит, легочную эмболию, венозный тромбоз, заболевание периферических сосудов и заболевание периферических артерий. Способ включает введение субъекту, нуждающемуся в лечении, терапевтически эффективного количества композиции, описанной в данном документе.
[0038] По меньшей мере в одном варианте осуществления предусмотрен способ лечения гипертензии и/или гиперлипидемии.
[0039] По меньшей мере в еще одном варианте осуществления предусмотрен способ лечения гипертриглицеридемии.
[0040] В определенных вариантах осуществления общее количество триглицеридов (TG) в крови субъекта-человека, у которого содержится ≥150 мг TG на дл сыворотки крови в начале применения схемы дозирования, снижается по меньшей мере на 20% в течение приблизительно 30 дней после введения композиций согласно определенным вариантам осуществления, описанным в данном документе.
[0041] По меньшей мере в еще одном варианте осуществления предусмотрен способ лечения субъекта-человека, у которого содержится ≥150 мг TG на дл сыворотки, который нуждается в таком лечении, причем указанный способ включает введение субъекту-человеку композиции согласно по меньшей мере одному варианту осуществления, описанному в данном документе, содержащей терапевтически эффективное количество сложных эфиров омега-3 жирных кислот.
[0042] Также предусмотрены варианты осуществления, где композиции, описанные в данном документе, упакованы вместе в виде набора с инструкциями по применению композиций для лечения сердечно-сосудистых состояний или нарушений.
[0043] В определенных вариантах осуществления поверхностно-активное вещество выбрано из группы, состоящей по меньшей мере из одного неионного поверхностно-активного вещества, катионного поверхностно-активного вещества, анионного поверхностно-активного вещества, цвиттерионного поверхностно-активного вещества или их комбинаций.
[0044] В определенных вариантах осуществления поверхностно-активное вещество выбрано из группы, состоящей по меньшей мере из одного анионного поверхностно-активного вещества, по меньшей мере одного неионного поверхностно-активного вещества и их комбинации.
[0045] В определенных вариантах осуществления, включающих по меньшей мере одно поверхностно-активное вещество, по меньшей мере одно поверхностно-активное вещество характеризуется гидрофильно-липофильным балансом (HLB), составляющим приблизительно 8,0.
[0046] В определенных вариантах осуществления, включающих по меньшей мере одно поверхностно-активное вещество, поверхностно-активное вещество может являться неионным поверхностно-активным веществом, выбранным из группы, состоящей по меньшей мере из одного полисорбата, по меньшей мере одного полоксамера и их комбинации.
[0047] В определенных вариантах осуществления, по меньшей мере одно поверхностно-активное вещество включает полисорбат, присутствующий в количестве от приблизительно 15% вес/вес до приблизительно 31% вес/вес композиции. В определенных вариантах осуществления полисорбат представляет собой полисорбат 80.
[0048] В определенных других вариантах осуществления по меньшей мере одно поверхностно-активное вещество включает полоксамер, присутствующий в количестве от приблизительно 0,1% до приблизительно 5% вес/вес композиции.
[0049] В определенных вариантах осуществления композиции, описанные в данном документе, содержат комбинацию полисорбата 80 и полоксамера Pluronic F87, [(НО(C2H4O)64(С3Н6О)37(C2H4O)64Н].
[0050] В определенных вариантах осуществления композиция дополнительно содержит по меньшей мере один антиоксидант. В таких вариантах осуществления по меньшей мере один антиоксидант выбран из группы, состоящей из токоферола, токотриенола или их комбинаций. В таких вариантах осуществления токоферол, токотриенол или их комбинации присутствуют в количестве от приблизительно 0,01% до приблизительно 5% по весу композиций. В определенных таких вариантах осуществления токоферолы, токотриенолы или их комбинации могут присутствовать в количестве приблизительно 0,01%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,8%, 0,9%, 1%, 1,5%, 2%, 2,5%, 3%, 3,5%, 4%, 4,5% или 5% по весу композиции. В определенных таких вариантах осуществления токоферолы, токотриенолы или их комбинации могут присутствовать в количестве приблизительно 0,4% по весу композиции. В определенных вариантах осуществления токоферол, токотриенол или комбинации присутствуют в количестве приблизительно 0,4% по весу композиции. В определенных вариантах осуществления, дополнительно включающих по меньшей мере один антиоксидант, антиоксидантом является токоферол в количестве приблизительно 0,4% по весу композиции.
[0051] В определенных вариантах осуществления композиция самостоятельно образует мицеллы в водной среде. В определенных других вариантах осуществления водная среда является водой. В определенных других вариантах осуществления водная среда имеет кислый рН. В определенных других вариантах осуществления водной средой является 0,1 н. HCl.
[0052] В определенных вариантах осуществления композиции, описанные в данном документе, самостоятельно образуют мицеллы в водной среде, где мицеллы имеют диаметр от приблизительно 1 мкм до приблизительно 10 мкм. В определенных вариантах осуществления композиции, описанные в данном документе, самостоятельно образуют мицеллы в водной среде, имеющей кислый рН, где мицеллы имеют диаметр от приблизительно 1 мкм до приблизительно 10 мкм. В определенных других вариантах осуществления композиции, описанные в данном документе, самостоятельно образуют мицеллы в 0,1 н. HCL, где мицеллы имеют диаметр от приблизительно 1 мкм до приблизительно 10 мкм. В определенных вариантах осуществления мицеллы имеют средний диаметр приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мкм.
[0053] В определенных вариантах осуществления композиции, описанные в данном документе, можно вводить с пищей или без пищи субъекту-человеку, нуждающемуся в таком введении, где биодоступность сложных эфиров омега-3 жирных кислот, составляющих композиции, практически не зависит от влияния пищи.
[0054] Определенные варианты осуществления предусматривают композиции, которые минимизируют или устраняют по меньшей мере один побочный эффект за счет введения композиции по настоящему раскрытию по сравнению с введением композиции, содержащей сложные эфиры омега-3 жирных кислот, которая практически не содержит поверхностно-активное вещество. В других вариантах осуществления неограничивающие примеры побочных эффектов включают регургитацию, частую отрыжку, гастроэзофагеальную рефлюксную болезнь (GERD), вздутие живота, увеличение количества кишечных газов, вкус рыбы, рыбный запах изо рта, запах рыбы, тошноту, диарею или их комбинации.
[0055] В определенных вариантах осуществления композиции, описанные в данном документе, содержат d-лимонен или натуральное апельсиновое масло. Такие композиции могут минимизировать или устранять по меньшей мере один побочный эффект за счет введения композиции по настоящему раскрытию по сравнению с введением композиции, содержащей сложные эфиры омега-3 жирных кислот, которая практически не содержит d-лимонен или натуральное апельсиновое масло. В других вариантах осуществления неограничивающие примеры побочных эффектов включают регургитацию, частую отрыжку, гастроэзофагеальную рефлюксную болезнь (GERD), вздутие живота, увеличение количества кишечных газов, вкус рыбы, рыбный запах изо рта, запах рыбы, тошноту, диарею или их комбинации.
[0056] В определенных вариантах осуществления композиции, описанные в данном документе, при введении субъекту-человеку, выбранному из группы, состоящей из индивидуумов, у которых содержится от приблизительно 155 до приблизительно 199 мг TG на дл сыворотки крови, от приблизительно 200 до приблизительно 499 мг TG на дл сыворотки крови и от приблизительно 500 мг или более TG на дл сыворотки крови, снижают указанные уровни TG в сыворотке субъекта по меньшей мере приблизительно на 20%.
[0057] Определенные варианты осуществления композиций, описанных в данном документе, можно вводить субъекту-человеку, нуждающемуся в таком введении, с гиполипидемическим средством, не являющимся сложным эфиром омега-3 жирной кислоты, выбранным из группы, состоящей из ингибиторов всасывания холестерина, секвестрантов желчных кислот/смол, статинов, ниацина и