Сульфосодержащие полимеры с собственной противовирусной активностью
Иллюстрации
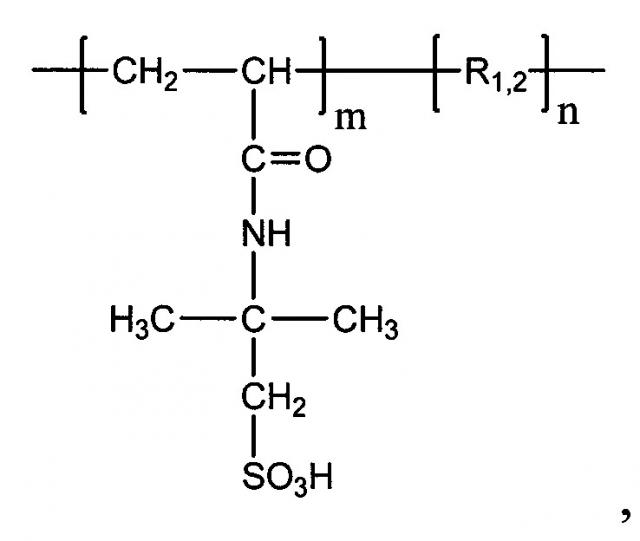
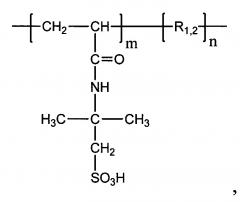
Показать всеИзобретение относится к высокомолекулярным соединениям медицинского назначения, а именно к новым синтетическим сульфосодержащим гомо- и сополимерам 2-акриламидо-2-метилпропансульфокислоты с собственной биоактивностью, которые могут быть использованы в фармакологии в качестве перспективных противовирусных средств или служить основой новых эффективных и безопасных противовирусных лекарственных средств и их лекарственных форм. Гомо- и сополимеры 2-акриламидо-2-метилпропансульфокислоты нижеуказанной формулы получают радикальной гетерофазной (со)полимеризацией в этаноле при 70°С в течение 24 ч. Гомо- и сополимеры 2-акриламидо-2-метилпропансульфокислоты имеют молекулярную массу ММ=(40-70)⋅103. Изобретение позволяет получить нетоксичные гомо- и сополимеры 2-акриламидо-2-метилпропансульфокислоты, имеющие собственную противовирусную активность против вирусов гриппа H3N2, H1N1. 1 табл., 2 пр.
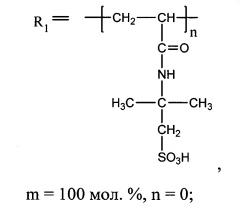
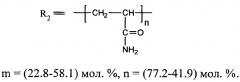
где
Реферат
Изобретение относится к химии высокомолекулярных соединений, а именно к получению биологически активных полимеров.
Известно, что многие полианионы обладают широким спектром противовирусной активности [Ершов Ф.И., Виноград И.А., Козловский М.М. Биологическая активность отечественного индуктора интерферона, созданного на основе малеинового ангидрида. Полимеры медицинского назначения ИНХС АН СССР. М.: Наука, 1988. С. 111-126; Сербин А.В., Стоцкая Л.Л., Кренцель Б.А. Сополимеры на основе фурана и малеинового ангидрида и перспективы их использования в медицине. Полимеры медицинского назначения. М.: Наука, 1988. С. 127-152; О.А. Тучная, О.В. Горлачук, В.А. Лившиц и др. Хим.-фарм. журн. 2008. Т. 42. №1. С. 6-12; К.Е. Gantlett, J.N. Weber and Q.J. Sattentan. Antiviral Res. 2007. Vol. 75. P. 188-197; A. Herrmann, T. Korte, K. Arnold, B. Hillebreht. Antiviral Res. 1992. Vol. 4. I. 1. P. 295-311]. Например, высокая противовирусная активность в отношении ряда вирусов выявлена у природных и синтетических полимеров, содержащих сульфогруппы [Wallac О. No entry for HIV. The next generation of HIV therapeutics are designed to prevent the virus from entering cells in the first place. Chem. in Britain. October 2000. P. 38-40; Lee Y.-X. Curdlan. Polysaccharides and Polyamides in the Food Industry. Ed. By A. Steinbuchel, S.K. Rhee. Wiley-VCH. Weinheim. 2005. Vol. 1. P. 210-232]. В частности, отмечена антивирусная активность декстран сульфата. Показано, что последний ингибирует слияние вируса гриппа при низком рН с мембранами эритроцитов и тем самым предотвращает гемолиз эритроцитов под действием вируса [Lee Y.-X. Curdlan. Polysaccharides and Polyamides in the Food Industry. Ed. By A. Steinbuchel, S.K. Rhee. Wiley-VCH. Weinheim. 2005. Vol. 1. P. 210-232].
Технической задачей и положительным результатом изобретения является получение сульфосодержащих полимеров с собственной противовирусной активностью, нетоксичных, эффективных в отношении штаммов вирусов гриппа H1N1 и H3N2.
Указанная задача достигается тем, что сульфосодержащие полимеры получены радикальной гетерофазной (со)полимеризацией в этаноле, инициируемой 2,2'-азобис(изобутиронитрилом) (AIBN), при 70°С в инертной атмосфере и представляют собой низкомолекулярные (молекулярной массы (ММ=(40-70)⋅103)) гомо- и сополимеры 2-акриламидо-2-метилпропансульфокислоты. Молекулярные массы гомо- и сополимеров определяли вискозиметрическим методом в 0.5 М NaCl при 25°С, используя уравнение [η]=1.95⋅10-5⋅Мη0.83 [Fisher L.W., Sochor A.R., Tan J.S. // Macromolecules. 1977. Vol. 10. P. 949-955].
где
Состав сополимеров акриламида (АА) с 2-акриламидо-2-метилпропансульфокислотой (ААМПСК) устанавливали по данным элементного анализа на содержание серы. Строение синтезированных полимеров подтверждали методами ИК- и ЯМР-спектроскопии. В ИК-спектре сополимеров наблюдаются полосы поглощения валентных колебаний (>С=O) групп при 1667 см-1 и характеристические полосы поглощения (-SO3H, SO3-) групп при 1219, 1038 и 624 см-1. Спектр ЯМР 1Н сополимеров, δ, м.д.: 1.42-1.7 (-СН2, СН3), 2.0-2.3 (-СН-), 3.1-3.6 (-CH2-SO3). Спектр ЯМР 13С сополимеров, δ, м.д.: 29.2 (СН3), 32.98-38.7 (-СН2), 44.4-46.12 (-СН-), 55.1 (>С<), 60.1-60.6 (-CH2-SO3), 178.5-178.6 (С=O) звеньев 2-акриламида-2-метилпропансульфокислоты, 182.2 (С=O) звеньев акриламида.
Более полно процесс получения гомо- и сополимеров 2-акриламидо-2-метилпропансульфокислоты изложен на следующих примерах.
Пример 1. Синтез поли-ААМПСК
.
Смесь 3.0 г (0.0145 моль) 2-акриламидо-2-метилпропансульфокислоты, 0.030 г (1.0 мас. %) AIBN, 8.9 мл этанола нагревали в атмосфере аргона в запаянной ампуле при 70°С в течение 24 ч, после чего выпавший полимер перемешивали в диэтиловом эфире, затем отфильтровали и высушили в вакууме. Выход: 2,97 г (99.0%). Далее продукт очищали диализом в течение 24 ч, при этом выделили 1.32 г полимера (44.0%), [η]=0.09 дл/г, Мη=26⋅103. Другие гомополимеры 2-акриламидо-2-метилпропансульфокислоты получали аналогичным образом.
Пример 2. Синтез сополимера АА-ААМПСК
Смесь 2.0 г (0.0281 моль) акриламида, 8.74 г (0.0422 моль) 2-акриламидо-2-метилпропансульфокислоты, 0.32 г (3.0 мас. %) AIBN, 43 мл этанола нагревали в запаянной ампуле в атмосфере аргона при 70°С 24 ч. По истечении указанного времени выпавший сополимер обработали диэтиловым эфиром, отфильтровали и высушили в вакууме. Выход: 10.6 г (98.7%). Затем сополимер очистили с помощью диализа (24 ч), после чего получили 7.8 г (72.6%) сополимера, содержащего 58.1 мол. % -SO3H групп, [η]=0.20 дл/г, Мη=68⋅103. Другие сополимеры 2-акриламидо-2-метилпропансульфокислоты получали аналогичным образом.
Данные по противовирусной активности синтезированных полимеров представлены в таблице.
Противовирусное действие исследуемых соединений определяли in vitro, рассчитывая Δlog ТИД50 - разницу логарифмов титра вируса в контроле и опыте, полученную для вируса гриппа методом реакции гемагглютинации при заражении клеток MDCK.
Анализ данных таблицы показывает, что все синтезированные полимеры обладают собственной противовирусной активностью. Следует подчеркнуть, однако, что значения Δlog ТИД50 равные и менее 1,25 относятся к случаям с низкой антивирусной активностью, такие полимеры не рассматриваются как противовирусные препараты. Значения Δlog ТИД50=2-2.5 считаются наиболее подходящими для противовирусных препаратов. Для поли-ААМПСК, ММ=26000, и сополимера АА-ААМПСК, ММ=68000, противовирусная активность имеет концентрационную зависимость. Для поли-ААМПСК, ММ=38000, и сополимера АА-ААМПСК, ММ=28000, противовирусный эффект наблюдается при фиксированной дозе 100 мкг/мл в отношении вируса гриппа H3N2. С увеличением ММ гомополимеров ААМПСК их противовирусный эффект проявляется при меньшей фиксированной концентрации. Исходя из данных таблицы, оптимальный состав сополимера представляется на уровне 22.8-58.1 мол. % -SO3H групп, так как снижение содержания -SO3H групп приводит к отсутствию активности в отношении вируса гриппа, а дальнейшее увеличение -SO3H групп не приводит к усилению противовирусной активности. Важную роль для проявления противовирусной активности как гомо-, так и сополимеров ААМПСК имеет их молекулярная масса, оптимальная, в данном случае, на уровне ММ=(40-70)⋅103, обеспечивающая одновременно использование таких полимеров в качестве самостоятельных противовирусных средств и в качестве безопасных носителей новых эффективных противовирусных лекарственных средств и их лекарственных форм.
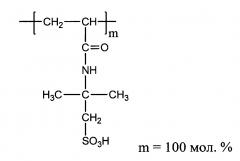
Сульфосодержащие полимеры с собственной противовирусной активностью против вируса гриппа H3N2, H1N1, характеризующиеся тем, что представляют собой гомо- и сополимеры 2-акриламидо-2-метилпропансульфокислоты молекулярной массы ММ=(40-70)⋅103, полученные радикальной гетерофазной (со)полимеризацией в этаноле при 70°С в течение 24 ч, общей формулы
где