Стабильный полимеризуемый уф-поглощающий краситель для интраокулярной линзы
Иллюстрации
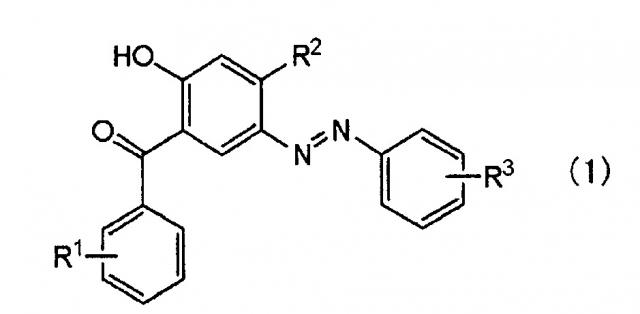
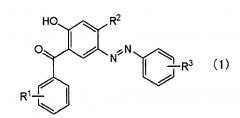
Показать всеИзобретение относится к соединению общей формулы (1), которое представляет собой полимеризуемый поглощающий УФ-свет окрашивающий мономер, обладающий превосходной стабильностью в щелочных условиях и являющийся пригодным полимерным материалом для интраокулярной линзы. В формуле (1) R1 представляет собой атом водорода, R2 представляет собой атом водорода, гидроксигруппу или алкоксигруппу, имеющую от 1 до 4 атомов углерода, и R3 представлен формулой (2), где R4 представляет собой атом водорода или метильную группу и R5 представляет собой алкиленовую группу, имеющую от 1 до 4 атомов углерода. Изобретение относится также к полимеру, содержащему указанное соединение, и интраокулярной линзе на его основе. 3 н. и 2 з.п. ф-лы, 3 ил., 14 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к красителю для интраокулярных линз. В частности, настоящее изобретение относится к полимеризуемому красителю, обладающему способностью поглощать ультрафиолетовый свет (УФ) и свет в голубой области.
УРОВЕНЬ ТЕХНИКИ
Катаракта представляет собой заболевание, при котором в хрусталике глаза возникают помутнение и пигментация, посредством этого вызывая состояние, при котором все поле зрение затуманивается. Что касается способа ее лечения, хирургическую операцию проводят так, чтобы удалить замутненный хрусталик глаза и ввести интраокулярную линзу (IOL) и установить в капсулу хрусталика глаза. Большинство материалов для интраокулярной линзы, которые применяют для лечения, основаны на акриловом или силиконовом полимере. В частности, например, до настоящего времени применяли полиметилметакрилат (PMMA).
Однако собственный хрусталик глаза обладает таким свойством, что через него не проходит ультрафиолетовый свет. Напротив, ультрафиолетовый свет проходит через традиционный полимер для интраокулярной линзы. Следовательно, существует риск, что сетчатка может быть повреждена.
Кроме того, собственный хрусталик глаза является слегка желтоватым, за счет чего обладает таким свойством, что часть света в синей области задерживается и не проходит через него. Однако свет в синей области практически полностью проходит через традиционный прозрачный полимер для интраокулярной линзы. Следовательно, пациенты жалуются на слепящий свет во многих случаях после операции по введению интраокулярной линзы. Кроме того, также есть риск того, что может быть вызвано заболевание, возникающее в сетчатке, включая, например, дегенерацию желтого пятна, когда свет в синей области, который имеет короткую длину волны и большую энергию, достигает внутренней части глаза.
Ввиду приведенного выше, требуется материал для интраокулярной линзы, который обладает способностью поглощать ультрафиолетовый свет, и окрашивание, осуществляемое желтым красителем. В последние годы, с точки зрения безопасности, поглощающий УФ мономер и/или мономер, придающий желтый цвет, сополимеризуют во многих полимерах для интраокулярной линзы. До настоящего времени были разработаны различные мономерные соединения, как описано выше (патентные документы 1-4). Также разработаны мономерные соединения, которые являются сополимеризуемыми с другими мономерами для материала интраокулярной линзы, каждый из которых имеет хромофор, такой как азогруппа или подобная, и поглощающую УФ часть, такую как на основе бензофеноновой структуры или подобной, в одной молекуле (патентные документы 5 и 6).
ДОКУМЕНТЫ ПРЕДШЕСТВУЮЩЕГО УРОВНЯ ТЕХНИКИ
Патентные документы:
Патентный документ 1: JP2685980B2;
Патентный документ 2: JPH10-251537A;
Патентный документ 3: JPH07-028911B2;
Патентный документ 4: JP2604799B2;
Патентный документ 5: JPH02-232056A;
Патентный документ 6: JP2006-291006A.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Проблемы, решаемые настоящим изобретением:
Полимеризуемые поглощающие УФ-свет окрашивающие мономеры, описанные в патентных документах 5 и 6, создают следующую проблему. А именно, мономеры недостаточно стабильны при изменении значения pH, особенно не стабильны в щелочных условиях, и окрашивающий фрагмент (хромофор и поглощающая УФ-свет часть) легко удаляется из полимера. В частности, в случае материала для интраокулярной линзы, который имплантируют в глаз на длительный период времени, риск удаления окрашивающего фрагмента дополнительно увеличивается. Ввиду приведенного выше, задача настоящего изобретения заключается в получении полимеризуемого поглощающего УФ-свет окрашивающего мономера, который является стабильным даже в щелочных условиях.
Способы решения проблем:
Изобретатели настоящего изобретения провели тщательные исследования для того, чтобы решить проблему, как описано выше. Как результат, было обнаружено, что проблема стабильности при изменении значения pH вызвана присутствием любой сложноэфирной связи между окрашивающим фрагментом и полимеризуемой группой в мономере. Кроме того, было обнаружено, что полимеризуемое поглощающее УФ-свет окрашивающее мономерное соединение, представленное следующей общей формулой (1), может решить проблему, как описано выше.
А именно, настоящее изобретение является следующим.
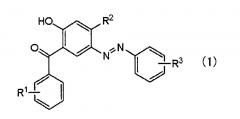
Один аспект настоящего изобретения относится к соединению, представленному следующей общей формулой (1) (далее называемому также "окрашивающее соединение настоящего изобретения").
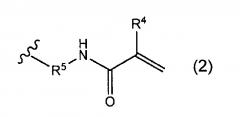
в общей формуле (1) R1 представляет собой атом водорода, гидроксигруппу, карбоксигруппу, алкильную группу, имеющую от 1 до 8 атомов углерода, алкоксигруппу, имеющую от 1 до 8 атомов углерода, группу сульфоновой кислоты или бензилоксигруппу, и предпочтительно атом водорода, метильную группу или этильную группу. R2 представляет собой атом водорода, гидроксигруппу или алкоксигруппу, имеющую от 1 до 4 атомов углерода, и предпочтительно атом водорода, гидроксигруппу, метоксигруппу или этоксигруппу. R3 представлен следующей формулой (2):
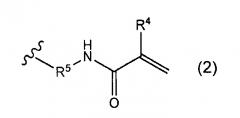
где R4 представляет собой атом водорода или метильную группу. Кроме того, R5 представляет собой одинарную связь или алкиленовую группу, имеющую от 1 до 4 атомов углерода, которая может иметь заместитель или заместители, предпочтительно алкиленовую группу, имеющую от 1 до 4 атомов углерода, которая не имеет заместителя.
Другой аспект настоящего изобретения относится к полимеру (далее называемому также "полимер настоящего изобретения"), содержащему окрашивающее соединение настоящего изобретения, описанное выше, и один или два или более видов других полимеризуемых мономеров, которые сополимеризуют друг с другом.
Еще один аспект настоящего изобретения относится к интраокулярной линзе (далее также называемой "интраокулярная линза настоящего изобретения"), содержащей полимер настоящего изобретения, описанный выше, который формуют.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложен полимеризуемый поглощающий УФ-свет окрашивающий мономер, который стабилен даже в щелочных условиях. Соединение, которое представлено общей формулой (1), имеет, в своей молекуле, бензофеноновую структуру, которая способна поглощать ультрафиолетовый свет, азобензольную структуру, которая способна поглощать свет в синей области, и полимеризуемую группу. Следовательно, соединение, представленное общей формулой (1), можно сополимеризовать с другим полимеризуемым мономером или полимеризуемыми мономерами, чтобы получить полимер. Полимер является пригодным в качестве материала для интраокулярной линзы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 показывает график, иллюстрирующий спектры поглощения в УФ и видимой области полимерного листа, полученного в примере 13.
Фиг. 2 показывает график, иллюстрирующий спектры поглощения в УФ и видимой области полимерного листа, полученного в примере 14.
Фиг. 3 показывает график, иллюстрирующий спектры поглощения в УФ и видимой области фильтратов, полученных после щелочной обработки полимеров.
СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение будет объяснено подробно ниже.
<1> Окрашивающее соединение настоящего изобретения
Окрашивающее соединение настоящего изобретения представлено следующей общей формулой (1).
В общей формуле (1) R1 представляет собой атом водорода, гидроксигруппу, карбоксигруппу, алкильную группу, имеющую от 1 до 8 атомов углерода, алкоксигруппу, имеющую от 1 до 8 атомов углерода, группу сульфоновой кислоты или бензилоксигруппу. Среди них, предпочтительно применять атом водорода, метильную группу или этильную группу с точки зрения реакционной эффективности при получении. В общей формуле (1) R2 представляет собой атом водорода, гидроксигруппу или алкоксигруппу, имеющую от 1 до 4 атомов углерода. Среди них предпочтительно применять атом водорода, гидроксигруппу, метоксигруппу или этоксигруппу с точки зрения реакционной эффективности при получении, и особенно предпочтительно применять гидроксигруппу с точки зрения характеристики поглощения лучей света. Как показано в общей формуле (1), окрашивающее соединение настоящего изобретения имеет бензофеноновую структуру и азобензольную структуру, и они представляют собой окрашивающие фрагменты. В общей формуле (1) R3 представлен следующей формулой (2).
В общей формуле (2) R4 представляет собой атом водорода или метильную группу.
В общей формуле (2) R5 представляет собой одинарную связь или алкиленовую группу, имеющую от 1 до 4 атомов углерода, которая может иметь заместитель или заместители, предпочтительно алкиленовую группу, имеющую от 1 до 4 атомов углерода, которая не имеет заместитель. Алкиленовая группа, имеющая от 1 до 4 атомов углерода, заданно обозначает метиленовую группу, этиленовую группу, пропиленовую группу или бутиленовую группу. Алкиленовая группа, как описано выше, может иметь заместитель или заместители, или алкиленовая группа, как описано выше, может не иметь заместителя. Когда алкиленовая группа, как описано выше, имеет заместитель или заместители, можно привести в качестве примера такой вариант, что заместитель или заместители включают, например, алкильную группу, имеющую от 1 до 2 атомов углерода, галогеновую группу, карбоксильную группу, карбокси-C1-C2-алкильную группу, гидрокси группу, гидроксиалкильную группу, имеющую от 1 до 2 атомов углерода, аминогруппу и аминоалкильную группу, имеющую от 1 до 2 атомов углерода, соединенных с атомом углерода или атомами алкиленовой группы.
Как описано выше, заместитель R3 представляет собой группу, в которой спейсер соединен с (мет)акрилоиламиногруппой, которая представляет собой полимеризуемую группу, и заместитель R3 представляет собой фрагмент, который участвует в сополимеризации, в окрашивающем соединении настоящего изобретения. Благодаря структуре, представленной общей формулой (2), окрашивающее соединение настоящего изобретения обладает таким свойством, что реакционная эффективность является высокой относительно других полимеризуемых мономеров.
Термин "(мет)акрилоил" обозначает "акрилоил" или "метакрилоил".
В общей формуле (1) предпочтительно, чтобы заместитель R3 был соединен с 3 положением или 4 положением азофенильной группы.
Окрашивающее соединение настоящего изобретения, представленное общей формулой (1), особым образом не ограничено, например, можно предпочтительно привести примеры соединений, имеющих следующую структуру.
Окрашивающее соединение настоящего изобретения содержит, в одной молекуле, бензофеноновую структуру (поглощающая УФ-свет часть), которая обладает способностью поглощать ультрафиолетовый свет, и азобензольную структуру (хромофор), которая обладает способностью поглощать свет в синей области. Благодаря присутствию его окрашивающей группы, окрашивающее соединение настоящего изобретения обладает способностью (храктеристика поглощения лучей света) подавлять пропускание лучей света в УФ области (длина волны: не более чем 380 нм) и в синей области (длина волны: от 380 до 500 нм). Окрашивающее соединение настоящего изобретения обладает превосходной характеристикой поглощения лучей света по сравнению с любым традиционным окрашивающим соединением (например, 2,4-дигидрокси-5-(4-(2-(N-2-метакрилоилоксиэтил)карбамоилокси)этилфенилазо)бензофеноном (BMAC), описанным в патентном документе 6. В особенности, когда измеряют спектры поглощения в УФ и видимой области, резкий рост кривой на графике возникает вблизи 420-500 нм, и соединение обладает превосходной способностью подавлять пропускание лучей света в УФ/синей области.
Кроме того, что касается окрашивающего соединения настоящего изобретения, часть, поглощающая УФ-свет, и хромофор (вместе также называемые "окрашивающий фрагмент") присутствуют в одной молекуле. Следовательно, почти не возникает неудобства, при котором хромофор повреждается ультрафиолетовым светом и краситель подвергается обесцвечиванию со временем.
Кроме того, полимеризуемая группа и окрашивающий фрагмент соединены амидной связью в окрашивающем соединении настоящего изобретения. Связь, как описано выше, является стабильной даже в щелочных условиях, и поэтому окрашивающий фрагмент не удаляется из полимера настоящего изобретения, как описано впоследствии. Как результат, достигается стабильность в щелочных условиях, которой обычно не хватает любому традиционному окрашивающему соединению, содержащему сложноэфирную связь, и любому сополимеру в данном применением.
Способ получения окрашивающего соединения настоящего изобретения особым образом не ограничен. Однако, например, окрашивающее соединение настоящего изобретения можно получить согласно способам синтеза 1-3, описанным ниже.
Способ синтеза 1
Данный способ включает стадию диазотирования аминоарильного соединения для получения соли диазония, стадию диазосочетания полученной соли диазония и бензофенонового соединения для получения диазосоединения, и стадию амидирования, заключающуюся в реакции полученного в результате диазосоединения, например, с соединением акриловой кислоты или с соединением метакриловой кислоты, посредством реакции амидирования для ввода полимеризуемой группы.
Краткое содержание способа синтеза 1 показано на следующей схеме реакций. В формуле R представляет собой блокирующую группу, R' представляет собой гидроксигруппу или атом галогена, и R1-R5 представляют собой одинаковые или эквивалентные заместители, как заместители, описанные выше.
Способ ситеза 2
Данный способ включает стадию амидирования аминоарильного соединения, например, соединением акриловой кислоты или соединением метакриловой кислоты, посредством реакции амидирования для ввода полимеризуемой группы, стадию диазотирования полученного полимеризуемого аминоарильного соединения для получения соли диазония, и стадию диазосочетания, заключающуюся в диазосочетании полученной в результате соли диазония с бензофеноновым соединением, для получения окрашивающего соединения настоящего изобретения.
Краткое содержание способа синтеза 2 показано на следующей схеме реакций. В формуле R представляет собой блокирующую группу, R' представляет собой гидроксигруппу или атом галогена, и R1-R5 представляют собой одинаковые или эквивалентные заместители, как заместители, описанные выше.
На стадии амидирования введения полимеризуемой группы в аминоарильное соединение, предпочтительно, чтобы аминогруппа в ароматической группе блокировалась блокирующей группой, и блокирующую группу удаляют, например, посредством кислотной обработки перед стадией диазотирования.
Способ синтеза 3
Данный способ включает стадию амидирования, заключающейся в применении нитроарильного соединения в качестве исходного соединения вместо аминоарильного соединения и реакции нитроарильного соеднинения, например, с соединением акриловой кислоты или с соединением метакриловой кислоты, посредством реакции амидирования для ввода полимеризуемой группы, стадию восстановления нитрогруппы полученного полимеризуемого нитроарильного соединения до аминогруппы, стадию диазотирования полученного полимеризуемого аминоарильного соединения для получения соли диазония, и стадию диазосочетания полученной в результате соли диазония с бензофеноновым соединением для получения окрашивающего соединения настоящего изобретения.
Краткое содержание способа синтеза 3 показано на следующей схеме реакций. В формуле R' представляет собой гидрокси группу или атом галогена, и R1-R5 представляют собой одинаковые или эквивалентные заместители, как заместители, описанные выше.
Альтернативно, окрашивающее соединение настоящего изобретения можно также получить, например, согласно способу синтеза, включающему стадию блокирования, заключающуюся в вводе блокирующей группы в алифатический амин аминоарильного соединения, стадию диазотирования аминоарильного соединения, в котором алифатический амин блокирован для получения соли диазония, стадию диазосочетания полученной в результате соли диазония с бензофеноновым соединением для получения диазосоединения, стадию деблокирования, заключающуюся в удалении блокирующей группы алифатического амина, например, посредством кислотной обработки, и стадию амидирования, заключающуюся в реакции полученного диазосоединения, например, с соединением акриловой кислоты или с соединением метакриловой кислоты, посредством реакции амидирования для ввода полимеризуемой группы.
Стадию диазотирования, которая включена в соответствующие способы синтеза, описанные выше, можно осуществлять согласно любому известному способу.
Можно применять, например, в качестве диазотирующего агента, нитрит натрия или водный раствор нитрита натрия, нитрит калия или водный раствор нитрита калия, изоамилнитрит и/или нитрозилсульфат (раствор серной кислоты). Применяемое количество диазотирующего агента особым образом не ограничено. Однако применяемое количество диазотирующего агента предпочтительно составляет 1,00-1,20 молей и более предпочтительно 1,02-1,10 молей на 1 моль аминоарильного соединения, содержащего полимеризуемую группу. Температура реакции на стадии диазотирования находится в диапазоне от -78°C до 50°C. Температура реакции предпочтительно находится в диапазоне от -20°C до 20°C и более предпочтительно в диапазоне от -20°C до 10°C. Предпочтительно, чтобы стадию диазотирования проводили в нейтральных или кислых условиях. Можно подходящим образом добавлять кислоту, такую как хлористоводородная кислота или подобная, к растворителю реакции.
Предпочтительно, чтобы стадию диазосочетания, которая включена в способы синтеза 2 и 3, проводили в слабо основных условиях, применяя слабое основание в качестве катализатора, по следующей причине. А именно, в случае сильного основания, включая, например, гидроксид натрия и гидроксид калия, обычно применяемые в реакции диазосочетания, амидная структура, которая находится в соли диазония полимеризуемого аминоарильного соединения, разлагается или удаляется, и выход целевого соединения снижается. Напротив, когда применяют слабое основание, то разложение заметно подавляется, и можно обеспечить достаточную реакционноспособность. Как результат, можно существенно повысить выход реакции. Дополнительно, известно, что винильная группа, которая находится в соли диазония, также полимеризуется в присутствии сильного основания, как описано выше, что вызывает заметное снижение выхода. Однако когда применяют слабое основание вместо сильного основания, также можно подавить данный недостаток.
Слабое основание, которое является пригодным в данном способе, особым образом не ограничено при условии, что слабое основание представляет собой соль, состоящую из сильной щелочи и слабой кислоты, где ее водный раствор не гидролизует амидную связь при 1 атм и 0°C-25°C, не вызывая реакции полимеризации винильной группы. Предпочтительно применять слабое основание, включая, например, карбонат натрия, гидрокарбонат натрия, карбонат калия, ацетат натрия и ацетат калия. Применяемое количество слабого основания предпочтительно составляет 4,0-10,0 молей и более предпочтительно 6,0-8,0 молей на 1 моль диазониевой соли, при переводе в натриевый эквивалент. Кроме того, температура реакции на стадии диазосочетания находится в диапазоне от -10°C до 10°C и более предпочтительно в диапазоне от -5°C до 5°C.
Можно применять, в качестве растворителя в реакции на стадии диазосочетания, органические растворители (спиртовой растворитель, такой как метанол, этанол, изопропиловый спирт и подобные, амидный растворитель, такой как N,N-диметилацетамид, N,N-диметилформамид, 1-метил-2-пирролидон и подобные, сульфоновый растворитель, такой как сульфоран и подобные, сульфоксидный растворитель, такой как диметилсульфоксид и подобные, уреидный растворитель, такой как тетраметилмочевина и подобный, галогенированный растворитель, такой как дихлорметан, хлороформ, 1,2-дихлорэтан и подобные, сложноэфирный растворитель, такой как этилацетат, бутилацетат и подобные, эфирный растворитель, такой как диэтиловый эфир, тетрагидрофуран и подобные, и пиридиновый растворитель, такой как пиридин, α-пиколин, 2,6-лутидин и подобные) отдельно или в виде смеси, состоящей из множества типов, а также в виде смеси, состоящей из органического растворителя и воды, и в виде системы, состоящей отдельно из воды. Однако среди них, предпочтительно применять спиртовой растворитель. Кроме того, также предпочтительно применять спиртовой растворитель при смешении его с водой. Кроме того, также допустимо добавлять и применять амидный растворитель, сложноэфирный растворитель и/или эфирный растворитель в добавление к спиртовому растворителю и воде, в зависимости от реакции.
Аминоарильное соединение, на которое ссылаются в настоящем изобретении, представлено (i) или (v) в схеме, описанной выше, и нитроарильное соединение представлено (ix) в схеме реакций. Кроме того, полимеризуемое аминоарильное соединение представлено (vi) или (vii) в схеме реакций, описанной выше, и полимеризуемое нитроарильное соединение представлено (x) в схеме реакций.
Полимеризуемое аминоарильное соединение или полимеризуемое нитроарильное соединение, описанные выше, можно получить, например, реакцией амидирования замещенного аминогруппой ароматического амина или замещенного нитрогруппой ароматического амина и (мет)акриловой кислоты, реакцией амидирования замещенного аминогруппой ароматического алкиламина или замещенного нитрогруппой ароматического алкиламина и (мет)акриловой кислоты, реакцией амидирования замещенного аминогруппой ароматического амина или замещенного нитрогруппой ароматического амина и хлорангидрида (мет)акриловой кислоты или реакцией амидирования замещенного аминогруппой ароматического алкиламина или замещенного нитрогруппой ароматического алкиламина и хлорангидрида (мет)акриловой кислоты. Что касается замещенного аминогруппой ароматического соединения, можно применять соединения, в которых амидная группа замещена блокирующей группой, включая, например, трет-бутоксикарбонильную группу, бензилоксикарбонильную группу, 9-флуоренилметилоксикарбонильную группу, 2,2,2-трихлорэтоксикарбонильную группу, аллилоксикарбонильную группу, п-толуолсульфонильную группу и 2-нитробензолсульфонильную группу.
Примеры полимеризуемого аминоарильного соединения, описанного выше, включают, например, N-(4-аминофенил)(мет)акриламид, N-[(4-аминофенил)метил](мет)акриламид, N-[2-(4-аминофенил)этил](мет)акриламид, N-[3-(4-аминофенил)пропил](мет)акриламид, N-[4-(4-аминофенил)бутил](мет)акриламид, N-[(3-аминофенил)метил](мет)акриламид, N-[2-(3-аминофенил)этил](мет)акриламид, N-[3-(3-аминофенил)пропил](мет)акриламид и N-[4-(3-аминофенил)бутил](мет)акриламид.
Дополнительно, примеры полимеризуемого нитроарильного соединения, описанного выше, включают, например, N-(4-нитрофенил)(мет)акриламид, N-[(4-нитрофенил)метил](мет)акриламид, N-[2-(4-нитрофенил)этил](мет)акриламид, N-[3-(4-нитрофенил)пропил](мет)акриламид, N-[4-(4-нитрофенил)бутил](мет)акриламид, N-[(3-нитрофенил)метил](мет)акриламид, N-[2-(3-нитрофенил)этил](мет)акриламид, N-[3-(3-нитрофенил)пропил](мет)акриламид и N-[4-(3-нитрофенил)бутил](мет)акриламид.
В качестве способа получения окрашивающего соединения настоящего изобретения, предпочтительно применять способ синтеза, в котором стадию амидирования проводят перед стадией диазосочетания, как в способе синтеза 2 или способе синтеза 3, по следующей причине. А именно, на стадии диазотирования способа синтеза 1, описанного выше, опасаются, что может образовываться любой побочный продукт, обладающий высокой реакционноспособностью, диазотированием ароматического амина. Напротив, согласно способу синтеза 2 или способу синтеза 3, описанным выше, стадию диазотирования проводят после предварительного введенния полимеризуемой группы, посредством, например, реакции амидирования. Следовательно, можно избежать образования побочного продукта, как описано выше. Как результат, согласно способу синтеза 2 или способу синтеза 3, реакционная эффективность является удовлетворительной, и можно получить окрашивающее соединение настоящего изобретения с высоким выходом.
Кроме того, нитроарильное соединение, которое применяют в качестве исходного соединения в способе синтеза 3, является более дешевым, чем аминоарильное соединение. Кроме того, в реакции амидирования, побочный продукт, в который введены две молекулы полимеризуемых групп относительно аминогруппы, обычно образуется при введении полимеризуемой группы. Однако, побочный продукт, который образуется при амидировании нитроарильного соединения, удаляется более легко, чем побочный продукт, который образуется, например, при амидировании аминоарильного соединения. Следовательно, принимая во внимание экономичность и также простоту рассматриваемой операции, способ синтеза 3, в котором нитроарильное соединение применяют в качестве исходного соединения, является особенно предпочтительным в качестве способа получения окрашивающего соединения настоящего изобретения. Окрашивающее соединение настоящего изобретения можно получить в промышленном масштабе, получая его согласно способу синтеза 2 или способу синтеза 3. Окрашивающее соединение настоящего изобретения является пригодным в качестве подходящего красителя или полимеризуемого поглощающего УФ-свет окрашивающего мономера.
<2> Полимер настоящего изобретения
Окрашивающее соединение настоящего изобретения можно превратить в полимер сополимеризацией окрашивающего соединения настоящего изобретения с одним видом или двумя или более видами другого сополимеризуемого мономера или мономеров. В окрашивающем соединении настоящего изобретения, хромофор и полимеризуемая группа стерически отделены друг от друга и, следовательно, полимеризация не ингибируется. Следовательно, окрашивающее соединение настоящего изобретения можно применять в качестве сополимеризуемого мономера, который обладает удовлетворительной реакционноспособностью относительно других сополимеризуемых мономеров. Другие сополимеризуемые мономеры, как описано выше, особым образом не ограничены, при условии, что мономеры применяют обыкновенным способом. Однако, например, примеры включают следующие мономеры.
Алкил(мет)акрилаты с нормальной, разветвленной цепью или циклические алкил(мет)акрилаты включают, например, метил(мет)акрилат, этил(мет)акрилат, пропил(мет)акрилат, изопропил(мет)акрилат, бутил(мет)акрилат, трет-бутил (мет)акрилат, изобутил (мет)акрилат, пентил(мет)акрилат, трет-пентил(мет)акрилат, гексил(мет)акрилат, гептил(мет)акрилат, октил(мет)акрилат, 2-этилгексил(мет)акрилат, нонил(мет)акрилат, децил(мет)акрилат, додецил(мет)акрилат, стеарил(мет)акрилат, циклопентил(мет)акрилат, циклогексил(мет)акрилат и фенокси(мет)акрилат;
кремнийсодержащие (мет)акрилаты, включая, например, пентаметилдисилоксанилметил(мет)акрилат, пентаметилдисилоксанилпропил(мет)акрилат, метилбис(триметилсилокси)силилпропил(мет)акрилат, трис(триметилсилокси)силилпропил(мет)акрилат, моно(метилбис(триметилсилокси)силокси)бис(триметилсилокси)силилпропил(мет)акрилат, трис(метилбис(триметилсилокси)силокси)силилпропил(мет)акрилат, метилбис(триметилсилокси)силилпропилглицерил(мет)акрилат, трис(триметилсилокси)силилпропилглицерил(мет)акрилат, моно(метилбис(триметилсилокси)силокси)бис(триметилсилокси)силилпропилглицерил(мет)акрилат, триметилсилилэтилтетраметилдисилоксанилпропилглицерил(мет)
акрилат, триметилсилилметил(мет)акрилат, триметилсилилпропил(мет)акрилат, триметилсилилпропилглицерил(мет)акрилат, пентаметилдисилоксанилпропилглицерил(мет)акрилат, метилбис(триметилсилокси)силилэтилтетраметилдисилоксанилметил(мет)акрилат, тетраметилтриизопропилциклотетрасилоксанилпропил(мет)акрилат и тетраметилтриизопропилциклотетрасилоксибис(триметил-силокси)силилпропил(мет)акрилат;
фторсодержащие (мет)акрилаты, включая, например, трифторэтил(мет)акрилат, тетрафторпропил(мет)акрилат, пентафторпропил(мет)акрилат, гексафторизопропил(мет)акрилат, тетрафтор-трет-пентил(мет)акрилат, гексафторбутил(мет)акрилат, гексафтор-трет-гексил(мет)акрилат, октафторпентил(мет)акрилат, 2,3,4,5,5,5-гексафтор-2,4-бис(трифторметил)пентил(мет)акрилат, додекафторгептил(мет)акрилат, 2-гидроксиоктафтор-6-трифторметилгептил(мет)акрилат, 2-гидроксидодекафтор-8-трифторметилнонил(мет)акрилат и 2-гидроксигексадекафтор-10-трифторметилундецил(мет)акрилат;
стирольные производные, включая, например, стирол, пентафторстирол, метилстирол, триметилстирол, трифторметилстирол, (пентаметил-3,3-бис(триметилсилокси)трисилоксанил)стирол, (гексаметил-3-триметилсилокситрисилоксианил)стирол и диметиламиностирол;
(мет)акрилаты, содержащие гидроксигруппу, включая, например, гидроксиэтил(мет)акрилат, гидроксипропил(мет)акрилат, гидроксибутил(мет)акрилат, дигидроксипропил(мет)акрилат, дигидроксидибутил(мет)акрилат, диэтиленгликольмоно(мет)акрилат, триэтиленгликольмоно(мет)акрилат и дипропиленгликольмоно(мет)акрилат;
(мет)акриловую кислоту;
винильные лактамы, включая, например, N-винилпирролидон, α-метилен-N-метилпирролидон, N-винилкапролактам и N-(мет)акрилоилпирролидон;
(мет)акриламиды, включая, например, (мет)акриламид, N-метил(мет)акриламид, N-этил(мет)акриламид, N-гидроксиэтил(мет)акриламид, N,N-диметил(мет)акриламид, N,N-диэтил(мет)акриламид и N-этил-N-аминоэтил(мет)акриламид;
аминоалкил(мет)акрилаты, включая, например, аминоэтил(мет)акрилат, N-метиламиноэтил(мет)акрилат и N,N-диметиламиноэтил(мет)акрилат;
(мет)акрилаты, содержащие алкоксигруппу, включая, например, метоксиэтил(мет)акрилат, этоксиэтил(мет)акрилат и метоксидиэтиленгликоль(мет)акрилат;
(мет)акрилаты, содержащие ароматическое кольцо, включая, например, бензил(мет)акрилат;
алкиловые эфиры, которые могут быть замещены алкильной группой, фторсодержащей алкильной группой или силоксанилалкильной группой, итаконовой кислоты, кротоновой кислоты, малеиновой кислоты, фумаровой кислоты и подобных;
глицидил(мет)акрилат;
тетрагидрофурфурил(мет)акрилат;
4-винилпиридин;
гетероциклические N-винильные мономеры, включая, например, винилимидазол, N-винилпиперидон, N-винилпиперидин и N-винилсукцинимид;
N-(мет)акрилоилпиперидин; и
N-(мет)акрилоилморфолин.
Термин "(мет)акрилат" обозначает "акрилат" или "метакрилат", и данное значение сохраняется тем же способом относительно производных (мет)акриловой кислоты.
Один вид или два или более видов сополимеризуемых мономеров, описанных выше, можно также выбирать и полимеризовать, получая макромономер, который можно применять в качестве одного из сополимеризуемых мономеров для получения полимера.
Полимер настоящего изобретения можно получить смешением окрашивающего соединения настоящего изобретения и одного вида или двух или более видов других сополимеризуемых мономеров в произвольных количествах, смешением их однородно или гомогенно, и затем их сополимеризацией. На соотношение, при котором окрашивающее соединение настоящего изобретения смешивают при сополимеризации полимера настоящего изобретения, влияет применение полимера, например, толщина в случае интраокулярной линзы. Однако соотношение предпочтительно составляет 0,001-5 масс. частей, более предпочтительно 0,005-2 масс. частей, и еще более предпочтительно 0,01-0,06 масс. частей на 100 масс. частей смеси всех сополимеризуемых мономеров. Если соотношение является меньшим чем 0,001 масс. частей, опасаются, что формирование цвета полимера может ухудшаться. С другой стороны, если соотношение превышает 5 масс. частей, опасаются, что прозрачность может снижаться из-за избыточной плотности окрашивания полимера, физические свойства (например, прочность) полимера могут ухудшаться, и/или окрашивающее соединение настоящего изобретения может легко вымываться из полимера.
Полимер настоящего изобретения можно синтезировать согласно любому способу, обычно осуществляемому в соответствующей области техники. Например, полимеризацию можно проводить однородным или гомогенным смешением окрашивающего соединения настоящего изобретения с одним видом или двумя или более видами других сополимеризуемых мономеров, добавлением инициатора полимеризации, при необходимости, и проведением постепенного нагревания в диапазоне температур от комнатной температуры до приблизительно 130°C, или подвергая воздействию электромагнитных волн, включая, например, микроволны, ультрафиолетовый свет и радиацию (гамма-излучение). Что касается полимеризации, можно приспособить различные способы, широко и обычно применяемые специалистами в данной области техники, включая, например, радикальную полимеризацию, полимеризацию в массе и полимеризацию в растворе (растворная полимеризация). При проведении полимеризации с нагреванием, также допустимо, чтобы температура повышалась постепенно.
Примеры инициатора полимеризации, описанного выше, включают, например, радикальные инициаторы полимеризации, включая, например, азобисизобутиронитрил, азобисдиметилвалеронитрил, 2,2'-азобис(2,4-диметилвалеронитрил), бензоилпероксид, трет-бутилгидропероксид, гидропероксид кумола и бензоилпероксид. Можно применять один вид или два или более видов из них. Предпочтительно, чтобы инициатор полимеризации применяли в количестве в диапазоне приблизительно 0,01-1 масс. частей на 100 масс. частей смеси всех сополимеризуемых мономеров. Когда полимеризацию проводят, применяя лучи света (излучение) или подобные, предпочтительно дополнительно добавлять фотоинициатор (фотоинициатор полимеризации) и сенсибилизатор.
При синтезировании полимера настоящего изобретения также можно применять в комбинации известный полимеризуемый поглотитель ультрафиолетовых лучей (поглотитель или абсорбент ультрафиолетовых лучей) (который в основном поглощает часть ультрафиолетового света) и полимеризуемый краситель (не обладающий способностью поглощать УФ-свет, в основном поглощает свет в синей области), а также полимеризуемый поглощающий УФ-свет краситель. Когда полимеризуемый поглотитель ультрафиолетовых лучей, полимеризуемый краситель и полимеризуемый поглощающий УФ-свет краситель, как описано выше, применяют в комбинации, посредством этого можно получить возможность точно регулировать баланс между способностью поглощать УФ-свет и способностью поглощать свет в синей области полимера. В частности, когда полимер настоящего изобретения применяют в качестве материала для интраокулярной линзы, как описано далее, применение в комбинации, как описано выше, является пригодным для того, чтобы регулировать цветовой тон интраокулярной линзы и/или в достаточной степени придавать способность поглощать УФ-свет. Регулирование осуществляют так, чтобы добавляемое количество являлось предпочтительно не большим чем 0,01 масс. частей и более предпочтительно не большим чем 0,05 масс. частей на 100 масс. частей смеси всех сополимеризуемых мономеров. Кроме того, для того чтобы обеспечить достаточную скорость полимеризации и достаточную степень полимеризации, регулирование осуществляют так, чтобы добавляемое количество являлось предпочтительно не большим чем 5 масс. частей и более предпочтительно не большим чем 3 масс. части на 100 масс. частей смеси всех сополимеризуемых мономеров.
Что каса