Комплекс для высокотемпературного воздействия на биологическую ткань (варианты)
Иллюстрации
Показать всеГруппа изобретений относится к медицинской технике, а именно к средствам локальной гипертермии. Комплекс для высокотемпературного воздействия на биологическую ткань содержит несколько модулей: модуль управления, соединенный с персональным компьютером, и связанные с этим модулем калибровочный модуль, не менее чем один модуль стабилизации температуры и для первого варианта - модуль ультразвукового введения. Каждый модуль содержит пульт управления и индикации и имеет соответствующие выводы для подачи напряжения питания. Калибровочный модуль выполнен с калибровочными пазами, предназначенными для размещения и калибровки в них устройств для передачи энергии в нагреваемую биоткань на заданную температуру. Каждый из модулей стабилизации температуры содержит связанный с модулем управления микроконтроллер с блоком памяти и каналы нагрева биоткани. Каждый канал нагрева биоткани образован блоком управления температурой, который содержит стабилизатор напряжения, управляющий ключ, усилитель, измерительный орган, выполненный в виде мостовой схемы, одно из плеч которой образовано нагревательным элементом устройства для передачи энергии в нагреваемую биоткань, и кожух. Устройство для передачи энергии в нагреваемую биоткань по первому варианту выполнено в виде игольчатого нагревателя, а по второму варианту - в виде поверхностного нагревателя. Кожух игольчатого нагревателя по первому варианту имеет возможность крепления к ультразвуковому излучателю модуля ультразвукового введения, связанному с ультразвуковым генератором. Использование изобретений позволяет повысить точность заданных значений температуры. 2 н. и 8 з.п. ф-лы, 2 ил.
Реферат
Заявляемое изобретение относится к области медицины, а именно к медицинской технике, и может быть использовано преимущественно в онкологии при лечении опухолевых заболеваний путем применения локальной гипертермии для воздействия на патологически измененные ткани тела человека или животных.
В настоящее время в лечении онкологических заболеваний используются различные способы, основанные на принципах высокотемпературного воздействия, а также комбинированные способы, одной из составляющих которых являются локальная гипертермия или термоабляция. Поэтому усовершенствование устройств, позволяющих эффективно реализовывать способы лечения заболеваний путем локальной гипертермии или термоабляции, является актуальным.
Из уровня техники известны устройства и комплексы разной степени сложности, применяемые для локального нагрева (локальная гипертермия) или высокотемпературного разрушения (термоабляция) биоткани, применяемые с целью лечения определенных опухолевых заболеваний.
Как отмечено в источнике [1. Патент РФ на изобретение №2332954, МПК А61В 18/04 (2006.01), опубл. 10.09.2008 г., Бюл. №25.], гипертермия - это нагревание опухоли до температуры 42-45 градусов, при которой наблюдается гибель раковых клеток и распад опухоли. «Злокачественная ткань менее устойчива к нагреванию, чем здоровая, по целому ряду причин. Во-первых, она изначально имеет более высокую температуру, так как обмен веществ в злокачественных клетках гораздо интенсивнее. Во-вторых, кровоснабжение опухолей гораздо хуже, чем у здоровых тканей, поэтому при нагревании они не способны эффективно охлаждаться увеличением кровотока, как здоровые. Кроме того, кислорода, доставляемого такими сосудами, начинает не хватать для энергообеспечения опухоли. В-третьих, сосуды в опухолях имеют аномальную структуру, поэтому при повышении температуры легко эмболизируются - закупориваются. В результате при повышении температуры в ткани опухоли развиваются гипоксия и ацидоз - закисление, которое приводит к нарушению функции и, в конечном итоге, гибели клеток. Таким образом, гипертермия обладает самостоятельным разрушающим воздействием на раковые клетки» [1].
Известно устройство для высокотемпературного разрушения биоткани [2. Патент на изобретение RU №2317793, опубл. 2008.02.27, МПК (2006.01) А61В 18/14, А61В 18/12, А61М 1/00, А61М 25/00, фиг. 2]. Это устройство [2] содержит биполярный электрод, генератор высокочастотного тока, блок управления, систему подвода теплоносителя. Биполярный электрод выполнен в виде изолированных друг от друга коаксиальных электродов, имеющих частичное покрытие из диэлектрика. Внутренний электрод выполнен в виде полой металлической иглы и не имеет изоляции на концевой части. Внешний электрод установлен с зазором относительно внутреннего электрода и имеет отверстие для подачи теплоносителя в биоткань. Термодатчик встроен в полость иглы внутреннего электрода. Внешний электрод снабжен тройником для подачи теплоносителя к зазору от системы подвода теплоносителя с встроенным в нее датчиком давления. Система подвода теплоносителя состоит из насоса, подводящего шланга и датчика давления. Блок управления содержит устройство регистрации температуры с термодатчика и устройство регулирования температуры теплоносителя. Биполярный электрод через фланец подключен к генератору и блоку управления. Блок управления связан также с насосом, который через датчик давления соединен с биполярным электродом.
Недостатком устройства является его сложность, обусловленная конструктивным выполнением его отдельных элементов, например биполярного электрода. Составные части биполярного электрода, выполненные в виде полых игл, коаксиально размещенных друг в друге с зазором, имеющих частичное покрытие из диэлектрика, и отверстия для подачи теплоносителя, требуют высокой точности их изготовления. Использование высокочастотного генератора, работающего на частоте 440 кГц и обеспечивающего нагрев теплоносителя, оказывает негативное воздействие как на клетки патологического участка, так и на клетки живой ткани. Кроме того, использование устройства такой конструкции предусматривает введение иглы непосредственно в опухоль, что может способствовать метастазированию опухолевой ткани. Также для работы данного устройства требуется сложная гидравлическая система, обеспечивающая прокачку под высоким давлением (до 1-2 бар) теплоносителя (дистиллированной воды), нагретого до 100-110°С. Такая система стабилизации не может обеспечить достаточно высокую точность поддержания заданного уровня температуры ввиду относительно длительного времени реагирования жидкого теплоносителя на изменение уровня подаваемой мощности высокочастотного генератора. При этом необходима высокая согласованность двух разнородных частей - генератора высокочастотного тока и системы подачи теплоносителя. Кроме того, необходима высокая степень стерильности внутренних поверхностей подводящего шланга, насоса, биполярного электрода, а также самого теплоносителя ввиду наличия открытого во внутренние ткани организма водяного контура.
Из уровня техники известен также комплекс для радиочастотного разрушения биоткани [3. Патент на полезную модель RU №82543, опубл. 10.05.2009, МПК (2006.01) А61В 18/12], который также может быть использован для локального нагрева биологической ткани. Этот комплекс содержит высокочастотный генератор с блоком управления (источник питания), резервуары с жидкостью, насосы, распределительное (коммутирующее) устройство. Комплекс [3] содержит также, по крайней мере, три устройства для передачи энергии в разрушаемую биоткань, одно из которых является центральным и имеет переменную полярность, а остальные (биполярные) - периферийными. Каждое из устройств для передачи энергии в разрушаемую биоткань выполнено в виде игольчатых электродов, имеющих один или несколько внутренних каналов для протекания охлаждающей жидкости. Выход высокочастотного генератора соединен с соответствующим игольчатым электродом через распределительное (коммутирующее) устройство, которое позволяет подключать электроды к высокочастотному генератору одновременно или в любой последовательности. Входы насосов соединены с соответствующим резервуаром, а выходы насосов подсоединены к соответствующим входам устройств передачи энергии в разрушаемую биоткань (игольчатых электродов) для охлаждения. Это устройство [3] позволяет увеличить объем коагулированной ткани и улучшить равномерность ее нагрева за счет введения в последовательность биполярных электродов дополнительного электрода с переменной полярностью.
Однако данная полезная модель [3] имеет ряд существенных недостатков. Во-первых, в [3] также как и в аналоге [2] в качестве источника энергии используется высокочастотный генератор, который оказывает негативное воздействие на здоровые клетки. Во-вторых, использование такого устройства возможно только в том случае, когда все игольчатые электроды (их как минимум три) введены непосредственно в опухолевую ткань, при этом центральный игольчатый электрод введен в центр опухолевой ткани - см. [3], что значительно повышает риск метастазирования опухоли при удалении электродов после окончания воздействия. В-третьих, такой комплекс [3] не обеспечивает равномерную температуру нагрева в заданном объеме биоткани. Так, согласно [3] при обеспечении зоны коагуляции до 5 см по уровню 50°С, температура в центре опухоли достигает 130°С, что является экстремальным для организма. В-четвертых, в комплексе [3] устройства для передачи энергии в разрушаемую биоткань (игольчатые электроды) имеют водяное охлаждение, для осуществления которого требуются соответствующие насосы и резервуары, что в целом усложняет и удорожает комплекс для радиочастотного разрушения биоткани. Кроме того, регулировка температуры в области воздействия осуществляется путем изменения как мощности радиочастотного генератора, так и скорости охлаждающей жидкости. При этом невозможно обеспечить высокую точность стабилизации температуры (в [3] температура изменялась в пределах 5°С).
Из уровня техники известен способ реализации локальной гипертермии [4. Патент на изобретение РФ №2467720, опубл. 27.11.2012, бюллетень №33, МПК (2006.01) А61В 18/12, A61N 7/00], в котором описано устройство для реализации этого способа (см. в описании пример конкретного выполнения). Устройство в источнике [4] содержит источник питания, который через выводы связан с соответствующими блоками управления температурой (в общем случае количество блоков управления соответствует количеству вводимых нагревательных игл и равно N). Каждый из блоков управления температурой выполнен как в источнике информации [5] и содержит регулятор напряжения, измерительный орган, усилитель, при этом измерительный орган выполнен в виде мостовой схемы с переменным резистором. Устройство в аналоге [4] содержит также ультразвуковой генератор, связанный с направляющими (в заявляемом изобретении направляющая названа кожухом игольчатого нагревателя). Направляющие предназначены для размещения в них соответствующих устройств для передачи энергии в разрушаемую биоткань - нагревательных игл (в заявляемом изобретении нагревательная игла названа игольчатым нагревателем). Каждая из нагревательных игл на своей поверхности имеет соответственно нагреватель (в заявляемом изобретении нагреватель назван нагревательным элементом). Каждый нагреватель связан с соответствующим блоком управления температурой. В устройстве [4] заданный уровень температуры, например 43-45°С, устанавливается вручную при помощи переменного резистора измерительного органа каждого из блоков управления температурой. В аналоге [4] приведен пример конкретного выполнения с использованием 8 каналов нагрева для передачи энергии в разрушаемую биоткань, и отмечено, что таких каналов нагрева может быть N. Устройство согласно аналогу [4] обеспечивает заданную, равномерную и стабильную температуру в требуемом объеме биологической ткани, содержащей опухоль и здоровую биоткань.
Однако в [4] заданный уровень температуры устанавливается с помощью ручной подстройки переменного резистора измерительного органа каждого из блоков управления температурой, что снижает точность устанавливаемого значения, тогда как для каждой процедуры нагрева в разных биотканях и при различных видах опухолей требуется индивидуальная установка данного параметра. Кроме того, устройство в [4] не обеспечивает возможность контроля процесса нагрева, который необходим особенно в тех случаях, когда оператор не может находиться рядом с устройством и пациентом, например, при реализации нагрева одновременно с лучевой терапией.
Близким техническим решением для обоих вариантов заявляемого изобретения является устройство для локального нагрева биологической ткани, описанное в [5. Патент на полезную модель RU №98116, опубл. 10.10.2010, МПК (2006.01) А61В 18/12]. Это устройство принято за прототип для каждого варианта изобретения. Устройство по прототипу [5] содержит источник питания, четыре устройства для передачи энергии в разрушаемую биоткань, связанные через соответствующие блоки управления температурой с источником питания. Каждый из блоков управления температурой включает измерительный орган, регулятор напряжения и усилитель. Каждое из устройств для передачи энергии в разрушаемую биоткань выполнено соответственно в виде иглы, имеющей на поверхности электрический нагреватель (нагревательный элемент). Каждый из измерительных органов выполнен в виде мостовой схемы с переменным резистором, одно из плеч которой образовано электрическим нагревателем иглы. В одну из диагоналей мостовой схемы измерительного органа включен усилитель, выход которого связан с управляющим входом регулятора напряжения. Регулятор напряжения имеет вывод, связанный с источником питания. Второй вывод регулятора напряжения связан с одной из вершин второй диагонали мостовой схемы измерительного органа, а другая вершина второй диагонали мостовой схемы подключена ко второму выводу источника питания. Это устройство [5] обеспечивает заданную, равномерную и стабильную температуру нагрева в локальном объеме биоткани. Заданный уровень температуры в примере конкретного выполнения [5] составляет 43-45°С и устанавливается вручную при помощи переменного резистора измерительного органа каждого из блоков управления температурой. Стабилизация температуры на электрических нагревателях на заданном уровне обеспечивается с точностью, которая определяется коэффициентом усиления усилителя. В примере конкретного выполнения, приведенном в [5], точность стабилизации температуры равна 0,1°С.
Однако на практике в зависимости от размеров и глубины расположения опухоли требуется использование нескольких устройств для передачи энергии в разрушаемую биоткань. Например, в аналоге [3] их количество равно трем, в аналоге [4] приведен пример конкретного выполнения с использованием 8 устройств для передачи энергии в разрушаемую биоткань. В аналоге [4] и в прототипе [5] отмечено, что таких устройств может быть N. Для осуществления эффективного нагрева необходимо, чтобы каждое из N устройств для передачи энергии в разрушаемую биоткань в любой зоне воздействия могло обеспечить требуемую температуру, необходимую для каждого конкретного случая.
В прототипе [5] заданный уровень температуры на нагревательном элементе устройства для передачи энергии в разрушаемую биоткань задается с помощью ручной подстройки переменного резистора измерительного органа каждого из блоков управления температурой, что можно осуществить только на специальном стенде, например, с жидкостным термостатом. Для этого необходимо заполнить специальную емкость жидкостного термостата жидким теплоносителем, например, водой и закрыть крышку емкости. Установить заданную температуру стабилизации. После ее достижения приоткрыть крышку емкости и поместить в нее один или несколько нагревателей. Выдержать некоторое время (не менее 1 минуты), после чего произвести калибровку нагревателя на заданную температуру с помощью ручной подстройки переменного резистора. При этом даже использование специального стенда не обеспечивает точность задаваемого значения температуры. Кроме того, для каждой конкретной процедуры высокотемпературного воздействия требуется установка своей заданной температуры, например в диапазоне 43-45°С для реализации локальной гипертермии, и/или нагрев выше 65°С - для реализации высокотемпературной абляции. В отдельных случаях может возникать необходимость в рамках одной процедуры нагрева одновременно устанавливать различные заданные значения температуры для разных нагревателей в пределах 43-65°С и выше и/или изменять их в процессе высокотемпературного воздействия. Потребность же в специальном стенде не позволяет осуществлять оперативную настройку и перенастройку заданного уровня температуры в процессе осуществления высокотемпературного воздействия. Кроме того, устройство по прототипу [5] (как и по аналогу [4]) не обеспечивает возможность дистанционного контроля и управления процессом нагрева биоткани, что особенно необходимо в тех случаях, когда оператор не может находиться рядом с устройством и пациентом, например, при реализации нагрева одновременно с лучевой терапией. Отмеченные выше недостатки в целом снижают эффективность использования устройства как по прототипу [5], так и по любому из указанных выше аналогов.
Таким образом, отмеченные выше недостатки позволяют сформулировать техническую проблему для обоих вариантов изобретения, связанную с необходимостью создания эффективного комплекса, обеспечивающего одновременно как заданную температуру, необходимую для каждого конкретного случая высокотемпературного «воздействия на биоткань, так и дистанционный контроль и управление процессом высокотемпературного нагрева биоткани.
Технический результат, достигаемый при решении указанной выше технической проблемы по каждому из вариантов изобретения, заключается в обеспечении точности заданных значений температуры для высокотемпературного воздействия на биоткань при одновременном дистанционном контроле и управлении процессом высокотемпературного воздействия.
Для решения технической проблемы и достижения технического результата по первому варианту изобретения заявляемый комплекс, как и прототип, содержит источник питания (на чертеже не показан) и, по крайней мере, три устройства для передачи энергии в нагреваемую биоткань, и, по крайней мере, три связанных с источником питания блока управления температурой. Каждый из блоков управления температурой включает измерительный орган, регулятор напряжения и усилитель, связанный с измерительным органом. Каждое из устройств для передачи энергии в нагреваемую биоткань выполнено в виде игольчатого нагревателя с нагревательным элементом. Измерительный орган выполнен в виде мостовой схемы, одно из плеч которой образовано нагревательным элементом игольчатого нагревателя.
В отличие от прототипа заявляемый комплекс по первому варианту содержит несколько модулей: модуль управления, имеющий возможность соединения с персональным компьютером для обеспечения дистанционного контроля и управления, и связанные с этим модулем калибровочный модуль, модуль ультразвукового введения и не менее одного модуля стабилизации температуры. Каждый из названных модулей содержит пульт управления и индикации и имеет соответствующий вывод для подачи напряжения питания. Калибровочный модуль выполнен с калибровочными пазами, предназначенными для размещения и калибровки в них устройств для передачи энергии в нагреваемую биоткань на заданную температуру. Каждый из модулей стабилизации температуры содержит связанный с модулем управления микроконтроллер с блоком памяти и каналы нагрева биоткани. Каждый канал нагрева биоткани каждого модуля стабилизации температуры образован блоком управления температурой, содержащим измерительный орган, выполненный в виде мостовой схемы (моста), включающей постоянные резисторы и нагревательный элемент игольчатого нагревателя, и кожухом, предназначенным для введения в него игольчатого нагревателя. Кожух игольчатого нагревателя имеет возможность крепления к ультразвуковому излучателю модуля ультразвукового введения, связанному с ультразвуковым генератором. Регулятор напряжения, входящий в блок управления температурой каждого канала нагрева биоткани, выполнен в виде стабилизатора напряжения, имеющего вход для подачи напряжения питания, и выход, связанный с первым входом управляющего ключа. Выход управляющего ключа связан с мостом, при этом второй вход управляющего ключа связан с соответствующим выводом микроконтроллера. Выход усилителя связан с соответствующим выводом микроконтроллера.
По второму варианту комплекс согласно заявляемому изобретению содержит источник питания (на чертеже не показан) и, по крайней мере, три устройства для передачи энергии в нагреваемую биоткань, и, по крайней мере, три связанных с источником питания блоков управления температурой. Каждый из блоков управления температурой включает измерительный орган, регулятор напряжения и усилитель, связанный с измерительным органом. Измерительный орган выполнен в виде мостовой схемы, одно из плеч которой образовано устройством для передачи энергии в нагреваемую биоткань.
В отличие от прототипа изобретение по второму варианту содержит несколько модулей: модуль управления, имеющий возможность соединения с персональным компьютером для обеспечения дистанционного контроля и управления, и связанные с этим модулем калибровочный модуль и не менее одного модуля стабилизации температуры. Каждый из названных модулей содержит пульт управления и индикации и имеет соответствующий вывод для подачи напряжения питания. Калибровочный модуль выполнен с калибровочными пазами, предназначенными для размещения и калибровки в них устройств для передачи энергии в нагреваемую биоткань на заданную температуру, выполненных, например, в виде поверхностных нагревателей. Каждый из модулей стабилизации температуры содержит связанный с модулем управления микроконтроллер с блоком памяти и каналы нагрева биоткани. Каждый канал нагрева биоткани каждого модуля стабилизации температуры образован блоком управления температурой, содержащим измерительный орган, выполненный в виде мостовой схемы (моста), включающей постоянные резисторы и нагревательный элемент поверхностного нагревателя. Регулятор напряжения, входящий в блок управления температурой каждого канала нагрева биоткани, выполнен в виде стабилизатора напряжения, имеющего вход для подачи напряжения питания, и выход, связанный с первым входом управляющего ключа. Выход управляющего ключа связан с мостом. Второй вход управляющего ключа связан с соответствующим выводом микроконтроллера. Выход усилителя связан с соответствующим выводом микроконтроллера.
В частных случаях в комплексе по первому и второму вариантам количество калибровочных пазов калибровочного модуля соответствует количеству каналов нагрева биоткани каждого модуля стабилизации температуры.
В частных случаях в комплексе по первому варианту игольчатый нагреватель имеет один или несколько внутренних каналов, а нагревательный элемент расположен внутри или на поверхности игольчатого нагревателя. Кроме того, ультразвуковой излучатель имеет разъем для крепления кожуха игольчатого нагревателя.
В частном случае в комплексе по второму варианту поверхностный нагреватель выполнен из эластичного или жесткого материала, а его нагревательный элемент расположен внутри или на его поверхности.
Оба варианта изобретения, по мнению авторов и заявителей, соответствуют критерию патентоспособности «новизна», поскольку в уровне техники не обнаружено комплекса для высокотемпературного воздействия на биологическую ткань, характеризуемого той же совокупностью признаков, что и заявляемый комплекс в обоих вариантах.
Из уровня техники не обнаружены комплекс (или устройство), которые обеспечивают точность заданной температуры для каждого конкретного случая в любой биоткани, подвергаемой температурному воздействию, при одновременном осуществлении дистанционного контроля и управления процессом нагрева. Это достигается за счет того, что комплекс выполнен в виде нескольких модулей: модуля управления, калибровочного модуля, модуля ультразвукового введения и N модулей стабилизации температуры, имеющих М каналов нагрева (по первому варианту изобретения) или модуля управления, калибровочного модуля, N модулей стабилизации температуры, имеющих М каналов нагрева (по второму варианту изобретения). При этом новое техническое выполнение модулей (частей комплекса) и новые связи, как между модулями, так и между конструктивными элементами внутри модулей обеспечивают конструктивное единство и общее функциональное назначение комплекса для высокотемпературного воздействия на биологическую ткань.
Оба варианта изобретения объединены единым изобретательским замыслом, поскольку решают одну и ту же техническую проблему, направлены на достижение одного и того же технического результата, то есть на создание эффективного комплекса, обеспечивающего точность требуемых значений температуры для различных заданных диапазонов высокотемпературного воздействия на биоткань при одновременном дистанционном контроле и управлении процессом высокотемпературного воздействия. Изобретение явным образом для специалиста не следует из уровня техники и соответствует, по мнению заявителей, требованиям критерия охраноспособности «изобретательский уровень».
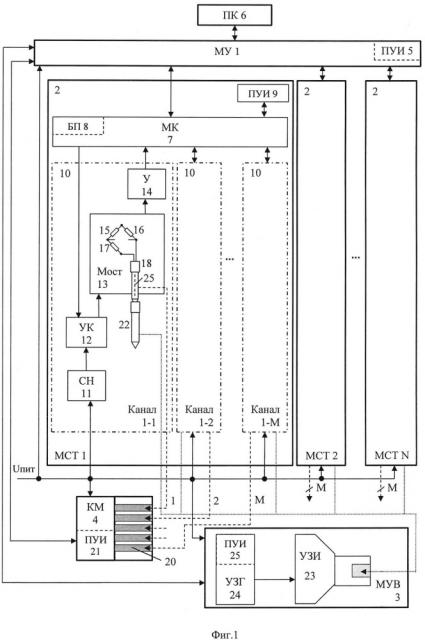
Сущность комплекса для высокотемпературного воздействия на биологическую ткань поясняется чертежами. На фиг. 1 показана блок-схема комплекса по первому варианту. На фиг. 2 показана блок-схема комплекса по второму варианту.
Комплекс по обоим вариантам (фиг. 1, 2) содержит модуль управления 1 МУ, N модулей стабилизации температуры 2 МСТ, модуль ультразвукового введения 3 МУВ, калибровочный модуль 4 КМ, на каждый из которых подается напряжение питания Uпит. Модуль управления 1 имеет пульт управления и индикации 5 ПУИ, предназначенный для установки и отображения параметров функционирования комплекса для высокотемпературного воздействия на биологическую ткань. Кроме того, модуль управления 1 связан с персональным компьютером 6 ПК, который позволяет осуществлять дистанционный контроль и управление процессом нагрева биоткани. Модуль управления 1 связан с каждым из N модулей стабилизации температуры 2. В состав каждого из N модулей стабилизации температуры входят микроконтроллер 7 с блоком памяти 8, пульт управления и индикации 9 и М каналов нагрева 10 (Канал). Каждый из М каналов нагрева 10 содержит стабилизатор напряжения 11, управляющий ключ 12, мост 13 и усилитель 14. Мост 13 состоит из резисторов 15-17 и нагревательного элемента 25 устройства для передачи энергии в нагреваемую биоткань (в частном случае, выполненного в виде игольчатого нагревателя 18 (первый вариант)) или нагревательного элемента 26 поверхностного нагревателя 19, выполненного в виде пластины (второй вариант см. фиг. 2). Нагревательные элементы 25 и 26, как в первом, так и во втором вариантах расположены либо на поверхности, либо внутри нагревателей 18 или 19 соответственно. В конкретном примере выполнения на фиг. 1, 2 показано размещение нагревательных элементов 25 и 26 внутри нагревателей позиции 18 и 19. В обоих вариантах для калибровки на заданную температуру нагревательных элементов 25 и 26 игольчатого нагревателя 18 и поверхностного нагревателя 19 соответственно используется калибровочный модуль 4 с М калибровочными пазами 20 и пультом управления и индикации 21, предназначенным для включения калибровочного модуля 4, установки его параметров и их отображения. Калибровочный модуль 4 позволяет осуществлять калибровку температуры нагревательных элементов 25 и 26 с точностью ±0,1°С. В первом варианте игольчатый нагреватель 18 может иметь внутренние каналы для подачи лекарственных средств.
В первом варианте (фиг. 1) кожух игольчатого нагревателя 22 имеет возможность крепления к ультразвуковому излучателю 23 модуля ультразвукового введения 3, подключенному к ультразвуковому генератору 24. Для установки параметров и их отображения модуль ультразвукового введения 3 содержит пульт управления и индикации 21.
В комплексе по второму варианту (фиг. 2) устройство для передачи энергии в нагреваемую биоткань выполнено в виде поверхностного нагревателя 19, например, плоскостного элемента - пластины. В других случаях форма поверхностного нагревателя 19 может быть любой, обеспечивающей плотное его прилегание к области нагрева.
Изобретение в обоих вариантах промышленно применимо. Его изготовление по обоим вариантам не вызывает трудностей у специалистов в области преобразовательной техники. Комплекс может быть неоднократно реализован с использованием общедоступных комплектующих элементов и блоков.
Комплекс работает следующим образом. После определения места расположения опухоли (например, при помощи томографического или ультразвукового исследования) намечаются точки для ввода игольчатых нагревателей 18 (при глубоком расположении опухоли) и/или области установки поверхностных нагревателей 19. При включении комплекса подается напряжение питания Uпит на все модули. Для включения каждого модуля, для запуска и контроля процессов калибровки и стабилизации температуры, а также для осуществления введения кожухов игольчатых нагревателей 22 могут использоваться персональный компьютер 6 (например, ноутбук Irbis NB10), пульт управления и индикации 5 модуля управления 1, а также пульты управления и индикации 9 (на модуле стабилизации температуры 2), 21 (на калибровочном модуле 4) и 25 (на модуле ультразвукового введения).
Процесс калибровки осуществляется следующим образом. На калибровочном модуле 4 задается температура, на которую будет осуществляться стабилизация температуры нагревательных элементов 25 или 26. Далее игольчатые нагреватели 18 или поверхностные нагреватели 19 помещаются в калибровочные пазы 20 калибровочного модуля 4 и выдерживаются там в течение не менее 1 минуты. После этого осуществляется сохранение необходимых параметров в блоке памяти 8 микроконтроллера 7 того модуля стабилизации температуры 2, к которому подключены калибруемые игольчатые нагреватели 18 или поверхностные нагреватели 19.
Далее (для случая глубокого расположения опухоли) кожухи игольчатых нагревателей 22 (в количестве, равном количеству откалиброванных игольчатых нагревателей 19) по одному крепятся к ультразвуковому излучателю 23 модуля ультразвукового введения 3. С помощью ультразвукового генератора 24 осуществляется генерация ультразвуковых колебаний и передача их на ультразвуковой излучатель 23 с кожухом игольчатого нагревателя 22. С помощью этих колебаний осуществляется введение кожухов игольчатых нагревателей 22 в биологическую ткань. После введения кожух игольчатого нагревателя 22 открепляется от ультразвукового излучателя 23 и данный процесс повторяется для каждого кожуха игольчатого нагревателя 22. Когда все кожухи игольчатых нагревателей 22 введены в биологическую ткань, в них вводятся игольчатые нагреватели 18. Для второго варианта осуществляется размещение необходимого количества поверхностных нагревателей 19 на поверхности области нагрева. После этого запускается процесс стабилизации температуры.
Процесс стабилизации температуры осуществляется следующим образом. Напряжение питания Uпит подается через стабилизатор напряжения 11 и управляющий ключ 12 на мост 13. Так как в состав моста входят резисторы 15-17 и нагревательный элемент 25 игольчатого нагревателя 18 или нагревательный элемент 26 поверхностного нагревателя 19, то при прохождении тока через мост 13 происходит повышение температуры нагревательного элемента 25 или 26. Резисторы 15-17 подобраны таким образом, чтобы максимальная мощность выделялась на нагревательном элементе 25 или 26. Разность напряжений в двух ветвях моста усиливается усилителем 14 и подается на микроконтроллер 7. Микроконтроллер 7 сравнивает текущее значение со значением, записанным в блоке памяти 8. Если текущее значение превышает записанное, то микроконтроллер 7 подает команду на закрытие управляющего ключа 12, в результате чего напряжение со стабилизатора напряжения 11 перестает поступать на мост 13 и нагревательный элемент 25 или 26 начинает остывать. Как только усиленное значение разности напряжений в ветвях моста 13 станет меньше значения, записанного в блоке памяти 8, микроконтроллер 7 подаст команду на открытие управляющего ключа 12, что приведет к повышению температуры нагревательного элемента 25 или 26. Этот процесс продолжается в течение всей процедуры нагрева в каждом задействованном модуле стабилизации температуры 2 для всех игольчатых нагревателей 18 и/или поверхностных нагревателей 19.
Приведенный пример конкретного выполнения обеспечивает точность калибровки температуры нагревательных элементов ±0,1°С и дистанционный контроль и управление процессом нагрева, что в целом обеспечивает эффективность использования комплекса для применения процедуры нагрева в лечении больных.
Приведенный пример не ограничивает область применения комплекса согласно обоим вариантам изобретения. Его применение будет также эффективно, например, в других областях медицины, когда требуются просто другие значения температуры воздействия для получения терапевтического эффекта.
1. Комплекс для высокотемпературного воздействия на биологическую ткань, содержащий источник питания и, по крайней мере, три устройства для передачи энергии в нагреваемую биоткань, и, по крайней мере, три связанных с источником питания блока управления температурой, каждый из которых включает измерительный орган, регулятор напряжения и усилитель, связанный с измерительным органом; при этом каждое из устройств для передачи энергии в нагреваемую биоткань выполнено в виде игольчатого нагревателя с нагревательным элементом, а измерительный орган выполнен в виде мостовой схемы, одно из плеч которой образовано нагревательным элементом игольчатого нагревателя, отличающийся тем, что дополнительно содержит несколько модулей: модуль управления, имеющий возможность соединения с персональным компьютером для обеспечения дистанционного контроля и управления, и связанные с этим модулем калибровочный модуль, модуль ультразвукового введения и не менее одного модуля стабилизации температуры, каждый из названных модулей содержит пульт управления и индикации и имеет соответствующие выводы для подачи напряжения питания; при этом калибровочный модуль выполнен с калибровочными пазами, предназначенными для размещения и калибровки в них устройств для передачи энергии в нагреваемую биоткань на заданную температуру, а каждый из модулей стабилизации температуры содержит связанный с модулем управления микроконтроллер с блоком памяти и каналы нагрева биоткани, при этом каждый канал нагрева биоткани каждого модуля стабилизации температуры образован блоком управления температурой, содержащим измерительный орган, выполненный в виде мостовой схемы (моста), включающей постоянные резисторы и нагревательный элемент игольчатого нагревателя, и кожухом, предназначенным для введения в него игольчатого нагревателя, при этом кожух игольчатого нагревателя имеет возможность крепления к ультразвуковому излучателю модуля ультразвукового введения, связанному с ультразвуковым генератором, кроме того, регулятор напряжения, входящий в блок управления температурой каждого канала нагрева биоткани, выполнен в виде стабилизатора напряжения, имеющего вход для подачи напряжения питания, и выход, связанный с первым входом управляющего ключа, выход которого связан с мостом, при этом второй вход управляющего ключа связан с соответствующим выводом микроконтроллера, а выход усилителя связан с соответствующим выводом микроконтроллера.
2. Комплекс для высокотемпературного воздействия на биологическую ткань по п. 1, отличающийся тем, что игольчатый нагреватель имеет один или несколько внутренних каналов.
3. Комплекс для высокотемпературного воздействия на биологическую ткань по п. 1, отличающийся тем, что нагревательный элемент расположен внутри или на поверхности игольчатого нагревателя.
4. Комплекс для высокотемпературного воздействия на биологическую ткань по п. 1, отличающийся тем, что количество калибровочных пазов калибровочного модуля соответствует количеству каналов нагрева биоткани каждого модуля стабилизации температуры.
5. Комплекс для высокотемпературного воздействия на биологическую ткань по п. 1, отличающийся тем, что ультразвуковой излучатель имеет разъем для крепления кожуха игольчатого нагревателя.
6. Комплекс для высокотемпературного воздействия на биологическую ткань, содержащий источник питания и, по крайней мере, три устройства для передачи энергии в нагреваемую биоткань, и, по крайней мере, три связанных с источником питания блока управления температурой, каждый из которых включает измерительный орган, регулятор напряжения и усилитель, связанный с измерительным органом; при этом измерительный орган выполнен в виде мостовой схемы, одно из плеч которой образовано устройством для передачи энергии в нагреваемую биоткань, отличающийся тем, что дополнительно содержит несколько модулей: модуль управления, имеющий возможность соединения с персональным компьютером для обеспечения дистанционного контроля и управления, и связанные с этим модулем калибровочный модуль и не менее одного модуля стабилизации температуры, каждый из названных модулей содержит пульт управления и индикации и имеет соответствующие выводы для подачи напряжения питания; при этом калибровочный модуль выполнен с калибровочными пазами, предназначенными для размещения и калибровки в них устройств для передачи энергии в нагреваемую биоткань на заданную температуру, выполненных в виде поверхностных нагревателей, а каждый из модулей стабилизации температуры содержит связанный с модулем управления микроконтроллер с блоком памяти и каналы нагрева биоткани, при этом ка