Производное циклического амина и его фармацевтическое применение
Иллюстрации
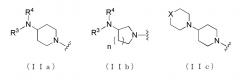
Показать всеИзобретение относится к области органической химии, а именно к производным циклического амина формулы (I), где A представляет собой группу, представленную общей формулой (IIa), (IIb) или (IIc), где, когда A представляет собой группу, представленную общей формулой (IIa) или (IIb), R1 представляет собой алкильную группу, содержащую 1 или 2 атома углерода и необязательно замещенную гидроксильной группой, аминогруппой или карбоксильной группой, R2 представляет собой атом водорода, R3 представляет собой атом водорода или алкильную группу, содержащую 1 или 2 атома углерода, R4 представляет собой атом водорода или алкилкарбонильную группу, содержащую 2 атома углерода, или алкильную группу, содержащую 1 или 2 атома углерода и необязательно замещенную алкилкарбониламиногруппой, содержащей 2 атома углерода, и n обозначает 1 или 2, в которой, когда R3 и R4, каждый, независимо, представляют собой алкильную группу, содержащую 1 или 2 атома углерода, R1 представляет собой алкильную группу, содержащую 1 или 2 атома углерода и замещенную гидроксильной группой, аминогруппой или карбоксильной группой; и когда A представляет собой группу, представленную общей формулой (IIc), R1 представляет собой алкильную группу, содержащую 1 атом углерода и замещенную карбоксильной группой, R2 представляет собой атом водорода, X представляет собой CH2, O или -NR5 и R5 представляет собой алкильную группу, содержащую 1 атом углерода. Также изобретение относится к пролекарству соединения формулы (I), лекарственному средству, анальгетическому агенту и терапевтическому агенту на основе соединения формулы (I) или его пролекарства. Технический результат: получены новые производные имидазола, полезные при лечении боли. 6 н. и 5 з.п. ф-лы, 24 ил., 5 табл., 73 пр.
Реферат
Область техники
[0001]
Настоящее изобретение относится к производному циклического амина и его фармацевтическому применению.
Предпосылки изобретения
[0002]
Боль является неприятным сенсорным и эмоциональным переживанием, связанным с фактическим или возможным повреждением тканей. В соответствии с причиной боль классифицируется на ноцицептивную боль, невропатическую боль и психогенную боль. В качестве боли, вызванной неизвестной причиной, известен синдром фибромиалгии.
[0003]
Невропатическая боль является патологической болью, вызванной дисфункцией периферической или центральной нервной системы, более конкретно, болью, вызванной, например, прямым повреждением и угнетением нервной ткани, несмотря на не ноцицептивный раздражитель ноцицептора. В качестве терапевтического агента при невропатической боли используется противосудорожное средство, антидепрессант, анксиолитическое средство или противоэпилептическое средство, такие как габапентин или прегабалин.
[0004]
Синдром фибромиалгии представляет собой расстройство, в котором системная боль является ведущим симптомом, а психоневрологические и нейровегетативные симптомы являются вторичными симптомами. В качестве терапевтических средств для лечения синдрома фибромиалгии, в основном, используются прегабалин, который был одобрен в Соединенных Штатах и Японии, дулоксетин и милнаципран, которые были одобрены в Соединенных Штатах. Кроме того, используются лекарственные средства, которые не утверждены в качестве терапевтического средства для лечения синдрома фибромиалгии, т.е. нестероидное противовоспалительное средство, опиоидное соединение, антидепрессант, противосудорожное средство и противоэпилептическое лекарственное средство. Тем не менее, обычно утверждают, что нестероидные противовоспалительные средства и опиумные соединения имеют низкий терапевтический эффект (непатентная литература 1).
[0005]
Помимо этого, в патентной литературе 1 описано, что замещенные пиперидины обладают кардиотоническое активностью; в патентной литературе 2 описано, что производные имидазола оказывают ингибирующее FXa действие; и в патентной литературе 3 высказано предположение, что замещенные пиперидины имеют потенциальную лекарственную эффективность против избыточного веса или ожирения.
Список цитируемой литературы
Патентная литература
[0006]
Патентная литература 1: патент Франции 2567885
Патентная литература 2: патентная публикация JP (Kokai) № 2006-008664
Патентная литература 3: международная публикация WO 2003/031432
Непатентная литература
[0007]
Непатентная литература 1: Recla, Journal of Pain Research, vol. 3, p. 89-103, 2010.
Сущность изобретения
Техническая задача
[0008]
Однако терапия с использованием обычного терапевтического средства для лечения невропатической боли чрезвычайно часто связана с побочными реакциями центральной нервной системы, такими как головокружение, тошнота или рвота. Из-за этого является сложным принимать обычный терапевтический агент в течение длительного времени. В связи с этим была желательна разработка нового терапевтического средства для лечения невропатической боли.
[0009]
Даже прегабалин, дулоксетин и милнаципран, которые были утверждены в качестве терапевтических средств для лечения синдрома фибромиалгии, не в состоянии обеспечить клинически удовлетворительный терапевтический эффект при синдроме фибромиалгии, и эффективность препарата значительно меняется среди пациентов. В связи с этим чрезвычайно желательным является разработка нового терапевтического агента для лечения синдрома фибромиалгии, который оказывал бы достаточный терапевтический эффект.
[0010]
Следует отметить, что в патентной литературе 1 высказано предположение о том, что описанные там замещенные пиперидины обладают эффективностью при лечении мигрени; однако в литературе не описано соединение, обезболивающее действие которого было обнаружено в настоящей заявке, и не было сделано предположения о релевантности анальгезирующего действия по отношению к химической структуре. В патентной литературе 2, где описаны производные имидазола, и в патентной литературе 3, где описаны замещенные пиперидины, не описаны и не предполагается возможность анальгезирующего действия, которыми обладают эти соединения.
[0011]
В этих обстоятельствах целью настоящего изобретения является разработка соединения, имеющего сильное анальгезирующее действие, для лечения боли, в частности, невропатической боли и/или синдрома фибромиалгии.
Решение задачи
[0012]
Авторы настоящего изобретения провели интенсивные исследования с целью решения вышеупомянутых проблем. В результате они обнаружили производное циклического амина, имеющее сильный анальгезирующий эффект против боли, в частности, невропатической боли и/или синдрома фибромиалгии.
[0013]
Более конкретно, настоящее изобретение относится к производному циклического амина, представленного следующей общей формулы, (I) или его фармакологически приемлемой соли.
[Формула 1]
где A представляет собой группу, представленную общей формулой (IIa), (IIb) или (IIc).
[Формула 2]
где, когда A является группой, представленной общей формулой (IIa) или (IIb), R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную атомом галогена, гидроксильной группой, амино группой или карбоксильной группой, R2 представляет собой атом водорода или атом галогена, R3 представляет собой атом водорода или алкильную группу, содержащую от 1 до 6 атомов углерода, R4 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 6 атомов углерода, или алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную алкилкарбониламино группой, содержащей от 2 до 6 атомов углерода, и n обозначает 1 или 2, в которой, когда R3 и R4, каждый, независимо, представляют собой алкильную группу, содержащую от 1 до 6 атомов углерода, R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и замещенную гидроксильной группой, амино группой или карбоксильной группой; и, когда A представляет собой группу, представленную общей формулой (IIc), R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и замещенную карбоксильной группой, R2 представляет собой атом водорода или атом галогена, X представляет собой CH2, O или -NR5, и R5 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода.
[0014]
В вышеуказанном производном циклического амина предпочтительным является, когда A представлен общей формулой (IIa) или (IIb), в которой, более предпочтительно, R3 представляет собой атом водорода, метильную группу или этильную группу; и далее, предпочтительно, когда R2 представляет собой атом водорода или атом хлора, R3 представляет собой атом водорода или метильную группу, и R4 представляет собой атом водорода, метилкарбонильную группу или алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную метилкарбониламино группой.
[0015]
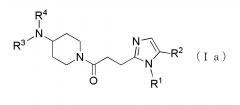
Более конкретно, например, предпочтительным является производное циклического амина, представленное следующей общей формулы (Ia) или (Ib), или его фармакологически приемлемая соль. Особенно предпочтительным является, когда R2 представляет собой атом водорода или атом хлора, R3 представляет собой атом водорода или метильную группу, R4 представляет собой атом водорода, метилкарбонильную группу или алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную метилкарбониламино группой, в которой, когда R3 и R4, оба, представляют собой метильные группы, R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и замещенную гидроксильной группой, амино группой или карбоксильной группой.
[Формула 3]
где R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную атомом галогена, гидроксильной группой, амино группой или карбоксильной группой, R2 представляет собой атом водорода или атом галогена, R3 представляет собой атом водорода или алкильную группу, содержащую от 1 до 6 атомов углерода, R4 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 6 атомов углерода, или алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную алкилкарбониламино группой, содержащей от 2 до 6 атомов углерода, в которой, когда R3 и R4, каждый, независимо, представляют собой алкильную группу, содержащую от 1 до 6 атомов углерода, R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и замещенную гидроксильной группой, амино группой или карбоксильной группой.
[Формула 4]
где R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную атомом галогена, гидроксильной группой, амино группой или карбоксильной группой, R2 представляет собой атом водорода или атом галогена, R3 представляет собой атом водорода или алкильную группу, содержащую от 1 до 6 атомов углерода, R4 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 6 атомов углерода, или алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную алкилкарбониламино группой, содержащей от 2 до 6 атомов углерода, в которой, когда R3 и R4, каждый, независимо, представляют собой алкильную группу, содержащую от 1 до 6 атомов углерода, R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и замещенную гидроксильной группой, амино группой или карбоксильной группой.
[0016]
Анальгезирующее действие может быть улучшено из-за значений определений, указанных выше.
[0017]
В вышеуказанном производном циклического амина предпочтительным является, когда A представлен общей формулой (IIc), и, более предпочтительным является, когда R2 представляет собой атом водорода или атом хлора, и R5 представляет собой метильную группу.
[0018]
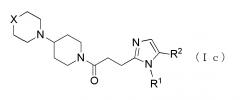
Более конкретно, например, предпочтительным является производное циклического амина, представленное следующей общей формулы (Ic), или его фармакологически приемлемая соль. Более предпочтительным является, когда R2 представляет собой атом водорода или атом хлора, и R5 представляет собой метильную группу.
[Формула 5]
где R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и замещенную карбоксильной группой, R2 представляет собой атом водорода или атом галогена, X представляет собой CH2, O или -NR5, и R5 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода.
[0019]
Анальгезирующее действие может быть улучшено.
[0020]
Настоящее изобретение относится к пролекарству вышеуказанного производного циклического амина или его фармакологически приемлемой соли. Пролекарство, предпочтительно, представляет собой пролекарство, полученное путем этерификации карбоксильной группы вышеуказанного производного циклического амина.
[0021]
Превосходную фармакокинетику можно ожидать на крысах при пероральном введении из-за значений определений, указанных выше.
[0022]
Настоящее изобретение относится также к лекарственному средству, содержащему в качестве активного ингредиента производное циклического амина, представленное вышеуказанной общей формулой (I), пролекарство производного циклического амина или его фармакологически приемлемую соль.
[0023]
Лекарственное средство, предпочтительно, представляет собой анальгетический агент, и, особенно предпочтительно, терапевтический агент при невропатической боли или терапевтический агент при синдроме фибромиалгии.
Положительный эффект изобретения
[0024]
Производное циклического амина по настоящему изобретению или его пролекарство, или его фармакологически приемлемая соль обладает сильным обезболивающим действием против боли, в частности, невропатической боли и синдрома фибромиалгии, и может быть использовано в качестве анальгезирующего средства, в частности, терапевтического средства для лечения невропатической боли или синдрома фибромиалгии, которое может в соответствии с ожиданиями уменьшить побочные эффекты центральной нервной системы и быть подходящим для длительного применения.
Краткое описание рисунков
[0025]
[Фигура 1] На фигуре 1 представлен график, показывающий влияние соединения по примеру 8 на моделях частичного лигирования седалищного нерва на мышах (пероральное введение).
[Фигура 2] На фигуре 2 представлен график, показывающий влияние соединения по примеру 2 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 3] На фигуре 31 представлен график, показывающий влияние соединения по примеру 4 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 4] На фигуре 4 представлен график, показывающий влияние соединения по примеру 2 на моделях частичного лигирования седалищного нерва на мышах (интравентрикулярное введение).
[Фигура 5] На фигуре 5 представлен график, показывающий влияние соединения по примеру 4 на моделях частичного лигирования седалищного нерва на мышах (интравентрикулярное введение).
[Фигура 6] На фигуре 6 представлен график, показывающий влияние соединения по примеру 6 на моделях частичного лигирования седалищного нерва на мышах (интравентрикулярное введение).
[Фигура 7] На фигуре 7 представлен график, показывающий влияние соединения по примеру 10 на моделях частичного лигирования седалищного нерва на мышах (интравентрикулярное введение).
[Фигура 8] На фигуре 8 представлен график, показывающий влияние соединения по примеру 12 на моделях частичного лигирования седалищного нерва на мышах (интравентрикулярное введение).
[Фигура 9] На фигуре 9 представлен график, показывающий влияние соединения по примеру 13 на моделях частичного лигирования седалищного нерва на мышах (интравентрикулярное введение).
[Фигура 10] На фигуре 10 представлен график, показывающий влияние соединения по примеру 15 на моделях частичного лигирования седалищного нерва на мышах (интравентрикулярное введение).
[Фигура 11] На фигуре 11 представлен график, показывающий влияние соединения по примеру 38 на моделях частичного лигирования седалищного нерва на мышах (пероральное введение).
[Фигура 12] На фигуре 12 представлен график, показывающий влияние соединения по примеру 13 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 13] На фигуре 13 представлен график, показывающий влияние соединения по примеру 18 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 14] На фигуре 14 представлен график, показывающий влияние соединения по примеру 22 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 15] На фигуре 15 представлен график, показывающий влияние соединения по примеру 25 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 16] На фигуре 16 представлен график, показывающий влияние соединения по примеру 27 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 17] На фигуре 17 представлен график, показывающий влияние соединения по примеру 29 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 18] На фигуре 18 представлен график, показывающий влияние соединения по примеру 31 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 19] На фигуре 19 представлен график, показывающий влияние соединения по примеру 33 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 20] На фигуре 20 представлен график, показывающий влияние соединения по примеру 66 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 21] На фигуре 21 представлен график, показывающий влияние соединения по примеру 68 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 22] На фигуре 22 представлен график, показывающий влияние соединения по примеру 70 на моделях частичного лигирования седалищного нерва на мышах (внутривенное введение).
[Фигура 23] На фигуре 23 представлен график, показывающий влияние соединения по примеру 13 на моделях синдрома фибромиалгии на крысах (внутривенное введение).
[Фигура 24] На фигуре 24 представлен график, показывающий влияние соединения по примеру 38 на моделях синдрома фибромиалгии на крысах (пероральное введение).
Описание вариантов изобретения
[0026]
Следующие термины, используемые в описании, если не указано иное, определяются следующим образом.
[0027]
В описании производное циклического амина по настоящему изобретению представлено следующей общей формулы (I).
[Формула 6]
где A представляет собой группу, представленную общей формулой (IIa), (IIb) или (IIc),
[Формула 7]
где, когда A представляет собой группу, представленную общей формулой (IIa) или (IIb), R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную атомом галогена, гидроксильной группой, амино группой или карбоксильной группой, R2 представляет собой атом водорода или атом галогена, R3 представляет собой атом водорода или алкильную группу, содержащую от 1 до 6 атомов углерода, R4 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 6 атомов углерода, или алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную алкилкарбониламино группой, содержащей от 2 до 6 атомов углерода, и n обозначает 1 или 2, в которой, когда R3 и R4, каждый, независимо, представляют собой алкильную группу, содержащую от 1 до 6 атомов углерода, R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и замещенную гидроксильной группой, амино группой или карбоксильной группой; и когда A представляет собой группу, представленную общей формулой (IIc), R1 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и замещенную карбоксильной группой, R2 представляет собой атом водорода или атом галогена, X представляет собой CH2, O или -NR5, и R5 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода.
[0028]
В производном циклического амина предпочтительным является, когда A представлен общей формулой (IIa) или (IIb) и R3 представляет собой атом водорода, метильную группу или этильную группу; и более предпочтительным является, когда R2 представляет собой атом водорода или атом хлора, R3 представляет собой атом водорода или метильную группу, и R4 представляет собой атом водорода или метилкарбонильную группу, или алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную метилкарбониламино группой.
[0029]
В производном циклического амина предпочтительным является, когда A представлен общей формулой (IIc), R2 представляет собой атом водорода или атом хлора, и R5 представляет собой метильную группу.
[0030]
Термин «атом галогена» относится к атому фтора, атому хлора, атому брома или атому йода.
[0031]
Термин «алкильная группа, содержащая от 1 до 6 атомов углерода» относится к линейной, разветвленной или циклической насыщенной углеводородной группе, содержащей от 1 до 6 атомов углерода. Например, может быть указана метильная группа, этильная группа, н-пропильная группа, изопропильная группа, циклопропильная группа, циклопропилметильная группа, н-бутильная группа, втор-бутильная группа, трет-бутильная группа, н-пентильная группа, изопентильная группа, н-гексильная группа, изогексильная группа или циклогексильная группа.
[0032]
Термин «алкильная группа, содержащая от 1 до 6 атомов углерода и необязательно замещенная атомом галогена, гидроксильной группой, амино группой или карбоксильной группой», относится к алкильной группе, содержащей от 1 до 6 атомов углерода, в которой атомы водорода, каждый, независимо и необязательно заменены на вышеупомянутые атом галогена или гидроксильную группу, амино группу или карбоксильную группу, и представляет собой, например, метильную группу, этильную группу, н-пропильную группу, изопропильную группу, циклопропильную группу, циклопропилметильную группу, н-бутильную группу, втор-бутильную группу, трет-бутильную группу, н-пентильную группу, изопентильную группу, н-гексильную группу, изогексильную группу или циклогексильную группу или 2-хлорэтильнуюя группу, 2,2-дифторэтильную группу, 2,2,2-трифторэтильную группу, 2-гидроксиэтильную группу, 3-гидроксипропильную группу, 2-аминоэтильную группу, 3-аминопропильную группу, 1-карбоксиметильную группу или 2-карбоксиэтильную группу.
[0033]
Термин «алкилкарбонильная группа, содержащая от 2 до 6 атомов углерода», относится к группе, полученной путем присоединения линейной, разветвленной или циклической насыщенной углеводородной группе, содержащей от 1 до 5 атомов углерода, к карбонильной группе. Например, может быть указана ацетильная группа, н-пропионильная группа, н-бутирильная группа или изобутирильная группа.
[0034]
Термин «алкилкарбониламино группа, содержащая от 2 до 6 атомов углерода», относится к группе, полученной путем присоединения вышеупомянутой алкилкарбонильной группы, содержащей от 2 до 6 атомов углерода, к амино группе. Например, могут быть указаны метилкарбониламино группа, этилкарбониламино группа, н-пропилкарбониламино группа или изопропилкарбониламино группа.
[0035]
Термин «алкильная группа, содержащая от 1 до 6 атомов углерода и необязательно замещенная алкилкарбониламино группой, содержащей от 2 до 6 атомов углерода», относится к вышеупомянутой алкильной группе, содержащей от 1 до 6 атомов углерода и необязательно замещенной вышеупомянутой алкилкарбониламино группой, содержащей от 2 до 6 атомов углерода. Например, метильная группа, этильная группа, н-пропильная группа, изопропильная группа, циклопропильная группа, циклопропилметильная группа, н-бутильная группа, втор-бутильная группа, трет-бутильная группа, н-пентильная группа, изопентильная группа, н-гексильная группа, изогексильная или циклогексильная группа или 2-(метилкарбониламино)этильная группа, 2-(этилкарбониламино)этильная группа, 2-(н-пропилкарбониламино)этильная группа, 2-(изопропилкарбониламино)этильная группа, 3-(метилкарбониламино)пропильная группа или 4-(метилкарбониламино)бутильная группа.
[0036]
Конкретные примеры предпочтительного соединения в качестве производного циклического амина, представленного вышеуказанной общей формулой (I) (указываемого далее как производное циклического амина (I)), показаны в таблицах от 1-1 до 1-3; однако, настоящее изобретение ими не ограничивается.
[0037]
| Таблица 1-1 |
[0038]
| Таблица 1-2 |
[0039]
| Таблица 1-3 |
[0040]
Следует учесть, что, когда в производном циклического амина (I) имеется асимметрический атом углерода, изобретением охватываются все энантиомеры и их смеси. Когда имеется стереоизомер, включены все стереоизомеры и их смеси.
[0041]
Пролекарство производного циклического амина (I) или его фармакологически приемлемая соль также включены в объем настоящего изобретения. Пролекарство производного циклического амина (I) относится к соединению, которое in vivo ферментативно или химически преобразуется в производное циклического амина (I). Активной формой пролекарства производного циклического амина (I) является производное циклического амина (I); однако пролекарство производного циклического амина (I) само по себе может обладать активностью.
[0042]
В качестве пролекарства производного циклического амина (I) могут быть указаны, например, соединения, полученные путем ацилирования, алкилирования, фосфорилирования или борирования гидроксильной группы или амино группы производного циклического амина (I), или соединения, полученные путем этерификации или амидирования карбоксильной группы производного циклического амина (I); однако предпочтительным является соединение, полученное путем этерификации карбоксильной группы. Указанные соединения, каждое, могут быть синтезированы исходя из производного циклического амина (I) в соответствии с известным способом.
[0043]
В качестве соединения, полученного путем этерификации карбоксильной группы производного циклического амина (I), может быть указано метил этерифицированное, этил этерифицированное, н-пропил этерифицированное, изопропил этерифицированное, циклопропил этерифицированное, н-бутил этерифицированное, изобутил этерифицированное, втор-бутил этерифицированное, трет-бутил этерифицированное, циклопропилметил этерифицированное, н-пентил этерифицированное, изопентил этерифицированное, циклопентил этерифицированное, н-гексил этерифицированное, изогексил этерифицированное, циклогексил этерифицированное, н-гептил этерифицированное, н-октил этерифицированное, (5-метил-2-оксо-1,3-диоксолен-4-ил)метил этерифицированное, ацетилоксиметил этерифицированное, 1-ацетилоксиэтил этерифицированное, пропионилоксиметил этерифицированное, 1-пропионилоксиэтил этерифицированное, валерилоксиметил этерифицированное, 1-валерилоксиэтил этерифицированное, изобутирилоксиметил этерифицированное, 1-изобутилилоксиэтил этерифицированное, пивалоилоксиметил этерифицированное, 1-пивалоилоксиэтил этерифицированное, этоксикарбонилоксиметил этерифицированное, 1-((этоксикарбонил)окси)этил этерифицированное, 1-((этоксикарбонил)окси)изобутил этерифицированное, циклогексилоксикарбонилметил этерифицированное, 1-((циклогексил)карбонил)оксиэтил этерифицированное, 2-(диметиламино)-2-оксоэтил этерифицированное, фталидил этерифицированное или инданил этерифицированное соединение; однако предпочтительным является метил этерифицированное, этил этерифицированное, н-пропил этерифицированное, изопропил этерифицированное, циклопропил этерифицированное, н-бутил этерифицированное, изобутил этерифицированное, втор-бутил этерифицированное, трет-бутил этерифицированное, циклопропилметил этерифицированное, н-октил этерифицированное, (5-метил-2-оксо-1,3-диоксолен-4-ил)метил этерифицированное, пивалоилоксиметил этерифицированное, 2-(диметиламино)-2-оксоэтил этерифицированное, фталидил этерифицированное или инданил этерифицированное соединение.
[0044]
Конкретные примеры предпочтительного соединения в качестве пролекарства производного циклического амина (I) показаны в таблице 2-1 и таблице 2-2; однако настоящее изобретение ими не ограничивается.
[0045]
| Таблица 2-1 |
[0046]
| Таблица 2-2 |
[0047]
Пролекарство производного циклического амина (I) может быть преобразовано в производное циклического амина (I) в физиологических условиях, описанных в известных литературных источниках («Development of pharmaceutical products», Hirokawa-Shoten Ltd., vol. 7, p. 163 to 198, 1990, и Prog. Med. 5, p. 2157 to 2161, 1985).
[0048]
Производное циклического амина (I) или его пролекарство могут быть мечены радиоизотопом. Примеры радиоизотопа для использования при введении метки включают 3H, 14C и/или 125I.
[0049]
Производное циклического амина (I) или его пролекарство может быть дейтерировано.
[0050]
В качестве фармакологически приемлемой соли производного циклического амина (I) можно указать, например, неорганическую соль, такую как гидрохлорид, сульфат, фосфат или гидробромид; или органическую соль, такую как оксалат, малонат, цитрат, фумарат, лактат, малат, сукцинат, тартрат, ацетат, трифторацетат, малеат, глюконат, бензоат, салицилат, ксинафоат, памоат, аскорбат, адипат, метансульфонат, п-толуолсульфонат или циннамат. Эти соли могут существовать в форме гидрата, сольвата или кристаллического полиморфа.
[0051]
Производное циклического амина (I) или его пролекарство может быть синтезировано способами получения, которые описаны далее. Следует отметить, что, производные циклического амина (I) или их пролекарства, полученные с помощью следующих методов производства, каждый, могут быть выделены/очищены с помощью известных средств, таких как экстракция растворителем, перекристаллизация и/или с помощью хроматографии и преобразованы в желаемые соли с помощью известных способов или аналогичных способов. Когда производное циклического амина (I) или его пролекарство получают в виде соли, оно может быть преобразовано в производное циклического амина (I) или его пролекарство, или другую желаемую соль известным способом или аналогичным способом.
[0052]
В отдельных реакциях способов получения, которые описаны далее, когда исходное соединение имеет гидроксильную группу, аминогруппу или карбоксильную группу, в этих группы могут быть введены защитные группы. Желаемое соединение может быть получено удалением защитной группы, если это необходимо, после реакции.
[0053]
В отдельных реакциях способов получения, которые описаны далее, когда исходное соединение имеет гидроксильную группу, аминогруппу или карбоксильную группу, пролекарство производного циклического амина (I) можно получить без удаления защитной группы, введенной в эти группы.
[0054]
В качестве защитной группы гидроксильной группы могут быть упомянуты, например, тритильная группа, аралкильная группа, содержащая от 7 до 10 атомов углерода (например, бензильная группой), или замещенная силильная группа (например, триметилсилильная группа, триэтилсилильная группа или трет-бутилдиметилсилильная группа).
[0055]
В качестве защитной группы аминогруппы может быть указана, например, алкилкарбонильная группа, имеющая от 2 до 6 атомов углерода (например, ацетильная группа), бензоильная группа, алкоксикарбонильная группа, содержащая от 1 до 6 атомов углерода (например, трет-бутоксикарбонильная группа или бензилоксикарбонильная группа), аралкильная группа, содержащая от 7 до 10 атомов углерода (например, бензильная группа), или фталоильная группа.
[0056]
В качестве защитной группы карбоксильной группы может быть указана, например, алкильная группа, содержащая от 1 до 6 атомов углерода (например, метильная группа, этильная группа или трет-бутильная группа) или аралкильная группа, содержащая от 7 до 10 атомов углерода (например, бензильная группа).
[0057]
Удаление защитной группы, которое варьируется в зависимости от вида защитной группы, может быть осуществлено в соответствии с известным способом (например, Greene, T. W., «Greene’s Protective Groups in Organic Synthesis», Wiley-Interscience) или подобным способом.
[0058]
1. Соединение (Ia) может быть синтезировано в соответствии со способом получения, который описан далее.
[0059]
1-1. Способ получения соединения (Ia-a):
[Формула 8]
где M представляет собой атом водорода или щелочной металл, такой как литий или натрий, R4a представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную алкилкарбониламино группой, содержащей от 2 до 6 атомов углерода, и другие условные символы имеют такие же значения, которые определены выше.
Соединение (Ia-a), которое представляет собой производное циклического амина (I), где A представляет собой группу, представленную общей формулой (IIa), и R4 представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную алкилкарбониламино группой, содержащей от 2 до 6 атомов углерода, может быть получено, например, путем реакции конденсации соединения (IIa-a) и соединения (III) с использованием конденсирующего агента в присутствии или в отсутствие основания.
[0060]
В реакции конденсации может быть использовано соединение (IIa-a) и его соль. В качестве соли в настоящем документе может быть указана, например, такая соль, как фармакологически приемлемая соль, которая упоминалась выше.
[0061]
В качестве соединения (IIa-a) и соединения (III) для использования в реакции конденсации могут быть непосредственно использованы коммерчески доступные соединения; однако они могут быть синтезированы, например, в соответствии со способами получения, которые описаны далее.
[0062]
В качестве основания для использования в реакции конденсации, может быть указан, например, ароматический амин, такой как пиридин или лутидин, или третичный амин, такой как триэтиламин, триизопропиламин, трибутиламин, циклогексилдиметиламин, 4-диметиламинопиридин, N,N-диметиланилин, N-метилпиперидин, N-метилпирролидин, N-метилморфолин или диизопропилэтиламин (DIEA).
[0063]
Количество основания для использования в реакции конденсации, предпочтительно, составляет от 0,5 до 10 молей относительно 1 моля соединения (IIa-a) и, более предпочтительно, от 0,8 до 5,0 молей.
[0064]
В качестве конденсирующего агента для использования в реакции конденсации может быть указан, например, O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат (HBTU), циклогексилкарбодиимид (DCC), N-(3-диметиламинопропил)-N'-этилкарбодиимид (EDC) или его гидрохлорид, 2-этокси-1-этоксикарбонил-1,2-дигидроксихинолин (EEDQ), карбонилдиимидазол (CDI), диэтилфосфорил цианид, бензотриазол-1-илокситриспирролидинoфосфония гексафторфосфат (PyBOP), дифенилфосфорилазид (DPPA), 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид (DMTMM), изобутил хлорформиат, диэтилацетил хлорид или триметилацетил хлорид. Эти конденсирующие агенты используются отдельно или в комбинации с добавкой, такой как N-гидроксисукцинимид (HONSu), гидроксибензотриазол (HOBT), 3-гидрокси-4-оксо-3,4-дигидро-1,2,3-бензотриазин (HOOBT) или 4-диметиламинопиридин (DMAP).
[0065]
Количество конденсирующего агента для использования в реакции конденсации, предпочтительно, составляет от 0,5 до 10 молей относительно 1 моля соединения (IIa-a) и, более предпочтительно, от 0,8 до 5,0 молей.
[0066]
Количество соединения (III) для использования в реакции конденсации, предпочтительно, составляет от 0,5 до 3 молей относительно 1 моля соединения (IIa-a) и, более предпочтительно, от 0,8 до 1,5 молей.
[0067]
Реакцию конденсации обычно осуществляют в растворителе, и, соответственно, в качестве растворителя может быть указан такой растворитель, как, например, ароматический амин, такой как пиридин; галогенированный углеводород, такой как дихлорметан, хлороформ или 1,2-дихлорэтан; простой эфир, такой как тетрагидрофуран или 1,4-диоксан; амид, такой как N,N-диметилформамид или N-метилпирролидон; спирт, такой как метанол, этанол или 2-пропанол; или алифатический нитрил, такой как ацетонитрил или пропионитрил. Может быть использована смесь эти