Способы и композиции для лечения воспаления и ишемического поражения
Иллюстрации
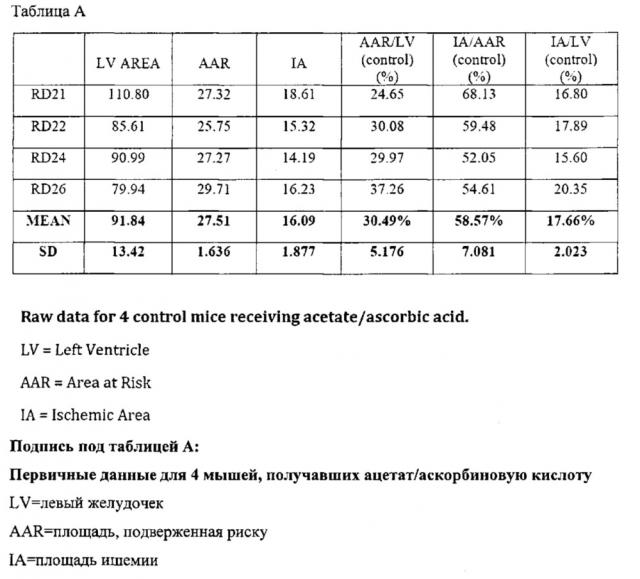
Показать всеГруппа изобретений касается фармакологии и медицины. Предложены: способ лечения субъекта, страдающего от ишемического повреждения или острого ишемического события, включающий введение цистеамина, цистамина или их соли до, одновременно с или сразу после ишемического события, в количестве, эффективном для уменьшения ишемического повреждения, причем субъект не страдает от гиперхолестеринэмии или диабетом II типа, где введение цистеамина, цистамина или их соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) (варианты); способ увеличения (варианты) уровней адипонектина LMW у указанной группы больных, включающий контактирование субъекта с эффективным количеством цистеамина, цистамина или их соли (варианты); применение цистеамина, цистамина или их соли при производстве медикамента при вышеуказанном лечении субъекта, страдающего от острого ишемического события и не страдающего от гиперхолестеринэмии или диабета II типа. Технический результат состоит в реализации заявленного назначения у указанной группы больных, при этом повышаются уровни всех мультиморов адипонектина, в течение 1 часа после воздействия цистеамина в сыворотке крови быстро и значимо повышался LMW адипонектина, введение цистеамина за 2 часа до ишемического инсульта значительно снижало площадь инфаркта и количество ишемических повреждений. 7 н. и 21 з.п. ф-лы, 18 ил., 2 табл., 3 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение касается способов и композиций для лечения ишемии или болезни или нарушения, вызывающего ишемию, включающие контактирование субъекта с цистеамином, производным цистеамина, цистамином или производным цистамина. В изобретении раскрыты также способы модулирования уровней адипонектина у субъекта, включающие контактирование субъекта с цистеамином, производным цистеамина, цистамином или производным цистамина.
Уровень техники
По подсчетам острый ишемический инсульт затрагивает ~2-2,5 из каждой тысячи человек, что влечет за собой приблизительно 4,5 миллиона смертей в год во всем мире и 9 миллионов пациентов, перенесших инсульт, при этом расходы в настоящее время превышают 50 биллионов $ только в США.
Раскрытие изобретения
Изобретение предоставляет способ лечения субъекта, страдающего от ишемического поражения или острого ишемического события, включающий введение субъекту цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли в количестве, эффективном для уменьшения ишемического повреждения. В одном варианте осуществления ишемическое поражение является результатом тромботического нарушения. В дополнительном варианте осуществления тромботическое нарушение является серповидноклеточной анемией, тромбозом глубоких вен, легочной эмболией, сердечной эмболией, состоянием гиперкоагуляции, тромбофилией, фактором V Ляйдена, дефицитом антитромбина III, дефицитом белка С, дефицитом белка S, мутацией гена протромбина (G20210A), гипергомоцистеинемией, синдромом антифосфолипидных антител (APS), синдромом антикардиолипиновых антител (ACLA) или синдромом волчаночного антикоагулянта (LA). В любом из упомянутых выше вариантов осуществления количество цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли является эффективным для уменьшения риска ишемического поражения, полученного в результате тромбоза.
Изобретение также предоставляет способ лечения субъекта с повышенным риском тромбообразования и возникающего в связи с этим ишемического поражения, включающий введение субъекту количества цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли, эффективного для уменьшения риска ишемического поражения, полученного в результате тромбоза.
В любом из упомянутых выше вариантов субъект может иметь рак, миелопролиферативное заболевание, множественную миелому, мог перенести операцию или травму, может находиться в состоянии иммобилизации, принимать пероральный контрацептив, принимать талидомид или его родственные соединения необязательно в комбинации со стероидным гормоном, может иметь гепарин-индуцированную тромбоцитопению, может быть беременным, может иметь воспалительную болезнь кишечника, нефротический синдром, ночную пароксизмальную гемоглобинурию, синдром повышенной вязкости крови или макроглобулинемию Вальденстрема.
Изобретение также предоставляет способ лечения субъекта с повышенным риском тромбообразования, включающий введение субъекту цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли в количестве, эффективном для снижения риска ишемического поражения вследствие тромбоза. В одном варианте осуществления субъект имеет рак, миелопролиферативное заболевание, множественную миелому, перенес операцию, имел травму, находится в состоянии иммобилизации, принимает пероральное противозачаточное средство, субъекту вводят талидомид или его родственные соединения необязательно в комбинации со стероидным гормоном, имеет гепарин-индуцированную тромбоцитопению, является беременным, имеет воспалительную болезнь кишечника, имеет нефротический синдром, имеет ночную пароксизмальную гемоглобинурию, имеет синдром повышенной вязкости крови или макроглобулинемию Вальденстрема.
В любом из упомянутых выше вариантов осуществления ишемическое поражение может быть результатом повреждения ткани, болезни или инсульта. В дополнительном варианте осуществления поражение является реперфузионным повреждением. В другом варианте осуществления реперфузионное повреждение является результатом хирургического вмешательства или трансплантации органа. В другом варианте осуществления болезнь является серповидноклеточной анемией.
В любом из упомянутых выше вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в пределах 72 часов после ишемического события. В дополнительном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в течение длительного времени после ишемического события. В любом из упомянутых выше вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в течение длительного времени субъекту с повышенным риском ишемического события.
Данный вариант предоставляет способ увеличения отношения уровней адипонектина с низким молекулярным весом (LMW) к уровням адипонектина со средним молекулярным весом (MMW) и/или высоким молекулярным весом (HMW) у субъекта, нуждающегося в этом, включающий введение субъекту цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли, в количестве, эффективном для увеличения отношения уровней адипонектина с низким молекулярным весом по сравнению с исходным уровнем до контактирования субъекта с цистеамином, производным цистеамина, цистамином, производным цистамина или их фармацевтически приемлемой солью, при этом субъект не страдает от гиперхолестеринемии или диабета II типа.
Изобретение также предоставляет способ лечения субъекта, имеющего не отвечающие нормам или ненормальные отношения адипонектина с высоким молекулярным весом (HMW) к адипонектину со средним молекулярным весом (MMW), адипонектина с HMW к адипонектину с низким молекулярным весом (LMW) или MMW : LMW, включающий введение субъекту цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли, в количестве, эффективном для улучшения соотношений адипонектина у субъекта по сравнению с субъектом, не получавшим цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемую соль.
В одном варианте осуществления упомянутый выше субъект имеет фактор риска возникновения ишемии, выбранный из группы, состоящей из гипертонической болезни, употребления табака, болезни сонной или других артерий, заболевания периферических артерий, мерцательной аритмии, другого заболевания сердца, преходящего ишемического нарушения (TIA), заболеваний крови, высокого уровня холестерина в крови, гиподинамии, ожирения, избыточного употребления алкоголя, использования запрещенных наркотиков, предшествующего инсульта, серповидно-клеточной анемии и предшествующего сердечного приступа. В другом варианте осуществления субъект ранее перенес ишемическое событие. В любом из упомянутых выше вариантов осуществления способ включает введение цистеамина, производного цистеамина или его фармацевтически приемлемой соли. В дополнительном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина, или фармацевтически приемлемая соль любого из вышеупомянутого вводится в концентрации в пределах примерно от 0,5 до 20 мг/кг веса тела указанного субъекта. В еще одном варианте осуществления общая ежедневная доза цистеамина, производного цистеамина, цистамина, производного цистамина или фармацевтически приемлемой соли любого из вышеупомянутого составляет около 0,5-4,0 г/м2. В еще одном дополнительном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или фармацевтически приемлемая соль любого из вышеупомянутого вводится перорально. В одном варианте осуществления цистеамин, производное цистеамина, цистамин или производное цистамина или их фармацевтически приемлемая соль является лекарственной формой с замедленным или контролируемым высвобождением. В любом из упомянутых выше вариантов осуществления цистеамин, производное цистеамина, цистамин или производное цистамина или их фармацевтически приемлемая соль вводится внутрибрюшинно. В дополнительном варианте осуществления цистеамин, производное цистеамина, цистамин или производное цистамина или их фармацевтически приемлемая соль вводится внутривенно или внутриартериально. В любом из упомянутых выше вариантов осуществления введение приводит к уменьшению ишемически-реперфузионного повреждения или воспаления в результате ишемического события. В другом варианте осуществления способ дополнительно включает введение одного или более дополнительных средств, пригодных для лечения ишемии. В дополнительном варианте осуществления одно или более дополнительных средств выбирают из группы, состоящей из реперфузионного средства, ловушки свободных радикалов и спиновой ловушки, нейропротекторного средства, антикоагулирующего средства, антитромбоцитарного средства, нимодипина и налоксона. В другом варианте осуществления способ дополнительно включает введение одного или более средств, пригодных для лечения тромботического нарушения: антикоагулирующего средства, гепарина, антагониста витамина К, производных 4-гидроксикумарина, варфарина, аценокумарола, дикумарола, этилбискумацетата, фенпрокумона, стрептокиназы, урокиназы, тканевого активатора плазминогена (tPA), альтеплазы (рекомбинантной tPA), ретеплазы, тенектеплазы и аргатробана. В другом варианте осуществления цистеамин, производное цистеамина, цистамин или производное цистамина или фармацевтически приемлемую соль любого из вышеперечисленного вводят менее чем четыре раза в день. В еще одном варианте осуществления цистеамин, производное цистеамина, цистамин или цистамин вводят два раза в день. В любом из перечисленных выше вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемую соль вводят непрерывно в течение дней, недель или месяцев.
Изобретение предоставляет способ лечения ишемического события, включающий контактирование субъекта, страдающего от ишемического события, с эффективным количеством цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли, при этом субъект имеет улучшенный поведенческий результат по сравнению с субъектом, который не получал цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемую соль. В одном варианте осуществления уровни адипонектина у субъекта увеличиваются после контактирования с цистеамином, производным цистеамина, цистамином, производным цистамина или их фармацевтически приемлемой солью. В другом варианте осуществления общая ежедневная доза цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли составляет около 0,5-4,0 г/м2. В еще одном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится внутрибрюшинно. В следующем варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится перорально. В следующем варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль представляет собой лекарственную форму с замедленным или контролируемым высвобождением, которая обеспечивает увеличенную доставку цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли в тонкий кишечник. В еще одном варианте осуществления лекарственная форма с замедленным или контролируемым высвобождением содержит энтеросолюбильное покрытие, которое высвобождает цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемую соль, когда цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль достигает тонкого кишечника или участка желудочно-кишечного тракта субъекта, в котором значение pH больше чем около pH 4,5. В одном варианте осуществления энтеросолюбильное покрытие является покрытием, выбранным из группы, состоящей из полимеризованного желатина, шеллака, сополимера метакриловой кислоты типа С NF, фталат бутирата целлюлозы, гидрофталата целлюлозы, фталата пропионата целлюлозы, поливинилацетата фталата (PVAP), ацетата фталата целлюлозы (CAP), ацетата тримеллитата целлюлозы (CAT), фталата гидроксипропил метилцеллюлозы, ацетата гидроксипропил метилцеллюлозы, сукцината диоксипропил метилцеллюлозы, карбоксиметилэтилцеллюлозы (CMEC), гидроксипропилметилцеллюлозы ацетата сукцината (HPMCAS) и полимеров и сополимеров акриловой кислоты, таких как метилакрилат, этилакрилат, метилметакрилат и/или этилметакрилат с сополимерами сложных эфиров акриловой и метакриловой кислоты. В еще одном варианте осуществления, когда цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится перорально, цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в составе композиции с биодоступным железом. В любом из вышеперечисленных вариантов осуществления введение приводит к уменьшению воспаления, наблюдающегося вследствие ишемического события.
Изобретение также предоставляет способ увеличения уровней адипонектина у субъекта, включающий контактирование субъекта с эффективным количеством цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли с целью увеличения уровней адипонектина по сравнению с исходным уровнем до контактирования субъекта с цистеамином, производным цистеамина, цистамином, производным цистамина или их фармацевтически приемлемой солью. В одном варианте осуществления общие уровни адипонектина повышаются. В другом варианте осуществления отношение адипонектина с низким молекулярным весом к адипонектину со средним и/или высоким молекулярным весом повышается. В еще одном варианте осуществления субъект страдает ожирением и имеет низкие уровни LMW-адипонектина по сравнению со здоровыми субъектами. В одном варианте осуществления субъект имеет диабет и имеет низкие уровни LMW-адипонектина по сравнению со здоровыми субъектами. В еще одном варианте осуществления субъект страдает от ишемических событий.
Изобретение также предоставляет применение цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли для лечения ишемии, ишемического повреждения, острого ишемического события, тромбоза или ишемического повреждения в результате тромбоза. В одном варианте осуществления ишемия или ишемическое повреждение является результатом тромботического нарушения. В другом варианте осуществления тромботическое нарушение является серповидно-клеточной анемией, тромбозом глубоких вен, легочной эмболией, состоянием гиперкоагуляции, тромбофилией, фактором V Ляйдена, дефицитом антитромбина III, дефицитом белка C, дефицитом белка S, мутацией гена протромбина (G20210A), гипергомоцистеинемией, синдромом антифосфолипидных антител (APS), синдромом антикардиолипиновых антител (ACLA) или синдромом волчаночного антикоагулянта (LA). В еще одном варианте осуществления применяют цистеамин, производное цистеамина или их фармацевтически приемлемую соль. В еще одном варианте осуществления ишемия возникает в результате фактора риска, выбранного из группы, состоящей из гипертонической болезни, употребления табака, болезни сонной или других артерий, заболевания периферических артерий, мерцательной аритмии, другого заболевания сердца, преходящего ишемического нарушения (TIA), заболеваний крови, высокого уровня холестерина в крови, гиподинамии, ожирения, избыточного употребления алкоголя, использования запрещенных наркотиков, предшествующего инсульта, серповидно-клеточной анемии и предшествующего сердечного приступа. В другом варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль заключается в состав для внутрибрюшинного введения. В любом из вышеперечисленных вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится внутрисосудистым способом. В еще одном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль заключается в состав для перорального введения. В другом варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль имеет энтеросоюлюбильоне покрытие. В любом из перечисленных выше вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в течение длительного времени. В другом варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится до, одновременно с или после ишемического события/кризиса. В другом варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль используется для увеличения уровней адипонектина у субъекта.
Детали одного или более вариантов осуществления раскрытия изложены в прилагаемых чертежах и описании ниже. Другие признаки, цели и преимущества станут очевидны на основе описания и чертежей, а также пунктов формулы изобретения.
Краткое описание чертежей
Фигура 1 показывает обработку эксплантатов жировой ткани цистеамином 90 мкМ в течение 45 мин, 90 мин и 24 часов. Значимое увеличение уровня общего адипонектина при обработке цистеамином 90 мкМ в течение 45 мин.: p=0.002; значимое различие уровня адипонектина HMW при обработке цистеамином 90 мкМ 45 мин.: p=0.04; значимое различие уровня адипонектина HMW при обработке цистеамином 90 мкМ 90 мин.: p=0.02.
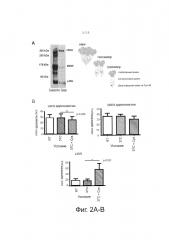
Фигура 2A-C показывает (A) схематическое изображение и относительный сдвиг подвижности LMW, MMW и HMW адипонектина; (В) показывает сыворотку, полученную при бандажировании желудка (GB), инкубированную при комнатной температуре, 37°C, 37°C + 45 мкМ цистеамина в течение 1 часа и получение мультимеров адипонектина. Не наблюдалось значимого различия между комнатной температурой и 37°C для любого мультимера. Однако: HMW значимо уменьшается при обработке цистеамином: p=0.009; MMW значимо изменяется при обработке цистеамином; и LMW значимо увеличивается при обработке цистеамином: p=0.05. (C) Средние значения BMI, ALT и AST, измеренные в начальный момент, через 24 недели обработки EC-цистеамином и затем через 16 недель после отмены ЕС-цистеамина). Значения P обозначаются как незначимые (ns), *P<.05, **P<.01. Среднее значение BMI не различалось достоверно в любых временных точках. Показана стандартная ошибка среднего (SEM).
Фигура 3 показывает in vivo действие цистеамина на мультимеризацию адипонектина у субъектов с NAFLD. Одиннадцать субъектов с NAFLD перорально лечили enteric-coated цистеамином с энтеросолюбильным покрытием в течение 24 недель и затем осуществляли контроль без лечения в течение 24 недель. Сыворотку анализировали в начальный момент времени, через 24 недели на фоне лечения и затем через 24 недели без лечения. Наблюдалось значимое увеличение общего, а также всех подформ адипонектина после 24 недель приема перорально ЕС-цистеамина, а затем значимое уменьшение через 24 недели после прекращения лечения.
Фигура 4 показывает уровень общего адипонектина in vivo при лечении цистеамином. Наблюдалось значимое увеличение общего адипонектина в течение 0-24 недель: p=0.05; значимое уменьшение абсолютного уровня в течение 24-40 недель: p=0.01; Не наблюдалось значимого различия между исходным уровнем и уровнем на 40 неделе.
Фигура 5 показывает аналогичные данные, как Фигура 3, но выраженные в виде среднего процентного изменения in vivo эффектов цистеамина на мультимеризацию адипонектина. Сыворотка от субъектов в момент времени 0 (исходный), через 24 недели обработки лечения и через 40 недель (после прекращения обработки цистеамином через 24 недели). Полуколичественный анализ проводили с помощью вестерн-блоттинга 1 мкл сыворотки в невосстанавливающих условиях. Данные субъекта нормировали, используя % изменения мультимеров адипонектина на 24 неделе в сравнении с исходным и на 40 неделе в сравнении с исходным.
Фигура 6 показывает in vitro эффекты цистеамина на абсолютные уровни адипонектина у худых (lean) контрольных субъектов. Безжировую контрольную сыворотку при комнатной температуре, 37°C, 37°C + 90 мкМ цистеамина инкубировали в течение 1 часа. Не наблюдалось значимого различия между комнатной температурой и 37°C; для любого мультимера HMW не наблюдалось значимого изменения при обработке цистеамином; наблюдалось значимое уменьшение абсолютного уровня MMW при обработке цистеамином; не наблюдалось значимого изменения абсолютного уровня LMW при обработке цистеамином (результаты проявляют тенденцию к значимому увеличению); значимое % изменение при обработке цистеамином.
Фигура 7 показывает безжировую контрольную сыворотку при комнатной температуре, 37°C, 37°C + 90 мкМ цистеамина после инкубации 1 час. Не наблюдалось значимого различия между комнатной температурой и 37°C для любого мультимера. Не наблюдалось значимого различия HMW при обработке цистеамином. Наблюдалось значимое различие абсолютного уровня MMW при обработке цистеамином; значимое процентное изменение при обработке цистеамином; и не наблюдалось значимого изменения абсолютного уровня LMW при обработке цистеамином (результаты проявляют тенденцию к значимому увеличению) значимое процентное изменение при обработке цистеамином.
Фигура 8 - графики, демонстрирующие эффект цистеамина in vitro на сыворотку, полученную от субъектов с бандажированием желудка. Концентрации цистеамина 0, 7,5, 15, 30, 45, 60, 90 мкМ при инкубации 1 час при 37°C.
Фигура 9 демонстрирует уровни адипонектина, измеренные через 1 час после добавления цистеамина (в различных концентрациях 0, 7,5, 15, 30, 45, 60 и 90 мкМ) к сыворотке 4 пациентов с ожирением.
Фигура 10 показывает процент изменения различных мультимеров адипонектина при разных концентрациях цистеамина.
Фигура 11 показывает среднее значение процентного изменения от исходного форм адипонектина после инкубации ВАТ1-16 сыворотки с разными концентрациями цистеамина в течение 1 час.
Фигура 12 показывает уровни всех форм мультимеров, повышенные после обработки цистеамином в течение 24 недель. Однако относительные пропорции каждого мультимера (которые давали повышение общего адипонектина) были значимо повышены для HMW, понижены для MMW и оставались неизмененными для LMW.
Фигура 13 показывает средние процентные изменения мультимеров адипонектина у субъектов (n=10) с NAFLD. Не наблюдалось значимого различия для любого мультимера, измеренного в пределах между комнатной температурой (RT белые столбики) и 37°C (темные столбики). В сыворотке, инкубированной с цистеамином при 45 мкМ при 37°C в течение одного часа (заштрихованные столбики), наблюдалось значимое уменьшение MMW и увеличение LMW по сравнению с необработанной сывороткой.
Фигура 14A-B демонстрирует эффекты цистеамина in vivo. (A) - график, показывающий значимое различие между обработкой цистеамином и контролем по площади ишемии в виде процента площади, подверженной риску (или участка сердечной мышцы с LAD артерией). (B) - график, показывающий значимое различие между обработкой цистеамином и контрольной группой по площади ишемии в виде процента площади левого желудочка.
Фигура 15A-B показывает диастолические объемы на моделях с обработкой цистеамином и без обработки. (A) показывает конечный диастолический объем в мкл на 24 час и 72 час в контрольной группе, получавшей только IV буфер. Не наблюдалось значимого различия в EDV между двумя временными точками, что указывает на то, что не наблюдалось улучшения в течение времени. (B) показывает конечный диастолический объем в мкл на 24 час и 72 час в контрольной группе, получавшей цистеамин в IV буфере. Наблюдалось значимое уменьшение EDV между двумя временными точками, свидетельствуя, что имелось улучшение с течением времени.
Фигура 16 - график, показывающий, что наблюдалось значимое различие между процентным изменением EDV между 24 час и 72 час. Уменьшение EDV говорит о меньшей дилатации желудочка после ишемии миокарда. Мыши теряли вес в пределах между 24 час и 72 час и были вялыми. Контрольные мыши потеряли 13%, а группа с цистеамином потеряла 14% веса тела.
Фигура 17A-B - графики конечного систолического объема (ESV) в контрольной и обработанной цистеамином группах животных с моделью ишемии. (A) показывает ESV в мкл на 24 час и 72 час в контрольной группе, получавшей только буфер IV. Наблюдалось значимое различие ESV. (B) показывает ESV в мкл на 24 час и 72 час в группе, получавшей IV цистеамин в буфере. Наблюдалось значимое различие ESV.
Фигура 18 - график процентного изменения ESV. Наблюдалось значимое различие процентного изменения ESV между 24 час и 72 час. Уменьшение ESV говорит от лучшем сокращении желудочков.
Осуществление изобретения
Использованные в описании и прилагаемых пунктах формулы изобретения формы единственного числа включают формы множественного числа, если контекст явно не диктует иначе. Таким образом, например, ссылка на "неопределенный (некоторый) антиоксидант" включает множество таких антиоксидантов, а ссылка на "конкретный (данный) антиоксидант" включает ссылку на один или более антиоксидантов и т.д.
Кроме того, использование "или" означает "и/или", если не указано иначе. Подобным образом, термины "содержать", "содержит", "содержащий", "включать", "включает" и "включающий" являются взаимозаменяемыми и не являются ограничивающими.
Кроме того, следует понимать, что в случаях, когда описания различных вариантов осуществления используют термин "содержащий", специалистам в данной области техники понятно, что в некоторых конкретных случаях вариант осуществления альтернативно может быть описан с использованием выражения "в основном состоящий из" или "состоящий из".
Если не указано иное, все технические и научные термины, использованные в описании, имеют то же самое значение, которое обычно понятно специалисту в той области техники, к которой относится данное раскрытие. Хотя при осуществлении на практике раскрытых способов и композиций могут использоваться способы и материалы, подобные или эквивалентные описанным здесь, типичные способы, устройства и материалы представлены в данном описании.
Рассмотренные выше или на всем протяжении текста публикации используются только для их раскрытия до даты подачи настоящей заявки. Ничто в данном описании не должно трактоваться как допущение, что изобретатели не имеют права датировать такое раскрытие на основании предшествующего раскрытия.
При использовании в описании ишемия относится к состоянию, являющемуся результатом уменьшения или отсутствия (недостаточности) тока крови и кислорода к части организма, например, мозгу, сердцу или другой ткани. Ишемическое повреждение имеет отношение в основном к ткани, которая является удаленной (дистальной) или по иным причинам находится под влиянием отсутствия тока крови и кислорода. Ишемическое повреждение часто является результатом недостатка кислорода и жидкостей, а также включает воспалительные каскады. Например, ишемия и ишемическое повреждение может происходить в результате сердечного, легочного или мозгового нарушения, трансплантации органа или хирургической процедуры, или болезни или расстройства (например, серповидноклеточной анемии или серповидноклеточной болезни).
Острая ишемия чаще всего наблюдается при инсультах и поражениях сердца. Однако существует целый ряд нарушений и травм, которые вызывают ишемические события, приводящие к гибели клеток и повреждению ткани. Например, острые сердечные приступы (т.е. инфаркты миокарда) представляют собой распространенное явление. Кроме того, индивидуум, у которого имеются признаки, указывающие на рецидивирующую умеренную сердечную ишемию (т.е. стенокардию), может получить пользу от применения цистеамина (вероятно в результате его длительного влияния на адипонектин). Инсульты, цереброваскулярные и сердечно-сосудистые осложнения являются результатом острого нарушения тока крови в участке мозга или сердца соответственно. В Соединенных Штатах наблюдается приблизительно 500000 случаев инсультов в год, из которых 30% являются фатальными, и, следовательно, инсульт является третьей из основных причин смерти в США. Приблизительно 80% инсультов являются "ишемическими" и происходят вследствие острой окклюзии (закупорки) мозговой артерии, в результате чего уменьшается ток крови. Остальная часть является "геморрагическими инсультами", происходящими вследствие разрыва мозговой артерии с кровоизлиянием в ткань мозга и последующей блокадой тока крови из-за отсутствия течения в дистальном участке разорванного сосуда и местного сдавливания ткани, создающего ишемию.
В большинстве случаев инсульт затрагивает индивидуумов старше 65-летнего возраста, при этом наиболее мощным фактором риска является повышенное кровяное давление. До недавнего времени не было утвержденного лечения острого инсульта, который лечили только общей медицинской поддержкой, а затем реабилитацией после повреждения. В 1996 FDA одобрило применение тканевого активатора плазминогена (tPA) в качестве терапии при остром ишемическом нарушении, исходя из небольшого количества контролируемых испытаний. Некоторые, но не все, из испытаний подтвердили 30-55% улучшение клинических результатов с общим снижением частоты осложнений, но не летальности. В связи с узким окном благоприятной возможности для лечения пациента с использованием tPA и существенных побочных эффектов, связанных с использованием tPA, данное лекарственное средство недоиспользуется. Даже при использовании tPA в тромболитической терапии лечение вызывает полную регрессию симптомов менее чем в 40% случаев, вот почему существует необходимость в дополнительных видах лечения. Многочисленные нейропротекторные стратегии были проверены в клинических испытаниях, но ни одна из них не была одобрена FDA для лечения ишемического инсульта.
Приблизительно восемьдесят процентов инсультов может быть вызвано тем, что слишком мало крови достигает участка мозга, что обычно связано с тромбом (сгустком крови), блокирующим кровеносный сосуд (т.е., например, тромбозом сосудов головного мозга). Это называется "ишемический инсульт". Этот тип инсульта иногда может приводить к кровоизлиянию в мозг, так как подвергнутая воздействию ткань мозга размягчается и это может приводить к разрушению небольших кровеносных сосудов. В дополнение к этому внутримозговое кровоизлияние может происходить в том случае, когда у людей имеются проблемы, связанные с образованием сгустков крови. Сгустки, представляющие собой способ остановки любого кровотечения в организме, образуются белками, называемыми факторами свертывания крови, и «липкими» клетками крови, называемыми тромбоцитами. Во всех случаях, когда факторы свертывания крови или тромбоциты плохо работают, или их количество является недостаточным, у человека может развиться склонность к чрезмерному кровотечению.
Ишемическим инсультам могут предшествовать преходящие нарушения мозгового кровообращения (транзиторные ишемические атаки) (TIA), причем по оценкам, около 300,000 людей в Соединенных Штатах страдает от TIA каждый год. Тромбообразование также способствует закупорке периферических артерий у пациентов с диабетом, серповидноклеточной анемией и других пациентов, при этом необходимы эффективные и безопасные средства против ишемического поражения у таких пациентов.
Приблизительно двадцать процентов инсультов включает кровотечение в мозг, повреждающее близлежащую ткань мозга (например, геморрагический инсульт). Геморрагический инсульт наблюдается при разрыве кровеносного сосуда внутри мозга. Мозг очень чувствителен к кровотечению, при этом повреждение может происходить очень быстро или по причине присутствия самой крови, или потому, что жидкость увеличивает давление на мозг и повреждает его, придавливая мозг к черепу. Кровотечение раздражает ткань мозга, вызывая отек. Окружающие ткани мозга сопротивляются распространению кровотечения, что отражается в образовании опухоли (например, внутримозговой гематомы). Отек и гематома сдавливают и смещают нормальную ткань мозга. Чаще всего геморрагический инсульт связан с высоким кровяным давлением, которое создает нагрузку на стенки артерий до тех пор, пока они не разрываются.
Ишемия при серповидноклеточной анемии является результатом закупорки капилляров и недопущения тока крови в ткань, которая лишается кислорода и глюкозы. Эта закупорка капилляров вызывается эритроцитами, которые утратили свою нормальную форму и гибкость, разрушились или деформировались в жесткие или полужесткие "серповидные" формы. Закупорка капилляров прекращает ток свежей крови через те участки органа или ткани, которые в норме обслуживаются заблокированными капиллярами.
У большинства пациентов серповидноклеточная анемия не является причиной постоянной или хронической боли. Однако большая часть пациентов с серповидноклеточной анемией страдает от спорадических повторяющихся приступов, которые иногда называются ишемическими кризисами. Во время таких кризисов пациент с серповидноклеточной анемией обычно испытывает сильную боль в одном или более местах, которые часто различаются между пациентами и между разными кризисами у отдельного пациента. Нередко случается, что один или более суставов становятся опухшими и болезненными, и/или пациент страдает от острой или разлитой боли в животе, которая, как предполагается, является следствием ишемических состояний в одном или более участках одного или более органов.
Как правило, многие пациенты с серповидноклеточной анемией переносят несколько таких ишемических кризисов в год. Во время этих кризисов пациента, как правило, госпитализируют, назначают постельный режим с небольшой нагрузкой или отсутствием физической нагрузки и лечат целым рядом лекарственных средств, включая сильные обезболивающие средства, такие как морфин, кодеин и меперидин, и антибиотики широкого спектра действия, и то и другое помогает контролировать какие-либо инфекции, которые могут вносить вклад в кризисы, и помогает предотвратить или уменьшить дополнительные инфекции в тканях или органах, которые ослабляются в результате ишемического кризиса.
Среди детей младшего возраста с серповидноклеточной анемией обычным является дактилит вследствие ишемического некроза небольших костей и хрящей кистей рук и ступней, а острая боль в животе часто является результатом накопления повреждений в селезенке. Острая боль в животе также может быть результатом инфаркта в печени или почке, или может быть связана с гематурией. Как правило, в возрасте 10 лет наблюдаются холецистит вследствие желчных камней, асептический некроз головки бедренной кости, радиологические данные об уширенном объеме костного мозга в черепе, остеопороз позвоночника и некроз мозгового вещества почки, а у пациентов старше 18 лет часто происходят патологические переломы, в частности головки бедренной кости и плечевой кости. Ножные язвы являются обычным явлением у взрослых пациентов, а также наблюдаются лобарная пневмония, инфаркты легкого, инсульт и поражение сетчатки глаза. Во всех случаях боль является тяжелой, часто блуждающей и распространенной.
Одной причиной геморрагического инсульта является аневризма. Это слабое место в стенке артерии, которое растягивается наружу вс