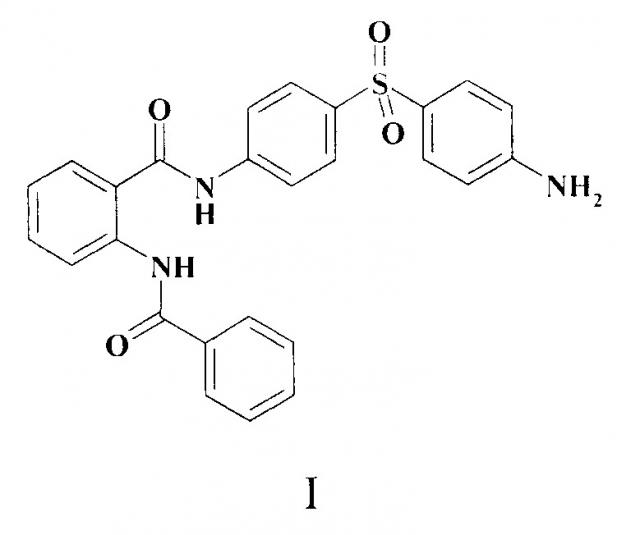
Противолепрозное средство, обладающее бактериостатической и бактерицидной активностью в отношении m. lufu, представляющее собой производное o-бензоиламинобензойной кислоты
Иллюстрации
Показать всеИзобретение относится к области химико-фармацевтической промышленности и медицины, конкретно к противолепрозному средству, представляющему собой производное о-бензоиламинобензойной кислоты указанной ниже формулы, которое обладает бактериостатической и бактерицидной активностью в отношении М. lufu. Средство является малотоксичным и обладает способностью подавлять размножение микобактерий. 1 пр., 5 табл.
Реферат
Изобретение относится к области химико-фармацевтической промышленности и медицины, точнее к новым производным о-бензоиламинобензойной кислоты, обладающим антилепрозной активностью, и касается соединений, которые могут быть использованы для создания лекарственных средств, активных в отношении Mycobacterium lufu. Предложен способ синтеза соединения формулы I, обладающего антилепрозным действием.
Предшествующий уровень техники
Известно, что для лечения лепры используют препараты дапсон, этионамид, а также антибиотики рифампицин, клофазимин, офлоксацин, моноциклин [http://apps.who.int/medicinedocs/en/d/Jh2988e/].
Рекомендуемые ВОЗ схемы лечения лепры включают препарат 4,4'-диаминодифенилсульфон («Дапсон»), выбранный нами в качестве прототипа. Однако этот препарат обладает значительными побочными эффектами, среди которых метгемоглобинемия, гемолитическая анемия, гипопластическая анемия с летальным исходом. Длительное использование 4,4'-диаминодифенилсульфона приводит к появлению резистентных штаммов, что требует поиска высокоэффективных и малотоксичных лекарственных средств. Соответственно к основным недостаткам этого препарата можно отнести высокую токсичность и длительность курса терапии.
Известны производные дихлормалейновой кислоты, обладающие антилепрозной активностью, однако синтез данных соединений экономически и препаративно уступает получению заявляемого вещества [А.с. 1131179 СССР, МКИ А61К 31/505. Опубл. 10.03.83 г.].
Вследствие этого актуальной задачей является поиск новых соединений, обладающих выраженной антилепрозной активностью в сочетании с низкой токсичностью.
Среди производных амидов антраниловой кислоты обнаружено немало соединений, обладающих широким спектром фармакологической активности и низкой токсичностью. К ним относятся производные о-бензоиламинобензойной кислоты, проявляющие противовоспалительную, актопротекторную, антигипоксическую активность и влияющие на ЦНС [Сочнев B.C., Кодониди И.П., Оганесян Э.Т., Кулешова С.А. и др. Синтез и противовоспалительная активность амидов антраниловой кислоты с фрагментами сульфаниламидов и дапсона ПМФИ - филиал ГБОУ ВПО ВолгГМУ Минздрава России. - Пятигорск, 2013. - Вып. 68. - С. 339-341; Кодониди И.П., Оганесян Э.Т., Жогло Е.Н., Сочнев B.C., Ивченко А.В., Манвелян Э.А., Сыса В.Ю. Целенаправленный синтез амидов о-бензоиламинобензойной кислоты в качестве предшественников хиназолинонов-4, обладающих влиянием на ЦНС [Новые направления в химии гетероциклических соединений: тез. докл. 3 междунар. науч. конф. - Ставрополь, 2013. - С. 280-281; Э.А. Манвелян, В.Ю. Сыса., И.П. Кодониди, Э.Т. Оганесян / Действие амидов орто-бензоиламинобензойной кислоты, производных предшественников хиназолинона-4, на поведение самцов крыс в «открытом поле» / Наука. Инновации. Технологии. - Ставрополь: Изд-во СКФУ, 2014. - №1. - С. 212-220].
Наиболее близкими по структуре к заявляемому объекту являются 2-бензоиламино-N-(4-сульфамоилфенил)-бензамиды, обладающие выраженным влиянием на ЦНС.
Эти данные свидетельствуют о перспективности поиска новых высокоэффективных и малотоксичных антилепрозных веществ в ряду производных амидов о-бензоиламинобензойной кислоты.
Целью изобретения является поиск малотоксичного соединения, обладающего способностью подавлять размножение микобактерий, синтез которого технологически прост, экономически выгоден и экологически безвреден. В связи с этим нами синтезировано соединение, относящееся к амидам о-бензоиламинобензойной кислоты, полученное путем модификации молекулы 4,4'-диаминодифенилсульфона.
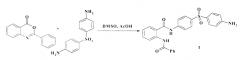
Способ получения соединения I основан на взаимодействии 2-фенилбензоксазин-4-она с 4,4'-диаминодифенилсульфоном при кипячении в смеси ледяной уксусной кислоты и диметилсульфоксида (схема 1).
ПРИМЕР СИНТЕЗА
N-[4-(4-аминобензсульфанил)-фенил]-2-бензоиламинобензамид (I)
Смесь 2,23 г (0,01 моль) 2-фенилбензо[d][1,3]оксазин-4-она и 2,48 г (0,01 моль) 4,4'-диаминодифенилсульфона кипятят 1 час в 9 мл ледяной уксусной кислоты и 0,5 мл диметилформамида. Охлаждают, осадок отфильтровывают, промывают эфиром диэтиловым. Получают 3,90 г N-[4-(4-аминобензсульфанил)-фенил]-2-бензоиламинобензамида, который подвергают перекристаллизации из этанола. Выход 83%. Вещество представляет собой белый кристаллический порошок, без запаха, нерастворим в воде, трудно растворим в этаноле, нерастворим в эфире. Т. пл. 249-250°С (из этанола).
Идентификация соединения I осуществлялась с использованием ИК- и 1Н ЯМР-спектроскопии.
Спектр 1Н ЯМР (300 МГц), δ, м.д., DMSO-d6: 6,11 (с, 2Н, NH2); 6,59-6,62 (д, 2Н, ArH); 7,27-7,32 (т, 1Н, ArH); 7,45-7,67 (м, 6Н, ArH); 7,79-7,93 (м, 7Н, ArH); 8,33-8,36 (т, 1Н, ArH); 10,80 (с, 1Н, NH); 11,33 (с, 1Н, NH).
Молекулярная масса: 471,5. Брутто формула: C26H21N3O4S
Элементный состав:
Найдено, %: С 66,29; Н 4,45; N 8,91; О 13,61; S 6,74.
Вычислено, %: С 66,23; Н 4,49; N 8,94; О 13,56; S 6,78.
Оценка фармакологической активности
Исследование способности N-[4-(4-аминобензсульфанил)фенил]-2-бензоиламинобензамида ингибировать рост микобактерий проводили в два этапа.
Первый этап осуществляли in vitro в отношении M.lufu [Иртуганова О.А., Урляпова Н.Г. Использование M.lufu для первичного отбора противолепрозных препаратов. - В кн.: Актуальные вопросы лепрологии. Астрахань, 1984, с. 147-150; SEYDEL, J.К., WEMPE, Е.G. Bacterial Growth Kinetics of "M. lufu" in the Presence and Absence of Various Drugs Alone and in Combination. A Model for the Development of Combined Chemotherapy Against M. leprae? // Int. J. Lepr. - 1982. - V. 50, №1. - P. 20-30] методом серийных разведений [Навашин С.М., Фомин И.П. Справочник по антибиотикам. - М.: Медицина, 1974. С. 54] на среде Школьниковой.
Сущность метода серийных разведений заключается в создании последовательных разведений вещества в питательной среде (в порядке геометрической или арифметической прогрессии). В наших опытах концентрация изучаемого соединения в ряду серийных разведений убывала в геометрической прогрессии с коэффициентом 2: 128 мкг/мл, 64 мкг/мл, 32 мкг/мл, 16 мкг/мл, 8 мкг/мл, 4 мкг/мл, 2 мкг/мл, 1 мкг/мл, 0,5 мкг/мл, 0,25 мкг/мл. Контролем служили пробирки, содержащие среду Школьниковой без ингибитора, а также ряды серийных разведений препарата сравнения - дапсона.
Навеску соединения (препарата) в 4 мг растворяли в 0,5 мл димексида, затем туда вносили 4,5 мл физиологического раствора - получали рабочий раствор, из которого путем разведения формировали ряд пробирок с заданными концентрациями.
Для приготовления взвеси микобактерий использовали двухнедельную культуру M.lufu, синхронизированную холодом (+4°С) в течение 72 часов. Суспензию микобактерий определенной плотности, соответствующей стандарту мутности 5 по McFarland, по 0,2 мл вносили в каждую пробирку ряда последовательных разведений изучаемого вещества, включая контроль. Посевы инкубировали в течение 10 дней при температуре +31°С. По истечении этого срока визуально оценивали наличие роста в каждой из пробирок: «-» - полная прозрачность среды; «+» - слабый рост; «++» - умеренный рост; «+++» - интенсивный рост.
Первую наименьшую концентрацию субстанции, при которой визуально не определялось помутнения среды, т.е. отсутствовал бактериальный рост, считали минимальной подавляющей концентрацией (МПК).
Далее содержимое пробирок центрифугировали при 1500 об/мин в течение 10 минут. Удаляли супернатант. Из каждой пробирки на среду Левенштейна-Йенсена высевали 0,05 мл содержимого осадка с целью определения жизнеспособности M.lufu. После высева на жизнеспособность из оставшегося осадка делали мазки, которые окрашивали: по методу Murohashi (1959) [Малая медицинская энциклопедия. - М.: Медицина, 1991-1996 г. г.] для определения соотношения «живых» и «мертвых» бактерий, и по Цилю-Нильсену [Малая медицинская энциклопедия. - М.: Медицина, 1991-1996] для определения наличия кислотоустойчивых (КУМ) и некислотоустойчивых форм (НКУМ). Посевы на среде Левенштейна-Иенсена инкубировали в течение 10 дней при температуре +31°С. Проводили подсчет колоний, выросших на косяке плотной среды. Минимальной бактерицидной концентрацией (МБК) соединения считали такую его концентрацию, после инкубации с которым на среде Левенштейна-Иенсена не имелось роста колоний тест-культуры.
Второй этап исследований проводили in vivo на экспериментальной модели лепры, предложенной Shepard С.С. [ Shepard С.С. The experimental disease that follows the infection of human leprosy bacilli info footpads of mice// J. Exp. Med., 1960, V. 112. P. 445-458], которая предполагает осуществление интраплантарного заражения мышей суспензией микобактерий, приготовленной из лепром или аутопсийной ткани нелеченого больного лепрой или из тканей экспериментальных мышей, ранее зараженных М. leprae от нелеченых больных, т.е. «из лапки в лапку».
Дапсон и соединение I животным вводили вместе с кормом. Для обеспечения постоянного поступления препарата в организм мышей готовили кормолекарственную смесь путем смешивания комбикорма с исследуемым веществом. Для приготовления кормолекарственной смеси использовали специальный роторный миксер «Rotomixer» (Англия). На 1 кг сухого комбикорма добавляли 100 мг вещества, получая, таким образом, смесь, содержащую 0,01% соединения I (или дапсона).
Введение препарата с пищей считается наиболее оптимальным, так как этим достигается постоянная концентрация в крови животных. Метод позволяет добиться адекватных результатов в ходе исследования. Учитывая, что мышь в сутки съедает около 5 г сухого корма, и это зависит от ее веса, который меняется с возрастом, такой способ введения вещества позволяет обеспечить строгий контроль за дозой, поступающей в организм [Батрак Г.Е., Кудрин А.Н. Дозирование лекарственных средств экспериментальным животным. М.: Медицина, 1979, 167 с.]. Использование кормолекарственных смесей рекомендовано ВОЗ в качестве стандартного метода введения лекарственных препаратов, испытываемых на противолепрозную активность. В данном случае использовали максимально эффективную дозу 25 мг/кг (МЭД) [Levi L. Activity of derivatives and analogs of dapsone against Micobacterium leprae // Antimicrobial Agente Chemother., 1978, V. 14. P. 791-793], сопоставимую по воздействию с дозой, применяемой при лечении больных лепрой людей (100 мг в сутки).
Животные были заражены М.leprae VIII пассаж от б-го М. (кл. №1693). Каждой мыши интраплантарно вводили 0,03 мл суспензии, содержащей 104 микробных тел. Мышей делили на три группы: 1 - контроль (зараженные, не получавшие специфического лечения), 2 - группа сравнения (зараженные, получавшие дапсон в дозе 25 мг/кг), 3 - опытная (зараженные, получавшие соединение I в дозе 25 мг/кг). Дапсон и соединение I начинали вводить на следующий день после заражения. Через 4, 9 и 11 месяцев с начала эксперимента по 10 животных из каждой группы забивали хлороформным наркозом, отсекали правую заднюю лапу.
Для подсчета микобактерий готовили суспензию. Для этого тщательно срезали ткани подушечки отсеченной лапки, измельчали ножницами. Измельченные ткани перетирали в фарфоровой ступке, добавив 2,0 мл дистиллированной воды. Полученную суспензию центрифугировали 3 мин при 1000 об/мин для осаждения грубых тканевых частиц, из супернатанта готовили мазок для подсчета микобактерий. Для приготовления мазка использовали специальные предметные стекла с нанесенными на них кругами площадью 1 см2. В середину каждого круга помещали 10 мкл 0,1% раствора альбумина в дистиллированной воде, добавляли 10 мкл исследуемой суспензии М.leprae. Жидкости смешивали и равномерно распределяли по поверхности круга так, чтобы наружный край мазка касался внутреннего края окружности круга. Мазок высушивали на воздухе и фиксировали над пламенем горелки, окрашивали по Цилю-Нильсону.
Подсчет количества микобактерий проводили по методу Shepard С.С., McRae D.H. [Shepard С.С. Drags against М.leprae in the mouse and in man // Int. J. Lepr., 1968, V. 36. P. 650].
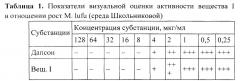
Визуальная оценка посевов на среде Школьниковой показала, что под действием субстанции вещества I в диапазоне концентраций 128-8 мкг/мл среда остается прозрачной, что предполагает практическое отсутствие роста бактерий. По мере снижения ее содержания в пробирках отмечали наличие мутности до полной потери прозрачности среды (таблица 1), что было сопоставимо с действием дапсона - основного противолепрозного препарата.
Первичная (визуальная оценка) позволила определить МПК исследованного соединения. Для вещества I она составила 8 мкг/мл, что было сопоставимо с показателями препарата сравнения.
Анализ мазков, окрашенных по Цилю-Нильсену, показал, что в рядах разведений соединения I в интервале концентраций 128-16 мкг/мл отсутствуют кислотоустойчивые формы, что было идентично при анализе соответствующих проб с дапсоном. С понижением концентраций действующих веществ содержание КУМ в пробах возрастало, но даже при самом большом разведении не превышало 40%.
При исследовании мазков, окрашенных по Murohashi, выявлено снижение содержания живых форм микобактерий. Доля нежизнеспособных бактерий уменьшалась с увеличением разведения как под действием соединения I, так и дапсона и составляла при минимальных концентрациях не более 50%, в то время как в контроле (без воздействия) она не превышала 8-10%.
Оценка наличия и интенсивности роста М. lufu на среде Левенштейна-Йенсена показала его полное отсутствие в пробирках после предварительной инкубации микобактерий на среде Школьниковой с веществом I в диапазоне концентраций 128-8 мкг/мл (таблица 2), т.е. МБК составила 8 мкг/мл. При более низких концентрациях наблюдали рост атипичных колоний (от слабой до средней интенсивности соответственно). МБК дапсона оказалась значительно выше (таблица 2): отсутствие роста наблюдали после инкубации М. lufu с дапсоном в диапазоне 128-64 мкг/мл, далее отмечали единичные атипичные колонии, а при снижении концентрации до 2 мкг/мл их интенсивный рост.
Таким образом, патентуемое производное о-бензоиламинобензойной кислоты проявляет как бактериостатическое, так и бактерицидное свойства в отношении М. lufu - тестовой культуры для оценки противолепрозной активности субстанций. По показателям активности в исследованиях in vitro оно либо сопоставимо с дапсоном (МПК), либо несколько превосходит его [Лужнова С.А., Габитова Н.М., Воронков А.В., Кодониди И.П., Ловягина С.А., Сочнев B.C. Оценка антимикобактериальной активности новых производных диазинона // Фундаментальные исследования. - 2015. - №2. Ч. 11. - С. 2377-2380].
Исследования, проведенные in vivo на экспериментальной модели лепры Шепарда, показали следующие результаты (таблица 3).
Как видно из таблицы 3, у контрольных мышей, не получавших лечения, среднее количество микобактерий в лапах через 4 месяца с начала эксперимента было практически на три порядка выше, чем при введении. В группах, получавших дапсон и соединение I, наблюдали угнетение процесса размножения микобактерий: более чем в 15 раз. Введение дапсона и соединения I в течение девяти месяцев также способствовало торможению процесса размножения бактерий. Выраженный бактериостатический эффект наблюдали при применении вещества I в течение 11 месяцев: «урожай» микобактерий в лапах был в 70 раз ниже, чем в контроле и статистически достоверно эффективнее, чем в группе получавшей дапсон (более чем в два раза).
Таким образом, соединение I в условиях in vivo обладает выраженным бактериостатическим действием, не только сопоставимым с действием дапсона, но и при более длительном курсе превосходящем его.
Хроническая токсичность
Учитывая, что дапсон обладает рядом негативных эффектов, приводящих к изменению показателей крови, проведено сравнительное исследование влияния курсового введения соединения I и препарата дапсон на гемограмму и показатели тромбоцитов.
Исследование выполнено на 60 крысах линии «Wistar» обоего пола, весом 190-205 г (на момент начала эксперимента). Животные содержались на стандартном пищевом рационе со свободным доступом к корму и воде. После двухнедельного карантина крысы были распределены на 6 групп по 10 особей в каждой. Группы 1 (самцы) и 2 (самки) являлись контрольными и получали эквивалентный объем дистиллированной воды из расчета 2 мл на 200 г веса животного. Животным 3 (самцы) и 4 (самки) групп вводили дапсон, 5 (самцы) и 6 (самки) - соединение I. Вещества вводили через зонд в желудок 1 раз в день в утреннее время в течение 30 дней в дозе 25 мг/кг (соответствует по эффективности 100 мг/кг в день для человека) [Лужнова С.А., Абдрешева Р.Ж. Коррекция альфа-токоферолом структурно-функционального статуса эритроцитов старых крыс при введении дапсона // Фундаментальные исследования. - 2013. - №10. - С. 344-348].
Забор крови у крыс осуществляли из подъязычной вены, которую стабилизировали гепарином (50 ЕД/мл). Показатели крови определяли с использованием системы ветеринарного автоматического гематологического анализа ВС 2800vet (Mindray).
Все манипуляции проводили согласно требованиям по гуманному обращению с животными [Руководством по проведению доклинических исследований лекарственных средств. Часть первая / Под ред. А.Н. Миронова. - М.: Гриф и К, 2012].
Статистическую обработку результатов осуществляли с помощью программ «BIOSTAT 2009». Показатель достоверности различий определяли по t - критерию Стьюдента.
Результаты проведенного исследования показали, что введение вещества I в течение 30 дней у крыс-самцов не вызывает изменения количества эритроцитов и уровня гемоглобина периферической крови, в то время как при применении препарата сравнения (дапсон) данные показатели статистически значимо снижаются (таблица 4). Среднее содержание гемоглобина в эритроците, коэффициент вариации остаются идентичными контролю, уровень гематокрита сопоставим с количеством эритроцитов и аналогичным показателем у крыс, не подвергавшимся воздействию. У животных, получавших дапсон, наблюдается повышение среднего содержания гемоглобина, что вполне согласуется со значительным снижением в крови количества эритроцитов. Коэффициент вариации эритроцитов статистически достоверно увеличивается, что свидетельствует о негативной нагрузке на систему крови [М.С. Gavilanes, A.L. Palacio, P.R. Chellini, [et al]. Dapsone hypersensitivity syndrome in a lepromatous leprosy patient - A Case Report//Lepr.Rev. - 2015. - Vol. 86, №2. P. 186-190].
Как известно, морфофункциональные характеристики, обеспечивающие целостность эритроцитов, способны изменяться под влиянием ряда факторов, в том числе под воздействием лекарственных препаратов, что может привести к снижению их резистентности. Распаду эритроцитов предшествует их сферуляция и набухание, что характеризует такой показатель крови, как средний объем эритроцита. Под действием соединения I после 30-дневного курса у крыс-самцов наблюдается в сравнении с контролем незначительное (на 3%), но статистически достоверное повышение среднего объема эритроцитов, по-видимому, компенсированное, что подтверждается тенденцией к повышению их количества. В сравнении, такой же курс препарата дапсон способствует увеличению среднего объема эритроцитов на 35% (таблица 4) при снижении их количества на 25%, что свидетельствует о необратимости гемолитического влияния дапсона [М.С. Gavilanes, A.L. Palacio, P.R. Chellini, [et al]. Dapsone hypersensitivity syndrome in a lepromatous leprosy patient - A Case Report//Lepr.Rev. - 2015. - Vol. 86, №2. P. 186-190].
У крыс-самок после курсового введения вещества I не выявлено каких-либо значимых изменений показателей красной крови (таблица 4). В условиях же применения дапсона у животных наблюдали тенденцию к снижению количества эритроцитов и гемоглобина, а средний объем и коэффициент вариации эритроцитов были статистически достоверно выше, чем в контрольной группе самок.
Наряду с эритроцитами, важным клеточным элементом внутреннего гемостаза являются тромбоциты, которые представляют собой не только компоненты свертывающей системы крови, но и оказывают ангиотрофическое действие и участвуют, выделяя факторы роста, в регенерации поврежденных тканей. Известно, что некоторые лекарственные препараты способны влиять на количественные и качественные характеристики тромбоцитов [Козинец Г.И., Высоцкий В.В., Погорелов В.М., Еровиченков А.А.. Малов В.А. Кровь и инфекция. - М.: Триада-фарм, 2001. - С. 456]. Был проведен сравнительный анализ влияния курсового введения вещества I и дапсона на некоторые показатели тромбоцитов.
Введение дапсона в течение 30 дней приводило к изменению количественных и качественных характеристик тромбоцитов как у самцов, так и у самок (таблица 5). В частности, в сравнении с контролем у крыс обоего пола наблюдали статистически достоверное уменьшение их числа и снижение показателей тромбокрита. При этом средний объем тромбоцитов и широта их распределения по объему (коэффициент вариации) возрастали, что свидетельствует о нарушении процесса мегакариоцитопоэза под действием дапсона.
Курсовое введение соединение вещества I значимых изменений показателей тромбоцитов не вызывало (таблица 5).
Таким образом, соединение I обладает специфической антимикобактериальной активностью и, в отличие от основного противолепрозного препарата дапсона, не оказывает токсического влияния на морфофункциональные характеристики эритроцитов и мегакариоцитопоэз, что обусловливает его перспективность для дальнейшей разработки. [Оценка влияния нового производного диазинона ПЯТd1 на некоторые показатели периферической крови крыс обоего пола / А.В. Воронков, С.А. Лужнова, С.А. Осыченко, Н.М. Габитова // Вестник Волгоградского государственного медицинского университета. - 2015. - №4 (56). - С. 124-126.]
Примечания: «-» - полная прозрачность среды; «+-» - неполная прозрачность среды; «+» - слабый рост; «++» - умеренный рост; «+++» - интенсивный рост.
Примечания: «-» - отсутствие колоний; «+» - единичные колонии; «++» - <= 50 %, «+++» - <= 75 %; «++++» - <= 100 % заселения площади косяка среды; АК -атипичные колонии.
Примечание: *- Рк<0,05; **- Рк<0,01;***- Рк<0,001 относительно контроля; # - Рд<0,05 относительно дапсона.
Примечание: *- Рк<0,05; **- Рк<0,02;**- Рк<0,01;****- Рк <0,001 относительно контроля. #### - Рд<0,001 относительно «дапсона».
Примечание: * - Рк<0,05; ** - Рк<0,02; ** - Рк<0.01; **** - Рк <0,001 относительно контроля.
Противолепрозное средство, представляющее собой производное о-бензоиламинобензойной кислоты общей формулы I,
обладающее бактериостатической и бактерицидной активностью в отношении М. lufu.