Способ и среда для ферментации синтез-газа
Иллюстрации
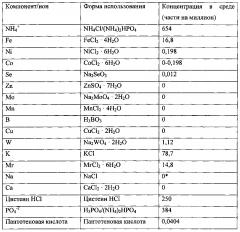
Показать всеГруппа изобретений относится к среде для ферментации синтез-газа и способу ферментации синтез-газа. Среда для ферментации синтез-газа содержит от 546 до 838 частей на миллион ионов NH4+, от 31,8 до 279 частей на миллион ионов фосфора, от 39,3 до 118 частей на миллион ионов калия, от 8,4 до 16,8 частей на миллион ионов железа, от 14,8 до 59,8 частей на миллион ионов магния, и 250 частей на миллион цистеина HCl, при этом среда для ферментации содержит менее чем 0,025 части на миллион ионов бора, менее чем 0,0025 части на миллион ионов марганца, менее чем 0,001 части на миллион ионов молибдена и менее чем 0,01 части на миллион ионов меди. Способ ферментации синтез-газа с использованием ацетогенных бактерий предусматривает ферментацию синтез-газа в указанной ферментационной среде. Изобретение обеспечивает удельный выход продукта за один проход в единицу (STY) по меньшей мере 1 грамма этанола/(л⋅сутки⋅грамм клеток). 2 н. и 15 з.п. ф-лы, 10 табл., 10 пр.
Реферат
Приоритет настоящей заявки испрашивается на основании предварительных патентных заявок US 61/650098, 61/650093, 61/650077, 61/650084, поданных 22 мая 2012 г., и предварительной патентной заявки US 61/726225, поданной 14 ноября 2012 г., которые во всей полноте в порядке ссылки включены в настоящую заявку.
Область техники
В изобретении предложены способы и среды ферментации синтез-газа. Более точно, предложены способы и среды, обеспечивающие высокий уровень производительности по этанолу даже после исключения или снижения содержания компонентов, ранее считавшихся существенными или необходимыми в определенных концентрациях.
Уровень техники
Ферментация происходит в определенных жидких средах. Эти среды обычно содержат различные источники питательных макро- и микроэлементов, важных для повышения эффективности ферментации. Для оптимизации характеристик сред, используемых в сочетании с менее распространенными носителями, такими как газообразные носители, требуется их строгое определение. Для анаэробной ферментации также требуются строго определенные среды.
Анаэробные микроорганизмы способны синтезировать этанол из окиси углерода (CO) путем ферментации газообразных носителей. В результате ферментации с участием анаэробных микроорганизмов рода Clostridium образуется этанол и другие полезные продукты. Например, в патенте US 5173429 описан анаэробный микроорганизм Clostridium ljungdahlii (АТСС №49587), который синтезирует этанол и ацетат из синтез-газа. В патенте US 5807722 описаны способ и устройство для конверсии отходящих газов в органические кислоты и спирты с использованием Clostridium ljungdahlii (АТСС №55380). В патенте US 6136577 описаны способ и устройство для конверсии отходящих газов в этанол с использованием Clostridium ljungdahlii (АТСС №55988 и №55989).
В патенте US 7285402 описаны среды, применимые для анаэробной ферментации газообразных носителей с целью получения этанола. Различные компоненты и их концентрации в среде обеспечивают высокие уровни производительности по этанолу. За счет исключения определенных компонентов и снижения требуемых концентраций других компонентов с сохранением производительности по этанолу может достигаться значительное снижение себестоимости, в особенности, при ферментации в промышленном масштабе.
Сущность изобретения
Предложены способ ферментации синтез-газа и ферментационная среда с высокой производительностью по этанолу при исключении компонентов среды, ранее считавшихся существенными. Исключение некоторых компонентов среды и снижение содержания других компонентов среды обеспечивает значительное сокращение эксплуатационных затрат в промышленном масштабе.
Согласно одной из особенностей способ ферментации включает ферментацию синтез-газа в ферментационной среде. Способ обеспечивает удельный STY по меньшей мере около 1 грамма этанола/(л⋅сутки⋅грамм клеток). Согласно этой особенности ферментационная среда содержит менее около 1,04 части на миллион бора, менее около 0,16 части на миллион марганца, менее около 0,26 части на миллион молибдена или менее около 0,16 части на миллион меди.
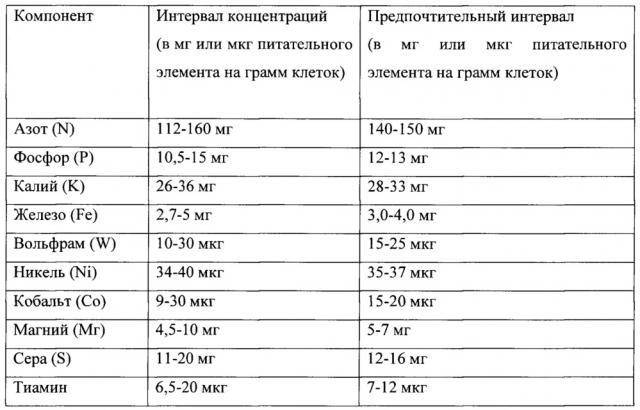
Согласно другой особенности ферментационная среда содержит по меньшей мере около 112 мг азота на грамм образовавшихся клеток, по меньшей мере около 10,5 мг фосфора на грамм образовавшихся клеток или по меньшей мере около 26 мг калия на грамм образовавшихся клеток. Согласно другой особенности ферментационная среда содержит менее около 1,04 части на миллион бора, менее около 0,16 части на миллион марганца, менее около 0,26 части на миллион молибдена или менее около 0,16 части на миллион меди.
Согласно другой особенности способ ферментации включает ферментацию синтез-газа в ферментационной среде. Способ обеспечивает удельный STY по меньшей мере около 1 грамма этанола/(л⋅сутки⋅грамм клеток). Ферментационная среда содержит NH4+ и В в весовом соотношении около 625:1 или более или NH4+ и Mn в весовом соотношении около 4050:1 или более, или NH4+ и Мо в весовом соотношении около 2500:1 или более, или NH4+ и Cu в весовом соотношении около 4050:1 или более; ферментационная среда содержит Р и В в весовом соотношении около 30:1 или более или Р и Mn в весовом соотношении около 190:1 или более, или P и Mo в весовом соотношении около 120:1 или более, или Mn и Cu в весовом соотношении около 190:1 или более; или ферментационная среда содержит K и B в весовом соотношении около 35:1 или более или K и Mn в весовом соотношении около 245:1 или более, или K и Mo в весовом соотношении около 150:1 или более, или K и Cu в весовом соотношении около 245:1 или более.
Подробное описание изобретения
Следующее далее описание не следует считать ограничивающим, и оно имеет целью лишь изложение общих принципов примеров осуществления. Объем изобретения следует определять на основании формулы изобретения.
В изобретении предложены способ и состав среды, неожиданно обеспечивающие высокий уровень производительности по этанолу даже после исключения или снижения содержания одного или нескольких компонентов, ранее считавшихся существенными или необходимыми в определенных концентрациях. Согласно этой особенности в среде могут быть снижены уровни содержания одного или нескольких питательных элементов, включающих B, Mn, Mo и Cu. Среда может иметь следующие содержания питательных элементов:
B: менее около 1,04 части на миллион, согласно другой особенности менее около 1,0 части на миллион, согласно другой особенности менее около 0,75 части на миллион, согласно другой особенности менее около 0,5 части на миллион и согласно другой особенности менее около 0,025 части на миллион;
Mn: менее около 0,16 части на миллион, согласно другой особенности менее около 0,15 части на миллион, согласно другой особенности менее около 0,10 части на миллион, согласно другой особенности менее около 0,05 части на миллион и согласно другой особенности менее около 0,0025 части на миллион;
Mo: менее около 0,26 части на миллион, согласно другой особенности менее около 0,25 части на миллион, согласно другой особенности менее около 0,20 части на миллион, согласно другой особенности менее около 0,10 части на миллион Mo и согласно другой особенности менее около 0,001 части на миллион; или
Cu: менее около 0,16 части на миллион, согласно другой особенности менее около 0,15 части на миллион, согласно другой особенности менее около 0,10 части на миллион, согласно другой особенности менее около 0,05 части на миллион и согласно другой особенности менее около 0,01 части на миллион.
Согласно другой особенности возможны следующие весовые соотношения:
NH4+ и B: около 625:1 или более, согласно другой особенности около 650:1 или более, согласно другой особенности около 675:1 или более, согласно другой особенности около 700:1 или более, согласно другой особенности около 750:1 или более и согласно другой особенности около 800:1 или более; или
NH4+ и Mn: около 4050:1 или более, согласно другой особенности около 4100:1 или более, согласно другой особенности около 4200:1 или более, согласно другой особенности около 4300:1 или более, согласно другой особенности около 4400:1 или более и согласно другой особенности около 4500:1 или более; или
NH4+ и Mo: около 2500:1 или более, согласно другой особенности около 2600:1 или более, согласно другой особенности около 2700:1 или более, согласно другой особенности около 2800:1 или более, согласно другой особенности около 2900:1 или более и согласно другой особенности около 3000:1 или более; или
NH4+ и Cu: около 4050:1 или более, согласно другой особенности около 4100:1 или более, согласно другой особенности около 4200:1 или более, согласно другой особенности около 4300:1 или более, согласно другой особенности около 4400:1 или более и согласно другой особенности около 4500:1 или более; или
P и B: около 30:1 или более, согласно другой особенности около 35:1 или более, согласно другой особенности около 40:1 или более, согласно другой особенности около 45:1 или более, согласно другой особенности около 50:1 или более и согласно другой особенности около 100:1 или более; или
P и Mn: около 190:1 или более, согласно другой особенности около 200:1 или более, согласно другой особенности около 225:1 или более, согласно другой особенности около 250:1 или более, согласно другой особенности около 275:1 или более и согласно другой особенности около 300:1 или более; или
P и Mo: около 120:1 или более, согласно другой особенности около 130:1 или более, согласно другой особенности около 140:1 или более, согласно другой особенности около 150:1 или более, согласно другой особенности около 175:1 или более и согласно другой особенности около 200:1 или более; или
P и Cu: около 190:1 или более, согласно другой особенности около 200:1 или более, согласно другой особенности около 225:1 или более, согласно другой особенности около 250:1 или более, согласно другой особенности около 275:1 или более и согласно другой особенности около 300:1 или более; или
K и B: около 35:1 или более, согласно другой особенности около 40:1 или более, согласно другой особенности около 45:1 или более, согласно другой особенности около 50:1 или более, согласно другой особенности около 75:1 или более и согласно другой особенности около 100:1 или более; или
K и Mn: около 245:1 или более, согласно другой особенности около 250:1 или более, согласно другой особенности около 260:1 или более, согласно другой особенности около 270:1 или более, согласно другой особенности около 280:1 или более и согласно другой особенности около 300:1 или более; или
K и Mo: около 150:1 или более, согласно другой особенности около 250:1 или более, согласно другой особенности около 260:1 или более, согласно другой особенности около 270:1 или более, согласно другой особенности около 280:1 или более и согласно другой особенности около 300:1 или более; или
K и Cu: около 245:1 или более, согласно другой особенности около 250:1 или более, согласно другой особенности около 260:1 или более, согласно другой особенности около 270:1 или более, согласно другой особенности около 280:1 или более и согласно другой особенности около 300:1 или более.
Определения
Если не указано иное, следующие термины, используемые в описании настоящего изобретения, имеют следующее значение согласно приведенным далее определениям в единственном или множественном числе.
Термин "около", предшествующий любому численному значению, означает отклонение от указанного значения в реальных условиях, например, в лаборатории, на экспериментальной установке или эксплуатационном объекте. Например, численное значение с предшествующим ему термином "около" применительно к ингредиенту смеси или измерению количества, включает отклонение и степень точности, обычно применяемую при измерениях в экспериментальных условиях на промышленной установке или в лаборатории. Например, численное значение с предшествующим ему термином "около" применительно к компоненту продукта включает отклонение в зависимости от партий во множестве экспериментов на установке или в лаборатории и отклонение, присущее методу анализа. Независимо от использования термина "около" численные значения включают эквиваленты этих значений. Любое приведенное в описании численное значение с предшествующим ему термином "около" также может применяться в настоящем изобретении без термина "около".
Термином "синтез-газа" или "синтетический газ" называют газовую смесь, содержащую варьирующие количества окиси углерода и водорода. Примеры получения синтез-газа включают паровой реформинг природного газа или углеводородов с целью получения водорода, газификацию каменного угля и получение энергии путем газификации отходов на установках некоторых типов. Происхождение термина объясняется тем, что синтез-газ используется в качестве промежуточного продукта при получении заменителя природного газа (SNG) и производстве аммиака или метанола. Синтез-газа является горючим и часто используется в качестве источника топлива или промежуточного продукта при производстве других химикатов.
Термины "ферментация", "процесс ферментации" или "реакция ферментации" и т.п. относятся как к фазе роста, так и фазе биосинтеза продуктов. Согласно одной из особенностей ферментация означает конверсию CO в спирт.
Термин "плотность клеток" означает массу клеток микроорганизмов на единицу объема ферментационной среды, например, грамм/литр. Согласно этой особенности способ и среды обеспечивают плотность клеток по меньшей мере на около 1,0 г/л. Плотность клеток может составлять от около 1 до около 25 г/л, согласно другой особенности от около 1 до около 20 г/л, согласно другой особенности от около 1 до около 10 г/л, согласно другой особенности от около 2 до около 8 г/л, согласно другой особенности от около 3 до около 6 г/л и согласно другой особенности от около 4 до около 5 г/л.
Термин "рециркуляция клеток" означает отделение клеток микроорганизмов от ферментационной среды и возврат всех или части этих отделенных клеток микроорганизмов в ферментер. Обычно для отделения и используется фильтрационное устройство.
Состав среды
Описанные в изобретении способы и среды обеспечивают высокий уровень производительности. Согласно этой особенности способ обеспечивает удельный STY (удельный выход продукта за один проход в единицу) по меньшей мере около 1 грамма этанола/(л⋅сутки⋅грамм клеток)), согласно другой особенности от около 1 до около 10, согласно другой особенности от около 2 до около 8, согласно другой особенности от около 3 до около 7 и согласно другой особенности от около 4 до около 6.
Согласно одной из сопутствующих особенностей производительность может выражаться как STY (выход продукта за один проход в единицу) в граммах этанола/(л⋅сутки)). Согласно этой особенности способ обеспечивает STY по меньшей мере около 10 г этанола/(л⋅сутки). Возможные величины STY включают от около 10 г этанола/(л⋅сутки) до около 200 г этанола/(л⋅сутки), согласно другой особенности от около 10 г этанола/(л⋅сутки) до около 160 г этанола/(л⋅сутки), согласно другой особенности от около 10 г этанола/(л⋅сутки) до около 120 г этанола/(л⋅сутки), согласно другой особенности от около 10 г этанола/(л⋅сутки) до около 80 г этанола/(л⋅сутки), согласно другой особенности от около 20 г этанола/(л⋅сутки) до около 140 г этанола/(л⋅сутки), согласно другой особенности от около 20 г этанола/(л⋅сутки) до около 100 г этанола/(л⋅сутки), согласно другой особенности от около 40 г этанола/(л⋅сутки) до около 140 г этанола/(л⋅сутки) и согласно другой особенности от около 40 г этанола/(л⋅сутки) до около 100 г этанола/(л⋅сутки).
Согласно другой особенности способы и среды обеспечивают конверсию по меньшей мере от около 5% до около 99% CO, согласно другой особенности от около 10% до около 90%, согласно другой особенности от около 20% до около 80%, согласно другой особенности от около 30% до около 70% и согласно другой особенности от около 40% до около 90% CO.
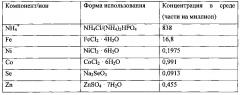
Согласно одной из особенностей среда содержит по меньшей мере один или несколько источников азота, по меньшей мере один или несколько источников фосфора и по меньшей мере один или несколько источников калия. Среда может содержать любой из трех источников, любое их сочетание и согласно одной из важных особенностей содержит все три источника. Источник азота может включать источник азота, выбранный из группы, включающей хлорид аммония, фосфат аммония, сульфат аммония, нитрат аммония и их смеси. Источник фосфора может включать источник фосфора, выбранный из группы, включающей фосфорную кислоту, фосфат аммония, фосфат калия и их смеси. Источник калия может включать источник калия, выбранный из группы, включающей хлорид калия, фосфат калия, нитрат калия, сульфат калия и их смеси.
Согласно одной из особенностей среда содержит одно или несколько из следующего: железо, вольфрам, никель, кобальт, магний, серу и тиамин. Среда может содержать любой один из этих компонентов, любое их сочетание и согласно одной из важных особенностей содержит все эти компоненты. Источник железа может включать источник железа, выбранный из группы, включающей хлорид железа, сульфат железа и их смеси. Источник вольфрама может включать источник вольфрама, выбранный из группы, включающей вольфрамат натрия, вольфрамат кальция, вольфрамат калия и их смеси. Источник никеля может включать источник никеля, выбранный из группы, включающей хлорид никеля, сульфат никеля, нитрат никеля и их смеси. Источник кобальта может включать источник кобальта, выбранный из группы, включающей хлорид кобальта, фторид кобальта, бромид кобальта, йодид кобальта и их смеси. Источник магния может включать источник магния, выбранный из группы, включающей хлорид магния, сульфат магния, фосфат магния и их смеси. Источник серы может включать цистеин, сульфид натрия и их смеси. Далее приведены концентрации различных компонентов.
При осуществлении способа поддерживается рН на уровне от около 4,2 до около 4,8. Среда содержит менее около 0,01 г/л дрожжевого экстракта и менее около 0,01 г/л углеводов. Синтез-газ
Может использоваться синтез-газа из любого известного источника. Согласно одной из особенностей источником синтез-газа может являться газификация углеродистых материалов. Газификация предусматривает частичное сжигание биомассы в условиях ограниченной подачи кислорода. Образующийся газ по большей части содержит СО и Н2. Согласно этой особенности синтез-газа содержит по меньшей мере около 10 мол. % CO, согласно одной из особенностей по меньшей мере около 20 мол. %, согласно одной из особенностей от около 10 до около 100 мол. %, согласно другой особенности от около 20 до около 100 мол. % CO, согласно другой особенности от около 30 до около 90 мол. % CO, согласно другой особенности от около 40 до около 80 мол. % CO и согласно другой особенности от около 50 до около 70 мол. % CO. Синтез-газ имеет молярное соотношение CO/CO2 по меньшей мере около 0,75, согласно другой особенности по меньшей мере около 1,0 и согласно другой особенности по меньшей мере около 1,5. Некоторые примеры применимых способов и устройств для газификации описаны в заявках US 13/427144, 13/427193 и 13/427247, поданных 22 марта 2012 г. и в порядке ссылки включенных в настоящую заявку.
Согласно другой особенности синтез-газом, используемым для размножения ацетогенных бактерий, может являться преимущественно CO. Используемый оборот "преимущественно CO" означает, что газ содержит по меньшей мере около 50 мол. % CO, согласно другой особенности по меньшей мере около 60 мол. % CO, согласно другой особенности по меньшей мере около 70 мол. % CO, согласно другой особенности по меньшей мере около 80 мол. % СО и согласно другой особенности по меньшей мере около 90 мол. % СО.
Биореактор
Согласно одной из особенностей ферментация начинается с добавления среды в реакционный сосуд. Стерилизуют среду, чтобы удалить нежелательные микроорганизмы, и засевают реактор желаемыми микроорганизмами. Согласно одной из особенностей используемые микроорганизмы включают ацетогенные бактерии. Примеры применимых ацетогенных бактерий включают бактерии рода Clostridium, такие как штаммы Clostridium ljungdahlii, включая штаммы, описанные в WO 2000/68407, ЕР 117309, патентах US 5173429, 5593886 и 6368819, WO 1998/00558 и WO 2002/08438, штаммы Clostridium autoethanogenum (DSM 10061 и DSM 19630, депонированные в DSMZ, Германия), включая штаммы, описанные в WO 2007/117157 и WO 2009/151342, Clostridium ragsdalei (P11, АТСС ВАА-622) и Alkalibaculum bacchi (СР11, АТСС ВАА-1772), включая штаммы, описанные, соответственно, в патенте US 7704723 и докладе "Biofuels and Bioproducts from Biomass-Generated Synthesis Gas", Hasan Atiyeh от 29 апреля 2010 г. на Ежегодной Конференции по экспериментальной программе содействия исследовательским проектам в штате Оклахома (Oklahoma EPSCoR Annual State Conference), и Clostridium carboxidivorans (АТСС PTA-7827), описанные в патентной заявке US 2007/0276447. Другие применимые микроорганизмы включают микроорганизмы рода Moorella, в том числе Moorella sp. HUC22-1, и микроорганизмы рода Carboxydothermus. Каждый из указанных документов в порядке ссылки включен в настоящую заявку. Могут использоваться смешанные культуры из двух или более микроорганизмов.
Некоторые примеры применимых бактерий включают Acetogenium kivui, Acetoanaerobium noterae, Acetobacterium woodii, Alkalibaculum bacchi СР11 (ATCC BAA-1772), Blautia producta, Butyribacterium methylotrophicum, Caldanaerobacter subterraneous, Caldanaerobacter subterraneous pacificus, Carboxydothermus hydrogenoformans, Clostridium aceticum, Clostridium acetobutylicum, Clostridium acetobutylicum P262 (DSM 19630, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 19630, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 10061, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 23693, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 24138, депонирована в DSMZ, Германия), Clostridium carboxidivorans P7 (АТСС PTA-7827), Clostridium coskatii (АТСС PTA-10522), Clostridium drakei, Clostridium ljungdahlii PETC (ATCC 49587), Clostridium ljungdahlii ERI2 (ATCC 55380), Clostridium ljungdahlii C-01 (ATCC 55988), Clostridium ljungdahlii O-52 (ATCC 55889), Clostridium magnum, Clostridium pasteurianum (DSM 525, депонирована в DSMZ, Германия), Clostridium ragsdali P11 (ATCC BAA-622), Clostridium scatologenes, Clostridium thermoaceticum, Clostridium ultunense, Desulfotomaculum kuznetsovii, Eubacterium limosum, Geobacter cepareducens, Methanosarcina acetivorans, Methanosarcina barkeri, Morrella thermoacetica, Morrella thermoautotrophica, Oxobacter pfennigii, Peptostreptococcus productus, Ruminococcus productus, Thermoanaerobacter kivui и их смеси.
После засева устанавливают начальный расход подаваемого газа для обеспечения начальной популяции микроорганизмов. Анализируют выходящий газ с целью определения его содержания. Используют результаты анализа для регулирования расхода подаваемого газа. После достижения желаемых уровней удаляют из реактора жидкую фазу и клеточный материал, и пополняют среду. Согласно этой особенности поддерживают в биореакторе плотность клеток по меньшей мере около 2 грамм/литр и согласно другой особенности от около 2 до около 50 грамм/литр, согласно различным другим особенностям от около 5 до около 40 грамм/литр, от около 5 до около 30 грамм/литр, от около 5 до около 20 грамм/литр, от около 5 до около 15 грамм/литр, от около 10 до около 40 грамм/литр, от около 10 до около 30 грамм/литр, от около 10 до около 20 грамм/литр и от около 10 до около 15 грамм/литр. Плотность клеток может регулироваться посредством фильтра рециркуляции. Некоторые примеры биореакторов описаны в предварительных заявках US 61/571654 и 61/571565, поданных 30 июня 2011 г., и предварительной заявке US 61/573845, поданной 13 сентября 2011 г., все из которых в порядке ссылки включены в настоящую заявку.
Примеры
Пример 1
Ферментация с ограничением концентрации бора, меди и марганца
Были проведены эксперименты в биореакторе (New Brunswick BioFlo I или IIc), который использовался как прямоточный CSTR без очистки пермеата. Использовали следующие условия эксплуатации биореактора:
тип культуры: Clostridium ljungdahlii С01,
поддерживаемая температура культуры: 38-39°С,
скорость перемешивания: около 850 об/мин на аналоговом индикаторе,
объем невыросшей культуры: около 1600-1650 мл.
Установили значение pH культуры 4,5. Использовали 7,7% раствор NaHCO3 для регулирования pH.
В качестве газа использовали синтезированную смесь 15% H2, 45% N2, 30% CO и 10% CO2, которую подавали в культуру со скоростью 282 мл/мин.
Скорость подачи среды в реактор составляла ~0,88 мл/мин или ~1300 мл/сутки.
Время удержания жидкости и клеток составляло приблизительно 29-31 час.
В качестве исходной среды использовали описанную далее среду.
Культура находилась в биореакторе до достижения высокопродуктивного стабильного состояния. Высокопродуктивное стабильное состояние было определено как плотность клеток ~2,5-3 г/л, концентрация этанола >20 г/л, поглощение CO >3,0 ммоль/мин и поглощение водорода >0,5 ммоль/мин. В процессе достижения высокопродуктивного стабильного состояния концентрация CaCl2⋅2H2O была доведена до нуля, концентрация аммония была снижена до 546 частей на миллион.
После достижения культурой высокопродуктивного стабильного состояния из препарата среды были исключены источники B, Mn и Cu. Непосредственно перед исключением этих компонентов культура имела следующие параметры/продуктивность:
плотность клеток - 2,9 г/л
конверсия CO - 86%
конверсия H2 - 32%
поглощение CO - 3,0 ммоль/мин
поглощение H2 - 0,54 ммоль/мин
концентрация этанола - 21,8 г/л
полная концентрация ацетила - 2,7 г/л
концентрация бутанола - 0,35 г/л.
Затем осуществили мониторинг параметров культуры с целью обнаружения неблагоприятного влияния на поглощение газа, H2 и CO, концентрацию продуктов и плотность клеток. Если исключение B, Cu и Mn не повлияло на эти параметры по истечении многократного (>3) времени удержания клеток, считалось, что они не являются необходимыми для культуры.
По истечении ~5,7-кратного времени удержания клеток (170 часов) концентрация бора, меди и марганца в культуральной жидкости упала до ~0,41% начальных концентраций (до 0,0043 части на миллион B, 0,0006 части на миллион Cu и 0,0068 части на миллион Mn от 1,05 части на миллион B, 0,149 части на миллион Cu и 1,67 части на миллион Mn). Определили расчетные остаточные концентрации компонентов в жидкости путем расчета вымывания с учетом исходной концентрации кальция, MFR, LRT и любых добавлений этих компонентов в биореактор в составе среды или путем инъекций. Неблагоприятное влияние на продуктивность среды отсутствовало.
Через 170 часов без добавления бора, меди и марганца культура имела следующие параметры/продуктивность:
плотность клеток - 2,9 г/л
конверсия CO - 86%
конверсия H2 - 36%
поглощение CO - 3,0 ммоль/мин
поглощение H2 - 0,61 ммоль/мин
концентрация этанола - 21,0 т/л
полная концентрация ацетила - 2,9 г/л
концентрация бутанола - 0,32 г/л.
Пример 2
Ферментация с ограничением концентрации кобальта
Были проведены эксперименты в биореакторе (New Brunswick BioFlo I или IIc), который использовался как прямоточный CSTR без очистки пермеата. Использовали следующие условия эксплуатации биореактора:
тип культуры: Clostridium ljungdahlii С01,
поддерживаемая температура культуры: 37-39°С,
скорость перемешивания: 850 об/мин на аналоговом индикаторе (фактическая скорость перемешивания составляла 931 об/мин согласно калибровочной кривой счетчика числа оборотов),
объем невыросшей культуры: ~1600-1650 мл,
объем выросшей культуры: ~1950 мл.
Установили значение pH культуры 4,5. Использовали 7,7% раствор NaHCO3 для регулирования pH.
В качестве газа использовали синтезированную смесь 15% H2, 45% N2, 30% СО и 10% СО2, которую подавали в культуру со скоростью 286 мл/мин.
Скорость подачи среды в реактор составляла от ~0,83 до ~0,86 мл/мин или ~1220 мл/сутки.
Время удержания жидкости и клеток составляло приблизительно 31-33 часа.
В качестве исходной среды, использовали описанную далее среду.
Использованная среда описана далее.
Культура находилась в биореакторе до достижения высокопродуктивного стабильного состояния. Высокопродуктивное стабильное состояние было определено как плотность клеток ~2,5-3 г/л, концентрация этанола >20 г/л, поглощение CO >3,0 ммоль/мин и поглощение водорода >0,5 ммоль/мин.
Затем осуществили мониторинг параметров культуры с целью обнаружения неблагоприятного влияния на поглощение газа, Н2 и CO, концентрацию продуктов и плотность клеток. Если снижение концентрации компонента не влияло на эти параметры по истечении многократного (>3) времени удержания клеток, концентрацию продолжали снижать. Если после снижения концентрации компонента происходило ухудшение параметров культуры, концентрацию снова доводили до предыдущего отвечающего требованиям уровня. Если культура восстанавливалась, концентрацию снова снижали иногда до такого же уровня, как и ранее, чтобы повторить полученный результат, а иногда до уровня между приемлемым и неприемлемым уровнями.
В начале эксперимента концентрация кобальта находилась на нормальном среднем уровне и составляла 0,991 части на миллион. Культура имела следующие стабильные параметры: плотность клеток ~3 г/л; концентрацию этанола 22-26 г/л; концентрацию ацетила 2,7-3,7 г/л; поглощение CO 3,1 ммоль/мин; и поглощение H2 0,5-0,7 ммоль/мин. Удалили кобальт из среды в момент t=0 часов. По мере вымывания кобальта из ферментера произошло лишь незначительное уменьшение поглощения СО с 3,1 до 2,9 ммоль/мин. Все остальные параметры оставались более или менее стабильными до момента t=121 час. В этот момент поглощение Н2 и СО уменьшилось до 0,16 и 2,6 ммоль/мин, соответственно. В этот момент также быстро снизилась полная концентрация ацетила до 0,77 г/л, что указывало на то, что концентрация кобальта упала до предельного уровня или ниже. Как показали расчеты вымывания кобальта, к тому моменту, когда параметры культуры стали изменяться вследствие низкой концентрации кобальта в реакторе, она упала до 0,0222 части на миллион или 2,24% первоначальной концентрации. Добавили в реактор кобальт, чтобы довести его концентрацию лишь до 23,3% нормального уровня или до 0,231 части на миллион. Был получен немедленный результат, выразившийся в увеличении поглощения СО, поглощения H2 и повышении концентрации кислоты. После этого в среду больше не добавляли кобальт, чтобы концентрация кобальта в реакторе еще раз снизилась до предельного уровня. Как и ранее, признаков ухудшения параметров культуры не наблюдалось, пока концентрация кобальта не упала ниже 0,0220 части на миллион. В момент t=210 часов поглощение H2 и СО, а также концентрация кислоты снова упала, что явилось результатом снижения концентрации кобальта. После этого в реактор и среду снова добавили кобальт, чтобы довести его концентрацию до 20% (0,198 части на миллион) в среде и до 21,2% (0,21 части на миллион) в реакторе. Как и ранее, результатом стало немедленное увеличение как поглощения газов, так и концентрации кислоты.
В результате двукратного вымывания кобальта из реактора до появления признаков ухудшения параметров культуры определили, что предельная концентрация кобальта в культуре составляет ~0,022 части на миллион. При концентрации кобальта 0,023 части на миллион культура являлась продуктивной без ухудшения параметров. На основании этой концентрации кобальта определили следующие расчетные параметры, использованные для улучшения корреляции добавления питательных элементов и продуктивности культуры: количество добавляемого кобальта составляло 0,005 мг на ммоль поглощаемого газа и ~9 мкг на грамм образовавшихся клеток. Восстановление после ограничения концентрации кобальта являлось быстрым и не сопровождалось длительными неблагоприятными эффектами. Культуре не наносился необратимый ущерб, если концентрацию кобальта повышали до того, как параметры ухудшались до такой степени, что возникали вторичные проблемы, т.е. токсичность газов или отсутствие кислоты.
Падение концентрации кобальта все же вызывало падение концентрации клеток. Отсутствовала явная корреляция между ограничением концентрации кобальта и синтезом бутанола. Ограничение концентрации кобальта оказывало влияние на конверсию/поглощение СО и H2, которое оставалось в пределах от незначительного до незаметного, пока концентрация кобальта в культуре не упала до ~0,022 части на миллион или ниже. Отсутствовало постепенное уменьшение конверсии газа. Тем не менее, после того, как концентрация кобальта упала ниже предельного уровня, конверсия СО и H2 очень быстро уменьшилась. После начала уменьшения конверсии СО и H2 концентрация кобальта в культуре уже находилась ниже критического уровня, и для восстановления культуры требовалось быстрое добавление кобальта. Более ранним признаком снижения концентрации кобальта являлся сдвиг от кислоты к этанолу в соотношении продуктов. Концентрация кислоты начинала падать, а концентрация этанола начинала расти даже до обнаружения уменьшения конверсии газов.
Пример 3
Ферментация с ограничением концентрации никеля
Были проведены эксперименты в биореакторе (New Brunswick BioFlo I или IIc), который использовался как прямоточный CSTR без очистки пермеата. Использовали следующие условия эксплуатации биореактора:
тип культуры: Clostridium ljungdahlii С01,
поддерживаемая температура культуры: 37-39°С,
скорость перемешивания: 700 об/мин на аналоговом индикаторе,
объем невыросшей культуры: ~1500-1650 мл,
объем выросшей культуры: ~1900 мл.
Установили значение pH культуры 4,5. Использовали 7,7% раствор NaHCO3 для регулирования pH.
В качестве газа использовали синтезированную смесь 15% Н2, 45% N2, 30% СО и 10% СО2, которую подавали в культуру со скоростью 290 мл/мин.
Скорость подачи среды в реактор составляла от ~0,86 до ~0,88 мл/мин или ~1250 мл/сутки.
Время удержания жидкости и клеток составляло приблизительно 27-31 час.
Использованная среда описана далее.
Культура находилась в биореакторе до достижения высокопродуктивного стабильного состояния. Высокопродуктивное стабильное состояние было определено как плотность клеток ~2,5-3 г/л, концентрация этанола >20 г/л, поглощение СО >3,0 ммоль/мин и поглощение водорода >0,5 ммоль/мин.
Затем осуществили мониторинг параметров культуры с целью обнаружения неблагоприятного влияния на поглощение газа, Н2 и CO, концентрацию продуктов и плотность клеток. Если снижение концентрации компонента не влияло на эти параметры по истечении многократного (>3) времени удержания клеток, концентрацию продолжали снижать. Если после снижения концентрации компонента происходило ухудшение параметров культуры, концентрацию снова доводили до предыдущего отвечающего требованиям уровня. Если культура восстанавливалась, концентрацию снова снижали иногда до такого же уровня, как и ранее, чтобы повторить полученный результат, а иногда до уровня между приемлемым и неприемлемым уровнями.
В начале этого эксперимента концентрация никеля в реакторе упала до 56% первоначальной концентрации никеля или до 0,11 части на миллион. Определили концентрацию никеля путем расчета вымывания с учетом концентрации никеля в среде, добавления никеля в среду и/или реактор и потоков жидкости через систему с целью вычисления изменения концентрации никеля в реакторе с течением времени. По мере продолжения вымывания никеля из реактора параметры культуры не изменялись. Плотность клеток оставалась ~2,8 г/л; поглощение СО составляло ~3,2 ммоль/мин; поглощение H2 составляло ~0,7 ммоль/мин; концентрация этанола составляла 24 г/л; а полная концентрация ацетила составляла ~2,5 г/л. Тем не менее, примерно в момент t=107 часов морфология клеток начала ухудшаться. Доля длинных клеток выросла с ~5% до 5-10%, и увеличивалась их длина. Теперь наблюдалась определенная деформация длинных клеток. Также увеличивалась общая длина клеток средней длины, но лишь с легкой деформацией или без деформации. Концентрация никеля в реакторе упала до 0,0996 части на миллион примерно в момент начала ухудшения морфологии клеток. К моменту t=~160 часов концентрация никеля в реакторе снизилась до 50% или до 0,0988 части на миллион. Как и ранее, параметры культуры значительно не изменились. Тем не менее, морфология клеток ухудшилась при наблюдении примерно в момент t=250 часов. Доля длинных клеток выросла до 10-20%, как и степень искривления или деформации этих длинных клеток. Остальные клетки культуры имели длину от средней до немного увеличенной с редким легким искривлением. Отсутствовали сильно искривленные клетки, такие как спиральные клетки, но наблюдалось несколько зернистых клеток и полых клеток. И в этом случае не изменились параметры культуры или концентрация никеля.
Концентрация никеля в реакторе оставалась на уровне 50% или 0,0988 части на миллион до момента t=1885 часов. При расходе среды ~0,87 мл/мин скорость подачи никеля составляла 0,12 мг/сутки. Параметры культуры оставались достаточно постоянными: плотность клеток ~2,8 г/л, поглощение СО ~3,2 ммоль/мин, поглощение Н2 ~0,7 ммоль/мин, концентрация этанола ~25 г/л, полная концентрация ацетила ~2,5 г/л, и концентрация бутанола ~0,3 г/л. При 50% скорости подачи никеля его добавляли в количестве ~34 мкг на грамм образовавшихся клеток или ~0,022 мкг на ммоль поглощаемого газа. Морфология клеток прекратила ухудшаться, когда концентрация никеля достигла 0,0988 части на миллион. В культуре оставалось ~10% длинных клеток с легкой деформацией, ~5% очень длинных клеток с умеренной деформацией, а остальные клетки имели длину от средней до немного увеличенной с редкой деформацией.
В момент t=445 часов концентрация никеля была снижена до 25% первоначальной концентрации или до 0,049 части на миллион. Почти немедленно началось медленное, но устойчивое изменение параметров культуры. Поглощение СО оставалось постоянным и соста