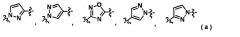Гетероароматическое метильное производное циклического амина
Иллюстрации
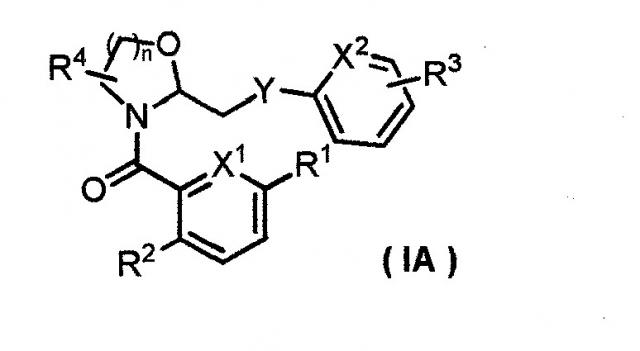
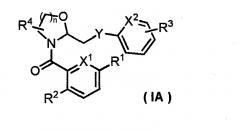
Показать всеИзобретение относится к соединению, представленному формулой (IA), где X1 и X2 являются одинаковыми или разными и означают атом азота или группу СН; Y означает любую структуру из следующей группы формул (а); n означает 1 или 2; R1 означает атом водорода, атом галогена или C1-6 алкильную группу; R2 означает триазолильную группу или пиримидинильную группу; R3 означает атом водорода или атом галогена; и R4 означает атом водорода или C1-6 алкильную группу; или его фармацевтически приемлемой соли. Также изобретение относится к соединению, представленному формулой (I), где X1 и X2 являются одинаковыми или разными и означают атом азота или группу СН; любой один из Y1 и Y2 означает атом азота, а другой означает СН; n означает 1 или 2; R1 означает атом водорода, атом галогена или C1-6 алкильную группу; R2 означает триазолильную группу или пиримидинильную группу; R3 означает атом водорода или атом галогена; и R4 означает атом водорода или C1-6 алкильную группу; или его фармацевтически приемлемой соли. Соединения по изобретению предназначены для изготовления фармацевтической композиции, обладающей антагонистической активностью в отношении рецепторов орексина OX1 и OX2. Технический результат – гетероароматическое метильное производное циклического амина, обладающее антагонистической активностью в отношении рецепторов орексина OX1 и OX2. 4 н. и 5 з.п. ф-лы, 6 табл., 85 пр.
,
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к соединению, обладающему антагонистической активностью в отношении рецепторов орексина (OX), и его фармацевтически приемлемой соли, а также к лекарственному средству для лечения или профилактики таких заболеваний, как нарушение сна, депрессия, тревожное расстройство, паническое расстройство, шизофрения, лекарственная зависимость, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, расстройство пищевого поведения, головная боль, мигрень, боль, желудочно-кишечные заболевания, эпилепсия, воспаление, болезни иммунной системы, эндокринные заболевания или гипертония, включающему такое соединение или его соль в качестве активного ингредиента.
Уровень техники
Орексин является нейропептидом, сплайсированным из препроорексина, который специфически экспрессируется в латеральной гипоталамической области. К настоящему времени были идентифицированы OX-A, состоящий из 33 аминокислот, и OX-B, состоящий из 28 аминокислот, которые оба вовлечены в регуляцию режима сна-бодствования и в регуляцию питания.
Как OX-A, так и OX-B действуют на рецепторы OX. К настоящему времени было клонировано два подтипа рецепторов OX, OX1 и OX2, которые оба, как известно, представляют собой содержащие семь трансмембранных спиралей рецепторы, сопряженные с G белком, экспрессируемые в основном в головном мозге. Рецептор OX1 специфически сопряжен с Gq из подклассов белка G, тогда как рецептор OX2 сопряжен с Gq и Gi/o (см. непатентный документ 1 и непатентный документ 2). Подтипы рецептора OX селективно экспрессируются в головном мозге, и рецептор OX1 экспрессируется с высокой плотностью в locus coeruleus (голубом пятне), являющихся начальными ядрами (nuclei originis) норадренергических нейронов, тогда как рецептор OX2 экспрессируется с высокой плотностью в туберомамиллярном ядре, являющемся начальными ядрами гистаминергических нейронов (см. непатентные документы 3, 4 и 5). Экспрессия обоих рецепторов, OX1 и OX2, была обнаружена в ядре шва, являющемся начальными ядрами серотонинэргических нейронов, и в вентральной области покрышки, являющейся начальными ядрами допаминергических нейронов (см. непатентный документ 3). Орексинсодержащие нейроны проецируются в моноаминергическую нейронную систему у мозгового ствола и гипоталамуса и оказывают возбуждающие эффекты на эти нейроны, кроме того, экспрессия рецептора OX2 была обнаружена также в холинергических нейронах стволовой части мозга, ответственных за регуляцию быстрого сна, и оказывает воздействие на их ядерную активность (см. непатентный документ 3 и непатентный документ 4).
В последние годы исследование рецепторов OX1 и OX2 было сфокусировано на их роли в регуляции сна и бодрствования и изучалась полезность антагонистов рецепторов OX. Когда OX-A вводили крысам интрацереброваскулярно, наблюдалась повышенная спонтанная двигательная активность (см. непатентный документ 6 и непатентный документ 7), усиленное стереотипное поведение (см. непатентный документ 7), увеличение времени, затраченного на пробуждение (см. непатентный документ 6) и т.д. Снижению продолжительности быстрого сна (REM), вызванному введением OX-A, полностью противодействовала предварительная обработка антагонистом рецептора OX (см. непатентный документ 8). Кроме того, сообщалось, что в результате введения перорально доступного антагониста рецепторов OX1 и OX2 снижается двигательная активность, укорачивается латентный период сна и увеличивается продолжительность периода небыстрого сна и быстрого сна (см. непатентные документы 9 и 10). Патентный документ 1 раскрывает гетероароматическое циклическое производное в качестве соединения, обладающего антагонистической активностью в отношении рецепторов OX, но не описывает соединения, имеющего скелет гетероароматического циклического метиламина, какой описан в настоящей заявке. Аналогично, соединения, например, имеющие различные структуры, описанные в непатентном документе 11, общеизвестны как антагонисты рецептора OX, но описываемые в настоящей заявке соединения, имеющие скелет гетероароматического циклического метиламина, не были описаны.
Список цитирования
Патентная литература
Патентный документ 1: WO 2003/002559
Непатентная литература
Непатентный документ 1: Zhu Y et al., J. Pharmacol. Sci., 92, 259-266, 2003.
Непатентный документ 2: Zeitzer JM et al., Trends Pharmacol. Sci., 27, 368-374, 2006.
Непатентный документ 3: Marcus JN et al., J. Comp. Neurol, 435, 6-25, 2001.
Непатентный документ 4: Trivedi JP et al., FEES Lett, 438, 71-75,1998.
Непатентный документ 5: Yamanaka Aet al., Biochem. Biophys. Res. Commun., 290, 1237-1245, 2002.
Непатентный документ 6: Hagan JJ et al., Proc. Natl. Acad. Sci. USA, 96, 10911-10916, 1999.
Непатентный документ 7: Nakamura T et al., Brain Res., 873, 181-187, 2000.
Непатентный документ 8: Smith MI et al., Neurosci. Lett., 341, 256-258, 2003.
Непатентный документ 9: Brisbare-Roch C et al., Nat. Med., 13, 150-155, 2007.
Непатентный документ 10: Cox CD et al., J. Med. Chem., 53, 5320-5332, 2010.
Непатентный документ 11: John G et al., ChemMedChem., 5, 1197-1214, 2010.
Сущность изобретения
Техническая проблема
Одной целью настоящего изобретения является поиск нового соединения, обладающего антагонистической активностью в отношении рецепторов OX, и обеспечение лекарственного средства для лечения или профилактики таких заболеваний, как нарушение сна, депрессия, тревожное расстройство, паническое расстройство, шизофрения, лекарственная зависимость, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, расстройство пищевого поведения, головная боль, мигрень, боль, желудочно-кишечные болезни, эпилепсия, воспаление, болезни иммунной системы, эндокринные заболевания или гипертония. Более конкретно, целью настоящего изобретения является обеспечение нового соединения, проявляющего хорошие фармакокинетические свойства и безопасность в сочетании с хорошей антагонистической активностью в отношении рецепторов OX.
Решение проблемы
Авторы настоящего изобретения широко исследовали новые скелетные соединения, обладающие антагонистической активностью в отношении рецепторов орексина, и нашли, что некоторые гетероароматические метильные производные циклического амина, представленные следующими формулами, обладают хорошей антагонистической активностью в отношении рецепторов OX, в соответствии с чем настоящее изобретение было завершено.
Ниже настоящее изобретение описывается подробно. Объекты настоящего изобретения (называемые далее "соединением по настоящему изобретению") следующие.
(1) Соединение, представленное формулой (IA):
Формула I
,
где
X1 и X2 являются одинаковыми или разными и означают атом азота или группу CH;
Y означает любую структуру из следующей группы формул (a):
Формула 2
n означает 1 или 2;
R1 означает атом водорода, атом галогена или C1-6 алкильную группу;
R2 означает триазолильную группу, пиридильную группу или пиримидинильную группу;
R3 означает атом водорода, атом галогена или C1-6 алкильную группу, где C1-6 алкильная группа необязательно может быть замещена 1-3 атомами галогена; и
R4 означает атом водорода или C1-6 алкильную группу;
или его фармацевтически приемлемая соль.
(2) Соединение или его фармацевтически приемлемая соль согласно (1), где в вышеуказанной формуле (IA):
R2 является триазолильной группой или пиримидинильной группой, и
R3 является атомом галогена.
(3) Соединение или его фармацевтически приемлемая соль согласно (1) или (2), где в вышеуказанной формуле (IA) n равно 2.
(4) Соединение, представленное формулой (I):
Формула 3
,
где
X1 и X2 являются одинаковыми или разными и означают атом азота или группу CH;
любой один из Y1 и Y2 означает атом азота, а другой означает CH;
n означает 1 или 2;
R1 означает атом водорода, атом галогена или C1-6 алкильную группу;
R2 означает триазолильную группу, пиридильную группу или пиримидинильную группу;
R3 означает атом водорода, атом галогена или C1-6 алкильную группу, где C1-6 алкильная группа необязательно может быть замещена 1-3 атомами галогена;
и
R4 означает атом водорода или C1-6 алкильную группу;
или его фармацевтически приемлемая соль.
(5) Соединение или его фармацевтически приемлемая соль согласно (4), где в вышеуказанной формуле (I):
R2 является триазолильной группой или пиримидинильной группой, и
R3 является атомом галогена.
(6) Соединение или его фармацевтически приемлемая соль согласно (4) или (5), где в вышеуказанной формуле (I) n равно 2.
(7) Соединение или его фармацевтически приемлемая соль согласно (1), представляющее собой соединение или смесь двух или более или соединений, выбранных из следующих:
(-)-(2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазолидин-3-ил)[5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-(2-{[4-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазолидин-3-ил)[5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-(2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил)[5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-(2-{[4-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил)[5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[(2S,5S)-2-{[4-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-5-метил-1,3-оксазолидин-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[(2S,5R)-2-{[4-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-5-метил-1,3-оксазолидин-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
[(2S,4R)-2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-4-метил-1,3-оксазолидин-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[(2S,4S)-2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-4-метил-1,3-оксазолидин-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(±)-2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазолидин-3-ил][5-метил-2-(пиримидин-2-ил)фенил]метанон,
(±)-(2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазолидин-3-ил)[5-фтор-2-(пиримидин-2-ил)фенил]метанон,
(±)-(2-{[3-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазолидин-3-ил)[5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(±)-(2-{[4-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазолидин-3-ил)[5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(±)-(2-{[4-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазолидин-3-ил)[5-метил-2-(пиримидин-2-ил)фенил]метанон,
(-)-(2-{[3-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазолидин-3-ил)[6-метил-3-(2H-1,2,3-триазол-2-ил)пиридин-2-ил]метанон,
(-)-(2-{[3-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил)[6-метил-3-(2H-1,2,3-триазол-2-ил)пиридин-2-ил]метанон,
(-)-(2-{[3-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил)[6-метил-3-(пиримидин-2-ил)пиридин-2-ил]метанон,
(-)-(2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил)[5-фтор-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-(2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил)[5-метил-2-(пиримидин-2-ил)фенил]метанон,
(-)-(2-{[4-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил)[6-метил-3-(2H-1,2,3-триазол-2-ил)пиридин-2-ил]метанон,
(-)-(2-{[4-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил)[6-метил-3-(пиримидин-2-ил)пиридин-2-ил]метанон,
(-)-[2-{[3-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил][5-фтор-2-(пиримидин-2-ил)фенил]метанон,
(-)-[2-{[4-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[2-{[5-(5-фторпиридин-2-ил)-1,2,4-оксадиазол-3-ил]метил}-1,3-оксазинан-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[2-{[5-(4-фторфенил)-1,2,4-оксадиазол-3-ил]метил}-1,3-оксазинан-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[2-{[5-(4-фторфенил)-1,2,4-оксадиазол-3-ил]метил}-1,3-оксазинан-3-ил][6-метил-3-(2H-1,2,3-триазол-2-ил)пиридин-2-ил]метанон,
[(2S,4S)-2-{[4-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-4-метил-1,3-оксазинан-3-ил}[5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[(2S*,5S*)-2-{[4-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-5-метил-1,3-оксазинан-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[2-{[3-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил][5-метил-2-(пиримидин-2-ил)фенил]метанон,
(±)-[2-{[1-(5-фторпиридин-2-ил)-1H-пиразол-4-ил]метил}-1,3-оксазинан-3-ил][5-метил-2-(пиримидин-2-ил)фенил]метанон,
(-)-[2-{[4-(4-фторфенил)-1H-пиразол-1-ил]метил}-1,3-оксазинан-3-ил][5-метил-2-(пиримидин-2-ил)фенил]метанон,
(-)-[2-{[1-(5-фторпиридин-2-ил)-1H-пиразол-4-ил]метил}-1,3-оксазинан-3-ил][5-фтор-2-(пиримидин-2-ил)фенил]метанон,
(-)-[2-{[1-(5-фторпиридин-2-ил)-1H-пиразол-3-ил]метил}-1,3-оксазолидин-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[2-{[1-(5-фторпиридин-2-ил)-1H-пиразол-4-ил]метил}-1,3-оксазолидин-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон,
(-)-[2-{[1-(5-фторпиридин-2-ил)-1H-пиразол-4-ил]метил}-1,3-оксазинан-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон, и
(-)-[(2S*,5R*)-2-{[4-(5-фторпиридин-2-ил)-1H-пиразол-1-ил]метил}-5-метил-1,3-оксазинан-3-ил][5-метил-2-(2H-1,2,3-триазол-2-ил)фенил]метанон.
(8) Фармацевтическая композиция, содержащая в качестве активного ингредиента соединение или его фармацевтически приемлемую соль согласно любому из вышеуказанных пунктов (1)-(7).
(9) Лекарственное средство для лечения или профилактики таких заболеваний, как нарушение сна, депрессия, тревожное расстройство, паническое расстройство, шизофрения, лекарственная зависимость, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, расстройство пищевого поведения, головная боль, мигрень, боль, желудочно-кишечные болезни, эпилепсия, воспаление, болезни иммунной системы, эндокринные заболевания или гипертония, содержащее в качестве активного ингредиента соединение или его фармацевтически приемлемую соль согласно любому из вышеуказанных пунктов (1)-(7).
Выгодные эффекты изобретения
Обнаружено, что гетероароматическое метильное производное циклического амина согласно настоящему изобретению имеет сродство в отношении рецепторов OX и обладает антагонистической активностью в отношении стимуляции рецепторов физиологическим лигандом.
Описание вариантов осуществления
Термины, используемые в настоящем описании, означают следующее.
"Атом галогена" относится к атому фтора, атому хлора, атому брома и атому иода.
"C1-6 алкильная группа" означает алкильную группу с линейной или разветвленной цепью, содержащую от 1 до 6 атомов углерода, примеры включают такие группы, как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, трет-пентил, 1-этилпропил, н-гексил, изогексил и неогексил.
Термин "нарушение сна", используемый в настоящем описании, относится к расстройствам при нарушении засыпания, сна, фаз сна или пробуждения, включая бессонницу.
Далее, классификация бессонницы включает нарушение засыпания, активацию во время сна, пробуждение ранним утром и расстройства глубокого сна.
Термин "фармацевтически приемлемая соль", используемый в настоящем описании, означает фармацевтически приемлемую кислотно-аддитивную соль, и примеры подходящих для применения кислот включают соли с неорганической кислотой, такой как серная кислота, соляная кислота, бромистоводородная кислота, фосфорная кислота и азотная кислота; и соли с органической кислой, такой как уксусная кислота, бензойная кислота, щавелевая кислота, молочная кислота, яблочная кислота, винная кислота, фумаровая кислота, малеиновая кислота, лимонная кислота, малоновая кислота, миндальная кислота, глюконовая кислота, галактаровая кислота, глюкогептоновая кислота, гликолевая кислота, глутаминовая кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, камфорсульфоновая кислота и нафталин-2-сульфоновая кислота. Превращение из свободного соединения в вышеуказанную соль можно осуществить обычным способом.
Ниже описаны предпочтительные варианты осуществления соединений по настоящему изобретению.
Предпочтительны соединения, в которых R1 является атомом галогена или C1-6 алкильной группой, причем более предпочтительными являются соединения, в которых R1 является атомом фтора или метильной группой, и еще более предпочтительны соединения, в которых R1 является метильной группой.
Предпочтительны соединения, в которых R2 означает триазолильную группу или пиримидинильную группу, причем более предпочтительны соединения, в которых R2 означает 1,2,3-триазол-2-ильную группу или пиримидин-2-ильную группу.
Предпочтительны соединения, в которых R3 является атомом галогена, причем более предпочтительны те, в которых R3 означает атом фтора или атом хлора, и еще более предпочтительны соединения, в которых R3 означает атом фтора.
Предпочтительны соединения, в которых R4 является атомом водорода или метильной группой.
Предпочтительны соединения, в которых n равно 2.
Кроме того, когда соединение по настоящему изобретению образует гидрат или сольват, они также включены в объем настоящего изобретения. Аналогично, фармацевтически приемлемые соли гидратов или сольватов соединения по настоящему изобретению также включены в объем настоящего изобретения.
Соединение по настоящему изобретению охватывает все энантиомеры, диастереомеры, равновесные соединения, их смеси в любом отношении, рацемические соединения и т.п.
Соединение согласно настоящему изобретению включает также соединения, в которых по меньшей мере один атом водорода, атом углерода, атом азота, атом кислорода и атом галогена замещен радиоактивным изотопом или стабильным изотопом. Эти меченые соединения полезны для изучения метаболизма и фармакокинетики и для биологического анализа или т.п. в качестве лиганда рецептора или т.п.
Соединения согласно настоящему изобретению можно вводить перорально или парентерально. Их лекарственная форма может представлять собой таблетки, капсулы, гранулы, порошки, пылевидные препараты, пастилки, мази, кремы, пластыри, эмульсии, суспензии, суппозитории, препараты для инъекций или т.п., любой из которых может быть получен рутинной фармацевтической методикой приготовления (например, способы, описанные в 15-ом издании Японской Фармакопеи, или т.п.). Эти лекарственные формы могут быть надлежащим образом выбраны в соответствии с симптомами пациента, возрастом, весом тела и целью лечения.
Эти фармацевтические препараты могут быть получены путем добавления фармакологически приемлемых носителей, более конкретно, эксципиентов (например, кристаллическая целлюлоза, крахмал, лактоза, маннит), связующих (например, гидроксипропилцеллюлоза, поливинилпирролидон), смазок (например, стеарат магния, тальк), разрыхлителей (например, кальций-карбоксиметилцеллюлоза) и различных других фармакологически приемлемых добавок, к композиции, содержащей соединение по настоящему изобретению.
Соединение по настоящему изобретению можно вводить перорально или парентерально взрослому пациенту в единичной дозе от 0,001 до 500 мг один раз в день или разделенной на несколько приемов в день. Кроме того, дозировку можно подходящим образом увеличивать или уменьшать в зависимости типа заболевания, которое лечат, возраста пациента, веса тела, симптомов и т.п.
Ниже на схемах A и B показаны типичные способы получения соединения (I) по настоящему изобретению.
Следующие способы являются примерами способа получения соединений по настоящему изобретению, и настоящее изобретение ими не ограничено. Кроме того, в следующих примерах способа получения соединения могут образовывать соль, если не модифицировать реакцию.
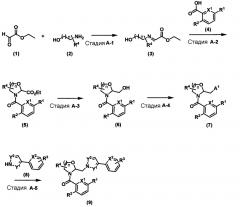
Схема A
Формула 4
где X1, X2, Y1, Y2, R1, R2, R3 и R4 определены выше. A1 означает атом галогена, метансульфонилоксигруппу, п-толуолсульфонилоксигруппу или трифторметансульфонилоксигруппу, n равно 1 или 2.
Стадия A-1: Соединение (3) может быть получено реакцией конденсации этилглиоксилата (1) и аминового соединения (2). Реакция на стадии A-1 может быть проведена в условиях, в которых основание реагирует с аминовым соединением или его гидрохлоридом в присутствии или в отсутствие дегидратирующего реагента, такого как молекулярное сито или безводный сульфат меди, в растворителе. Примеры оснований для применения в настоящей реакции включают органические амины, такие как пиридин, триэтиламин и диизопропилэтиламин, неорганические основания, такие как гидроксид натрия, гидроксид калия и гидрокарбонат натрия, и ацетат, такой как ацетат натрия и ацетат калия. Примеры растворителя для применения в настоящей реакции включают простые эфирные растворители, такие как тетрагидрофуран и 1,4-диоксан, апротонные полярные растворители, такие как N,N-диметилформамид и ацетонитрил, галогенсодержащие растворители, такие как дихлорметан и хлороформ, ароматические углеводородные растворители, такие как толуол, этилацетат, и смеси этих растворителей. Указанная реакция может быть проведена при температуре от 0°C до 100°C.
Стадия A-2: Соединение (5) может быть получено реакцией конденсации соединения (3) и карбоновой кислоты (4). Реакция на стадии A-2 может быть проведена обычным способом амидирования карбоновой кислоты. Примеры включают способ, в котором карбоновую кислоту превращают в галогенангидрид карбоновой кислоты, такой как хлорангидрид карбоновой кислоты или бромангидрид карбоновой кислоты, и затем приводят в реакцию с соединением (3), и способом, в котором карбоновую кислоту приводят в реакцию с соединением (3) в присутствии дегидратирующей конденсирующей добавки. Все эти реакции можно проводить в присутствии или в отсутствие основания в растворителе. Примеры галогенирующего агента для применения в настоящей реакции могут включать тионилхлорид, оксалихлорид, оксихлорид фосфора или оксибромид фосфора. Равным образом, примеры подходящей для применения в настоящей реакции дегидратирующей конденсирующей добавки включают 1-этил-3-(3-диметиламинопропил)карбодиимид-гидрохлорид (EDC-HC1), [O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат] (HATU), ангидрид пропанфосфорной кислоты, дициклогексилкарбодиимид (DDC), дифенилфосфорилазид (DPPA) и карбонилдиимидазол (CDI), при необходимости можно использовать активатор, такой как 1-гидроксибензотриазол или гидроксисукцинимид. Примеры растворителя для применения в настоящей реакции включают эфирные растворители, такие как тетрагидрофуран и 1,4-диоксан, апротонные полярные растворители, такие как N,N-диметилформамид и ацетонитрил, галогенсодержащие растворители, такие как дихлорметан и хлороформ, ароматические углеводородные растворители, такие как толуол, этилацетат или смеси этих растворителей. Примеры оснований для применения в настоящей реакции включают органические амины, такие как пиридин, триэтиламин и диизопропилэтиламин, и неорганические основания, такие как карбонат калия, карбонат натрия и гидрокарбонат натрия. Вышеуказанная реакция обычно может быть проведена при температуре от 0°C до 150°C, предпочтительно от 0°C до 80°C.
Стадия A-3: Соединение (6) может быть получено реакцией восстановления сложного эфира соединения (5). Реакция на стадии A-3 может быть проведена в условиях, в которых соединение (5) реагирует с восстановителем, таким как гидрид лития-алюминия, гидрид диизобутилалюминия, борогидрид натрия или борогидрид лития, в спиртовом растворителе, таком как метанол или этанол, эфирном растворителе, таком как тетрагидрофуран или 1,4-диоксан, ароматическом углеводородном растворителе, таком как толуол, или в смеси этих растворителей. Указанная реакция может быть проведена при температуре от -80°C до 150°C, предпочтительно от 0°C до 25°C.
Стадия A-4: Соединение (7) может быть получено путем превращения гидроксигруппы соединения (6) в обычную уходящую группу. Примеры реакции на стадии A-4 включают хлорирование, бромирование, йодирование, метансульфонилоксилирование и п-толуолсульфонилоксилирование. Один пример реакции хлорирования включает способ, в котором уходящую группу получают, используя, например, метансульфонилхлорид или т.п., с последующим замещением атомом хлора. Кроме того, подходит способ, в котором используется тетрахлоридуглерода и трифенилфосфин, и способ, в котором используется тионилхлорид или оксихлорид фосфора. Во время этих операций можно добавить хлорид, такой как хлорид натрия или хлорид калия. Пример реакции бромирования включает способ, в котором используется, например, тетрабромид углерода и трифенилфосфин. Пример реакции йодирования включает способ, в котором используется, например, йод, трифенилфосфин и имидазол. Метансульфонилоксилирование и п-толуолсульфонилоксилирование можно осуществить, используя, например, метансульфонилхлорид, п-толуолсульфонилхлорид или т.п. соответственно. Во время этих реакций можно добавить подходящее основание. Примеры основания для добавления включают органические основания, такие как триэтиламин и диизопропилэтиламин, или неорганические основания, такие как карбонат калия. Примеры реакционных растворителей включают эфирные растворители, такие как тетрагидрофуран и 1,4-диоксан, апротонные полярные растворители, такие как N,N-диметилформамид и ацетонитрил, галогенсодержащие растворители, такие как дихлорметан и хлороформ, ацетонитрил, или смеси этих растворителей, причем реакции могут быть проведены в температурных условиях от примерно -80°C до примерно точки кипения такого растворителя.
Стадия A-5: Соединение (9) может быть получено реакцией соединения (7) и соединения (8). Реакция на стадии A-5 протекает в спиртовом растворителе, таком как метанол и этанол, в эфирном растворителе, таком как тетрагидрофуран и 1,4-диоксан, апротонном полярном растворителе, таком как N,N-диметилформамид и ацетонитрил, галогенсодержащем растворителе, таком как дихлорметан и хлороформ, в диметилсульфоксиде, ацетонитриле, воде или в смеси этих растворителей, в присутствии неорганического основания, такого как гидрид натрия, гидроксид натрия, карбонат натрия, карбонат калия или карбонат цезия, щелочного металла, такого как этоксид натрия или трет-бутоксид калия, или органического основания, такого как низший алкоксид щелочно-земельного металла, в температурных условиях от примерно -80°C до примерно точки кипения такого растворителя.
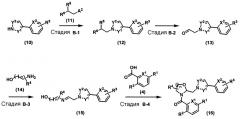
Схема B
Формула 5
где X1, X2, Y1, Y2, R1, R2, R3 и R4 определены выше. R5 и R6 означают алкоксигруппу, и A2 означает атом галогена, метансульфонилоксигруппу, п-толуолсульфонилоксигруппу или трифторметансульфонилоксигруппу.
Стадия B-1: Соединение (12) может быть получено реакцией соединения (10) и соединения (11). Реакция на стадии B-1 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-5.
Стадия B-2: Соединение (13) может быть получено из соединения (12). Реакция на стадии B-2 может быть проведена в условиях, в которых соединение (12) реагирует с кислотой, такой как соляная кислота, трифторуксусная кислота или п-толуолсульфоновая кислота, в содержащим воду спиртовом растворителе, таком как водосодержащий метанол или водосодержащий этанол, в эфирном растворителе, таком как тетрагидрофуран или 1,4-диоксан, в галогенсодержащем растворителе, таком как дихлорметан или хлороформ, кетоновом растворителе, таком как ацетон, в воде или в смеси таких растворителей. Данная реакция может быть проведена при температуре от 0°C до 80°C.
Стадия B-3: Соединение (15) может быть получено реакцией конденсации соединения (13) и соединения (14). Реакция на стадии B-3 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-1.
Стадия B-4: Соединение (16) может быть получено реакцией конденсации соединения (4) и соединения (15). Реакция на стадии B-4 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-2.
Схема C
Формула 6
где X1, X2, R1, R2, R3 и R4 определены выше. R5 и R6 означают алкоксигруппу.
Стадия C-1: Соединение (19) может быть получено реакцией амидоксимирования соединения (17). Реакция на стадии C-1 может быть проведена в условиях, в которых нитрильное соединение (17) реагирует с гидроксиламином (18) или его гидрохлоридом в спиртовом растворителе, таком как метанол или этанол. Указанная реакция может быть проведена при температуре от 0°C до 100°C.
Стадия C-2: Соединение (21) может быть получено реакцией оксадиазольной циклизации соединения (19) и соединения (20). Реакция на стадии C-2 может быть проведена в условиях, в которых соединение (19) реагирует с карбоновой кислотой (20) и дегидратирующей конденсирующей добавкой, такой как 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (EDC-HCl), дициклогексилкарбодиимид (DDC), карбонилдиимидазол (CDI), в эфирном растворителе, таком как тетрагидрофуран или 1,4-диоксан, в апротонном полярном растворителе, таком как N,N-диметилформамид, в галогенсодержащем растворителе, таком как дихлорметан или хлороформ, ароматическом углеводородном растворителе, таком как толуол, этилацетат, ацетонитрил, или в смеси таких растворителей. Указанная реакция проводится обычно при температуре от 0°C до 150°C, предпочтительно от 0°C до 90°C.
Стадия C-3: Соединение (22) может быть получено кислотным гидролизом соединения (21). Реакция на стадии C-3 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии B-2.
Стадия C-4: Соединение (23) может быть получено реакцией конденсации соединения (14) и соединения (22). Реакция на стадии C-4 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-1.
Стадия C-5: Соединение (24) может быть получено реакцией конденсации соединения (4) и соединения (23). Реакция на стадии C-5 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-2.
Схема D
Формула 7
где X1, X2, R1, R3 и R4 определены выше. R8 означает триазолильную группу, пиридильную группу или атом галогена, и A3 означает атом галогена.
Стадия D-1: Соединение (27) может быть получено нуклеофильной реакцией или реакцией сочетания соединения (25) и соединения (26). Реакция на стадии D-1 может быть проведена в соответствии с теми же условиями нуклеофильной реакции, что и на стадии A-5. Реакция сочетания может быть проведена обычным способом, в котором атом азота азольного соединения замещается ароматическим кольцом при использовании катализатора и лиганда в присутствии основания. Примеры включают способ, описанный в Synlett, 2003, 15, 2428-2439, или способ, соответствующий ему. Примеры катализатора для применения в настоящей реакции включают медный катализатор, такой как медь(0), йодид меди(I), хлорид меди(I) и оксид меди(I). Примеры лиганда для применения в настоящей реакции включают N,N'-диметилэтилендиамин, N,N'-диметилциклогексан-1,2-диамин, 2-аминопиридин, 1,10-фенантролин и 2-гидроксибензальдегидоксим. Примеры основания для применения в настоящей реакции включают карбонат калия, фосфат калия, гидроксид калия, трет-бутоксид калия, карбонат цезия, карбонат натрия, бикарбонат натрия, ацетат натрия, метоксид натрия и гидроксид тетрабутиламмония. Примеры растворителя для применения в настоящей реакции включают спиртовые растворители, такие как метанол и этанол, эфирные растворители, такие как тетрагидрофуран и 1,4-диоксан, апротонные полярные растворители, такие как N,N-диметилформамид, диметилсульфоксид и ацетонитрил, галогенсодержащие растворители, такие как дихлорметан и хлороформ, ароматические углеводородные растворители, такие как толуол, воду или смеси этих растворителей. Вышеуказанная реакция может быть проведена обычно при температуре от 0°C до 150°C, предпочтительно от 25°C до 100°C.
Стадия D-2: Соединение (28) может быть получено реакцией окисления гидроксильной группы соединения (27). Реакция на стадии D-2 может быть проведена в условиях, в которых соединение (27) реагирует с гипервалентным соединением йода, таким как реактив Десса-Мартина или 2-иодоксибензойная кислота, хроматами, такими как хлорхромат пиридиния или дихромат пиридиния, или с окислителем, таким как тетрапропиламмония перрутенат или диоксид марганца, в галогенсодержащем растворителе, таком как дихлорметан или хлороформ, или в апротонном полярном растворителе, таком как диметилсульфоксид или ацетонитрил. Вышеуказанная реакция может быть проведена при температуре от 0°C до 150°C, предпочтительно от 25°C до 80°C.
Стадия D-3: Соединение (29) может быть получено реакцией конденсации соединения (14) и соединения (28). Реакция на стадии D-3 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-1.
Стадия D-4: Соединение (31) может быть получено реакцией конденсации соединения (29) и соединения (30). Реакция на стадии D-4 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-2.
Стадия D-5: Соединение (33) может быть получено реакцией сочетания соединения (31) и соединения (32). Реакция на стадии D-5 может быть получена в условиях реакции сочетания Стилле, когда реакция проводится с использованием органического соединения олова в апротонном полярном растворителе, таком как N,N-диметилформамид, в ароматическом углеводородном растворителе, таком как толуол, или в смеси таких растворителей. Всесторонний обзор по реакции сочетания Стилле можно найти, например, в Angew. Chem. Int. Ed., 43, 4704, (2004).
Схема E
Формула 8
где X1, X2, R1, R2, R3, R4 и A3 определены выше. R7 означает обычную защитную группу карбоновой кислоты, например группы, описанные в Protective Groups in Organic Chemistry, автор J.F.W. McOmie, и Protective Groups in Organic Synthesis, авторы T.W. Greene и P.G.M. Wuts, и означает, например, C1-6 алкильную группу и бензильную группу.
Стадия E-1: Соединение (34) может быть получено нуклеофильной реакцией или реакцией сочетания соединения (26) и соединения (33). Реакция на стадии E-1 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии D-1.
Стадия E-2: Соединение (35) может быть получено реакцией восстановления сложного эфира соединения (34). Реакция на стадии E-2 может быть проведена в условиях, в которых соединение (34) реагирует с восстановителем, таким как литий-алюминий гидрид, гидрид диизобутилалюминия, борогидрид натрия или борогидрид лития, в спиртовом растворителе, таком как метанол или этанол, в эфирном растворителе, таком как тетрагидрофуран или 1,4-диоксан, в ароматическом углеводородном растворителе, таком как толуол, или в смеси таких растворителей. Вышеуказанная реакция может быть проведена при температуре от -80°C до 150°C, предпочтительно от 0°C до 25°C.
Стадия E-3: Соединение (36) может быть получено реакцией окисления гидроксильной группы соединения (35). Реакция на стадии E-3 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии D-2.
Стадия E-4: Соединение (38) может быть получено реакцией Виттига соединения (36) и соединения (37). Реакция на стадии E-4 может быть проведена в условиях, в которых метоксиметилтрифенил фосфонийхлорид обрабатывают основанием, таким как гидрид натрия, гидрид калия, трет-бутоксикалий, натрийбис(триметилсилил)амид или литийбис(триметилсилил)амид в эфирном растворителе, таком как тетрагидрофуран или 1,4-диоксан, в ароматическом углеводородном растворителе, таком как толуол, или в смеси таких растворителей с последующей реакцией с альдегидом. Вышеуказанные реакции могут быть проведены при температуре от 0°C до 120°C. Реакция может быть проведена в условиях, в которых полученный простой эфир енола гидролизуют, используя неорганическую кислоту, такую как соляная кислота, трифторуксусная кислота или п-толуолсульфоновая кислота, органическую кислоту или кислоту Льюиса, такую как ацетат ртути. Вышеуказанная реакция может быть проведена при температуре от 0°C до 80°C.
Стадия E-5: Соединение (39) может быть получено реакцией конденсации соединения (14) и соединения (38). Реакция на стадии E-5 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-1.
Стадия E-6: Соединение (40) может быть получено реакцией конденсации соединения (4) и соединения (39). Реакция на стадии E-6 может быть проведена в соответствии с теми же реакционными условиями, что и на стадии A-2.
Схема F
Формула 9