Способы и композиции для лечения астмы с использованием антител против il-13
Иллюстрации
Показать всеГруппа изобретений относится к медицине, а именно к иммунологии, и может быть использована для лечения астмы. Способ лечения астмы у индивида, являющегося человеком, включает внутривенное введение индивиду антитела против IL-13 или его антигенсвязывающей части в дозе, равной приблизительно 0,3 мг/кг. Антитело против IL-13 или его антигенсвязывающая часть содержат вариабельную область тяжелой цепи SEQ ID NO: 2 и вариабельную область легкой цепи SEQ ID NO: 3, где по меньшей мере одна фармакокинетическая характеристика, выбранная из группы, состоящей из: (a) максимальной сывороточной концентрации (Смакс), равной от приблизительно 55 до приблизительно 90 мкг/мл, и (b) площади под кривой концентрация-время для сыворотки (AUC), равной от приблизительно 20000 до приблизительно 34000 мкгч/мл, достигается после введения антитела или его антигенсвязывающей части указанному индивиду. Группа изобретений относится также к вариантам способа лечения бронхиальной астмы от легкой до умеренной формы. Использование данной группы изобретений позволяет подобрать оптимальную дозировку и схему введения вышеуказанного антитела в дозировке 0,3 мг/кг и 3 мг/кг с получением определенных фармакокинетических характеристик. 4 н. и 5 з.п. ф-лы, 4 пр., 7 табл., 12 ил.
Реферат
РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет предварительной заявки США № 61/507347, поданной 13 июля 2011 г., содержание которой включено в настоящий документ в качестве ссылки в полном объеме.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Астма является хроническим воспалительным заболеванием дыхательных путей, характеризующимся хрипами, удушьем, сдавленностью в груди и кашлем. Астма поражает приблизительно 20 миллионов людей в США, и приблизительно 75% пациентов с астмой являются взрослыми людьми. Из числа пациентов с астмой, приблизительно 60% пациентов с астмой страдают легкой формой заболевания, приблизительно 20% страдают умеренной тяжестью заболевания и оставшиеся 20% страдают тяжелой формой заболевания.
Полагают, что интерлейкин-13 (IL-13) является ключевым в патогенезе астмы человека, поскольку повышенные уровни IL-13 присутствуют в легких пациентов с астмой, и эти уровни коррелируют с тяжестью заболевания (фигура 1). Аналогично, повышенное количество IL-13 присутствует как в мокроте, так и в биопсийных пробах пациентов с умеренной до тяжелой формами астмы, которые получают лечение ингалируемыми кортикостироидами (ICS) или системными кортикостероидами и, которые продолжают проявлять симптоматику. Более того, генетические полиморфизмы IL-13 человека связаны с астмой и атопией (аллергической гиперчувствительностью). IL-13 связывается с двумя рецепторами, IL-13Rα1 и IL-13Rα2. IL-13 является хорошо известной мишенью для астмы, так как была продемонстрирована эффективность действия с использованием разнообразных средств антагонизма IL-13 на множественных, доклинических моделях астмы.
Вследствие роли IL-13 человека при разнообразных расстройствах у человека, были разработаны терапевтические подходы для ингибирования или противодействия активности IL-13. В частности, проводится поиск антител, которые связываются с IL-13 и нейтрализуют его, в качестве средства для ингибирования активности IL-13. Однако в данной области существует необходимость в усовершенствованных антителах, способных к связыванию IL-13 для лечения астмы.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и композициям для лечения астмы, например, легкой или умеренной формы, с использованием антитела против IL-13, или его антигенсвязывающей части.
В одном из аспектов изобретение относится к выделенной композиции, содержащей антитело против IL-13, или его антигенсвязывающую часть, которые, если их вводят внутривенно индивиду при дозе, равной приблизительно 0,3 мг/кг антител или их антигенсвязывающей части, способны к проявлению: (a) площади под кривой (AUC) между приблизительно 1500 и приблизительно 2700 мкгч/мл; (b) объема распределения между приблизительно 65 и 125 мл/кг; (c) пиковой концентрации (Cмакс) между приблизительно 5 и приблизительно 8 мкг/мл; и (d) скорости выведения между приблизительно 0,1 и приблизительно 0,2 мл/ч/кг.
В еще одном аспекте изобретение относится к выделенной композиции, содержащей антитело против IL-13 или его антигенсвязывающую часть, в которой, если композицию вводят внутривенно индивиду при дозе, равной приблизительно 3 мг/кг, антитела или их антигенсвязывающая часть способны к проявлению: (a) площади под кривой (AUC) между приблизительно 21000 и приблизительно 33500 мкгч/мл; (b) объема распределения между приблизительно 55 и приблизительно 100 мл/кг; (c) пиковой концентрации (Cмакс) между приблизительно 55 и приблизительно 90 мкг/мл; и (d) скорости выведения между приблизительно 0,08 и приблизительно 0,15 мл/ч/кг.
В еще одном аспекте изобретение относится к выделенной композиции, содержащей антитела против IL-13, или их антигенсвязывающую часть, в которой, если ее вводят внутривенно индивиду при дозе, равной приблизительно 10 мг/кг, антитела, или их антигенсвязывающая часть, способны к проявлению: (a) площади под кривой (AUC) между приблизительно 75 и приблизительно 100 мкгч/мл; (b) объема распределения между приблизительно 90 и приблизительно l30 мл/кг; (c) пиковой концентрации (Cмакс) между приблизительно 185 и приблизительно 250 мкг/мл; и (d) скорости выведения между приблизительно 0,1 и приблизительно 0,15 мл/ч/кг.
В еще одном аспекте изобретение относится к выделенной композиции, содержащей антитела против IL-13, или их антигенсвязывающую часть, в которой, если ее вводят подкожно индивиду при дозе, равной приблизительно 0,3 мг/кг, антитела или их антигенсвязывающая часть, способны к проявлению: (a) площади под кривой (AUC) между приблизительно 125 и приблизительно 800 мкгч/мл; и (b) пиковой концентрации (Cмакс) между приблизительно 1.0 и приблизительно 6,0 мкг/мл.
В еще одном аспекте изобретение относится к выделенной композиции, содержащей антитело против IL-13, или его антигенсвязывающую часть, в которой, если ее вводят подкожно индивиду при дозе, равной приблизительно 3 мг/кг, антитела или их антигенсвязывающая часть, способны к проявлению: (a) площади под кривой (AUC) между приблизительно 1100 и приблизительно 8500 мкгч/мл; и (b) пиковой концентрации (Cмакс) между приблизительно 12 и приблизительно 60 мкг/мл.
В одном из вариантов осуществления антитело против IL-13, или его антигенсвязывающая часть, представляют собой 13C5.5 или их антигенсвязывающую часть. В еще одном варианте осуществления композиция представляет собой фармацевтическую композицию.
В еще одном аспекте изобретение относится к способам лечения или профилактики астмы у индивида посредством введения композиции по изобретению индивиду, посредством чего происходит лечение или профилактика астмы. В одном из вариантов осуществления композицию вводят однократно. В еще одном варианте осуществления композицию вводят еженедельно. В еще одном другом варианте осуществления композицию вводят в течение приблизительно 3 недель.
В одном из вариантов осуществления астма является астмой в легкой до умеренной форме. В еще одном варианте осуществления индивид является человеком.
В еще одном варианте осуществления способ дополнительно включает введение дополнительного средства. В одном из вариантов осуществления дополнительное средство выбрано из группы, состоящей из терапевтического средства, средства визуализации, цитотоксического средства, ингибитора ангиогенеза, ингибитора киназы, блокатора молекул со-стимуляции, блокатора молекул адгезии, антител против цитокинов или их функционального фрагмента; метотрексата, циклоспорина, рапамицина, FK506, детектируемой метки или репортера, антагониста ФНО, противоревматического средства, мышечного релаксанта, наркотического средства, нестероидного противовоспалительного лекарственного средства (NTHE), анальгезирующего средства, анестезирующего средства, седативного средства, местного анестезирующего средства, нейромышечного блокатора, противомикробного средства, антипсориатического средства, кортикостероида, анаболического стероида, эритропоэтина, средства для иммунизации, иммуноглобулина, иммуносупрессора, гормона роста, средства для гормонозаместительной терапии, радиофармпрепарата, антидепрессанта, антипсихотического средства, стимулятора, медикамента для лечения астмы, бета-агониста, ингалируемого стероида, перорального стероида, эпинефрина или аналога, цитокина и антагониста цитокина.
В еще одном аспекте изобретение относится к способам лечения астмы у индивида посредством введения внутривенно индивиду антител против IL-13, или их антигенсвязывающей части, где по меньшей мере одна фармакокинетическая характеристика выбрана из группы, состоящей из: (a) максимальной сывороточной концентрации (Cмакс) между приблизительно 5 и приблизительно 235 мкг/мл, и (b) площади под кривой концентрация-время для сыворотки (AUC) между приблизительно 1500 и приблизительно 98000 мкгч/мл, достигаемую после введения антител, или их антигенсвязывающей части индивиду.
В одном из вариантов осуществления антитела или их антигенсвязывающую часть, вводят при дозе, равной приблизительно 0,3 мг/кг. В одном из вариантов осуществления Cмакс находится между приблизительно 5 и приблизительно 10 мкг/мл. В одном из вариантов осуществления AUC находится между приблизительно 1500 и приблизительно 2700 мкгч/мл.
В еще одном варианте осуществления антитела или их антигенсвязывающую часть вводят при дозе, равной приблизительно 3 мг/кг. В одном из вариантов осуществления Cмакс находится между приблизительно 55 и приблизительно 90 мкг/мл. В еще одном варианте осуществления AUC находится между приблизительно 20000 и приблизительно 34000 мкгч/мл.
В еще одном варианте осуществления антитела или их антигенсвязывающую часть, вводят при дозе, равной приблизительно 10 мг/кг. В одном из вариантов осуществления Cмакс находится между приблизительно 190 и приблизительно 235 мкг/мл. В одном из вариантов осуществления AUC находится между приблизительно 75000 и приблизительно 100000 мкгч/мл.
В еще одном варианте осуществления значение Cмакс находится между приблизительно 20 и приблизительно 30 (мкг/мл)/(мг/кг) после нормализации дозы. В еще одном варианте осуществления AUC находится между приблизительно 6000 и приблизительно 10000 (мкгч/мл)/(мг/кг) после нормализации дозы.
В еще одном другом аспекте изобретение относится к способам лечения астмы у индивида посредством введения подкожно индивиду антител против IL-13, или их антигенсвязывающей части, где по меньшей мере одна фармакокинетическая характеристика выбрана из группы, состоящей из: (a) максимальной сывороточной концентрации (Cмакс) между приблизительно 1 и приблизительно 60 мкг/мл и (b) площади под кривой концентрация-время для сыворотки (AUC) между приблизительно 125 и приблизительно 8100 мкгч/мл, достигают после введения антитела, или его антигенсвязывающей части индивиду.
В одном из вариантов осуществления антитела или их антигенсвязывающую часть вводят при дозе, равной приблизительно 0,3 мг/кг. В одном из вариантов осуществления Cмакс находится между приблизительно 1 и приблизительно 6 мкг/мл. В еще одном варианте осуществления AUC находится между приблизительно 100 и приблизительно 800 мкгч/мл.
В еще одном варианте осуществления антитела или их антигенсвязывающую часть вводят при дозе, равной приблизительно 3 мг/кг. В одном из вариантов осуществления Cмакс находится между приблизительно 12 и приблизительно 60 мкг/мл. В еще одном варианте осуществления AUC находится между приблизительно 1100 и приблизительно 8100 мкгч/мл.
В одном из вариантов осуществления антитела против IL-13, или их антигенсвязывающая часть представляют собой 13C5.5 или их антигенсвязывающую часть. В еще одном варианте осуществления индивид является человеком. В еще одном варианте осуществления антитела против IL-13 или их антигенсвязывающую часть вводят однократно. В еще одном варианте осуществления антитела против IL-13 или их антигенсвязывающую часть вводят еженедельно. В еще одном другом варианте осуществления антитела против IL-13, или их антигенсвязывающую часть, вводят в течение трех недель.
В одном из вариантов осуществления астма представляет собой астму от легкой до умеренной формы.
В еще одном варианте осуществления способ дополнительно включает введение дополнительного средства. В одном из вариантов осуществления дополнительное средство выбрано из группы, состоящей из терапевтического средства, средства визуализации, цитотоксического средства, ингибитора ангиогенеза, ингибитора киназы, блокатора молекул со-стимуляции, блокатора молекул адгезии, антител против цитокинов или их функционального фрагмента; метотрексата, циклоспорина, рапамицина, FK506, детектируемой метки или репортера, антагониста ФНО, противоревматического средства, мышечного релаксанта, наркотического средства, нестероидного противовоспалительного лекарственного средства (NTHE), анальгезирующего средства, анестезирующего средства, седативного средства, местного анестезирующего средства, нейромышечного блокатора, противомикробного средства, антипсориатического средства, кортикостероида, анаболического стероида, эритропоэтина, средства для иммунизации, иммуноглобулина, иммуносупрессора, гормона роста, средства для гормонозаместительной терапии, радиофармпрепарата, антидепрессанта, антипсихотического средства, стимулятора, медикамента для лечения астмы, бета-агониста, ингалируемого стероида, перорального стероида, эпинефрина или аналога, цитокина и антагониста цитокина.
В еще одном другом аспекте изобретение относится к способам лечения астмы у индивида посредством введения подкожно индивиду антител против IL-13, или их антигенсвязывающей части, при дозе, равной приблизительно 0,3 мг/кг, где по меньшей мере одна фармакокинетическая характеристика выбрана из группы, состоящей из: (a) времени полужизни между приблизительно 24 и 31 днями; (b) Tмакс между от приблизительно 3 до приблизительно 5 днями; и (c) биодоступности, равной по меньшей мере приблизительно 60%, которых достигают после введения антител или их антигенсвязывающей части индивиду. В одном из вариантов осуществления биодоступность составляет по меньшей мере приблизительно 70%.
В еще одном другом аспекте изобретение относится к способам лечения астмы у индивида посредством введения подкожно индивиду антител против IL-13, или их антигенсвязывающей части при дозе, равной приблизительно 3 мг/кг, где по меньшей мере одна фармакокинетическая характеристика выбрана из группы, состоящей из: (a) времени полужизни между приблизительно 23 и 26 днями; (b) Tмакс меньшего чем или равного до приблизительно 5 дней; и (c) биодоступности, равной по меньшей мере приблизительно 60%, достигаемой после введения антител или их антигенсвязывающей части индивиду. В одном из вариантов осуществления биодоступность составляет по меньшей мере приблизительно 70%.
В еще одном аспекте изобретение относится к способам лечения астмы у индивида, включающим введение внутривенно индивиду антител против IL-13, или их антигенсвязывающей части при дозе, равной приблизительно 0,3 мг/кг, где по меньшей мере одна фармакокинетическая характеристика выбрана из группы, состоящей из: (a) скорости выведения между от приблизительно 0,11 до приблизительно 0,19 мл/час/кг; и (b) объема распределения между от приблизительно 70 до приблизительно 130 мл/кг, достигаемых после введения антител, или их антигенсвязывающей части индивиду.
В еще одном аспекте изобретение относится к способам лечения астмы у индивида посредством введения внутривенно индивиду антител против IL-13, или их антигенсвязывающей части при дозе, равной приблизительно 3 мг/кг, где по меньшей мере одна фармакокинетическая характеристика выбрана из группы, состоящей из: (a) скорости выведения между приблизительно 0,08 до приблизительно 0,14 мл/час/кг; и (b) объема распределения между приблизительно 55 до приблизительно 100 мл/кг, достигаемых после введения антител или их антигенсвязывающей части индивиду.
В еще одном аспекте изобретение относится к способам лечения астмы у индивида, включающим введение внутривенно индивиду антител против IL-13, или их антигенсвязывающей части при дозе, равной приблизительно 10 мг/кг, где по меньшей мере одна фармакокинетическая характеристика выбрана из группы, состоящей из: (a) скорости выведения между от приблизительно 0,09 до приблизительно 0,13 мл/час/кг; и (b) объема распределения между от приблизительно 85 до приблизительно 130 мл/кг, которых достигают после введения антител, или их антигенсвязывающей части индивиду.
В одном из вариантов осуществления антитела против IL-13, или их антигенсвязывающая часть представляют собой 13C5.5, или их антигенсвязывающую часть. В еще одном варианте осуществления индивид является человеком. В одном из вариантов осуществления антитела против IL-13 или их антигенсвязывающую часть, вводят однократно. В еще одном варианте осуществления антитела против IL-13, или их антигенсвязывающую часть, вводят еженедельно. В еще одном другом варианте осуществления антитела против IL-13, или их антигенсвязывающую часть, вводят в течение 3 недель.
В одном из вариантов осуществления астма представляет собой астму от легкой до умеренной формы.
В еще одном варианте осуществления способы дополнительно включают введение дополнительного средства. В одном из вариантов осуществления дополнительное средство выбрано из группы, состоящей из терапевтического средства, средства визуализации, цитотоксического средства, ингибитора ангиогенеза, ингибитора киназы, блокатора молекул со-стимуляции, блокатора молекул адгезии, антител против цитокинов или их функционального фрагмента; метотрексата, циклоспорина, рапамицина, FK506, детектируемой метки или репортера, антагониста ФНО, противоревматического средства, мышечного релаксанта, наркотического средства, нестероидного противовоспалительного лекарственного средства (NTHE), анальгезирующего средства, анестезирующего средства, седативного средства, местного анестезирующего средства, нейромышечного блокатора, противомикробного средства, антипсориатического средства, кортикостероида, анаболического стероида, эритропоэтина, средства для иммунизации, иммуноглобулина, иммуносупрессора, гормона роста, средства для гормонозаместительной терапии, радиофармпрепарата, антидепрессанта, антипсихотического средства, стимулятора, медикамента для лечения астмы, бета-агониста, ингалируемого стероида, перорального стероида, эпинефрина или аналога, цитокина и антагониста цитокина.
В одном из вариантов осуществления индивид представляет собой человека.
В еще одном аспекте изобретение относится к выделенной композиции, содержащей антитела против IL-13, или их антигенсвязывающую часть, где, когда ее вводят внутривенно индивиду при дозе, равной приблизительно 0,3 мг/кг, 1 мг/кг, 3 мг/кг или 10 мг/кг, антитела или их антигенсвязывающая часть способны к проявлению какого-либо из фармакокинетического параметра, представленного в описании, Таблицах или на Фигурах.
В еще одном аспекте изобретение относится к выделенной композиции, содержащей антитела против IL-13, или их антигенсвязывающую часть, где, когда ее вводят подкожно индивиду при дозе, равной приблизительно 0,3 мг/кг, 1 мг/кг или 3 мг/кг, антитела или их антигенсвязывающая часть является способными к проявлению какого-либо из фармакокинетического параметров, представленного в описании, Таблицах или на Фигурах.
В еще одном аспекте изобретение относится к способам лечения или профилактики астмы у индивида посредством введения внутривенно индивиду антител против IL-13 или их антигенсвязывающей части при дозе, равной приблизительно 0,3 мг/кг, 1 мг/кг, 3 мг/кг или 10 мг/кг, где по меньшей мере одна из фармакокинетических характеристик, представленных в описании, Таблицах или на Фигурах достигается после введения антител или их антигенсвязывающей части индивиду.
В еще одном другом аспекте изобретение относится к способам лечения или профилактики астмы у индивида посредством введения подкожно индивиду антител против IL-13 или их антигенсвязывающей части при дозе, равной приблизительно 0,3 мг/кг, 1 мг/кг, 3 мг/кг или 10 мг/кг, где по меньшей мере одна из фармакокинетических характеристик представленная в описании, Таблицах или на Фигурах достигается после введения антител, или их антигенсвязывающей части индивиду.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигуре 1 представлен график, отображающий то, что экспрессия IL-13 предшествует дисфункции легких.
На фигуре 2 показано, что 13C5.5, антитела против IL-13, получают из гибридомы с уникальными эпитопами и клеточной линией.
На фигуре 3 показано, что 13C5.5, антитела против IL-13, нейтрализуют IL-13 в легком.
На фигуре 4 показана схема первого дозирования у человека (FIN), применяемого на Фазе I клинических испытаний.
На фигуре 5 показан профиль зависимости средней концентрации 13C5.5 в сыворотке от времени после однократных внутривенных инфузий по 0,3 мг/кг, 1 мг/кг, 3 мг/кг и 10 мг/кг 13C5.5 здоровым индивидам по линейной шкале.
На фигуре 6 показаны фармакокинетические параметры 13C5.5, антител против IL-13.
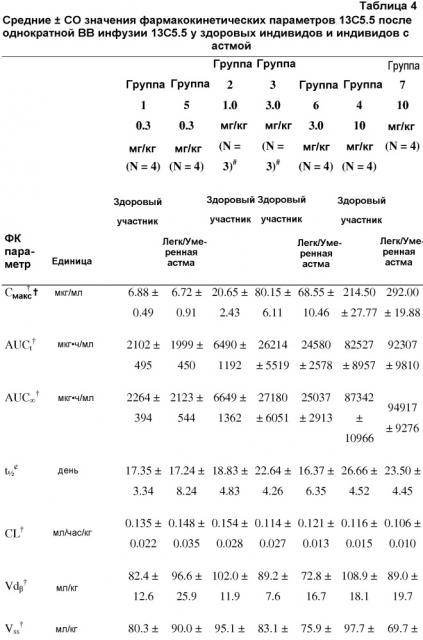
На фигуре 7 показан профиль зависимости средней концентрации в сыворотке от времени после однократных внутривенных инфузий по 0,3 мг/кг, 1 мг/кг, 3 мг/кг и 10 мг/кг 13C5.5 здоровым индивидам и индивидам с астмой по линейной шкале.
На фигуре 8 показаны фармакокинетические параметры 13C5.5 антител против IL-13.
На фигуре 9 показаны фармакокинетические параметры 13C5.5, антител против IL-13.
На фигуре 10 показаны фармакокинетические параметры 13C5.5 антител против IL-13. Биодоступность после подкожного введения оценивали, как равную приблизительно 70%.
На фигуре 11 показано нормализованные значения Cмакс для средней дозы после трех подкожных инъекций еженедельно по 0,3 мг/кг 13C5.5 (Группа 8) и 3 мг/кг 13C5.5 (Группа 9) (Часть 3 клинического испытания).
На фигуре 12 показано нормализованные значения AUC0-168 для средней дозы после трех подкожных инъекций 13C5.5 еженедельно по 0,3 мг/кг (Группа 8) и 3 мг/кг (Группа 9) (Часть 3 клинического испытания).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и композициям для лечения астмы, например, легкой или умеренной формы, с использованием антител против IL-13 или их антигенсвязывающей части.
Настоящее изобретение будет более понято после определения некоторых терминов.
Термин "полипептид", как используется в настоящей заявке, относится к любой полимерной цепи из аминокислот. Термины "пептид" и "белок" используют взаимозаменяемо с термином полипептид и также относят к полимерной цепи из аминокислот. Термин "полипептид" охватывает нативные или искусственные белки, фрагменты белка и полипептидные аналоги белковой последовательности. Полипептид может быть мономерным или полимерным.
Термин "выделенный белок" или "выделенный полипептид" означает белок или полипептид, который по своей природе или источнику выделения не связан с природными компонентами, которые находятся вместе с ним в его нативном состоянии; не содержит по существу других белков того же вида; экспрессируется клетками различных видов; или не встречается в природе. Таким образом, полипептид, который химически синтезирован или синтезирован в клеточной системе, отличной от клетки, в которой он существует в природе, будет "выделен" от его природных компонентов. Белок, по существу не содержащий природных компонентов, может также быть получен посредством выделения с использованием способов очистки белка, хорошо известных в данной области.
Термин "выделение" как используют в настоящем описании, относится к способу получения химических типов, таких как полипептид, по существу не содержащих природных компонентов посредством выделения, например, с использованием способов очистки белка, хорошо известных в данной области.
Термины "IL-13" и "IL-13 дикого типа" (сокращенные в настоящем описании как IL-13, IL-13 дт), как используют в настоящем описании, включают цитокин, который секретируется прежде всего Т-хелперными клетками второго типа. Термин включает мономерный белок из полипептида с массой 13 кДа. Структура IL-13 дополнительно описана, например, в статье Moy, Diblasio et al. 2001 J Mol Biol 310 219-30. Подразумевают, что термин IL-13 включает рекомбинантный IL-13 человека (рч IL-13), который может быть получен стандартными способами рекомбинантной экспрессии. Аминокислотная последовательность IL-13 человека, SEQ ID NO:1, является известной в данной области.
Последовательность IL-13 человека - SEQ ID NO: 1
MALLLTTVIALTCLGGFASPGPVPPSTALRELIEELVNITQNQKAPLCNGSMVWS INLTAGMYCAALESLINVSGCSAIEKTQRMLSGFCPHKVSAGQFSSLHVRDTKIE VAQFVKDLLLHLKKLFREGRFN
Термин "вариант IL-13" (сокращенный в настоящем описании как IL-13v), как используют в настоящем описании, включает вариант IL-13, где аминокислотный остаток в положении 130 SEQ ID NO:1 заменен с Аргинина на Глутамин (R130Q).
"Биологическая активность", как используют в настоящем описании, относится ко всем характерным биологическим свойствам цитокина. Биологические свойства IL-13 включают, но ими не ограничены, связывание с рецептором IL-13; (другие примеры включают изотип иммуноглобулина, переходящий в IgE в B-клетках человека и подавляющий продукцию воспалительного цитокина).
Термины "специфическое связывание" или "специфически связываясь с", как используют в настоящем описании, со ссылкой на взаимодействие антитела, белка или пептида со вторым химическим видом, означает, что взаимодействие зависит от присутствия конкретной структуры (например, антигенной детерминанты или эпитопа) у химического вида; например, антитело распознает и связывается с конкретной белковой структурой в большей степени, чем с белками в целом. Если антитело является специфичным для эпитопа "A", присутствие молекулы, содержащей эпитоп (или свободный, немеченный A), в реакции, содержащей меченный "A" и антитело, будет снижать количество меченного А, связанного с антителом.
Термин "антитело", как используют в настоящем описании, в широком смысле относится к любой иммуноглобулиновой (Ig) молекуле, состоящей из четырех полипептидных цепей, двух тяжелых (H) цепей и двух легких (L) цепей, или любому их функциональному фрагменту, мутанту, варианту или деривату, который сохраняет существенные признаки связывания с эпитопом молекулы Ig. Такие форматы мутанта, варианта или производного антитела являются известными в данной области. Их неограничивающие варианты осуществления обсуждаются в настоящем документе. В одном из вариантов осуществления антитело, используемое в композициях и способах по изобретению, представляет собой антитело против IL-13, 13C5.5, описанное в патенте США № 7915388, включенном в настоящее описание в качестве ссылки. В еще одном варианте осуществления антитело, используемое в композициях и способах по изобретению, представляет собой антитело 6A1, 3G4, тралокинумаб, лебрикизумаб, QAZ-576, IMA-638 или IMA-026.
В полноразмерном антителе каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращенной в настоящем описании как HCVR или VH) и константной области тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов, CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенной в настоящем описании как LCVR или VL) и константной области легкой цепи. Константная область легкой цепи состоит из одного домена, CL. Области VH и VL могут быть дополнительно подразделены на области гипервариабельности, называемые области, определяющие комплементарность (CDR), перемежающиеся с областями, которые являются более консервативными, называемыми каркасные области (FR). Каждая VH и VL составлена из трех CDR и четырех FR, расположенных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Иммуноглобулиновые молекулы могут принадлежать к любому типу (например, IgG, IgE, IgM, IgD, IgA и IgY), классу (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подклассу.
Термин "антигенсвязывающая часть" антитела (или просто "часть антитела"), как используют в настоящем описании, относится к одному или нескольким фрагментам антитела, которые сохраняют способность специфически связываться с антигеном (например, IL-13). Было показано, что антигенсвязывающая функция антитела может осуществляться фрагментами полноразмерного антитела. Такие варианты осуществления антитела могут также иметь биспецифический, с двойной специфичностью или мультиспецифичные форматы; специфически связываясь с двумя или или несколькими различными антигенами. Примеры связывающих фрагментов, охваченные термином "антигенсвязывающая часть" антитела включают (i) Fab-фрагмент, моновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) F(ab')2-фрагмент, бивалентный фрагмент, содержащий два Fab фрагмента, связанные посредством дисульфидной области в шарнирной области; (iii) Fd-фрагмент, состоящий из доменов VH и CH1; (iv) Fv-фрагмент, состоящий из доменов VL и VH одиночного плеча антитела, (v) dAb-фрагмент (Ward et al., (1989) Nature 341:544-546, Winter et al., опубликованная заявка PCT WO 90/05144 A1, включенная в настоящее описание в качестве ссылки), которая содержит одиночный вариабельный домен; и (vi) выделенная область, определяющая комплементарность (CDR). Кроме того, несмотря на то, что два домена Fv-фрагмента, VL и VH, кодируются раздельными генами, они могут быть объединены, с использованием рекомбинантных способов, посредством синтетического линкера, который обеспечивает им получение в виде единственной белковой цепи, в которой области VL и VH образуют пару с образованием моновалентных молекул (известных как Fv с одиночной цепью (scFv); см., например, Bird et al. (1988) Science 242:423-426; и Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Подразумевают, что такие антитела с одиночной цепью охватываются термином "антигенсвязывающая часть" антитела. Другие формы антител с одиночной цепью, такие как диатела также являются охваченными. Диатела представляют собой бивалентные, биспецифические антитела, в которых домены VH и VL экспрессируются на одиночной полипептидной цепи, но с использованием линкера, который является слишком коротким, чтобы обеспечить возможность спаривания между двумя доменами на той же цепи, посредством этого заставляя домены спариваться с комплементарными доменами еще одной другой цепи и создавать два участка связывания антигена (см., например, Holliger, P., et al. (1993) Proc. Natl. Acad. Sci. USA 90:6444-6448; Poljak, R. J., et al. (1994) Structure 2: 1121-1123). Такие части связывания антител являются известными в данной области (Kontermann and Dubel eds., Antibody Engineering (2001) Springer-Verlag. New York. 790 pp. (ISBN 3-540-41354-5).
Термин "конструкция антитела", как используют в настоящем описании, относится к полипептиду, содержащему одну или несколько антигенсвязывающих частей по изобретению, связанных с линкерным полипептидом или константным доменом иммуноглобулина. Линкерные полипептиды содержат два или несколько аминокислотных остатков, соединенных посредством пептидных связей, и применяют для связывания одной или нескольких антигенсвязывающих частей. Такие линкерные полипептиды являются хорошо известными в данной области (см., например, Holliger, P., et al. (1993) Proc. Natl. Acad. Sci. USA 90:6444-6448; Poljak, R. J., et al. (1994) Structure 2: 1121-1123). Константный домен иммуноглобулина относится к константному домену тяжелой или легкой цепи. Аминокислотные последовательности константного домена тяжелой цепи и легкой цепи IgG человека являются известными в данной области и раскрыты в Таблице 2 Патента США № 7915388, полное содержание которого включено в настоящее описание в качестве ссылки.
Более того, антитело или его антигенсвязывающая часть могут быть частью более крупных молекул иммуноадгезии, образованных посредством ковалентной или нековалентной связи антитела или части антитела с одним или несколькими другими белками или пептидами. Примеры таких молекул иммуноадгезии включают применение центральной области стрептавидина для создания тетрамерной молекулы scFv (Kipriyanov, S. M., et al. (1995) Human Antibodies and Hybridomas 6:93-101) и применение цистеинового остатка, маркерного пептида и C-концевой полигистидиновой метки для получения бивалентных и биотинилированных молекул scFv (Kipriyanov, S. M., et al. (1994) Mol. Immunol. 31: 1047-1058). Части антитела, такие как фрагменты Fab и F(ab')2, могут быть получены из цельных антител с использованием общепринятых способов, таких как расщепление папаином или пепсином, соответственно, цельных антител. Более того, антитела, части антител и молекулы иммуноадгезии могут быть получены с использованием стандартных способов рекомбинантных ДНК, как описано в настоящем описании.
Подразумевают, что термин "выделенное антитело", как используют в настоящем описании, относится к антителу, которое по существу не содержит других антител, имеющих отличные антигенные специфичности (например, выделенное антитело, которое специфически связывается с IL-13, по существу не содержит антитела, которые специфически связываются с антигенами, отличными от IL-13). Выделенное антитело, которое специфически связывается с IL-13, может, однако, иметь перекрестную реактивность по отношению к другим антигенам, таким как молекулы IL-13 от другого вида. Кроме того, выделенное антитело может по существу не содержать другого клеточного материала и/или химикатов.
Подразумевают, что термин "антитело человека", как используют в настоящем описании, включает антитела, имеющие вариабельные и константные области, происходящие от последовательностей иммуноглобулинов человека эмбрионального типа. Антитела человека по изобретению могут включать аминокислотные остатки, некодируемые последовательностями иммуноглобулинов человека эмбрионального типа (например, посредством мутаций, вводимых посредством разупорядоченного или сайт-специфического мутагенеза in vitro или посредством соматической мутации in vivo), например в CDR и, в частности, CDR3. Однако, термин "антитело человека", как используют в настоящем описании, не подразумевает включение антител, в которых последовательности CDR, происходящие от эмбрионального типа еще одного вида млекопитающих, такого как мышь, были привиты на каркасные последовательности человека.
Термин "рекомбинантное антитело человека", как используют в настоящем описании, предназначен для включения всех антител человека, которые получают, экспрессируют, создают или выделяют посредством рекомбинантных средств, таких как антитела, экспрессируемые с использованием рекомбинантного вектора экспрессии, трансфицированного в клетку-хозяина (описанные дополнительно в Патенте США № 7915388, содержание которого включено в настоящем описании в качестве ссылки), антитела, выделенные из рекомбинантных, комбинаторных библиотек антител человека (Hoogenboom H. R., (1997) TIB Tech. 15:62-70; Azzazy H., and Highsmith W. E., (2002) Clin. Biochem. 35:425-445; Gavilondo J. V., and Larrick J. W. (2002) BioTechniques 29: 128-145; Hoogenboom H., and Chames P. (2000) Immunology Today 21:371-378), антитела, выделенные из животного (например, мыши), которое является трансгенным для генов иммуноглобулинов человека (см., например, Taylor, L. D., et al. (1992) Nucl. Acids Res. 20:6287-6295; Kellermann S-A., and Green L. L. (2002) Current Opinion in Biotechnology 13:593-597; Little M. et al (2000) Immunology Today 21:364-370) или антитела, полученные, экспрессируемые, создаваемые или выделенные посредством любого другого средства, которое включает сплайсинг генной последовательности иммуноглобулина человека к другой последовательности ДНК. Такие рекомбинантные антитела человека имеют вариабельные и константные области, происходящие от последовательностей иммуноглобулинов человека эмбрионального типа. В некоторых вариантах осуществления, однако, такие рекомбинантные антитела человека подвергают мутагенезу in vitro (или, когда используют животное, трансгенное для последовательности Ig человека, соматическому мутагенезу in vivo) и, таким образом, аминокислотные последовательности областей VH и VL рекомбинантных антител, представляют собой последовательности, которые, будучи производными от и относящимся к последовательностям VH и VL эмбрионального типа человека, могут естественным образом не существовать в эмбриональном наборе антитела человека in vivo. Один вариант осуществления предоставляет полностью человеческие антитела, способные к связыванию с IL-13 человека, которые можно получать с использованием способов, хорошо известных в данной области, таких как, но ими не ограничиваясь, с использованием библиотек фагов Ig человека, таких как библиотеки, раскрытые в Jermutus et al., опубликованная заявка PCT № WO 2005/007699 A2.
Термин "химерное антитело" относится к антителам, которые содержат последовательности вариабельной области тяжелой и легкой цепи от одного вида и последовательности константной области от еще одного вида, такие как антитела, имеющие вариабельные области тяжелой и легкой цепи мыши, связанные с константными областями человека.
Термин "CDR-привитое антитело" относится к антителам, которые содержат последовательности вариабельной области тяжелой и легкой цепи от одного вида, но в которых последовательности одной или нескольких из областей CDR VH и/или VL заменены на CDR-последовательности еще одного вида, такие как антитела, имеющие мышиные вариабельные области тяжелой и легкой цепи, в которых одну или несколько из CDR мыши (например, CDR3) заменяют на последовательности CDR человека.
Термин "гуманизированное антитело" относится к антителам, которые содержат последовательности вариабельной области тяжелой и легкой цепи от нечеловеческого вида (например, мыши), но в которых по меньшей мере часть последовательности VH и/или VL была изменена, чтобы быть более "человекоподобной", т.е., более сходной с вариабельными последовательностями эмбрионального типа человека. Одним типом гуманизированного антитела является CDR-привитое антитело, в котором последовательности CDR человека вводят в по