Стабильная кристаллическая форма типирацила гидрохлорида и способ ее кристаллизации
Иллюстрации
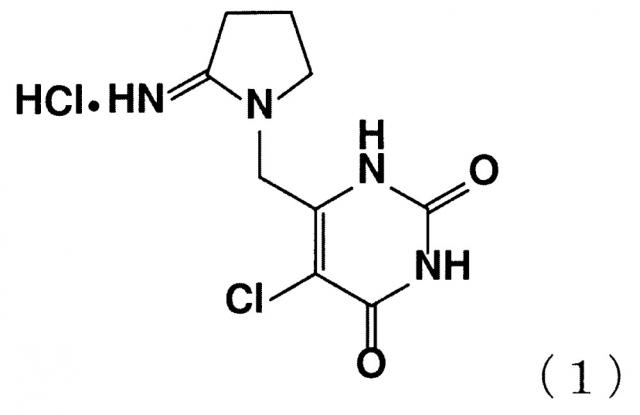
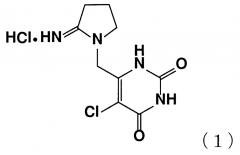
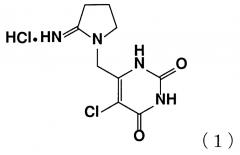
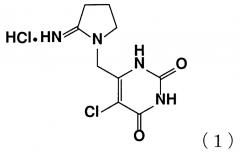
Показать всеИзобретение относится к новой кристаллической форме гидрохлорида 5-хлор-6-(2-иминопирролидин-1-ил)метил-2,4(1H,3H)пиримидиндиона формулы (I), указанной ниже. Соединение обладает свойствами ингибитора тимидинфосфорилазы и может быть использовано в качестве противоопухолевого средства. Кристаллическая форма соединения формулы (1)
демонстрирует характеристические пики порошковой рентгеновской дифракции при углах 11,6°, 17,2°, 17,8°, 23,3°, 27,1° и 29,3°, в качестве дифракционного угла (2θ±0,1°) в безводной форме и эндотермический пик, определяемый методом термогравиметрии и дифференциального термического анализа, при температуре, составляющей около 262°C. Кристалл показывает, в анализе монокристаллов, следующие данные по кристаллу: кристаллическая система: моноклинная система, пространственная группа: P2l/n (No. 14), константа кристаллической решетки: a = 11,6006 (9) Å, b = 10,3106 (11) Å, с = 10,3036 (10) Å, α = 90°, β = 101,951 (7)°, γ = 90° и объем элементарной ячейки решетки: 1205,7 (2) Å3. 3 н. и 10 з.п. ф-лы, 3 ил., 3 табл., 7 пр.
Реферат
Область техники
Настоящее изобретение относится к стабильной кристаллической форме гидрохлорида типирацила, имеющей превосходную стабильность и используемую в качестве активного ингредиента лекарственных средств, а также к способу ее кристаллизации.
Уровень техники
Обычно, когда соединение используют в качестве активного ингредиента для лекарственных средств, соединение должно иметь химическую и физическую стабильность для сохранения стабильного качества и/или для удобства его хранения и применения. По этой причине такое соединение, предпочтительно, получают в стабильной кристаллической форме. При этом, когда соединение используется в качестве активного фармацевтического ингредиента в лекарственном средстве, выбирают наиболее стабильную кристаллическую форму соединения. Кроме того, Guideline for Residual Solvents (Руководство по определению остаточных растворителей) в рекомендациях ICH (Международная конференция по гармонизации технических требований к регистрации лекарственных препаратов для человека) дает рекомендации относительно того, какие из множества растворителей, и их приемлемые количества, должны быть исключены/ограничены/использованы. Некоторые растворители, используемые в получения лекарственных средств, являются токсичными, и поэтому, с точки зрения безопасности, количество такого растворителя, остающегося после производственного процесса, должно быть, желательно, минимальным. Кроме того, в процессе производства лекарственные средства могут заряжаться статическим электричеством. Заряженные лекарственные средства могут прилипать к поверхностям производственной машины, разделительной и упаковочной машины и т.п., и возникают проблемы, связанные с ухудшением выхода продукта и несоответствующей упаковки. Для устранения таких проблем предпочтительными являются лекарственные средства, имеющие низкую поляризуемость.
В патентной литературе 1 описывается, что одно из производных урацила, гидрохлорид типирацила (химическое название: гидрохлорид 5-хлор-6-(2-иминопирролидин-1-ил)метил-2,4(1H,3H)-пиримидиндиона, далее иногда называемый как "TPI" (5-хлор-6-(2-иминопирролидин-1-ил)метил-2,4(1H,3H)-пиримидиндион, иногда называемый как "типирацил")), представленный следующей формулой (1)
,
обладает ингибирующим действием в отношении человеческой тимидинфосфорилазы, и усиливающим действием в отношении противоопухолевого эффекта трифлуридина (далее иногда называемый как "FTD"). Противоопухолевое средство "TAS-102" состоит из смеси FTD и TPI с молярном соотношением 1 к 0,5, которое в настоящее время находится на стадии разработки в качестве перорального препарата, и уже было одобрено в Японии в качестве терапевтического средства для лечения поздней стадии злокачественной опухоли толстой и прямой кишки или рецидивирующей злокачественной опухоли толстой и прямой кишки (непатентный документ 1 и 2).
Примеры ранее описанных способов получения типирацила гидрохлорида включают: способ, в котором типирацил моногидрохлорид 1/10 гидрат получают следующим образом: 5-хлор-6-хлорметилурацил, 2-иминопирролидин и раствор этоксида натрия в N,N-диметилформамиде перемешивают при комнатной температуре в течение 14 часов; кристаллизованное вещество отделяют фильтрованием и суспендируют в воде; суспензию нейтрализуют уксусной кислотой; нерастворимое вещество отделяют фильтрованием и растворяют в 1н соляной кислоте; добавляют активированный уголь; смесь фильтруют; фильтрат концентрируют при пониженном давлении; и остаток промывают этанолом и отделяют фильтрованием (патентная литература 1). В другом описанном способе типирацил гидрохлорид получают следующим образом: 2-иминопирролидина гидрохлорид, 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и 5-хлор-6-(хлорметил)пиримидин-2,4(1H,3H)-дион подвергают взаимодействию в метаноле; полученный осадок растворяют в 2н соляной кислоте при температуре 90°С и при нагревании; этанол добавляют к реакционной жидкости; и жидкость оставляют отстаиваться при комнатной температуре с получением кристаллов белого цвета (непатентный документ 3). Тем не менее, как выяснилось впоследствии, белые кристаллы, полученные этими способами, представляли собой смешанные кристаллы, содержащие описанный ниже Кристалл III.
В настоящее время не известен способ, при котором стабильная кристаллическая форма высоко чистого безводного типирацила гидрохлорида может быть получена с высокой воспроизводимостью.
Список ссылок
Патентная литература
PTL 1: WO 96/30346
Непатентная литературе
НПЛ 1: International Journal of Oncology 25: 571-578, 2004
НПЛ 2: Invest New Drugs 26{5): 445-54, Октябрь 2008
НПЛ 3: Bioorganic & Medicinal Chemistry 12 (2004) 3443-3450
Сущность изобретения
Техническая задача
Задачей настоящего изобретения является обеспечение стабильной кристаллической формы типирацил гидрохлорида, используемого в качестве активного ингредиента лекарственных средств.
Решение задачи
Авторы настоящего изобретения провели тщательные исследования и обнаружили следующее: типирацил гидрохлорид имеет три кристаллические формы (Кристалл I, Кристалл II и Кристалл III); Кристалл I и Кристалл III обладают более высокой стабильностью хранения, чем Кристалл II; и Кристалл I по сравнению с Кристаллом III является более безопасным в качестве лекарственного средства благодаря меньшему содержанию остаточного растворителя, и его проще обрабатывать благодаря наличию меньшего электрического заряда. Кроме того, авторы настоящего изобретения провели эксперименты при сочетаниях очень большого количества условий, таких как вид растворителя, температура, концентрация, время покоя и время охлаждения, время перемешивания и скорость перемешивания, и методом проб и ошибок обнаружили предпочтительный технологический способ получения Кристалла I высокой чистоты при определенных условиях. В результате дальнейших исследований авторы настоящего изобретения осуществили настоящее изобретение.
То есть, настоящее изобретение относится к следующему: (1)-(14).
(1) Кристалл гидрохлорида 5-хлор-6-(2-иминопирролидин-1-ил)метил-2,4(1H 3H)пиримидиндиона, демонстрирующий пики при двух или более углах, выбранных из группы, состоящей из 11,6°, 17,2°, 17,8°, 23,3°, 27,1° и 29,3°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции.
(2) Кристалл в соответствии с пунктом (1), демонстрирующий пики при углах 11,6°, 17,2°, 17,8°, 23,3°, 27,1° и 29,3°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции.
(3) Кристалл в соответствии с вышеуказанными пунктами (1) или (2), демонстрирующий эндотермический пик, определяемый методом термогравиметрии и дифференциального термического анализа при температуре около 262°С.
(4) Кристалл в соответствии с любым из вышеуказанных пунктов (1)-(3), который показывает, в анализе монокристаллов, следующие данные по кристаллу:
Кристаллическая система: моноклинная система
Пространственная группа: P2l/n (№ 14)
Константа кристаллической решетки:
a = 11,6006 (9) Å
b = 10,3106 (11) Å
с = 10,3036 (10) Å
α = 90°
β = 101,951 (7)°
γ = 90°
Объем элементарной ячейки решетки: 1205,7 (2) Å3.
(5) Кристалл по любому из пунктов (1)-(4) в безводной форме.
(6) Кристалл по любому из пунктов (1)-(5), имеющий чистоту 90% по массе или более.
(7) Кристалл в соответствии с любым из вышеуказанных пунктов (1)-(6), демонстрирующий пики при двух или более углах, выбранных из группы, состоящей из 11,6°, 17,2°, 17,8°, 23,3°, 27,1° и 29,3°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции после 6-месячного хранения при 40°С в исследовании стабильности.
(8) Кристалл гидрохлорида 5-хлор-6-(2-иминопирролидин-1-ил)метил-2/4(1H,3H)пиримидиндиона, демонстрирующий пики при двух или более углах, выбранных из группы, состоящей из 10,5°, 19,6°, 23,7°, 26,2° и 31,2°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции.
(9) Кристалл в соответствии с вышеуказанным пунктом (8), демонстрирующий пики при углах, составляющих 10,5°, 19,6°, 23,7°, 26,2° и 31,2°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции.
(10) Кристалл в соответствии с вышеуказанным пунктом (8) или (9), демонстрирующий эндотермический пик, определяемый методом термогравиметрии и дифференциального термического анализа при температуре, составляющей около 245°C.
(11) Кристалл в соответствии с любым из вышеуказанных пунктов (8)-(10), который показывает при анализе монокристаллов следующие данные по кристаллу:
Кристаллическая система: моноклинная система
Пространственная группа: P2l
Константа кристаллической решетки:
a = 10,3221 (14) Å
b = 9,8634 (13) Å
с = 11,6643 (16) Å
α = 90°
β = 100,317°
γ = 90°
Объем элементарной ячейки решетки: 1169,5 (3) Å3.
(12) Кристалл в соответствии с любым из вышеуказанных пунктов (8)-(11) в безводной форме.
(13) Способ производства кристалла в соответствии с любым из вышеуказанных пунктов (1)-(7), включающий растворение гидрохлорида 5-хлор-6-(2-иминопирролидин-1-ил)метил-2,4(1H,3H)-пиримидиндиона в смешанном растворителе, содержащем воду и этанол, при нагревании, и кристаллизацию раствора при температуре 40°С или выше с последующим охлаждением.
(14) Фармацевтическая композиция, содержащая кристалл по любому из вышеуказанных пунктов (1)-(12) и фармацевтически приемлемый носитель.
Положительные эффекты изобретения
Кристалл I и Кристалл III типирацила гидрохлорида в соответствии с настоящим изобретением имеют превосходную стабильность при хранении. Таким образом, эти кристаллические формы являются значительно более превосходными по сравнению с другими формами с точки зрения, например, чистоты, обрабатываемости (более низкая гигроскопичность), текучести, измельчаемости и/или контроля качества, и могут быть использованы в виде кристаллических веществ, подходящих для фармацевтической композиции.
Кристалл I и Кристалл III по настоящему изобретению имеют описанный выше замечательный параметр стабильности при хранении по настоящему изобретению, сохраняя превосходную стабильность даже при контакте с теплом, светом, кислородом, влагой или другими молекулами (например, FTD). Кроме того, Кристалл I и Кристалл III по настоящему изобретению имеют превосходную фильтрующую способность, характеристики сушки и текучесть, и могут быть получены эффективным способом в промышленных масштабах.
Кроме того, Кристалл I по настоящему изобретению, в котором количество остаточного растворителя находится ниже эталонного значения, описанного в Руководстве по определению остаточных растворителей в рекомендациях ICH (Международная конференция по гармонизации технических требований к регистрации лекарственных препаратов для человека), является безопасным в качестве лекарственного средства. Кроме того, Кристалл I, имеющий меньшую величину электрического заряда, проще в обработке при производстве и упаковке лекарственных средств по сравнению с Кристаллом III.
Краткое описание чертежей
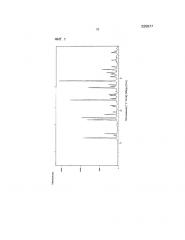
На фиг. 1 показана порошковая дифракционная рентгенограмма Кристалла I.
На фиг. 2 показана порошковая дифракционная рентгенограмма Кристалла II.
На фиг. 3 показана порошковая дифракционная рентгенограмма Кристалла III.
Описание вариантов осуществления
Кристалл I по настоящему изобретению в безводной форме может быть получен с высокой чистотой способом, в котором типирацила гидрохлорид (далее иногда называемый как "соединение (1)") растворяют в смешанном растворителе, содержащем воду и этанол, при нагревании, и раствор подвергают кристаллизации при температуре 40°С или выше, и затем охлаждают.
Соединение (1), для использования в способе кристаллизации по настоящему изобретению, может быть, например, соединение получено путем добавления соляной кислоты к свободному основанию соединения (1) в соответствии со способом, описанным в WO 96/30346. Соединение (1), предназначенное для использования, может быть после его синтеза в некристаллическом состоянии или быть выделено в виде кристаллов (неочищенных кристаллов). Тем не менее, для дальнейшего повышения чистоты кристаллов, соединение (1), получаемое в форме кристаллов, является предпочтительным. Кристаллы могут быть в любом виде, Кристалл I, Кристалл II, Кристалл III.
Соотношение составляющих в смеси растворителя, состоящего из воды и этанола, могут быть выбраны в зависимости от ситуации, и соотношение (объем/объем) воды и этанола, предпочтительно составляет от 1:1 до 1:10, более предпочтительно от 1:2 до 1:6, и особенно предпочтительно 1:4. Во время использования смешанного растворителя, состоящего из воды и этанола, предпочтительно, раствор, полученный растворением соединения (1) в воде с нагреванием, добавляют к этанолу в количестве, определенным таким образом, чтобы получить вышеуказанное соотношение. Концентрация соединения (1) конкретно не ограничивается, но предпочтительно составляет от 1 до 15% (масса/объем) в растворе соединения (1) в смеси вода-этанол.
Для получения Кристалла I с высокой чистотой, контроль температуры раствора соединения (1) в смеси вода-этанол в процессе кристаллизации является чрезвычайно важным. Температура раствора для кристаллизации составляет 40°С и выше, и предпочтительно от 44 до 63°С. Продолжительность кристаллизации может быть установлена в зависимости от обстоятельств. Когда температура является низкой, время может быть увеличено, а когда температура высокая, время может быть снижено. Например, время может быть установлено, равным 1,5 часа или больше при температуре в диапазоне от 44 до 50°С, и оно может быть установлено равным 0,5 часа или больше при температуре в диапазоне от 50 до 63°С. Принимая во внимание эффективность производства, раствор предпочтительно выдерживают при температуре от 44 до 55°С в течение от 1,5 до 7 часов (более предпочтительно от 1,5 до 3 часов), или при температуре от 50 до 63°С в течение от 0,5 до 7 часов (более предпочтительно в течение от 0,5 до 3 часов). Когда температура составляет 40°С или ниже, Кристалл II, который имеет низкую долговременную стабильность хранения, осаждается. Когда температура составляет 63°С или выше, количество продуктов распада соединения (1) является значительным, и соответственно, температура ниже 63°С является предпочтительной для эффективного получения Кристалла I, содержащего меньше примесей.
Соответствующее количество Кристалла I соединения (1) или смешанных кристаллов, содержащих Кристалл I, может быть добавлено в качестве затравочных кристаллов для ускорения кристаллизации. Количество добавляемого затравочного кристалла составляет от 0,01 до 5% (масса/объем) относительно количества растворителя и, предпочтительно, составляет от 0,03 до 1% (масса/объем). Смешанные кристаллы, содержащие Кристалл I, подразумевают смесь, содержащую 25% или больше Кристалла I. Кроме того, для уменьшения времени кристаллизации и контроля диаметра частиц, можно дать возможность протекать кристаллизации при перемешивании.
Авторы настоящего изобретения провели исследования сочетаний большого числа факторов, таких как рН, концентрация, температура и время перемешивания, которые могут оказать влияние на формирование Кристалла I соединения (1) при его производстве. В результате проб и ошибок, авторы изобретения обнаружили, что следующий способ является особенно предпочтительным с промышленной точки зрения, то есть, с точки зрения управления процессом, необходимого времени, чистоты кристаллов, воспроизводимости и т.д. Использование затравочного кристалла, безусловно, является необходимым. Предпочтительный способ получения Кристалла I подробно описан ниже. Кристалл I может быть получен способом, в котором кристаллы соединения (1) растворяют в воде при нагревании, раствор добавляют к этанолу так, чтобы соотношение (объем/объем) воды и этанола составляло от 1:1 до 1:10, и смесь перемешивают при температуре от 44 до 63°С, и затем охлаждают. Более предпочтительно, Кристалл I может быть получен способом, в котором кристаллы соединения (1) растворяют в воде при нагревании, раствор добавляют к этанолу так, чтобы соотношение (объем/объем) воды и этанола составляло 1:2-1:6, полученную смесь перемешивают при температуре от 44 до 50°С в течение от 1,5 до 7 часов или при температуре от 50 до 63°С в течение 0,5 до 7 часов, а затем охлаждают в течение 0,5 часа или более, и полученный Кристалл I собирают. Этот метод кристаллизации может эффективно продуцировать безводный Кристалл I соединения (1) высокой чистоты без влияния случайных факторов. Кроме того, в области химии известно, что получение нового превосходного кристалла, даже с большими стараниями, не может быть достигнуто, не полагаясь на удачу.
Кроме того, Кристалл III соединения (1) высокой чистоты может быть получен в соответствии с примером 2. Термин "высокая чистота", используемый в настоящем изобретении, означает, что, по крайней мере, 90% по массе, предпочтительно, 95% по массе и более предпочтительно 99% по массе кристаллов соединения (1) являются кристаллами по настоящему изобретению.
Термин "охлаждение", используемый в настоящем изобретении, означает, что температура раствора поддерживается на уровне 40°С или ниже, и, предпочтительно, при температуре 15°С или ниже. Время охлаждения предпочтительно составляет 0,5 часа или больше, и более предпочтительно 1 час или больше.
Выпавшие в осадок кристаллы могут быть выделены и очищены из вышеописанного раствора, где кристаллы растворены в растворителе или смешанном растворителе, известным способом выделения и очистки, такими как фильтрование, промывка органическим растворителем и сушка при пониженном давлении. Примеры органического растворителя, используемого для промывки, включают низшие спирты, ацетон и ацетонитрил.
Как показано на фиг. 1, порошковая дифракционная рентгенограмма полученного таким образом кристалла по настоящему изобретению (Кристалл I) показывает характерные пики при углах 11,6°, 17,2°, 17,8°, 23,3° 27,1° и 29,3°, в качестве дифракционного угла (2θ±0,1°). Таким образом, кристалл по настоящему изобретению (Кристалл I) представляет собой кристалл типирацила гидрохлорида, демонстрирующий пики при двух или более углах, выбранных из группы, состоящей из 11,6°, 17,2°, 17,8°, 23,3°, 27,1° и 29,3°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции. Кристалл предпочтительно представляет собой кристалл типирацила гидрохлорида, демонстрирующий пики при трех или более углах, выбранных из группы, состоящей из 11,6°, 17,2°, 17,8°, 23,3°, 27,1° и 29,3°, в качестве дифракционного угла (2θ±0,1°), и особенно предпочтительно кристалл типирацила гидрохлорида, демонстрирующий пики при углах, составляющих 11,6°, 17,2°, 17,8°, 23,3°, 27,1° и 29,3°, в качестве дифракционного угла (2θ°±0,1) в порошковой рентгеновской дифракции. Кроме того, результаты термогравиметрии и дифференциального термического анализа (TG/DTA) показывают эндотермический пик при температуре, равной около 262°C.
Напротив, как показано на фиг. 2, порошковая дифракционная рентгенограмма Кристалла II показывает характерные пики при углах 6,5°, 20,6°, 25,5°, 26,1°, 27,0° и 30,2°, в качестве дифракционного угла (2θ±0,1°). Кроме того, результаты TG/DTA не показывают определенный эндотермический пик.
Как показано на фиг. 3, порошковая дифракционная рентгенограмма Кристалла III показывает характерные пики при углах 10,5°, 19,6°, 23,7°, 26,2° и 31,2°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции. Таким образом, кристалл по настоящему изобретению (Кристалл III), является кристаллом типирацила гидрохлорида, демонстрирующим пики при двух или более углах, выбранных из группы, состоящей из 10,5°, 19,6°, 23,7°, 26,2° и 31,2°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции. Кристалл предпочтительно представляет собой кристалл типирацила гидрохлорида, демонстрирующий пики при трех или более углах, выбранных из группы, состоящей из 10,5°, 19,6°, 23,7°, 26,2° и 31,2°, в качестве дифракционного угла (2θ±0,1°), и особенно предпочтительно кристалл типирацила гидрохлорида, демонстрирующий пики при углах, составляющих 10,5°, 19,6°, 23,7°, 26,2° и 31,2°, в качестве дифракционного угла (2θ±0,1°) в порошковой рентгеновской дифракции. Кроме того, результаты TG/DTA показывают эндотермический пик при температуре, составляющей около 245°C.
Каждое значение пика в спектре порошковой рентгеновской дифракции может иметь погрешность, относящуюся к измерительному оборудованию или условиям измерения, таким как условия считывания пиков. При этом каждый пиковое значение может иметь погрешность измерения в диапазоне приблизительно ±0,2°.
Температура эндотермического пика (максимальное значение пика), измеренная в анализе TG/DTA, может изменяться в зависимости от повышения температуры в минуту, чистоты образца или тому подобного. Термин "примерно", используемый в настоящем документе, означает ±5,0°C.
Кристалл по настоящему изобретению обладает чрезвычайно высокой стабильностью при хранении, преимуществом в области контроля качества, а также превосходной пригодностью для обработки. В частности, как показано в примерах, описанных ниже, даже после длительного хранения в условиях высокой температуры и высокой влажности, Кристалл I и Кристалл III почти не содержали аналогичные вещества и не показали каких-либо изменений своих кристаллических форм. В противоположность этому, Кристалл II имеет недостаточную стабильность при длительном хранении, что является недостатком при его использовании в качестве лекарственного средства, и, соответственно, является нежелательным. Кристалл I по настоящему изобретению имеет преимущество относительно Кристалла III вследствие меньшего содержания остаточного растворителя и меньшего электрического заряда. Как показано в примерах, описанных ниже, Кристалл III содержит используемый для производства растворитель в количестве, большем, чем нормальное значение, указанное в Руководстве по определению остаточных растворителей в рекомендациях ICH, и, следовательно, является нежелательным в качестве лекарственного средства. В противоположность этому, Кристалл I содержит остаточный растворитель в количестве ниже нормального значения и имеет высокую безопасность, и, следовательно, является предпочтительным в качестве лекарственного средства. Кроме того, как показано в примерах, описанных ниже, Кристалл I, который имеет меньшую величину электрического заряда по сравнению с Кристаллом III, почти не прилипает к производственным машинам или упаковкам при производстве, упаковке и использованию лекарственных средств, что обеспечивает простоту производства и обработки.
Кристалл по настоящему изобретению может быть обработан непосредственно или после измельчения с получением фармацевтических композиций в различных формах, таких как пероральные препараты, включающие таблетки, капсулы, гранулы, мелкие гранулы, порошок и сухой сироп, препараты для местного применения, включающие суппозиторий, средство для ингаляции, назальные капли, мазь, пластырь и аэрозольное средство и инъекция. Кристалл, предпочтительно, используется для пероральных препаратов. Эти фармацевтические композиции могут быть получены с использованием фармацевтически приемлемого носителя способом, известным специалистам в данной области техники. При получении перорального твердого препарата, наполнитель и, при необходимости, связующее, разрыхлитель, смазывающее вещество, краситель, ароматизатор, маскирующее запах вещество и тому подобное, добавляют к активному ингредиенту, и затем таблетки, таблетки с покрытием, гранулы, порошок, сухой сироп, капсулы и тому подобное, могут быть получены обычным способом. При получении жидкого перорального препарата, ароматизатор, буфер, стабилизатор, маскирующее запах вещество и тому подобное, добавляют к активному ингредиенту, а затем пероральное жидкое лекарственное средство, сироп и т.п., могут быть получены обычным способом. При получении инъекции, к активному ингредиенту добавляют регулятор рН, буфер, стабилизатор, вещество, регулирующее тоничность, местный анестетик и т.п., и затем обычным способом могут быть получены подкожная инъекция, внутримышечная инъекция и внутривенная инъекция. При получении ректального суппозитория, к активному ингредиенту добавляют наполнитель и, при необходимости, поверхностно-активное вещество и т.п., и затем суппозиторий может быть получен обычным способом. При получении мази или препарата в форме, например, пасты, крема или геля, при необходимости, добавляют обычно используемые основу, стабилизатор, увлажняющее средство, консервант и тому подобное, и смешивают и получают обычным способом. В качестве основы могут быть использованы, например, белый вазелин, парафин, глицерин, производные целлюлозы, полиэтиленгликоль, силиконы, бентонит и тому подобное. В качестве консерванта можно использовать метилгидроксибензоат, этилгидроксибензоат, пропилпарагидроксибензоат и т.п. При производстве клейкого кожного пластыря, вышеуказанную мазь, крем, гель, пасту и т.п., наносят обычным способом на нормальный поддерживающий материал. В качестве поддерживающего материала используют ткани и нетканые материалы, содержащие хлопок, штапельное волокно и химическое волокна, а также пленки и вспененные тонкие листы, содержащие эластичный поливинилхлорид, полиэтилен и полиуретан.
Эти фармацевтические композиции могут быть использованы в качестве средства для усиления противоопухолевых эффектов трифтортимидина (FTD), средства для снижения побочных эффектов, вызванных химиотерапией, анти-ВИЧ активного средства, средства для лечения воспалительных заболеваний кишечника, а также средства для усиления эффектов лучевой терапии (WO 96/30346, WO 00/56337, WO 01/34162, WO 07/122812, WO 2008/001502).
Количество Кристалла I, смешиваемого в приведенной выше фармацевтической композиции, изменяется в зависимости от симптомов пациента, которому вводят композицию, формы препарата или тому подобного. По этой причине количество смешиваемого Кристалла I не является определенным, однако, обычно, в пероральном препарате Кристалл I желательно содержится в количестве примерно от 5 до 1000 мг, в инъекции желательно содержится в количестве примерно от 0,1 до 500 мг, и в суппозитории или в препарате для наружного применения желательно содержится в количестве примерно от 5 до 1000 мг на единицу дозирования. Аналогично, суточная доза Кристалла I в фармацевтической композиции также изменяется в зависимости от симптомов, способа введения, возраста пациента и тому подобного. Соответственно, доза не может быть определена в фиксированном виде и определяется в соответствии с предписанием врача. Обычно предпочтительная доза составляет примерно от 0,1 до 5000 мг.
Примеры
Способ получения по настоящему изобретению конкретно описан со ссылкой на нижеследующие примеры, ссылочные примеры, примеры исследований, однако настоящее изобретение ими не ограничивается.
После того, как соответствующее количество аналитического вещества незначительно измельчали, при необходимости, в агатовой ступке, данные порошковой рентгеновской дифракции измеряли в соответствии со следующими условиями исследований.
Мишень: Cu
Ток рентгеновской трубки: 40 мА
Напряжение рентгеновской трубки: 45 кВ
Диапазон сканирования: 2θ = 3,0-40,0°
Стадия: 2θ = 0,01671
Средняя продолжительность/стадия: 10,160 с
Изменяемая щель расходимости: радиационная длина = 15 мм
Исследование методом термогравиметрии и дифференциального термического анализа (TG/DTA) выполняли с использованием около 10 мг исследуемого вещества в соответствии со следующими условиями исследований.
Контейнер для образцов: контейнер из алюминия
Скорость возрастания температуры: через 5 мин при 25°C, 10°C/мин с 25 до 300°C.
Атмосферный газ: азот (100 мл/мин)
Контрольное вещество: α-оксид алюминия
Кроме того, ИК-спектры поглощения (IR) измеряли в соответствии со следующими условиями исследований.
Количество стадий интегрирования: 20 стадий
Разрешение: 2 см-1
Диапазон пропускания: 0-100%
Способ измерения: способ с использованием пластинки бромида калия
Пример 1
Получение Кристалла I типирацила гидрохлорида
(1) Сначала 100 мл 6н соляной кислоты и 220 мл воды смешивали, и в этой смеси растворяли 95,1 г типирацила, полученного в соответствии со способом, описанным в WO 96/30346, при нагревании. Раствор подвергали горячему фильтрованию при температуре, составляющей около 60°С, и затем добавляли 1280 мл этанола. Смесь выдерживали при температуре, составляющей около 60°С, в течение 2 часов при нагревании, и смесь охлаждали льдом. Полученные кристаллы отделяли фильтрованием, и таким образом получали 89,3 г безводного Кристалла I типирацила гидрохлорида (скорость восстановления: 82%). Порошковая дифракционная рентгенограмма полученного кристалла показала характеристические пики при углах 11,6°, 17,2°, 17,8°, 23,3°, 27,1° и 29,3°, в качестве дифракционного угла (2θ±0,1°), как и в случае с графическим изображением, представленным на фиг. 1. Кроме того, 1H-ЯМР спектр (ДМСО-d6, тетраметилсилан (TMS)) полученного кристалла показал, что количество остаточного этанола, содержащегося в кристаллах, было ниже контрольного значения (5000 частей на миллион), указанного в Руководстве по определению остаточных растворителей в рекомендациях ICH.
(2) Типирацила гидрохлорид, полученный в соответствии со способом, описанным в WO 96/30346, растворяли в воде при нагревании. Раствор подвергали горячему фильтрованию при температуре, составляющей около 60°С, а затем добавляли этанол и затравочный кристалл (Кристалл I), полученный в вышеописанном пункте (1). Смесь выдерживали при температуре, составляющей около 60°С, в течение 2 часов при нагревании. Полученные кристаллы отделяли фильтрованием и таким образом получали безводный Кристалл I типирацила гидрохлорида. Порошковая дифракционная рентгенограмма полученного кристалла показала характеристические пики при углах 11,6°, 17,2°, 17,8°, 23,3°, 27,1°, и 29,3°, в качестве дифракционного угла (29±0,1°), как показано на фиг. 1. Кроме того, результаты анализа TG/DTA показывают эндотермический пик при температуре 262,2°С.
Пример 2
Получение Кристалла III типирацила гидрохлорида
(1) В 20 мл 6н соляной кислоты и 230 мл воды растворяли 22,0 г типирацила, полученного в соответствии со способом, описанным в WO 96/30346,. Раствор фильтровали и затем концентрировали и добавляли 100 мл этанола при комнатной температуре. Полученные кристаллы отделяли фильтрованием и таким образом получали 19,7 г Кристалла III гидрохлорида типирацила (скорость восстановления: 78%). Порошковая дифракционная рентгенограмма полученного кристалла показала характеристические пики при углах 10,5°, 19,6°, 23,7°, 26,2° и 31,2°, в качестве дифракционного угла (2θ±0,1°), как и в случае с графическим изображением, представленным на фиг. 3. Кроме того, 1H-ЯМР спектр (ДМСО-d6, TMS) полученного кристалла показал, что количество этанола, содержащегося в кристаллах, составляло 16000 частей на миллион. Это значение превышает контрольное значение (5000 частей на миллион) для этанола, указанное в Руководстве по определению остаточных растворителей в рекомендациях ICH.
(2) Типирацил, полученный в соответствии со способом, описанным в WO 96/30346, растворяли в этаноле и добавляли концентрированную соляную кислоту. Смесь перемешивали при температуре 64°С в течение 1 часа и охлаждали до температуры 30°С. Полученные кристаллы отделяли фильтрованием и промывали метанолом и таким образом получали Кристалл III гидрохлорида типирацила. Порошковая дифракционная рентгенограмма полученного кристалла показала характеристические пики при углах 10,5°, 19,6°, 23,7°, 26,3°, и 31,3°, в качестве дифракционного угла (2θ±0,1°), как показано на фиг. 3. Кроме того, результаты анализа TG/DTA показывают эндотермический пик при температуре 245,1°С. Кроме того, результаты анализа полученного кристалла методом газовой хроматографии (парофазный метод) показывают, что количество метанола, содержащегося в кристаллах, составляло 49862 частей на миллион. Это значение превышает предельное значение концентрации (3000 частей на миллион) для этанола, описанное в Руководстве по определению остаточных растворителей в рекомендациях ICH.
Ссылочный пример 1
Получение Кристалла II типирацила гидрохлорида
(1) Сначала смешивали 50 мл 6н соляной кислоты и 500 мл воды, и в этой смеси растворяли 61,5 г типирацила, полученного в соответствии со способом, описанным в WO 96/30346. Раствор обрабатывали активированным углем, фильтровали и затем концентрировали, и добавляли 200 мл этанола при комнатной температуре. Полученные кристаллы отделяли фильтрованием, и таким образом получали 57,9 г содержащего воду Кристалла II типирацила гидрохлорида (скорость восстановления: 77%). Порошковая дифракционная рентгенограмма полученного кристалла показала характеристические пики при углах 6,5°, 20,6°, 25,5°, 26,1°, 27,0° и 30,2°, в качестве дифракционного угла (2θ±0,1°), как и в случае с графическое изображение, представленным на фиг. 2. Кроме того, 1H-ЯМР спектр (ДМСО-d6, ТМС), полученного кристалла показал, что количество остаточного этанола, содержащегося в кристаллах, было ниже контрольного значения (5000 частей на миллион), описанного в Руководстве по определению остаточных растворителей в рекомендациях ICH.
(2) Типирацила гидрохлорид, полученный в соответствии со способом, описанным в WO 96/30346, добавляли к воде и растворяли при температуре 60°С. Раствор фильтровали и затем добавляли к этанолу при охлаждении льдом. Полученные кристаллы отделяли фильтрованием и таким образом получали Кристалл II типирацила гидрохлорида. Порошковая дифракционная рентгенограмма полученного кристалла показала характеристические пики при углах 6,5°, 20,6°, 25,7°, 26,2°, 27,0° и 30,2°, в качестве дифракционного угла (2θ±0,1°), как показано на фиг. 2. Кроме того, результаты анализа TG/DTA не показывают определенный эндотермический пик.
Пример 3
Исследование стабильности
Кристалл I, Кристалл III и Кристалл II типирацила гидрохлорида, полученный в соответствии с примером 1, примером 2 и сравнительным примером 1 соответственно, подвергали исследованию на предмет стабильности хранении после хранения в течение шести месяцев при температуре 40°С.
Результаты показали, что Кристалл I, Кристалл II и Кристалл III являются чрезвычайно стабильными, поскольку на порошковой рентгеновской дифрактограмме кристаллов не было обнаружено каких-либо изменений. Кроме того, количество аналогичных веществ в Кристалле I и Кристалле III было небольшим и не увеличилось даже по истечении 6 месяцев.
В отличие от этого, порошковая дифракционная рентгенограмма Кристалла II не была аналогичной, показывая, что Кристалл II является нестабильной.
Пример 4
Анализ условий кристаллизации
Анализировали влияния температуры кристаллизации и времени кристаллизации на кристаллическую форму гидрохлорида типирацила на стадии очистки кристалла. В 240 мл воды растворяли 60 г кристаллов гидрохлорида типирацила, полученного в соответствии с примером 1, примером 2 или ссылочным примером 1, при нагревании. Раствор разделяли на три части и добавляли 320 мл этанола. Полученные образцы подвергали кристаллизации при различных температурах (от 32 до 63°С) и промежутках времени (от 0,5 до 3 часов). Кристаллические формы полученных кристаллов определяли методом ИК-спектроскопии и DSC (дифференциальной сканирующей калориметрии). Результаты представлены в таблице 1.
Результаты показывают, что Кристалл II, который имеет низкую стабильность при хранении, получали, когда температура кристаллизации была ниже 35°C. Когда температуру кристаллизации поддерживали при 44°С или выше, Кристалл I, который имеет высокую стабильность при хранении, эффективно получали с высокой чистотой.
| Таблица 1 | ||||
| Время кристаллизации | ||||
| 0,5 час | 1,5 час | 3 час | ||
| Температура кристаллизации | 60-63°C | Кристалл I | Кристалл I | Кристалл I |
| 44-50°C | Кристалл II |