Способ получения модифицированного фотокатализатора на основе диоксида титана
Иллюстрации
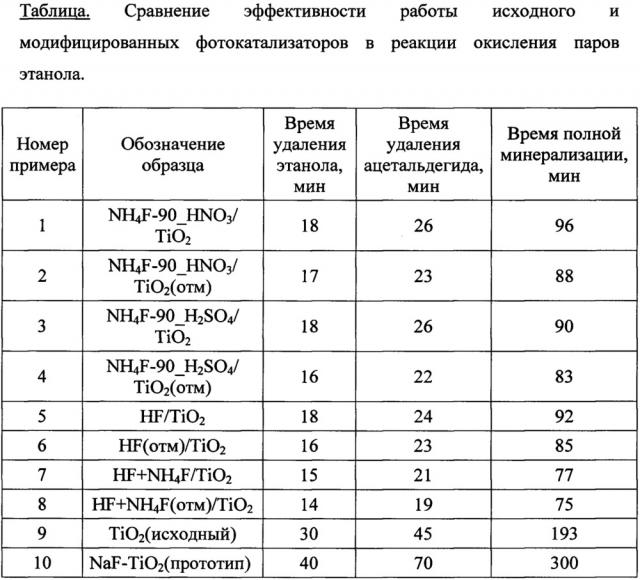
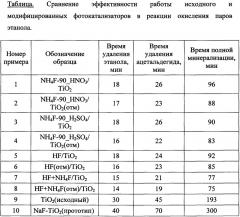
Показать всеИзобретение относится к области получения модифицированных фотокатализаторов для очистки воздуха. Предложен способ получения модифицированного фотокатализатора на основе диоксида титана для фотокаталитической очистки воздуха, заключающийся в том, что нанокристаллический порошок диоксида титана в анатазной модификации с удельной поверхностью свыше 300 м2/г подвергают обработке водным раствором фторсодержащего агента при мольном соотношении фторсодержащего агента и диоксида титана 0,09-0,11:1 с последующей обработкой полученной суспензии минеральной кислотой для достижения pH=4-4,5. Технический результат заключается в получении высокоактивного фотокатализатора, позволяющего сократить время, необходимое при очистке воздуха от летучих органических соединений (ЛОС) и от промежуточных продуктов неполного окисления в ходе фотокатализа, в 2 и более раз за счет увеличения скорости фотокаталитического окисления. 3 з.п. ф-лы, 1 табл., 10 пр.
Реферат
Изобретение относится к области разработки способа получения модифицированного фотокатализатора на основе диоксида титана. Фотокатализатор предназначен преимущественно для применения в фотокаталитической очистке воздуха от малых концентраций летучих органических соединений (ЛОС), присутствующих в воздухе в качестве нежелательных примесей в условиях атмосферных (или комнатных) температуры и влажности.
Воздух может быть загрязнен различными примесями, находящимися в твердом, жидком или газообразном агрегатном состоянии. Задачу очистки воздуха от гетерогенных примесей решают путем применения различных механических и электрических фильтров, циклонов, скрубберов. Для очистки воздуха от гомогенных (газообразных) примесей применяют в основном адсорбционный и каталитический способы. К недостаткам адсорбционного способа очистки можно отнести ограниченную емкость адсорбента, что в совокупности с закупориванием пор аэрозольными частицами приводит к необходимости регулярной замены адсорбента. Кроме того, поглотительная способность адсорбентов различна по отношению к различным веществам, что требует специального подбора адсорбента в зависимости от загрязнителей. В случае традиционных каталитических систем очистки воздуха их эффективное использование зачастую сопряжено с обеспечением относительно высокой температуры воздуха, что может оказаться невыгодно экономически, особенно при больших потоках очищаемого воздуха.
Указанные проблемы удается обойти при использовании фотокаталитических систем очистки воздуха, которые хорошо зарекомендовали себя при очистке больших объемов воздуха с небольшой концентрацией загрязнителей (на уровне ppm и ниже). Сущность фотокаталитической очистки заключается в одновременном образовании активных окислителей и восстановителей на поверхности широкозонного полупроводника, который и является фотокатализатором при облучении светом с энергией кванта выше ширины запрещенной зоны полупроводника. Затем образовавшиеся активные окислители и восстановители реагируют с адсорбированными молекулами загрязнителей и кислорода воздуха с образованием, в конечном итоге, углекислого газа и воды. Если загрязнитель содержит другие атомы, то они превращаются в менее токсичные неорганические формы.
Среди возможных фотокатализаторов наибольшее распространение получил диоксид титана (TiO2) благодаря сочетанию ряда свойств, таких как относительно высокая активность, стабильность, нетоксичность и низкая стоимость. Тем не менее из-за относительно большой ширины запрещенной зоны и значительной рекомбинации фотогенерированных носителей заряда общая фотокаталитическая эффективность TiO2 ограничена. Другой важной проблемой при использовании диоксида титана является образование вредных продуктов неполного окисления органических загрязнителей - формальдегида и ацетальдегида, а также, в меньшей степени, муравьиной и уксусной кислот [А.Т. Hodgson, D.Р. Sullivan, W.J. Fisk, Evaluation of Ultra-Violet Photocatalytic Oxidation (UVPCO) for Indoor Air Applications: Conversion of Volatile Organic Compounds at Low Part-per-Billion Concentrations, Report, LBNL-58936, 2005].
Для улучшения фотокаталитической активности TiO2 и повышения его эффективности, в том числе в видимом диапазоне, применяют различные способы модифицирования. Среди прочих можно особо выделить способы приготовления модифицированных катализаторов путем допирования диоксида титана ионами благородных металлов (Pd, Pt, Ru, Au, Ag,), приготовление композитов с полупроводниками или адсорбентами (TiO2-C, TiO2-SiO2, TiO2-ZnO, TiO2-CdS), а также допирование некоторыми неметаллами (N, S, C, B, I, F). Именно эти способы позволяют в том или ином аспекте улучшить эффективность очистки воздуха фотокаталитическим способом. Прочие подходы оказались в целом малоэффективны для реакций полного окисления [Н. Park, Y. Park, W. Kim, W. Choi, Surface modification of TiO2 photocatalyst for environmental applications, J. Photochem. Photobiol. C. 15 (2013) 1-20. doi:10.1016/j.jphotochemrev.2012.10.001] [1], хотя и позволяют для ряда специфичных реакций (преимущественно это реакции парциального окисления) добиться увеличения эффективности [P. Pichat, Photocatalysis and Water Purification. From Fundamentals to Recent Applications, WILEY-vch Verlag GmbH & Co. KGaA, 2013].
Описан способ получения комбинаций фотокатализатор-адсорбент [D.S. Selishchev, Р.А. Kolinko, D.V. Kozlov, Influence of adsorption on the photocatalytic properties of TiO2/AC composite materials in the acetone and cyclohexane vapor photooxidation reactions, J. Photochem. Photobiol. A. 229 (2012) 11-19. doi:10.1016/j.jphotochem.2011.12.006, RU 2478413], характеризующихся более высокой адсорбционной способностью, особенно на начальных стадиях процесса очистки воздуха. Данный способ позволяет быстро уменьшить концентрацию загрязнителей в начале процесса, но не позволяет значительно уменьшить концентрацию промежуточных продуктов неполного окисления в ходе фотокатализа.
Известен также способ получения фотокатализатора на основе диоксида титана, допированного платиной [RU 2614761, D.V. Kozlov, А.V. Vorontsov, Sulphuric acid and Pt treatment of the photocatalytically active titanium dioxide, J. Catal. 258 (2008) 87-94. doi:10.1016/j.jcat.2008.05.030]. Такой катализатор проявляет высокую скорость окисления по отношению к монооксиду углерода даже в условиях комнатной температуры и влажности и некоторым углеводородам [D.V. Kozlov, А.А. Panchenko, D.V. Bavykin, E.N. Savinov, P.G. Smirniotis, Influence of humidity and acidity of the titanium dioxide surface on the kinetics of photocatalytic oxidation of volatile organic compounds, Russ. Chem. Bull. 52 (2003) 1100-1105. doi:10.1023/A:1024796905146], но не способствует решению проблемы образования побочных продуктов окисления. К недостаткам этого способа можно также отнести высокую стоимость катализатора, получаемого этим способом.
В последние годы предпринимались значительные усилия по разработке способов получения диоксида титана, модифицированного неметаллами. Помимо экономической привлекательности [J. Schneider, М. Matsuoka, М. Takeuchi, J. Zhang, Y. Horiuchi, M. Anpo, et al., Understanding TiO2 Photocatalysis: Mechanisms and Materials, Chem. Rev. 114 (2014) 9919-9980. doi:10.1021/cr5001892], связанной с низкими затратами при получении, такие образцы перспективны с точки зрения возможности проводить фотокатализ при облучении видимым светом.
Ряд фотокатализаторов, способных проводить окислительные реакции под видимым светом, действительно был получен, например при допировании азотом [M.V. Dozzi, Е. Selli, Doping TiO2 with p-block elements: Effects on photocatalytic activity, J. Photochem. Photobiol. C. 14 (2013) 13-28. doi:10.1016/j.jphotochemrev.2012.09.002], или углеродом [US 7524793 (B2), US 2012270028 (A1)], однако общая эффективность таких катализаторов (при облучении как видимым, так и ультрафиолетовым светом) зачастую оказывается существенно ниже, чем у недопированного диоксида титана [M.V. Dozzi, Е. Selli, Doping TiO2 with p-block elements: Effects on photocatalytic activity, J. Photochem. Photobiol. C. 14 (2013) 13-28. doi:10.1016/j.jphotochemrev.2012.09.002].
Более интересные результаты были получены при использовании диоксида титана, допированого фтором. Так, в присутствии фторид-ионов наблюдали увеличение скорости окисления фенола в растворе [С. Minero, G. Mariella, V. Maurino, Е. Pelizzetti, Photocatalytic Transformation of Organic Compounds in the Presence of Inorganic Anions. 1. Hydroxyl-Mediated and Direct Electron-Transfer Reactions of Phenol on a Titanium Dioxide-Fluoride System, Langmuir. 16 (2000) 2632-2641. doi:10.1021/la9903301]. Кроме того, сообщалось о повышении фотокаталитической активности допированных образцов даже для загрязнителя (ацетона) в газовой фазе [J. Yu, J. Zhang, A simple template-free approach to TiO2 hollow spheres with enhanced photocatalytic activity., Dalton Trans. 39 (2010) 5860-5867. doi:10.1039/c0dt00053a, Q. Xiang, K. Lv, J. Yu, Pivotal role of fluorine in enhanced photocatalytic activity of anatase TiO2 nanosheets with dominant (0 0 1) facets for the photocatalytic degradation of acetone in air, Appl. Catal. В Environ. 96 (2010) 557-564. doi:10.1016/j.apcatb.2010.03.020]. К недостатком указанных способов можно отнести наличие относительно длительной и энергозатратной стадии гидротермального созревания катализаторов (12-24 ч при температуре 180°C). К тому же в описанных выше случаях не указана влажность воздуха, при которой проводилось измерение фотокаталитической активности, хотя хорошо известно, что этот фактор оказывает очень сильное влияние на скорость фотокаталитического окисления [T.N. Obee, R.T. Brown, TiO2 Photocatalysis for Indoor Air Applications: Effects of Humidity and Trace Contaminant Levels on the Oxidation Rates of Formaldehyde, Toluene, and 1,3-Butadiene, Environ. Sci. Technol. 29 (1995) 1223-1231. doi:10.1021/es00005a013].
Описан также другой способ получения модифицированного фотокатализатора на основе диоксида титана, допированного фтором, который может применяться для создания самоочищающихся поверхностей, антибактериальных поверхностей, противозапотевающего действия а также для очистки воздуха [пат. US 6074981]. Предложенный способ заключается в смешении растворимых соединений титана, замещенных или незамещенных алкоксидов титана (IV) и фторирующего агента, например трифторуксусной кислоты, NH4F или плавиковой кислоты на первом этапе, с последующим нанесением полученной смеси на подложку (стеклянные или кварцевые пластины, минеральное волокно) путем погружения подложки в указанный раствор и ее постепенным извлечением (со скоростью 3-6 см/мин) на втором этапе и заключительном отжиге при температуре 500°C. Полученное таким способом фторсодержащее фотокаталитическое покрытие в несколько раз эффективнее при окислении пленки 1,3,5,7-тетраметилтетрасилоксана по сравнении с фотокаталитическим покрытием из чистого TiO2. Главным и очевидным недостатком этого способа является наличие стадии высокотемпературного отжига, что помимо технологической сложности приводит к существенному снижению удельной площади поверхности фотокатализатора, что влечет за собой и снижение его активности. Другим недостатком является использование алкоксидов титана - относительно дорогих соединений по сравнению с неорганическими источниками титана.
Описанные выше способы достаточно трудоемки. Кроме того, положительный эффект зачастую проявляется слабо или же этот эффект проявляется в условиях, далеких от условий атмосферного и комнатного воздуха. В подавляющем большинстве случаев предложенные способы представляют собой способы непосредственного синтеза диоксида титана из прекурсора, а не способы модифицирования готового к использованию диоксида титана. В последнем случае отпадает необходимость в проведении таких типичных для получения диоксида титана стадий, как гидролиз прекурсора в гидротермальных условиях или вызревание золь-геля с его последующей сушкой и прокаливанием, что существенно сокращает время получения улучшенного катализатора.
Известен способ получения модифицированного фотокатализатора на основе диоксида титана, допированного фтором, принятый за прототип [H. Kim, W. Choi, Effects of surface fluorination of TiO2 on photocatalytic oxidation of gaseous acetaldehyde, Appl. Catal. В Environ. 69 (2007) 127-132. doi:10.1016/j.apcatb.2006.06.011], заключающийся на первом этапе в приготовлении смеси из диоксида титана и водного раствора полиэтиленгликоля с массовым содержанием TiO2 20%, нанесением полученной смеси тонким слоем на стеклянную подложку и прокаливании при 450°C. На втором этапе подложку с прокаленной смесью помещали на 30 минут в раствор NaF (концентрация 10-30 ммоль/л) с pH, предварительно доведенным до значения 3,5 с помощью HCl, и затем высушивали на воздухе. Известный фотокатализатор, полученный по известному способу, недостаточно активный при очистке воздуха от летучих органических соединений (ЛОС). Указанный способ позволяет в несколько раз снизить адсорбционную емкость по ацетальдегиду для модифицированного образца, что приводит к меньшему времени, необходимому для окисления предварительно адсорбированного ацетальдегида на таком образце по сравнению с немодифицированным образцом. Примечательно при этом, что в проточном режиме работы при условиях, когда степень конверсии ацетальдегида составляет величину ~50% модифицированный и немодифицированный фотокатализаторы имеют практически равную эффективность (в пределах 7-10%), что говорит, что в случае практического применения модифицированного таким способом фотокатализатора выгода от его использования будет минимальной, что безусловно относится к недостатком этого способа модифицирования. Таким образом, недостатком известного способа получения модифицированного фотокатализатора на основе диоксида титана является недостаточно высокая фотокаталитическая активность катализатора и трудоемкость и энергозатратность процесса его получения (использование полиэтиленгликоля в смеси с TiO2 для создания пасты, обладающей адгезионными свойствами, а также наличие стадии высокотемпературного отжига при температуре 450°C).
Подводя итог имеющемуся уровню техники, можно заключить, что несмотря на интенсивные исследования в данной области не удалось добиться того, чтобы способ получения модифицированного диоксида титана удовлетворял одновременно нескольким требованиям: обеспечивал получение высокоактивного фотокатализатора, т.е. быстро удаляющего из воздуха уже присутствующие в нем вредные вещества (ЛОС) и обеспечивающего существенный прогресс в решении проблемы образования нежелательных промежуточных продуктов в процессе использования фотокатализатора-формальдегида и ацетальдегида в условиях атмосферного и/или комнатного воздуха, а также был относительно прост в техническом исполнении, не включал в себя длительные и энергозатратные стадии, например отжиг при высокой температуре, и недорогостоящим в реализации.
Технической задачей предлагаемого изобретения является разработка способа получения высокоактивного фотокатализатора на основе диоксида титана для очистки воздуха, а также упрощение технологии его получения и удешевление процесса.
Поставленная техническая задача достигается предлагаемым способом получения модифицированного фотокатализатора на основе диоксида титана для фотокаталитической очистки воздуха, заключающимся в том, что нанокристаллический порошок диоксида титана в анатазной модификации с удельной поверхностью свыше 300 м2/г подвергают обработке водным раствором фторсодержащего агента при мольном соотношении фторсодержащего агента и диоксида титана 0,09-0,11:1 с последующей обработкой полученной суспензии минеральной кислотой для достижения pH=4-4,5.
В качестве фторсодержащего агента используют, преимущественно, фторид аммония, или плавиковую кислоту, либо их смесь, взятую в мольном соотношении 0,23-0,25:1 соответственно.
В качестве минеральной кислоты используют, например, азотную, или серную, или плавиковую кислоту.
С целью дополнительного увеличения активности и эффективности полученного катализатора его промывают дистиллированной водой.
Предлагаемый способ характеризуется тем, что коммерчески доступный, готовый для применения диоксид титана в анатазной модификации с высокой удельной поверхностью (свыше 300 м2/г) обрабатывают водным раствором фторсодержащего агента, при этом окончание обработки проводят при pH 4-4,5. В результате реализации предлагаемого способа получен высокоактивный фотокатализатор. Данные активности полученного фотокатализатора приведены в таблице и на чертеже.
В качестве исходного фотокатализатора для проведения модифицирования хорошо подходят образцы TiO2 анатазной модификации с высокой удельной поверхностью - 300 м2/г или более, хотя не исключается использование образцов рутила, смесей рутила с анатазом.
Таким образом, совокупность предложенных признаков способа, таких как обработка нанокристаллического порошка диоксида титана в анатазной модификации с удельной поверхностью свыше 300 м2/г водным раствором фторсодержащего агента при мольном соотношении фторсодержащего агента и диоксида титана 0,09-0,11:1 с последующей обработкой полученной суспензии минеральной кислотой для достижения pH=4-4,5, позволяет получить высокоактивный фотокатализатор, способный увеличить скорость фотокаталитического окисления как ЛОС, так и промежуточных продуктов неполного окисления в ходе фотокатализа в 2 и более раз. При этом предложенный способ не требует применения дорогостоящих веществ и материалов и остается простым в исполнении (отсутствует стадия, например, высокотемпературного отжига).
Сущность изобретения иллюстрируется в описанных ниже примерах. В качестве исходного TiO2 использовался диоксид титан в модификации анатаз, марки Hombikat UV-100 (Sachtleben chemie), с удельной поверхностью 300 м2/г. Характеристики других использованных реагентов: плавиковая кислота, HF - осч 27-5 (ООО «НПФ ЛК»), фторид аммония, NH4F - осч (Реахим), кислота азотная, HNO3 - хч. фторид натрия - чда (Реахим), серная кислота - хч (Вектон). Уровень pH измеряли с помощью универсальной индикаторной бумаги.
Пример 1.
Фторид аммония в количестве 90 мг (2,43 ммоль) растворили в 60 мл дистиллированной воды, затем прибавили в этот раствор 2,0 г диоксида титана (25,1 ммоль). К полученной суспензии по каплям, при перемешивании добавили разбавленную азотную кислоту (0,6% масс.) до достижения pH=4. Общее количество добавленной кислоты составило 4,5 мл. Тщательно перемешав, суспензию оставили отстаиваться в течение 30 минут. Затем маточный раствор над осадком (~50 мл) слили методом декантации, оставшуюся смесь высушили в токе воздуха при комнатной температуре. Полученный катализатор обозначили как NH4F-HNO3/TiO2.
Пример 2.
Получение катализатора проводили, как описано в примере 1, с тем отличием, что к осадку, полученному после сливания маточного раствора, добавили 200 мл дистиллированной воды. После этого суспензию вновь тщательно перемешали и оставили отстаиваться в течение 3-х часов. После отстаивания маточный раствор (~170 мл) слили с осадка методом декантации, оставшуюся смесь высушили в токе воздуха при комнатной температуре. Полученный катализатор обозначили как NH4F-HNO3/TiO2 (отм).
Пример 3.
Получение катализатора проводили, как описано в примере 1, с тем отличием, что на стадии добавления минеральной кислоты использовали раствор не азотной, а серной кислоты (0,6% масс.). Потребовалось 7,0 мл такого раствора Полученный катализатор обозначили как NH4F-H2SO4/TiO2.
Пример 4.
Получение катализатора проводили. как описано в примере 3, с тем отличием, что к осадку, полученному после сливания маточного раствора в примере (выше), добавили 200 мл дистиллированной воды. После этого суспензию вновь тщательно перемешали и оставили отстаиваться в течение 3-х часов. После отстаивания маточный раствор (~170 мл) слили с осадка методом декантации, оставшуюся смесь высушили в токе воздуха при комнатной температуре. Полученный катализатор обозначили как NH4F-H2SO4/TiO2 (отм).
Пример 5
Приготовили суспензию из 20,0 г диоксида титана (251 ммоль) и 200 мл дистиллированной воды. К суспензии при постоянном перемешивании добавили 9 мл 5%-ного раствора HF (22,8 моль). Затем к суспензии медленно добавляли более разбавленный раствор плавиковой кислоты до достижения pH 4. Для этого потребовалось 4,2 мл 0,6% раствора HF. После отстаивания маточный раствор (~120 мл) слили с осадка методом декантации, оставшуюся смесь высушили в токе воздуха при комнатной температуре. Полученный катализатор обозначили как HF/TiO2.
Пример 6.
Катализатор готовили, как указано в примере 5. После сливания маточного раствора к осадку добавили 400 мл дистиллированной воды. После этого суспензию вновь тщательно перемешали и оставили отстаиваться в течение 3-х часов. После отстаивания маточный раствор слили с осадка методом декантации, оставшийся осадок высушили в токе воздуха при комнатной температуре. Полученный катализатор обозначили как HF (отм)/TiO2.
Пример 7.
Приготовили суспензию из 20,0 г диоксида титана (251 ммоль) и 200 мл дистиллированной воды. К суспензии при постоянном перемешивании добавили 9 мл 5%-ного раствора плавиковой кислоты (22,8 ммоль). Затем к полученной смеси добавили 190 мг фторида аммония (5,1 ммоль) в виде 10 мл водного раствора. После этого к смеси при перемешивании малыми порциями добавляли плавиковую кислоту (1% раствор) до достижения pH 4,0. На этой стадии потребовалось 4 мл 1%-ного раствора HF. Тщательно перемешав, суспензию оставили отстаиваться в течение 30 минут. Затем маточный раствор над осадком (~120 мл) слили методом декантации, оставшуюся смесь высушили в токе воздуха при комнатной температуре. Полученный катализатор обозначили как HF+NH4F/TiO2.
Пример 8.
Приготовили суспензию из 20,0 г диоксида титана (251 ммоль) и 200 мл дистиллированной воды. К суспензии при постоянном перемешивании добавили 9 мл 5%-ного раствора плавиковой кислоты (22,8 ммоль). Затем к полученной смеси добавили 190 мг фторида аммония (5,7 ммоль) в виде 10 мл водного раствора. После этого к смеси при перемешивании малыми порциями добавляли плавиковую кислоту (1% раствор) до достижения pH 4,5. На этой стадии потребовалось 4 мл 1%-ного раствора HF. Тщательно перемешав, суспензию оставили отстаиваться в течение 30 минут. Затем маточный раствор над осадком (~120 мл) слили методом декантации. После сливания маточного раствора к осадку добавили 400 мл дистиллированной воды. После этого суспензию вновь тщательно перемешали и оставили отстаиваться в течение 3-х часов. После отстаивания маточный раствор слили с осадка методом декантации, оставшуюся смесь высушили в токе воздуха при комнатной температуре. Полученный катализатор обозначили как HF+NH4F (отм)/TiO2.
Пример 9. (сравнительный).
Использовали порошок диоксида титана в модификации анатаз, марки Hombikat UV-100 (Sachtleben chemie), с удельной поверхностью 300 м2/г.
Пример 10. Фотокатализатор, полученный по прототипу (сравнительный).
200 мг диоксида титана смешали с 1 мл 50%-ного водным раствора полиэтиленгликоля, затем нанесли полученную смесь ровным слоем на внутренную поверхность чашки Петри и высушили на воздухе. После этого чашку Петри с нанесенной смесью выдерживали при температуре 450°C в течение 30 мин. Чашку Петри с прокаленной смесью поместили на 30 мин в водный раствор фторида натрия с концентрацией 30 ммоль/л и pH, предварительно доведенным до 3.5 с помощью HCl, и затем высушили на воздухе. Полученный катализатор обозначили как NaF-TiO2 (прототип). Каталитические эксперименты проводились в герметичном пластиковом боксе, снабженном УФ и ИК-прозрачными стеклами для облучения образца и in-situ регистрации ИК-спектров газовой фазы соответственно. Образцы (200 мг катализатора, нанесенных на чашку Петри диаметром 60 мм) облучались флуоресцентной ртутной лампой (λUVmax=365 нм, I=5 мВт/см2). Перед проведением фотокаталитической реакции влажность воздуха внутри устанавливалась в пределах 37.5±0.5% относительной влажности при температуре 20.0±0.5°C. Этанол (96%) объемом 1 мкл, что соответствует концентрации 150 ppm, вводился в камеру бокса с помощью микрошприца. За изменением концентраций этанола и продуктов реакции следили по ИК-спектрам газовой фазы.
Основные результаты проведенных испытаний представлены на чертеже и в таблице. На чертеже показаны кинетические кривые образования и удаления ацетальдегида в ходе фотокаталитического окисления паров этанола на катализаторах, описанных в сравнительных примерах 9 (кривая 1) и 10 (кривая 2), а также в предлагаемых примерах 1 (кривая 3) и 8 (кривая 4). В таблице представлены данные об эффективности катализаторов в фотокаталитическом окислении паров спирта и побочных продуктов неполного окисления для всех полученных катализаторов показывает столбец 3. Столбец 4 показывает время, необходимое для полного удаления из газовой фазы ацетальдегида, а столбец 5 – время, необходимое для полного удаления из газовой фазы других полупродуктов (преимущественно уксусная и муравьиная кислота).
Из сравнения данных, представленных в таблице, можно видеть, что все модифицированные образцы (№№1-8) существенно сокращают время присутствия ацетальдегида в газовой фазе. При этом в соответствии с рисунком и таблицей можно видеть, что пиковая концентрация ацетальдегида если и возрастает, то не более чем на 10%. Для всех модифицированных образцов время присутствия ацетальдегида в газовой фазе сокращается приблизительно вдвое, что свидетельствует о существенном прогрессе в борьбе с альдегидными полупродуктами, так как концентрации формальдегида и ацетальдегида хорошо коррелируют в процессе фотокаталитического окисления [А.Т. Hodgson, D.P. Sullivan, W.J. Fisk, Evaluation of Ultra-Violet Photocatalytic Oxidation (UVPCO) for Indoor Air Applications: Conversion of Volatile Organic Compounds at Low Part-per-Billion Concentrations, Report, LBNL-58936, 2005]. Меньшая эффективность образца NaF-TiO2 (прототип), полученного способом, взятым за прототип, даже по сравнению с немодифицированным диоксидом титана вызвана, по-видимому, рядом причин, указанных ранее. Однако не менее важно и то, что все модифицированные образцы сокращают время, необходимое для превращения этанола в воду и углекислый газ (см. столбец 5 таблица). Говоря иными словами, увеличивают скорость полного фотокаталитического окисления в 2 и более раз.
Техническим результатом предлагаемого изобретения является получение высокоактивного фотокатализатора предложенным способом, позволяющего сократить время, необходимое при очистке воздуха как от летучих органических соединений (ЛОС), так и от промежуточных продуктов неполного окисления в ходе фотокатализа в 2 и более раз за счет увеличения скорости фотокаталитического окисления. При этом предложенный способ не требует применения дорогостоящих веществ и материалов и остается простым в исполнении.
1. Способ получения модифицированного фотокатализатора на основе диоксида титана для фотокаталитической очистки воздуха, заключающийся в том, что нанокристаллический порошок диоксида титана в анатазной модификации с удельной поверхностью свыше 300 м2/г подвергают обработке водным раствором фторсодержащего агента при мольном соотношении фторсодержащего агента и диоксида титана 0,09-0,11:1 с последующей обработкой полученной суспензии минеральной кислотой для достижения рН=4-4,5.
2. Способ получения модифицированного фотокатализатора по п. 1, отличающийся тем, что в качестве фторсодержащего агента используют фторид аммония или плавиковую кислоту либо их смесь, взятую в мольном соотношении 0,23-0,25:1 соответственно.
3. Способ получения модифицированного фотокатализатора по п. 1, отличающийся тем, что в качестве минеральной кислоты используют азотную, или серную, или плавиковую кислоту.
4. Способ получения модифицированного фотокатализатора по п. 1, отличающийся тем, что полученный фотокатализатор дополнительно промывают дистиллированной водой.