Способ биомиметического синтеза sr - содержащего карбонатгидроксилапатита, модифицированного брушитом
Иллюстрации
Показать всеИзобретение относится к области медицины. Описан способ биомиметического синтеза Sr-содержащего карбонатгидроксилапатита, модифицированного брушитом, приближенного к неорганическому матриксу кости, из модельного раствора синовиальной жидкости человека, включающий получение неорганического вещества, в искусственно созданной среде для этого готовят модельную среду указанного состава: CaCl2 - 0,67155 г/л, Na2HPO4⋅12H2O - 7,4822 г/л, NaCl - 2,8798 г/л, NaHCO3 - 2,0160 г/л, MgCl2⋅6H2O - 0,4764 г/л, Na2SO4 - 1,6188 г/л, KCl - 0,3427 г/л и дистиллированной воды, при этом концентрация ионов Sr должна составлять, 0,6715 г/л, проводят осаждение при значении pH 7.4 в течение 21 дня. Полученный осадок фильтруют, сушат при температуре 100°C в течение 4 часов. Материал может быть использован при лечении больных, страдающих остеопорозом и принимающих Sr-содержащие препараты. 2 ил., 2 табл.
Реферат
Изобретение относится к области медицины и созданию новых материалов биомедицинского назначения, а именно к способам получения смесей фосфатов кальция (ФК), которые являются биологически активными соединениями. Материалы на основе фосфатов кальция широко применяются для создания новых керамических, композиционных материалов, цементных масс и лечебных паст для травматологии, ортопедии, челюстно-лицевой хирургии и стоматологии, для регенерации поврежденных костных тканей посредством постепенного замещения материала новообразующейся костной тканью.
Известен способ получения наноразмерного порошка для биоматериалов на основе системы ГА - карбонат кальция (патент РФ №2440149). В прототипе двухфазные смеси получали в результате химического осаждения из водных растворов гидрокарбоната и гидрофосфата аммония и водного раствора, содержащего взвесь гидроксида кальция, с последующей промывкой в этаноле, фильтрованием и сушкой до удаления жидкой фазы. Согласно изобретению сразу после осаждения порошок подвергают старению в маточном растворе в течение не менее 14 суток. В результате получают продукт состава 75÷85 масс. % ГА и 15÷25 масс. % карбоната кальция, характеризующийся площадью удельной поверхности не менее 210 г/м2.
К недостаткам данного технического решения можно отнести наличие фазы CaCO3, которая, как известно, не является составляющей нормальной костной ткани, трудность регулирования состава смеси и площади удельной поверхности и растворимости.
Наиболее близким по технической сущности к заявляемому является способ получения Sr-замещенного гидроксилапатита (Terra J, Dourado E.R., Eon J.G., Ellis D.E., Gonzalez G., Rossi A.M. The structure of strontium-doped hydroxyapathe: an experimental and theoretical study // Phys Chem Chem Phys. 2009 Jan 21; 11 (3): 568-77). По данному способу образцы стронция-замещенного гидроксилапатита, были синтезировали с помощью добавления в водный раствор, содержащий Ca (NO3)2 и Sr (NO3)2 по каплям (NH4)2HPO4 при скорости потока 5 мл /мин и температуре 90°C. Значение pH 10 поддерживалась NH4OH. После осаждения суспензию выдерживали в течение 3 ч.
Осадок затем отделяли фильтрованием и многократно промывали кипящей деионизированной водой и сушили при 100°C.
Способ позволяет получать нанокристаллы Sr-содержащего гидроксилапатита с различным содержанием стронция в гидроксилапатите. К недостаткам метода следует отнести отсутствие возможности получения смесей Sr-содержащего карбонатгидроксил апатита и брушита, синтез проводится при значении рН 10, исключающем образование кристаллов брушита.
Задачей заявляемого изобретения является разработка биомиметического синтеза порошкового материала на основе Sr-содержащего карбонатгидроксиапатита, модифицированного брушитом, который в дальнейшем может быть использован для адресной доставки лекарственных средств.
Указанный технический результат обеспечивается тем, что предложен способ биомиметического синтеза Sr-содержащего карбонатгидроксилапатитом, модифицированного брушитом, приближенного к неорганическому матриксу кости, из модельного раствора синовиальной жидкости человека, включающий получение неорганического вещества в искусственно созданной среде, для приготовления которого используют дистиллированную воду, CaCl2 - 0,6715 г/л, Na2HPO4⋅12H2O - 7,4822 г/л, NaCl - 2,8798 г/л, NaHCO3 - 2,0160 г/л, MgCl2⋅6H2O - 0,4764 г/л, Na2SO4 - 1,6188 г/л, KCl - 0,3427 г/л и SrCl2⋅6H2O в количестве, обеспечивающем концентрацию ионов Sr - 0,6715 г/л, проводят осаждение при значении рН 7.4, в течение 21 дня, полученный осадок фильтруют, сушат при температуре 100°C в течение 4 часов.
Синовиальная жидкость является биологической средой, уникальной по биофизическим, физико-химическим свойствам и составу и выполняет в суставах ряд функций: метаболическую (обменную), барьерную (защитную), протекторную (биомеханическую). Метаболическая функция синовиальной жидкости играет большую роль в лечении больных с костными патологиями, выполняя роль носителя различных неорганических и органических ионов, которые могут встраиваться в структуру костного апатита и способствовать изменению его биофизических, структурных и морфологических особенностей. Так в последнее время на основании экспериментальных и клинических исследований были получены доказательства того, что соединения стронция и препараты на его основе стимулируют процесс образования костной ткани, подавляют процесс ее разрушения.
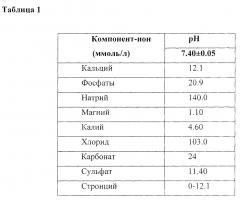
Синтез Sr-содержащего карбонатгидроксилапатита осуществлялся из модельной среды, приближенной по ионно-электролитному составу, рН, ионной силы к синовиальной жидкости человека. Осаждение из растворов проводилось при значении рН 7.4, что соответствует физиологическому значению кислотности синовии в норме [Лунева С.Н. Биохимические изменения в тканях суставов при дегенеративно-дистрофических заболеваниях и способы биологической коррекции: Дис. … д-ра биол. наук. Курган. 2003. 297 с.]. При этом корректировка pH до требуемых физиологических значений осуществлялась путем добавления 20%-ного раствора NaOH или концентрированной НО. Данные концентрационные диапазоны соответствуют содержанию ионов в синовиальной жидкости человека [Кирсанов А.И. Концентрация химических элементов в разных биологических средах человека. Клиническая лабораторная диагностика. 2001. №3. С. 16-20]. При этом содержание остальных минеральных составляющих соответствовали таковым для синовиальной жидкости человека. Средние концентрации неорганических ионов синовиальной жидкости человека при разных значениях pH, ммоль/л приведены в таблице 1.
Для приготовления модельных растворов использовались соли (CaCl3, Na2HPO4⋅12H2O, MgCl2⋅6H2O, NaHCO3, Na2SO4, KCl, NaCl, SrCl2⋅6H2O) марки ч.д.а, х.ч. и дистиллированная вода. Соли и их количество подбирались таким образом, чтобы концентрации их ионов в растворе и ионная сила были максимально приближены к данным параметрам моделируемой системы, а именно синовиальной жидкости. Для получения порошкового материала на основе Sr-содержащего карбонатгидроксиапатита и брушита в модельные опыты добавляли ионы стронция 50% от максимально возможной концентрации ионов кальция. В качестве источников ионов Sr2+ были использованы неорганическая соль SrCl2*6H2O. Кристаллизация твердой фазы осуществлялась в течение 21, 28 дней. Осадок высушивали при температуре ~100°C. Синтетические твердые фазы исследовали с применением комплекса физико-химических методов: РФА (D8 Advance, Bruker; программа TOPAS 3.0 (Bruker) - количественный фазовый анализ поликомпонентных образцов, расчет размеров кристаллитов (областей когерентного рассеяния - ОКР)). Идентификация фаз выполнялась с применением базы данных ICDD PDF для порошковой дифракции; ИК-Фурье-спектроскопия (Фурье-спектрометры IRPrestige-21, «Shimadzu», таблетки с KBr); элементный состав продуктов синтеза определен методом атомно-эмиссионого анализа (Varian 710-ES «Agilent Techologies»).
В полученных твердых фазах с помощью атомно-эмиссионого анализа было определено содержание ионов стронция. Результаты этого анализа показывают, что в состав полученных образцов входит стронций. При этом содержание ионов стронция в осадках коррелирует с фазовым составом полученных твердых фаз. Для определения качественного состава синтезированного материала использовалась ИК-спектроскопия.
На фиг. 1 представлены ИК-спектры для образцов порошков 1 и 2, полученных при времени синтеза - 21 день и 28 дней соответственно.
Все ИК-спектры полученных порошков характеризуются наличием полос валентных колебаний OH-групп в области длин волн 3570-3730 см-1 и деформационных колебаний при 3000-3600 см-1 - О-Н групп, участвующих в образовании водородных связей. Можно также отметить полосы деформационных колебаний υ4 О-Р-О в РО43- 640-550 см-1, асимметричных валентных колебаний υ3 P-O в РО43- 1060-1030 см-1, деформационных колебаний O-C-O в СО32- 870-879 см-1. Установлено, что карбонат-ионы включены в структуру гидроксилапатита в позиция гидроксильных групп (OH-) свидетельствует о том, что результатом синтеза является карбонатгидроксилапатит A-типа.
На фиг. 2 представлены результаты РФА для образцов порошков 1 и 2, полученных при времени синтеза - 21 день и 28 дней соответственно. По данным РФА обнаружены пики O - брушита - OCaHPO4(H2O)2 с моноклинной решеткой (пр. группа Ia(9)) и пики * - гидроксилапатита, широкие рефлексы плохо окристаллизованной фазы со структурой, близкой к гексагональной структуре.
Гидроксилапатит, как известно, относится к пространственной группе Р 63/m (176) с параметрами решетки , (01-074-0565). Так как в исходный состав синовиальной жидкости входят карбонат-ионы, то можно предположить, что образующееся соединение может являться Sr-Ca-карбонат-фосфат-гидратом с возможной формулой Ca8-nSrnH2(PO)4⋅6H2O⋅NaHCO3⋅H2O. Что касается фазы брушита, то здесь можно отметить следующее: кроме того, что в образцах присутствует текстурирование в направлении [010], наблюдается размытие пиков с увеличением угла дифракции выше 30°. Для образца, синтезированного через 28 дней, пики брушита на рентгенограмме не наблюдаются, присутствуют только пики фазы по структуре, близкой к гидроксилапатиту, с параметрами кристаллической решетки , . Полученные рентгенографические данные указывают на то, что при замещении Ca на Sr происходит увеличение параметров элементарной ячейки без изменения структуры и смещения отражений [002] и [300] в сторону малых углов 2θ. Установлено, что с увеличением времени выдерживания осадков под маточным раствором происходит превращение кинетически устойчивой фазы брушита в термодинамически более устойчивую Sr-содержащего карбонатгидроксилапатита.
Установлено, что в ходе синтеза возможно получение порошкового материала на основе Sr-содержащего карбонатгидроксиапатита и брушита, при фиксированном значении ионов стронций и кальция и варьировании времени синтеза, характеристики полученных порошков представлены в таблице 2.
Результаты данного исследования могут быть использованы, травматологами и ортопедами при лечения больных, страдающих остеопорозом и принимающих Sr-содержащие препараты, а также для разработки новых форм лекарственных препаратов, способствующих адресной доставки лекарственных средств.
Способ биомиметического синтеза Sr-содержащего карбонатгидроксилапатита, модифицированного брушитом, приближенного к неорганическому матриксу кости, из модельного раствора синовиальной жидкости человека, включающий получение неорганического вещества, в искусственно созданной среде для приготовления которого используют дистиллированную воду, CaCl2 - 0,6715 г/л, Na2HPO4⋅12H2O - 7,4822 г/л, NaCl - 2,8798 г/л, NaHCO3 - 2,0160 г/л, MgCl2⋅6H2O - 0,4764 г/л, Na2SO4 - 1,6188 г/л, KCl - 0,3427 г/л и SrCl2⋅6H2O в количестве, обеспечивающем концентрацию ионов Sr - 0,6715 г/л, проводят осаждение при значении рН 7.4 в течение 21 дня, полученный осадок фильтруют, сушат при температуре 100°C в течение 4 часов.