Повязка с пролонгированным выделением активных веществ
Иллюстрации
Показать всеГруппа изобретений относится к медицине. Описаны повязки на основе полисульфатированных олигосахаридов, демонстрирующим пролонгированное выделение указанных активных веществ, а также способ их получения, причем способ включает этап обработки этиленоксидом. Изобретение относится к применению этих повязок для ухода за ранами и для лечения и/или предупреждения образования рубцов и растяжек кожи. Способом достигается более высокое выделение активных веществ. 5 н. и 11 з.п. ф-лы, 4 ил., 2 пр.
Реферат
Настоящее изобретение относится к новым повязкам на основе полисульфатированных олигосахаридов, демонстрирующим пролонгированное выделение указанных активных веществ. Оно относится также к способу их получения, причем этот способ включает этап обработки этиленоксидом. Кроме того, изобретение относится к применению этих повязок для ухода за ранами и для лечения и/или предупреждения рубцов и растяжек кожи.
Уровень техники
Олигосахариды являются углеводами, гидролиз которых дает только моносахариды. Они представляют собой сахара, образованные объединением по меньшей мере двух молекул простых сахаров (или моносахаридов). К олигосахаридам относится сахароза - дисахарид, образованный конденсацией 2 моносахаридов: одной молекулы глюкозы и одной молекулы фруктозы.
В литературе известны различные сульфатированные олигосахаридные соединения, обладающие множественными биологическими, косметическими и/или терапевтическими активностями. К этим соединениям относятся, в частности, различные соли октасульфата сахарозы, такие как калиевая соль октасульфата сахарозы, натриевая соль октасульфата сахарозы, комплекс гидроксида алюминия и октасульфата сахарозы, а также соли аминокислот и октасульфата сахарозы.
Последние соединения известны своими благоприятными действиями, в частности на проблемы желудочных воспалений, а также на заживление ран.
Заживление ран является естественным биологическим процессом, так как ткани животных и человека способны самостоятельно восстанавливать локализованные повреждения путем процессов восстановления и регенерации.
Естественное заживление раны протекает в основном через три последовательные фазы, каждая из которых обладает собственной клеточной и молекулярной активностью. Так, было обнаружено, что последовательно протекают:
- воспалительная фаза, которая начинается сразу после травмы путем осуществления воспалительных и васкулярных процессов, таких как образование сгустка крови, состоящего, наряду с прочим, из фибрина, посредством разных клеточных и молекулярных факторов, и на которой образуется временный матрикс, называемый фибринозной тканью или желтой тканью.
- Фаза грануляции, которая характеризуется поступлением к месту ранения фибробластов и новых эндотелиальных клеток, необходимых для неоваскуляризации поврежденной ткани. После активирования фибробласты превращаются в миофибробласты и участвуют, таким образом, в созревании грануляционной ткани.
- Фаза эпителизации, которая характеризуется реорганизацией внеклеточного матрикса. Например, коллаген типа 3 заменяется коллагеном типа 1. Наблюдается пролиферация большинства клеток. Сначала они имеют инвазивное поведение, типа миофибробластов, фибробластов и эндотелиальных клеток, но затем их активность заметно снижается. Эта фаза позволяет в конечном счете прийти к преобразованному рубцу, мягкому и больше не вызывающему болезненных ощущений, но только в рамках нормального процесса рубцевания раны. Однако иногда случается, что на этом этапе появляются патологические рубцы из-за неправильного осуществления конечных этапов заживления.
Много общих проблем, связанных с процессом заживления, или с рубцами, уже были объектом исследований, в частности, проводимыми авторами настоящей заявки.
Одной из первых проблем, с которыми сталкиваются, была проблема удаления некротических и/или фиброзных тканей в воспалительной фазе. Действительно, когда процесс естественного очищения раны, который состоит в удалении этих тканей, оказывается недостаточным, процесс заживления нарушается. В прошлом предлагалось множество решений, таких, как помощь в очищении, типа механической или хирургической, ферментативной, аутолитической или же биологической. Целью всех этих решений является очистить рану от фиброзных и некротических тканей, из которых она состоит.
Однако эти разные методы имеют много недостатков. Они оказываются или слишком болезненными для пациента, либо очень низкоэффективными.
Эти проблемы были решены благодаря действию соединений, описанных в заявке FR 2956322 (фирма Laboratoires URGO). Этот документ описывает применение соединения, выбранного из полисульфатированных олигосахаридов, содержащих от 1 до 4 моносахаридных звеньев, их солей или их комплексов, в качестве средства очищения раны.
Из этих соединений калиевая соль октасульфата сахарозы была ранее известна как применяющаяся для обработки ран в фазе рубцевания благодаря ее действию на фибробласты. Это действие описано, например, в патентных заявках EP 230023, WO 89/05645 или WO 98/22114. Это соединение использовали после искусственного очищения раны, то есть после удаления некротических и/или фибринозных тканей. Таким образом, его использовали на чистой и промытой ране.
Благоприятное действие некоторых соединений семейства полисульфатированных олигосахаридов в заживлении раны также уже было описано. Так, заявки FR 2824474 и FR 2953522 описывают композиции на основе сукральфата, одного или в комбинации с солями переходных металлов, для применения в заживлении, регенерации, а также для решения проблем воспаления кожи.
Другая проблема, которую стремятся решить, относится к патологическим рубцам и к растяжкам кожи.
Под патологическими рубцами понимаются атрофические, втягивающиеся или же гипертрофические рубцы.
Растяжки появляются вследствие быстрого и грубого растягивания кожи. Такое растягивание может быть следствием увеличения веса и/или гормонального изменения. Каждая растяжка похожа на место разрыва кожи. В действительности же изменилась кожная ткань в результате превращения фибробластов в миофибробласты. Растяжки (striae distensae) образуют на коже параллельные и длинные полоски (стрии) длиной несколько сантиметров и шириной до 1 сантиметра. Иногда растяжки кожи являются тонкими и почти незаметными, но они могут иметь небольшие углубления, придающие коже неровный вид. Сначала они меняются от бледно-розового до пурпурно-красного (незрелые или воспаленные растяжки). Со временем они, как правило, изменяют цвет и приобретают жемчужно-белый вид (зрелые растяжки кожи). Тогда они становятся менее заметными, но рубец остается. Гормональные изменения в комбинации с увеличением веса приводят к появлению растяжек кожи у многих женщин во время беременности. На их появление влияют также генетические факторы. Растяжки кожи могут также появляться параллельно с некоторыми физиологическими или патологическими состояниями и могут быть симптомом, свидетельствующим о генетическом заболевании. Основными пусковыми факторами являются воспаление, механическое напряжение и гормональный фон. Совокупность этих факторов вызывает растяжение, разориентацию и дезорганизацию волокон коллагена и эластина без разрыва опорной ткани. Растяжки кожи подобны шрамам (так как они проходят через те же этапы формирования, что и после повреждения кожи). Избавление от них в настоящее время невозможно, но возможно ослабление и улучшение поражений. Лечебные обработки являются в основном локальными: топические обработки производными ретиноевой кислоты или фруктовых кислот, применение пилинга или лазера. Однако обработки, известные в настоящее время, не вполне удовлетворительны, в частности, они не всегда хорошо переносятся, и их эффективность нельзя считать полностью удовлетворительной. Существует потребность в разработке продукта, позволяющего эффективно предотвращать и/или лечить растяжки кожи при приемлемой переносимости кожи.
Известны, в частности, из заявки FR 2956322, повязки, содержащие соединение, выбранное из группы, состоящей из полисульфатированных олигосахаридов, содержащих 1-4 моносахаридных звена, их солей или их производных, находящееся предпочтительно в массе для смазывания или пропитки повязки, чтобы гарантировать эффективную биодоступность активного вещества в месте рубца у пациента.
Эти повязки позволяют гарантировать пролонгированную биодоступность активного вещества для предупреждения или решения проблем очищения, заживления, растяжек кожи или же патологических рубцов. Однако было установлено, что после нескольких часов применения выделение активного вещества становится недостаточным. Кроме того, только часть активного вещества, содержащегося в повязке, выделяется на обрабатываемую кожу. И после нескольких часов применения требуется накладывать новую повязку, если желательно сохранить на коже уровень активного вещества, достаточный для ожидаемой эффективности. Кроме непосредственно следуемых из этого расходов, регулярная смена повязок не всегда совместима с занятиями пользователя/пациента. Чтобы иметь улучшенную эффективность лечения, стремились создать повязки, обладающие значительно более высоким уровнем пролонгированной биодоступности активного вещества. Другими словами, были разработаны повязки, имеющие повышенную эффективную концентрацию активного вещества в месте повреждения, причем эта эффективность сохраняется более длительное время. Этот результат также является следствием пролонгированного и повышенного выделения, или высвобождения, активного вещества, содержащегося в повязке. Эти новые повязки позволяют более быстрое и более эффективное лечение пациента.
Кроме того, из предшествующего уровня техники известен способ стерилизации повязок путем обработки их этиленоксидом. Однако этот тип обработки до настоящего времени не применялся для повязок на основе полисульфатированных олигосахаридов. Кроме того, в уровне техники не упоминалось и не предполагалось, что такая обработка позволит увеличить продолжительность выделения активного вещества и увеличить полное количество выделившегося активного вещества, скорее наоборот. Согласно предшествующему уровню техники, было выявлено, что все способы стерилизации (например, стерилизация облучением, стерилизация в автоклаве или же стерилизация этиленоксидом) априори оказывают неблагоприятное влияние на выделение активного вещества, содержащегося в повязке, обрабатываемой этими способами, из-за того, что при этом типе стерилизации либо разлагается само активное вещество, либо изменяются реологические и/или структурные свойства микроадгезивной эластомерной массы, в которую введено или на которую нанесено одно или несколько активных веществ (Radiation effects on polypropylene/polybutylene blends, Richard J. Rolando, June 1993 Tappi Journal, Vol. 76, N°6, и Influence of processing conditions on medical material degradation/failure, Michael T.K. Ling et al, Antec 200 p. 2724-2730).
Сущность изобретения
Согласно одному предпочтительному варианту осуществления, настоящее изобретение относится к повязке, содержащей по меньшей мере одну микроадгезивную граничную поверхность, причем указанная микроадгезивная граничная поверхность содержит по меньшей мере одно соединение, выбранное из полисульфатированных олигосахаридов, содержащих 1-4 моносахаридных звена, их солей и их комплексов, причем указанная повязка была обработана этиленоксидом.
Согласно одному предпочтительному варианту осуществления, олигосахаридное полисульфатированное соединение выбрано из:
- калиевой соли октасульфата сахарозы,
- соли серебра и октасульфата сахарозы,
- комплекса гидроксиалюминия и октасульфата сахарозы.
Согласно одному предпочтительному варианту осуществления, повязка содержит от 0,5 до 2 мг/см2, предпочтительно от 0,7 до 1,9 мг/см2, благоприятно от 0,9 до 1,7 мг/см2 соединения, выбранного из полисульфатированных олигосахаридов с 1-4 моносахаридными звеньями, их солей и их комплексов.
Согласно одному предпочтительному варианту осуществления, микроадгезивная граничная структура представляет собой эластомерный азгезивный состав.
Согласно одному предпочтительному варианту осуществления, микроадгезивная граничная поверхность содержит:
- от 10 до 60 вес. % по меньшей мере одной смолы, придающей клейкость,
- от 2 до 20 вес. %, предпочтительно от 12 до 16 вес. % по меньшей мере одного гидроколлоидного соединения,
- от 10 до 65 вес. % по меньшей мере одного минерального масла-пластификатора,
- от 3 до 25 вес. % по меньшей мере одного эластомерного полимера.
Предпочтительно, слой адгезионной эластомерной массы содержит:
- от 0,05 до 1 вес. % по меньшей мере одного антиоксиданта,
- от 10 до 60 вес. % по меньшей мере одной смолы, придающей клейкость,
- от 2 до 20 вес. %, предпочтительно от 12 до 16 вес. % по меньшей мере одного гидроколлоидного соединения,
- от 10 до 65 вес. % по меньшей мере одного минерального масла-пластификатора,
- от 3 до 25 вес. % по меньшей мере одного эластомерного полимера,
- от 1 до 15 вес. % по меньшей мере одного стабилизатора.
Согласно одному предпочтительному варианту осуществления, повязка содержит от 1 до 15 вес. %, предпочтительно от 5 до 10 вес. %, в расчете на полный вес микроадгезивной граничной поверхности, по меньшей мере одного соединения, выбранного из полисульфатированных олигосахаридов с 1-4 моносахаридными звеньями, их солей и их комплексов.
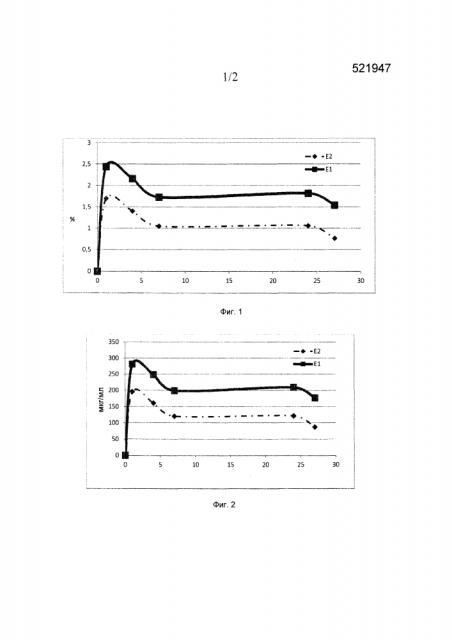
Изобретение относится также к повязке, содержащей микроадгезивную граничную поверхность, в которую введено или на которую нанесено по меньшей мере одно соединение, выбранное из полисульфатированных олигосахаридов, содержащих 1-4 моносахаридных звена, их солей и их комплексов, демонстрирующей пролонгированное выделение указанного соединения, отличающейся растворением, больше или равным 4% за 5 ч, больше или равным 5% за 10 ч, больше или равным 5,5% за 15 ч, больше или равным 6% за 20 ч, измеренным методом пакета в среде растворения, состоящей из 40 мл физиологического раствора.
Согласно одному предпочтительному варианту осуществления, повязка имеет пролонгированное выделение указанного олигосахарида, отличающееся растворением, больше или равным 5% за 5 ч, больше или равный 5,5% за 10 ч, больше или равным 6% за 15 ч, больше или равным 7% за 20 ч, измеренным методом пакета в среде растворения, состоящей из 40 мл физиологического раствора.
Согласно одному предпочтительному варианту осуществления изобретения, указанная микроадгезивная граничная поверхность придает повязке прочность приклеивания к стальной пластине от 0,5 до 100 сН/см, предпочтительно от 5 до 40 сН/см.
Согласно другому варианту осуществления, изобретение относится к повязке для ее применения в очищении или заживлении раны, для ее применения для предупреждения и лечения растяжек кожи, а также для предупреждения и лечения рубцов, в частности, патологических рубцов.
Согласно последнему варианту осуществления, изобретение относится к способу получения повязки, включающему в себя:
(a) нанесение или введение, соответственно на или в микроадгезивную граничную поверхность повязки, по меньшей мере одного соединения, выбранного из полисульфатированных олигосахаридов, содержащих 1-4 моносахаридных звена, их солей и их комплексов,
(b) обработка указанной повязки этиленоксидом.
Согласно одному предпочтительному варианту осуществления, этап (b) обработки этиленоксидом содержит по меньшей мере следующие этапы:
(i) этап предварительного кондиционирования,
(ii) этап воздействия этиленоксида,
(iii) этап промывки.
Согласно одному предпочтительному варианту осуществления:
- на этапе (i) предварительного кондиционирования повязку или активный слой подвергают воздействию температуры от 25 до 60°C и относительной влажности от 50 до 95% в течение периода от 5 до 15 ч,
- этап (ii) содержит обработку газообразным этиленоксидом при давлении больше или равном 920 мбар в камере с относительной влажностью больше или равной 50% и температурой больше или равной 30°C, в течение по меньшей мере 2 часов,
- этап (iii) содержит по меньшей мере две последовательные серии введения азота с последующим снижением давления.
Согласно последнему варианту осуществления, изобретение заключается в способе предупреждения и/или косметического лечения растяжек кожи, или рубцов, или повреждений кожи, вызванных растяжками, причем способ включает нанесение повязки на соответствующую зону или зоны кожи. Этот же способ применим для предупреждения и/или косметического лечения рубцов или повреждений кожи.
Подробное описание
Другие характеристики и преимущества изобретения выявятся более четко при изучении, в сочетании с приложенными фигурами, нижеследующего описания предпочтительного варианта осуществления изобретения, данного в качестве примера.
Совершенно неожиданно авторы заявки разработали новые повязки, содержащие микроадгезивную граничную поверхность на основе полисульфатированных олигосахаридов, демонстрирующие пролонгированное и повышенное выделение активного вещества.
Эти повязки получены способом, включающим нанесение или введение, соответственно на или в граничную поверхность повязки, предназначенной для соприкосновения с кожей или с раной, по меньшей мере одного соединения, выбранного из полисульфатированных олигосахаридов, содержащих 1-4 моносахаридных звена, причем способ включает, кроме того, обработку этиленоксидом.
Эти повязки содержат по меньшей мере одно соединение, выбранное из полисульфатированных олигосахаридов, содержащих 1-4 моносахаридных звена, и отличаются пролонгированным и более высоким выделением этих активных веществ по сравнению с повязками, не обрабатывавшимися этиленоксидом.
Повязки согласно изобретению содержат и получены, исходя из по меньшей мере одного соединения, выбранного из полисульфатированных олигосахаридов, содержащих 1-4 моносахаридных звена, их солей и их комплексов.
Олигосахариды, подходящие для применения в настоящем изобретении, являются олигомерами, образованными из 1-4 моносахаридных звеньев, предпочтительно из 1 или 2 моносахаридных звеньев, обычно соединенных между собой альфа- или бета-гликозидной связью. Другим словами, речь идет о моно-, ди-, три- или тетрасахаридах, предпочтительно о моно- или дисахаридах. Особых ограничений относительно природы моносахаридных звеньев этих полисахаридов не имеется. Предпочтительно, речь идет о пентозах или гексозах.
В качестве примеров моносахаридов можно назвать глюкозу, галактозу или маннозу. В качестве примеров дисахаридов можно назвать мальтозу, лактозу, сахарозу или трегалозу. В качестве примера трисахарида можно назвать мелезитозу. В качестве примера тетрасахарида можно назвать стахиозу. Предпочтительно, олигосахарид является дисахаридом, еще более предпочтительно сахарозой.
Под "полисульфатированным олигосахаридом" понимается олигосахарид, у которого по меньшей мере две, а предпочтительно все гидроксильные группы в каждом моносахариде были замещены сульфатной группой. Предпочтительно, полисульфатированный олигосахарид является октасульфатом сахарозы.
Полисульфатированные олигосахариды, используемые в рамках настоящего изобретения, могут находиться в виде солей или комплексов.
Как правило, в настоящей заявке выражение "полисульфатированные олигосахариды" распространяется на соли и комплексы этих соединений.
В качестве примера солей можно назвать соли щелочного металла, такие, как соли натрия, кальция или калия; соли переходного металла, такие, как соли серебра, соли цинка и соли аминокислоты.
В качестве примера комплексов можно назвать комплексы с гидроксиалюминием.
Особенно предпочтительными соединениями для осуществления изобретения являются следующие:
- калиевая соль октасульфата сахарозы,
- соль серебра и октасульфата сахарозы,
- комплекс гидроксиалюминия и октасульфата сахарозы, общеизвестный под названием сукральфат (от sucrose aluminium sulfate = алюминийсульфат сахарозы).
Соединение, выбранное из полисульфатированных олигосахаридов с 1-4 моносахаридными звеньями, их солей и их комплексов, применяется для получения повязки предпочтительно в тонкоизмельченной форме.
Описанные выше соединения могут применяться по отдельности или в смеси, или же в комбинации с одним или несколькими другими активными веществами, позволяющими вызвать или ускорить заживление или способными играть благоприятную роль при лечении раны, или способными лечить и/или предупреждать растяжки кожи или рубцы, патологические или нет.
Из этих активных соединений в качестве примеров можно назвать, в частности:
- бактерицидные средства, такие, как соли или комплексы серебра (как сульфаты серебра, нитраты серебра, сульфамиды серебра или же цеолиты на основе серебра), соли цинка или меди, метронидазол, неомицин, пенициллины, клавулановая кислота, тетрациклины, моноциклин, хлоротетрациклин, аминогликозиды, амикацин, гентамицин, пробиотики;
- антисептики, такие, как хлоргексидин, триклозан, бигуанид, гексамидин, тимол, люголь, повидон-йод, хлорид бензалкония и бензетония;
- противоболевые средства, такие, как парацетамол, кодеин, декстропропоксифен, трамадол, морфин и его производные, кортикоиды и их производные;
- местные анестетики, такие, как лидокаин, бензокаин, дибукаин, гидрохлорид прамоксина, бупивакаин, мепивакаин, прилокаин, этидокаин;
- противовоспалительные средства, как нестероидные противовоспалительные средства (AINS), аспирин или ацетилсалициловая кислота, ибупрофен, кетопрофен, флурбипрофен, диклофенак, ацеклофенак, кеторолак, мелоксикам, пироксикам, теноксикам, напроксен, индометацин, напроксинод, нимесулид, целекоксиб, эторикоксиб, парекоксиб, рофекоксиб, валдекоксиб, фенилбутазон, нифлумовая кислота, мефенаминовая кислота.
Разумеется, соединения, использующиеся в повязках согласно изобретению, могут также применяться в сочетании с одним или несколькими другими соединениями, известными своей активностью в фазе очищения, как, например:
- ферменты;
- мочевина.
Полисульфатированные олигосахаридные соединения, использующиеся в повязках согласно изобретению, могут также применяться в сочетании с одним или несколькими другими соединениями, известными для лечения растяжек кожи, такими, как:
- производные ретиноевой кислоты,
- фруктовые кислоты.
Полисульфатированные олигосахаридные соединения, использующиеся в повязках согласно изобретению, могут также применяться в сочетании с одним или несколькими другими соединениями, известными своим заживляющим действием, такими, как ретинол, витамин A, витамин E, N-ацетил-гидроксипролин, экстракты centella asiatica, папаин, эфирные масла тимьяна, каепутового дерева, розмарина, шалфея, гиалуроновая кислота, аллантоин, мочевина, протеолитические ферменты, такие, как стрептокиназа, трипсин или коллагеназа, ингибиторы протеаз.
В рамках настоящего изобретения полисульфатированные олигосахаридные соединения вводятся в повязку посредством массы для смазывания или пропитки, образующей микроадгезивную граничную поверхность.
Под повязкой в настоящем изобретении понимается любое медицинское устройство типа повязки, содержащее по меньшей мере одну микроадгезивную граничную поверхность.
В частности, изобретение применимо к повязкам, использующимся для обработки ран, и к повязкам, использующимся для лечения рубцов, к косметическим пластырям.
Выбор повязки зависит от типа повреждения, требующего лечения. Например, в случае лечения ран предпочтительны абсорбирующие повязки, так как в фазе очищения раны часто являются сильно экссудирующими.
Чтобы способствовать быстрому эффекту, это полисульфатированное олигосахаридное соединение (или содержащую его массу для смазывания или пропитки) предпочтительно вводят в слой повязки, который будет контактировать с кожей, или наносят на поверхность повязки, которая будет контактировать с кожей.
Такие методы нанесения хорошо известны специалисту, некоторые из них описаны, например, в патентной заявке WO 2006/007844.
Предпочтительно, если полисульфатированное олигосахаридное соединение не находится в массе для смазывания или пропитки, его осаждают на поверхность слоя, предназначенного для контакта с кожей, т.е. слоя, который прошел через предварительный этап нанесения или пропитки массой для смазывания или пропитки, не содержащей полисульфатированного олигосахаридного соединения:
- либо в жидкой форме, например, путем испарения содержащего его раствора или суспензии;
- либо в твердой форме, например, путем просеивания и/или напыления порошка, содержащего это соединение.
Напротив, в конфигурации, когда полисульфатированное олигосахаридное соединение заблаговременно находится в массе для смазывания или пропитки, ее осаждают на поверхность слоя, предназначенного для контакта с кожей, либо непрерывно (ровным покрытием, сплошным нанесением или нанесением сеткой), либо дискретно (параллельными полосками покрытия).
Можно также предусмотреть прямое получение полисульфатированного олигосахаридного соединения в составе особого слоя повязки в ходе ее изготовления.
Количество полисульфатированного олигосахаридного соединения, использующегося в повязке, подбирается в зависимости от желаемой кинетики выделения. Предпочтительно, предусматривается, чтобы повязка содержала от 0,5 до 2 мг/см2, предпочтительно от 0,7 до 1,9 мг/см2, благоприятно от 0,9 до 1,7 мг/см2 активного вещества полисульфатированный олигосахарид. Это значение рассчитано на активную поверхность повязки, то есть поверхность, предназначенную для выделения активного вещества, причем неактивные части повязки, называемые также "дорожкой", обычно позволяют фиксацию повязки вокруг обрабатываемой зоны.
В рамках его использования в элементе повязки, полисульфатированное олигосахаридное соединение вводится в таком количестве, чтобы количество этого соединения, выделившегося через 24 часа, составляло от 70 до 140 мкг/см2, предпочтительно от 80 до 130 мкг/см2. Это значение относится к активной поверхности повязки.
Повязки согласно настоящему изобретению содержат по меньшей мере одну микроадгезивную граничную структуру, такую как эластомерный слой, на который нанесен или в который введен полисульфатированный олигосахарид.
Из известных повязок, которые могут применяться в рамках настоящего изобретения, можно упомянуть, например:
- полиуретановые пленки, такие, например, как продукты, выпускаемые фирмой Smith&Nephew под маркой Opsite®, или фирмой 3M под маркой Tegaderm®, или же фирмой Laboratoires URGO под маркой Optiskin®. Эти повязки состоят из прозрачной тонкой пленки (порядка 20-50 мкм) полиуретанового клея. Их прозрачность делает возможным визуальный контроль обрабатываемой зоны. Эти полиуретановые пленки являются полупроницаемыми, они проницаемые для газообмена и непроницаемы для жидкостей и бактерий. Они придают механическую защиту от процессов трения, натирания и сдвига.
- Гидроцеллюлярные повязки, такие, например, как продукты, выпускаемые фирмой Mölnlycke под маркой Mepilex® или фирмой Smith&Nephew под маркой Allevyn®, или же Laboratoires URGO под маркой Cellosorb®. Эти повязки обычно состоят из подложки, которая может быть полиуретановой пленкой или нетканым материалом, из абсорбирующего слоя, который может быть из пенополиуретана. Сторона этого абсорбирующего слоя, предназначенная для контакта с раной, может быть или не быть покрыта микроадгезивной массой для смазывания. Эти повязки обладают повышенной способностью поглощения по механизму капиллярности и/или удержания внутри гидроцеллюлярной структуры.
- Гидроволоконные повязки, такие, например, как продукты, выпускаемые фирмой Convatec под маркой Aquacel®. Эти повязки представляют собой нетканые волокна чистых гидроколлоидов (натрий-карбоксиметилцеллюлоза). Эти повязки являются очень гидрофильными и превращаются в связный гель при контакте с экссудатами. Они обладают очень высокой поглощающей способностью и позволяют также "улавливать" бактерии, контролируя тем самым бактериальное заражение.
- Альгинаты, такие, например, как продукты, выпускаемые фирмой Smith&Nephew под маркой Algisite®, или Coloplast под маркой Seasorb® мягкий, или же Laboratoires URGO под маркой Urgosorb®. Эти повязки имеют обычно вид компрессов или тампонов. Они состоят из натуральных полисахаридов и превращаются в гель при контакте с экссудатами. Они обладают очень высокой поглощающей способностью и могут также "улавливать" бактерии, контролируя тем самым бактериальное заражение.
- Гидроколлоидные повязки, такие, например, как продукты, выпускаемые фирмой Convatec под маркой Duoderm®, или фирмой Coloplast под маркой Comfeel®, или же Laboratoires URGO под маркой Algoplaque®, или, в массовом применении, фирмой Johnson&Johnson под маркой Compeed®, или же Laboratoires URGO под маркой ампулы URGO®. Эти продукты обычно состоят из подложки, являющейся полиуретановой пленкой, и адгезивной эластомерной массы, содержащей гидроколлоиды. Эти повязки являются гидрофильными, и адгезивная эластомерная масса, которая содержит гидроколлоиды, превращается в гель при контакте с экссудатами. Они клеятся к здоровой коже, но не к ране.
Повязки согласно настоящему изобретению, какие описаны выше, содержат по меньшей мере одну микроадгезивную граничную структуру, такую как эластомерный слой, на который нанесен или в который введен полисульфатированный олигосахарид. Эта микроадгезивная граничная поверхность предназначена для контакта с кожей или с раной.
Чтобы не повредить здоровые ткани или края раны, в частности, при удалении повязки, предпочтителен адгезив, способный прилипать к коже, не прилипая к ране. В качестве примера такого адгезива можно назвать клеи на основе силиконовых или полиуретановых эластомеров, такие как силиконовые или полиуретановые гели, и гидроколлоидные адгезивы.
Предпочтительно, повязки согласно изобретению содержат микроадгезивную граничную поверхность, выбранную из слоев адгезивной эластомерной массы или композиции, в которую введено одно или несколько полисульфатированных олигосахаридных соединений.
Такие адгезивные эластомерные композиции состоят из эластомерной матрицы на основе одного или нескольких эластомеров, выбранных из блок-сополимеров поли(стирол-олефин-стирол) в комбинации с одним или несколькими соединениями, выбранными из масел-пластификаторов, таких, как минеральные масла, а также в комбинации со смолами, придающими клейкость, или же с некоторым количеством, предпочтительно небольшим, гидроколлоида (от 3 до 20 вес. %), как, например, натрий-карбоксиметилцеллюлоза, и, при необходимости, с антиоксидантами.
Составы таких адгезивных эластомерных масс хорошо известны и описаны, например, в патентной заявке FR 2916356.
Полисульфатированное олигосахаридное соединение используется предпочтительно в количестве от 1 до 15 вес. %, предпочтительно от 5 до 10 вес. %, в расчете на полный вес адгезивной композиции.
Предпочтительно, в повязке согласно изобретению слой адгезионной эластомерной массы содержит, в частности, следующие элементы: эластомерное соединение, гидроколлоид, по меньшей мере одну смолу, придающую клейкость, и по меньшей мере одно масло-пластификатор. Кроме того, слой содержит по меньшей мере одно соединение, выбранное из полисульфатированных олигосахаридов с 1-4 моносахаридными звеньями, их солей и их комплексов.
Слой адгезионной эластомерной массы позволяет сформировать слой микроадгезивной граничной поверхности, состоящий из липидо-коллоидной матрицы, позволяющей облегчить атравматическое наложение, а также удаление и позиционирование повязки. Эта временная фиксация может также помочь обслуживающему персоналу или пользователю зафиксировать повязку с помощью других средств фиксации, например, покрыть повязку сверху средством иммобилизации или клейкой лентой. В этом случае граничный слой может быть выбран таким образом, чтобы повязка имела прочность приклеивания к стальной пластине от 0,5 до 100 сН/см, предпочтительно от 5 до 40 сН/см. Эта клеящая способность измеряется согласно методу EN 1939, в котором образец повязки шириной 20 мм и длиной 150 мм помещают на стальную пластину и через 10 минут измеряют клеящую способность динамометром при скорости растяжения 100 мм/мин под углом 90°. Под эластомерным соединением понимается любой трехблочный блок-сополимер поли(стирол-олефин-стирол), возможно в сочетании с двухблочными сополимерами. Трехблочные сополимеры могут быть блок-сополимерами поли(стирол-этилен-бутилен-стирол), называемыми также SEBS, продаваемые под названием Kraton G1651®, Kraton G1654® или же Kraton G1652®. Двухблочные сополимеры могут быть блок-сополимерами поли(стирол-этилен-пропилен-стиролом), называемыми также SEPS. Эластомерное соединение может быть также выбрано из эластомеров, относящихся к семейству трехблочных сополимеров поли(стирол-изопрен-стирол) (сокращенно поли(SIS)), и из смесей трехблочных сополимеров поли(SIS) и двухблочных сополимеров поли(стирол-изопрен).
Под гидроколлоидами понимается любое подходящее гидроколлоидное соединение, как, например, пектин, альгинаты, натуральные растительные смолы (камедь карайи), производные целлюлозы, такие, как карбоксиметилцеллюлоза и ее соли с щелочным металлом (натриевая или кальциевая соли карбоксиметилцеллюлозы, известные под названием КМЦ Blanose 7H4XF®), а также синтетические полимеры на основе суперабсорбирующих солей акриловой кислоты, как, наряду с прочими, продукты, выпускаемые фирмой BASF® под наименованием Luquasorb 1003®, или фирмой CIBA Speciality Chemicals® под наименованием Salcare SC91®, а также смеси этих соединений. Эти гидроколлоиды предпочтительно применяются в виде частиц для получения адгезивных композиций.
Придающие клейкость смолы, входящие в состав гидроколлоидных адгезивных масс, выбраны, в частности, из низкомолекулярных полиизобутиленов. Как правило, предпочтительно использовать гидрированные смолы, такие, как смолы Escorez® серии 5000, еще более предпочтительна смола Escorez 5380®.
Из масел-пластификаторов, подходящих для осуществления изобретения, можно назвать, в частности, минеральные масла, полибутены или фталатные производные. Предпочтительно используют минеральное масло-пластификатор, выбранное из продуктов, выпускаемых фирмой Shell® под наименованием Ondina 917®, Ondina 919® или же Ondina 933®. Согласно одному частному варианту осуществления, некоторое количество выбранного масла Ondina® может быть заменено эквивалентным количеством вазелина Codex A®, выпускаемого фирмой Aiglon®.
Слой адгезивной гидроколлоидной массы может содержать дополнительные соединения, такие как антиоксидант, стабилизатор и пластификатор.
Под "антиоксидантом" понимается любая молекула, которая уменьшает или препятствует окислению других химических веществ. Антиоксидант может быть выбран из фенольных антиоксидантов, как, например, продукты, выпускаемые фирмой CIBA-GEIGY® под наименованием Irganox 1010®, Irganox 565® и Irganox 1076®, а также серосодержащие антиоксиданты, как, например, дибутилдитиокарбамат цинка, выпускаемый фирмой AKZO® под наименованием PERKACIT ZDBC®. Предпочтительно использовать в качестве антиоксиданта Irganox 1010®.
Под стабилизатором понимается любое соединение, позволяющее оптимизировать скорость гелеобразования, смачиваемость и даже скорость выделения активных веществ, возможно присутствующих в композиции, такое как полимер SEPINOV® EMT10, выпускаемый фирмой SEPPIC, известный также как сополимер соли 2-метил-2[(1-оксо-2-пропенил)амино]-1-пропансульфоновой кислоты и 2-гидроксиэтилового сложного эфира пропеновой кислоты.
Предпочтительно, помимо одного или нескольких полисульфатированных олигосахаридов слой адгезионной эластомерной массы состоит по существу из следующего:
10-60 вес. % по меньшей мере одной смолы, придающей клейкость,
2-20 вес. %, предпочтительно 12-16 вес. % по меньшей мере одного гидроколлоидного соединения,
10-65 вес. % по меньшей мере одного минерального масла-пластификатора,
3-25 вес. % по меньшей мере одного эластомерного полимера.
Если полисульфатированное олигосахаридное соединение находится в слое адгезионной эластомерной массы, эта масса предпочтительно состоит в основном из следующего:
10-60 вес. % по меньшей мере одной смолы, придающей клейкость,
2-20 вес. %, предпочтительно 12-16 вес. % по меньшей мере одного гидроколлоидного соединения,
10-65 вес. % по меньшей мере одного минерального масла-пластификатора,
3-25 вес. % по меньшей мере одного эластомерного полимера,
1-15 вес. % полисульфатированного олигосахарида.
Помимо одного или нескольких полисульфатированных олигосахаридов, слой адгезионной эластомерной массы предпочтительно, состоит по существу из следующего:
0,05-1% вес. по меньшей мере одного антиоксиданта,
10-60 вес. % по меньшей