Длинные жесткие спейсеры для улучшения кинетики связывания в иммуноанализах
Иллюстрации
Показать всеГруппа изобретений относится к области детектирования молекулы-мишени в образце. Устройство для детектирования молекулы-мишени в образце содержит контейнер для образцов для количественного определения молекулы-мишени в образце; по меньшей мере одну первую частицу, функционализированную первой связывающей молекулой, способной к специфическому связыванию с молекулой-мишенью; поверхностную структуру, содержащую вторую связывающую молекулу, где поверхностная структура покрывает плоскую поверхность или присутствует на по меньшей мере одной второй частице. При этом первая частица, образовавшая захватывающий комплекс с молекулой-мишенью, способна к связыванию второй связывающей молекулы поверхностной структуры напрямую или ненапрямую; где каждая первая и/или вторая связывающая молекула присоединена к поверхности частицы одной из первой и/или второй частиц и/или плоской поверхности посредством длинной и жесткой линкерной молекулы; где длина линкерной молекулы выбрана так, чтобы в результате была получена средняя протяженность удлинения линкера более 60 нм; и где количество кластеров первых и/или вторых частиц, связанных друг с другом, или связанных первых и/или вторых частиц прямо или обратно пропорционально соотносится с количеством молекул-мишеней, представленных в образце. Также раскрывается способ детектирования наличия или количества молекулы-мишени в образце. Группа изобретений обеспечивает повышение вероятности связывания функционализированной частицы, связавшей молекулу-мишень, с поверхностью. 2 н. и 22 з.п. ф-лы, 13 ил., 2 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к устройству для детектирования молекулы-мишени в образце, содержащему контейнер для образцов для количественного определения молекулы-мишени в образце, первую частицу, где указанная первая частица функционализирована первой связывающей молекулой, способной к специфическому связыванию с указанной молекулой-мишенью, и поверхностной структурой, содержащей вторую связывающую молекулу, где указанная поверхностная структура покрывает плоский сенсор или присутствует на второй частице, где указанная первая частица способна к связыванию указанной второй связывающей молекулы поверхностной структуры напрямую или ненапрямую; где указанная первая и/или вторая связывающая молекула ненапрямую присоединена к поверхности частицы указанной первой и/или второй частицы и/или поверхности плоского сенсора посредством длинной и жесткой линкерной молекулы; где длина и консистенция указанной линкерной молекулы выбраны так, чтобы в результате была получена средняя протяженность удлинения указанного линкера более 60 нм; и где количество кластеров частиц или связанных частиц прямо или обратно пропорционально соотносится с количеством молекул-мишеней, представленных в образце. В дополнительном аспекте настоящее изобретение относится к способу детектирования наличия или количества молекулы-мишени в образце. Настоящее изобретение также описывает применение частицы в соответствии с изобретением для детектирования молекулы-мишени в образце.
УРОВЕНЬ ТЕХНИКИ, ПРЕДШЕСТВУЮЩИЙ ИЗОБРЕТЕНИЮ
Потребность в повсеместном и эффективном медицинском обслуживании направляет область in vitro диагностики к интегрированному произвольному доступу и решениям по месту лечения. Для достижения таких решений требуется, чтобы тесты были быстрыми, чувствительными, количественными и точными. Кроме того, необходимо, чтобы платформа, на которой выполняется тест, была простой в применении и компактной.
В аффинных анализах применяются биологические молекулы, захватывающие специфические молекулы-мишени из образца и позволяющие определение их концентрации. Как правило, аффинный захват достигается посредством диспергирования нано- или микрочастиц, покрытых захватывающими молекулами в пробную жидкость (Luchini et al., 2008, Nano Lett., 8(1), 350-361). Типичные основанные на аффинности анализы, таким образом, применяются в огромном количестве приложений, таких как диагностические анализы, детектирование биомолекул в исследовании, таких как белки, пептиды и нуклеиновые кислоты, при этом применяя аффинные молекулы, такие как, например, антитела, которые, как правило, характеризуются высокой аффинностью связывания по отношению к специфической биомолекуле. По существу, функционализированные магнитные частицы прикреплены к сенсорной поверхности, где частицы могут ненапрямую, т.е. посредством захваченного аналита, или напрямую связываться с зондами захвата, такими как антитела, размещенные на поверхности. Количество связанных частиц прямо или обратно пропорционально соотносится с количеством молекул-мишеней, представленных в образце. Как правило, в таких биосенсорных приложениях частицы могут быть детектированы с применением любой технологии, чувствительной к частице рядом с поверхностью, часто такие технологии основаны на оптическом детектировании, таком как детектирование рассеянного света или нарушенного полного внутреннего отражения (FTIR), как описано, например, в Bruls et al., Lab Chip, 2009, 9, 2504-3510.
WO 2008/0833 A1 раскрывает способы, реагенты и устройства для детектирования агентов. Описаны виды анализов для детектирования одного или более целевых агентов в образце на основании общепринятых прямых и непрямых сандвичевых анализов.
US 2004/110220 A1 раскрывает способы и устройства для детектирования нуклеиновых кислот. В частности, система детектирования в основном основана на наночастицах с прикрепленными к ним олигонуклеотидами (конъюгаты наночастица-олигонуклеотид). Олигонуклеотиды, описанные в этом документе, имеют участок, который комплементарен участку последовательности нуклеиновой кислоты (распознающий участок) для предоставления возможности гибридизации с целевой нуклеиновой кислотой.
WO 2009/005552 A2 описывает способы и композиции для мультивалентного связывания и количественного захвата компонентов в образце. В частности, описаны модификации общепринятых сандвичевых видов анализа такие, чтобы в результате были получены поливалентные "авидные" связующие вещества для повышения наблюдаемой Kd. Это достигается посредством закрепления более чем одного антитела или антигена на "остове", который может являться основной цепью полимера, такого как одно- или двухцепочечная нуклеиновая кислота, такая как ПНК, ДНК, РНК и т.д.
US 2009/148863 раскрывает платформы для детектирования на основании функционализированных наночастиц. В частности, наночастицы содержат компонент первого монослоя, который приспособлен для связывания биологической группы, которая в свою очередь может быть приспособлена для связывания с аналитом. Поверхность наночастиц может дополнительно содержать компонент второго монослоя, который вносит вклад в экспонирование первого компонента монослоя на поверхности. Наночастицы связаны посредством первого и второго монослоя с захватываемой молекулой, например, антителом, которое позволяет детектирование одиночной молекулы в реальном времени.
ЕР 1441217 А2 описывает анализ связывания с оптическим волноводом на основании детектирования рассеяния света, направленного в TIR элементы или волноводные устройства посредством иммобилизации компонентов специфического связывания (SBM) различными средствами.
US 2005/0048599 раскрывает детектирование микроорганизмов на фиксированном субстрате. Связывание основано на предоставление сандвичевой конфигурации и происходит посредством связывающего метку компонента, который связывает метку с мишенью при помощи средства, которое является специфичным к мишени (например, антитела или аптамеры). Индикаторный компонент является обнаруживаемым детектором.
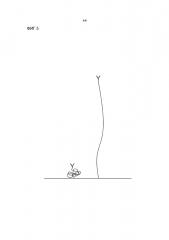
Существенным недостатком аффинных анализов предшествующего уровня техники, тем не менее, является тот факт, что связывание функционализированных частиц, имеющих связанную молекулу-мишень с поверхностью, все еще является очень медленным, ограничивающим скорость и неэффективным. Одна из причин этой медленной реакции в числе прочего заключается в трудности связывания относительно большой (например, приблизительно 500 нм) частицы с поверхностью посредством маленькой (например, приблизительно 10 нм) молекулы-мишени. Диспропорция изображена на фиг.3, иллюстрирующей относительные размеры мишени и частицы. Как следствие, существует не много ориентаций комплекса частица-мишень, которые в результате приводят к эффективному связыванию. Хотя частица может поворачиваться, находясь в контакте с поверхностью, вероятность связывания все-таки остается маленькой.
Таким образом, существует сильная потребность в разработке новых структур частица-мишень, которые способны к эффективному связыванию с поверхностью, такой как поверхность плоского сенсора или поверхность частицы.
ОБЪЕКТЫ И СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на указанные потребности и предоставляет средство для увеличения эффективности связывания частиц с поверхностями. Вышеупомянутая цель, в частности, достигается посредством устройства для детектирования молекулы-мишени в образце, содержащего контейнер для образцов для количественного определения молекулы-мишени в образце, первую частицу, где указанная первая частица функционализирована первой связывающей молекулой, способной к специфическому связыванию с указанной молекулой-мишенью и поверхностной структурой, содержащей вторую связывающую молекулу, где указанная поверхностная структура покрывает плоский сенсор или присутствует на второй частице, где указанная первая частица способна к связыванию указанной второй связывающей молекулы поверхностной структуры напрямую или ненапрямую; где указанная первая и/или вторая связывающая молекула ненапрямую присоединена к поверхности частицы указанной первой и/или второй частицы и/или поверхности плоского сенсора посредством длинной и жесткой линкерной молекулы; где длина и консистенция указанной линкерной молекулы выбраны так, чтобы в результате была получена средняя протяженность удлинения указанного линкера более 60 нм; и где количество кластеров частиц или связанных частиц прямо или обратно пропорционально соотносится с количеством молекул-мишеней, представленных в образце.
Изобретение описывает то, как вероятность связывания большой частицы с поверхностью с мишенью может быть значительно повышена прикреплением к частице линкерных молекул, имеющих некоторую длину. Неожиданно, возможно было наблюдать то, что предоставление длинной и жесткой линкерной или спейсерной молекулы устраняет трудности связывания частиц, которые были в предшествующем уровне техники, и таким образом позволяет более эффективное связывание.
Фиг. 4 иллюстрирует принцип, лежащий в основе настоящего изобретения. Количество возможных ориентаций, в которых частица может связываться с поверхностью, сильно возрастает, если точка присоединения расположена более далеко от частицы. Применение длинной спейсерной молекулы, однако, не в обязательном порядке решает задачу. Фиг. 5 иллюстрирует, что даже если применен очень длинный линкер, например, молекула ПЭГ, то гибкость молекулы скорее всего приведет к сворачиванию с получением в результате глобулярной структуры и таким образом незначительному удлинению захватывающей молекулы от поверхности частиц.
Без привязки к какой-либо теории, одним объяснением для наблюдаемой повышенной эффективности связывания является то, что применение длинных и жестких линкерных молекул для размещения связывающей молекулы далеко от поверхности частицы значительно улучшает кинетику связывания частицы с поверхностью. Авторы данной заявки обнаружили, что получающееся в результате расстояние от конца до конца цепи является функцией средней протяженности удлинения, контурной длины и жесткости молекулы, и смогли продемонстрировать, что такие характеристики вносят значительный вклад в наблюдаемое улучшение кинетики связывания.
В эксперименте с применением покрытых стрептавидином 500 нм наночастиц и жестких дцДНК молекул в качестве линкерных молекул варьирующейся длины, можно в частности показать, что количество связанных частиц возрастает с длиной дцДНК-линкера (смотрите фиг. 6). В частности, авторы смогли продемонстрировать, что длина линкерных молекул на частицах вносит существенный вклад в количество связанных на поверхности сенсора частиц. Эти обнаружения и другое обнаружение, которое будет описано подробно в данном документе, привели к разработке усовершенствованной конструкции линкера. Следовательно конфигурация линкера, как описано в данном документе, обуславливает улучшенную кинетику связывания, таким образом повышая скорость, эффективность и точность аффинных анализов на основе наночастиц.
В предпочтительном варианте осуществления настоящего изобретения первая и/или вторая частица представляет собой магнитную частицу.
В дополнительном предпочтительном варианте осуществления диаметр указанной первой и/или второй частицы составляет по меньшей мере приблизительно 100 нм. В дополнительных предпочтительных вариантах осуществления средняя протяженность удлинения линкера, как упомянуто выше, составляет по меньшей мере 10% диаметра частицы, имеющей диаметр по меньшей мере приблизительно 100 нм.
В еще одном предпочтительном варианте осуществления указанная жесткая линкерная молекула имеет среднюю протяженность удлинения по меньшей мере 20% от контурной длины указанной линкерной молекулы.
В другом предпочтительном варианте осуществления настоящего изобретения первая связывающая молекула является антителом или его фрагментом, аптамером, лигандом или комплементарной нуклеиновой кислотой.
В конкретном варианте осуществления настоящего изобретения жесткость и длина указанной линкерной молекулы определяются через корень из квадрата среднего расстояния от конца до конца цепи линкера √<R2>, где <R2> может быть описана в соответствии с формулой
<R2>=2Pl[1-(P/l)(1-el/p)],
в которой P является персистентной длиной полимера и l является контурной длиной линкера.
В предпочтительном варианте осуществления настоящего изобретения линкерная молекула представляет собой или содержит молекулу нуклеиновой кислоты или небиологический полимер. В особенно предпочтительном варианте осуществления линкерная молекула может быть выбрана из группы, состоящей из двухцепочечной нуклеиновой молекулы, такой как дцДНК, молекула ПНК, дуплекс ПНК-ДНК и дуплекс РНК-ДНК.
В еще одном особенно предпочтительном варианте осуществления двухцепочечная молекула нуклеиновой кислоты представляет собой дцДНК, дуплекс ПНК-ДНК или дуплекс РНК-ДНК.
В наиболее предпочтительном варианте осуществления настоящего изобретения линкерная молекула представляет собой дцДНК.
В другом предпочтительном варианте осуществления настоящего изобретения первая частица дополнительно содержит отталкивающую поверхностную структуру, которая непосредственно присоединена к поверхности указанной частицы, где указанная отталкивающая поверхностная структура покрывает поверхность частицы так, чтобы в результате были получены специфический результирующий заряд и/или стерическое отталкивание частицы, и где указанная отталкивающая поверхностная структура переносит отталкивающий эффект на указанные частицы по отношению к указанной сенсорной поверхности.
В еще одном предпочтительном варианте осуществления настоящего изобретения линкерная молекула является более длинной, чем указанная отталкивающая поверхностная структура.
В дополнительном предпочтительном варианте осуществления настоящего изобретения указанная отталкивающая поверхностная структура является заряженной структурой.
В особенно предпочтительном варианте осуществления заряженная структура представляет собой или содержит молекулу, выбранную из группы, состоящей из нуклеиновой кислоты, такой как двухцепочечная нуклеиновая кислота, например, дцДНК, ПНК, дуплекса ПНК-ДНК, РНК-ДНК, гидрогеля и полимера.
В дополнительном особенно предпочтительном варианте осуществления настоящего изобретения указанная отталкивающая поверхностная структура представляет собой пространственное покрытие.
В другом предпочтительном варианте осуществления настоящего изобретения линкерная молекула и/или указанная отталкивающая поверхностная структура не расщепляется ДНКазой и/или рестрикционным ферментом, способным к разрезанию молекулы двухцепочечной нуклеиновой кислоты.
В другом предпочтительном варианте осуществления настоящего изобретения линкерная молекула дополнительно содержит по меньшей мере один короткий гибкий спейсер.
В еще одном предпочтительном варианте осуществления короткий гибкий спейсер содержит одноцепочечную нуклеиновую кислоту.
Настоящее изобретение в дополнительном аспекте относится к способу детектирования наличия или количества молекулы-мишени в образце, содержащему стадии:
(a) приведения образца в контакт с первой связывающей молекулой, присоединенной к первой частице, в устройстве в соответствии с настоящим изобретением; и
(b) приведения образца в контакт с
i) второй связывающей молекулой, способной к присоединению к плоской поверхности или ко второй частице, где первая связывающая молекула и/или вторая связывающая молекула способны к специфическому связыванию с указанной молекулой-мишенью, или
ii) аналогом молекулы-мишени, присоединенным к плоской поверхности или ко второй частице; где молекула-мишень способна препятствовать связыванию первой связывающей молекулы с аналогом молекулы-мишени; и
(c) детектирования количества первой частицы, связанной с плоской поверхностью или со второй частицей посредством связывания первой связывающей молекулы со второй связывающей молекулой,
где количество кластеров частиц или связанных частиц прямо или обратно пропорционально соотносится с количеством молекул-мишеней, представленных в образце.
В дополнительном предпочтительном варианте осуществления настоящего изобретения сила магнитного поля применяется для приведения частиц в непосредственную близость с указанной твердой подложкой или друг с другом, для того чтобы облегчить кластеризацию частиц.
В дополнительном предпочтительном варианте осуществления настоящего изобретения присоединение указанной второй связывающей молекулы к плоской поверхности или второй частице происходит перед или после связывания второй связывающей молекулы с молекулой-мишенью.
В другом предпочтительном варианте осуществления настоящего изобретения детектирование связанных частиц происходит с помощью нарушенного полного внутреннего отражения (FTIR) или с помощью измерения рассеянного света от указанных связанных частиц рядом с поверхностью или с помощью оптического детектирования кластерообразования.
В дополнительном аспекте настоящее изобретение описывает применение частицы в соответствии с данным документом для детектирования молекулы-мишени в образце.
В особенно предпочтительном варианте осуществления настоящего изобретения молекула-мишень, как упомянуто в отношении устройства, способа или применения, как описано выше в данном документе, представляет собой сердечный тропонин I (cTnI), NT-proBNP (N-терминальный фрагмент мозгового натрийуретического пептида) или паратиреоидный гормон.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
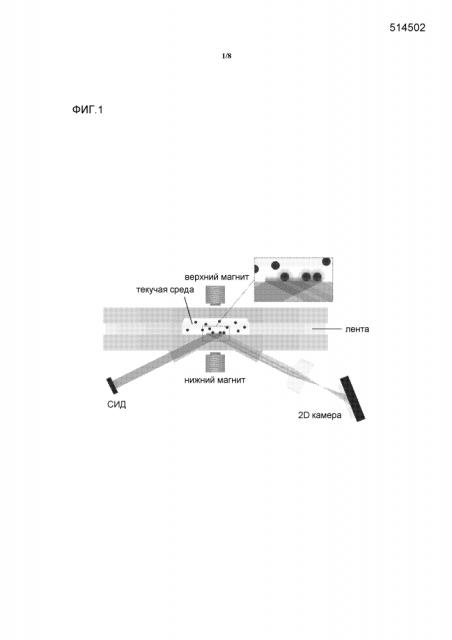
Фиг. 1 демонстрирует принцип FTIR детектирования. Свет из источника света проникает в картридж, отражается от границы раздела картридж/жидкость и отображается на детекторе. Если частицы представлены в рассеянном поле, создаваемом на этой границе раздела, то интенсивность отраженного света снижается.
Фиг. 2 демонстрирует сандвичевый иммуноанализ с применением технологии Magnotech. На панели (1) магнитные частицы, покрытые первичным антителом, направленным против мишени, распределяются в жидком образце и связывают мишень. На панели (2) верхний и нижний витки приводят в движение магнитные частицы пульсирующим образом, приводя в результате к связыванию с поверхностью сенсора, где вторичное антитело может связываться со связанной молекулой-мишенью. На панели (3) несвязанные частицы удаляются с сенсорной поверхности и связанные частицы детектируются с применением рассеянного поля.
Фиг. 3 иллюстрирует относительные размеры 10 нм молекулы-мишени (черный), расположенной между поверхностью сенсора и 500 нм частицей (изображена не полностью). Слева: частица соответствующим образом ориентирована для образования связи; справа: частица не ориентирована соответствующим образом для образования связи.
Фиг. 4 иллюстрирует повышенное количество ориентаций, в которых частица может связываться с поверхностью, если точка присоединения (отображенная маленьким черным кругом) дополнительно отдалена от частицы.
Фиг. 5 демонстрирует схему, сравнивающую удлинение антитела, присоединенного к поверхности посредством ПЭГ линкера (слева) или дцДНК линкера (справа), оба из которых имеют одинаковую контурную длину.
Фиг. 6 изображает график, демонстрирующий количество связанных частиц в виде функции длины ДНК линкера. Покрытые стрептавидином 500 нм частицы инкубировали с дцДНК варьирующейся длины. Каждая молекула ДНК содержала одну группу биотина на одном конце молекулы ДНК, молекулу техасского красного на другом конце молекулы. Раствор, содержащий частицы и ДНК, вводили в картридж, и он связывался с поверхностью сенсора, покрытой антителами против техасского красного с использованием магнитного притяжения. Посредством многократного регистрирования количества частиц, которые были связаны с поверхностью после короткого магнитного этапа промывания, который удалял несвязанные частицы с поверхности, определяли скорость связывания (выраженную в количестве связанных частиц в единицу времени).
Фиг. 7 изображает график, демонстрирующий количество связанных частиц как функцию длины ДНК линкера. Подробности аналогичны фиг. 6, однако использовали частицы с диаметром 1000 нм.
Фиг. 8 демонстрирует частицу с высокой поверхностной плотностью линкерных молекул. Хотя линкерные молекулы относительно растянуты, сильное пространственное затруднение будет снижать подвижность линкера.
Фиг. 9 изображает эффект поверхностной плотности линкера на кинетику связывания. Сверху: схема формата анализа: 500 нм частица, покрытая стрептавидином (линкер), связана с одиночной молекулой-мишенью, цепью дцДНК с биотином на одном конце и молекулой техасского красного, присоединенной к другому концу (синий ромб), которая доступна для связывания с поверхностью сенсора, покрытой антителами против техасского красного. Впоследствии, различные количества нефункциональных дцДНК такой же длины (но без молекулы техасского красного) также были связаны с частицей, и сравнивали способность частиц связываться с поверхностью сенсора. В середине: эксперимент нагрузки частиц с применением дцДНК из 1999 п.о., отражающий относительное количество частиц, связывающихся при загрузке нефункциональной ДНК, по сравнению с частицей с только 1 функциональной молекулой ДНК. Внизу: такая же диаграмма, но для ДНК из 497 п.о.
Фиг. 10 демонстрирует частицу, предварительно нагруженную захватывающими молекулами, присоединенными к поверхности посредством длинного жесткого линкера. Во время анализа молекула-мишень (ромб) связана с частицей и впоследствии с поверхностью.
Фиг. 11 изображает частицу, предварительно нагруженную захватывающими молекулами, присоединенными непосредственно к поверхности. Во время анализа молекула-мишень (ромб) связана с частицей и второй захватывающей молекулой, распознающей мишень, которая соединена с длинным жестким линкером. Другой конец линкера соединен с распознаваемым элементом (например, биотин), который может связываться с совместимой захватывающей молекулой (например, стрептавидин) на поверхности сенсора.
Фиг. 12 демонстрирует частицы, связанные с поверхностью посредством специфического взаимодействия (слева) или неспецифического взаимодействия (справа).
Фиг. 13 демонстрирует возможную конструкцию линкера.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Настоящее изобретение относится к средству и способам для детектирования молекулы-мишени в образце. Хотя настоящее изобретение будет описано применительно к конкретным вариантам осуществления, это описание не должно истолковываться в ограничивающем смысле.
Перед подробным описанием иллюстративных вариантов осуществления настоящего изобретения приведены определения, существенные для понимания настоящего изобретения.
В использованном в данном описании и в прилагаемой формуле изобретения значении формы единственного числа также включают соответствующие формы множественного числа, если в контексте особым образом не указано обратное.
В контексте настоящего изобретения термины "приблизительно" и "примерно" обозначают интервал с точностью, которая, как поймет специалист в данной области, все еще обеспечивает технический эффект рассматриваемого свойства. Термин, как правило, указывает отклонение от указанной численной величины на ±20%, предпочтительно ±15%, более предпочтительно ±10% и еще более предпочтительно ±5%.
Необходимо понимать, что термин "содержащий" не является ограничивающим. В целях настоящего изобретения считается, что термин "состоящий из" является предпочтительным вариантом термина "содержащий". Если в дальнейшем в этом документе группа определяется как содержащая по меньшей мере некоторое количество вариантов осуществления, это означает, что также охватывается группа, которая предпочтительно состоит только из этих вариантов осуществления.
Кроме того, термины "первый", "второй", "третий" или "(a)", "(b)", "(c)", "(d)" и т.д. и тому подобные в описании и формуле изобретения, применяются для различения между подобными элементами и необязательно для описания последовательного или хронологического порядка. Необходимо понимать, что термины, используемые таким образом, являются взаимозаменяемыми при соответствующих обстоятельствах, и что варианты осуществления изобретения, описанные в данном документе, могут функционировать в отличных от описанных или проиллюстрированных в данном документе последовательностях.
В случае терминов "первый", "второй", "третий" или "(a)", "(b)", "(c)", "(d)" "i", "ii" и т.д. относительно этапов способа или применения или анализа не существует времени или временного интервала между этапами, т.е. этапы могут быть осуществлены одновременно или могут иметь место временные интервалы из секунд, минут, часов, дней, недель, месяцев или даже лет между такими этапами, если в заявке особым образом не указано обратное, как установлено в данном документе ранее или далее.
Необходимо понимать, что это изобретение не ограничивается конкретной методологией, протоколами, реагентами и т.д., описанными в данном документе, так как все это может изменяться. Также необходимо понимать, что терминология, применяемая в данном документе, предназначена только для целей описания конкретных вариантов осуществления и не подразумевается, что она ограничивает объем настоящего изобретения, который будет ограничен только прилагающейся формулой изобретения. Если особым образом не указано иное, все технические и научные термины, применяемые в данном документе, имеют такие же значения, как общепринято среди специалистов в данной области.
Как было указано выше, настоящее изобретение в одном аспекте относится к устройству для детектирования молекулы-мишени в образце, содержащему контейнер для образцов для количественного определения молекулы-мишени в образце, первую частицу, где указанная первая частица функционализирована первой связывающей молекулой, способной к специфическому связыванию с указанной молекулой-мишенью, и поверхностную структуру, содержащую вторую связывающую молекулу, где указанная поверхностная структура покрывает плоский сенсор или присутствует на второй частице, где указанная первая частица способна к связыванию указанной второй связывающей молекулы поверхностной структуры напрямую или ненапрямую; в котором указанная первая и/или вторая связывающая молекула ненапрямую присоединена к поверхности частицы указанной первой и/или второй частицы и/или поверхности плоского сенсора посредством длинной и жесткой линкерной молекулы; где длина и консистенция указанной линкерной молекулы выбраны так, чтобы в результате была получена средняя протяженность удлинения указанного линкера более 60 нм; и в котором количество кластеров частиц или связанных частиц прямо или обратно пропорционально соотносится с количеством молекул-мишеней, представленных в образце.
Настоящим изобретением предусматривается пригодное устройство, предпочтительно для детектирования молекулы-мишени с применением биосенсорной системы. Различные аналитические процедуры для детектирования наличия и/или количества аналита в тестируемом образце или объеме образца известны в данной области. Как правило, такая система детектирования может оптически детектировать частицы, которые функционализированы с пригодной связывающей молекулой для того, чтобы связывать целевой аналит. Наличие или количество аналита может быть определено из количества аналита, связанного с частицами. Наличие или количество аналита может быть также определено из количества кластеров частиц. В конкретных вариантах осуществления настоящего изобретения биосенсорную систему, содержащую устройство, как описано в данном документе, можно применять для детектирования одиночных частиц, связанных с плоским сенсором, как описано в данном документе, или наличия кластера частиц, и приведением частиц в движение магнитным полем, генерируемым генератором магнитного поля.
"Генератор магнитного поля" как это применяется в данном документе, как правило, содержит один или более магнитов внутри оптомагнитного устройства, как описано в данном документе, для генерирования магнитного поля в камере для образцов, где указанное магнитное поле будет направлять магнитные частицы к поверхности контакта. Магнитное поле будет, как правило, иметь ненулевой градиент, который позволяет воздействовать магнитными силами на магнитные (дипольные) частицы. Пригодные примеры таких генераторов магнитного поля или пригодных систем, содержащих такие генераторы магнитного поля известны специалисту в данной области. В конкретных вариантах осуществления настоящего изобретения генератор магнитного поля может представлять собой генератор магнитного поля, как описано в Bruls et al., Lab Chip, 2009, 9, 2504-3510, или содержаться в или являться частью системы как описано в Ranzoni et al., 2011, Nano Lett., 11, 2017-2022.
Как правило, магнитные частицы могут быть приведены в движение применением магнитного поля так, что аналитическая процедура может быть ускорена. В конкретных вариантах осуществления настоящего изобретения также предусмотрено, что применение магнитного поля может снизить фоновый сигнал благодаря удалению неспецифически связанных частиц. Фиг. 2 демонстрирует пример того, как частицы могут быть приведены в движение для эффективного удаления неспецифических или несвязанных частиц с плоского сенсора, как описано в этом документе. Верхний и нижний магнит, который может приводится в действие пульсирующим образом, эффективно удаляет несвязанные частицы так, что связанные частицы детектируются на поверхности сенсора.
Магнитное приведение в движение, как это используется в контексте настоящего изобретения, может быть применено по-другому, а именно для расположения магнитных частиц в образце в цепи для того, чтобы ускорить кластеризацию частиц. Также настоящим изобретением предусмотрено применение магнитного поля для приведения в движение для вибрирования и вращения кластеров частиц для определения наличия и количества образованных кластеров. В конкретных вариантах осуществления магнитное приведение частиц в движение может происходить в виде импульсного, т.е. приводящее в движение поле по меньшей мере один раз прерывается паузой. Было обнаружено, что динамическое приведение в движение на основе повторных импульсов снижает неспецифические взаимодействия и увеличивает количество событий связывания. Дополнительные подробности и параметры относительно детектирования молекулы-мишени на основании детектирования кластеров частиц должны быть известны специалисту в данной области или могут быть получены из Ranzoni et al., 2011, Nano Lett., 11, 2017-2022.
Биосенсорные системы, пригодные для применения в данном изобретении могут содержать, к примеру, биосенсорный картридж, содержащий контейнер для образца, сенсорное устройство для обнаружения частиц, систему детектирования и необязательно генератор магнитного поля. Системы могут в дополнительных вариантах осуществления содержать один или более добавочных функциональных блоков, таких как система считывания, например, экран или принтер, интерфейс для базы данных или компьютерной системы, блок калибровки, прямую или непрямую связь с устройствами с высокой пропускной способностью и т.д. Конкретно настоящим изобретением предусмотрены портативные устройства для быстрого и незамедлительного анализа, куда может быть введен картридж, содержащий формат анализа. Как правило, такое устройство содержит источник электропитания, предпочтительно в виде перезаряжаемых батарей, дисплей, возможность беспроводного подключения, такого как WLAN, для быстрого доступа к базе данных или доступа к информационной системе лаборатории. Иллюстративная биосенсорная система, которая может быть применена в контексте настоящего изобретения, описана в Bruls et al., Lab Chip, 2009, 9, 2504-3510.
Особенно предпочтительными являются устройства обнаружения на основании оптического детектирования частиц рядом или на поверхности. Иллюстративное устройство без ограничения им, показано на фиг.1, оно содержит источник света и систему детектирования света.
"Образец", как это применяется в данном документе, относится к любому образцу, который содержит молекулу-мишень, как определено в данном документе. Такие образцы могут, к примеру, включать в себя образцы, полученные из или содержащие стул, цельную кровь, сыворотку, плазму, слезы, слюну, начальную жидкость, мокроту, ушную жидкость, генитальную жидкость, грудную жидкость, молоко, молозиво, плацентарную жидкость, амниотическую жидкость, перспират, синовиальную жидкость, жидкость асцитов, цереброспинальную жидкость, желчь, желудочную жидкость, внутриглазную жидкость, стекловидное тело, желудочно-кишечную жидкость, эксудат, транссудат, плевральную жидкость, плевральную жидкость, сперму, жидкость верхних дыхательных путей, перитонеальную жидкость, жидкость, отобранную из участка иммунологической реакции, жидкость, отобранную из объединенного участка отбора, бронхиальный лаваж, мочу, биопсийный материал, например, из пригодных органов, например, легкое, мышца, мозг, печень, кожа, поджелудочная железа, желудок и т.д., образец ядросодержащей клетки, жидкость, относящуюся к поверхности слизистой оболочки, волосы или кожу. Дополнительно могут быть использованы образцы из источников окружающей среды, например, образцы воды, образцы мяса или домашней птицы, образцы из источников потенциального заражения и т.д.
Термин "молекула-мишень", как это применяется в данном документе, относится к любой молекуле, связанной связывающей молекулой и может, к примеру, являться биологическим веществом, таким как биомолекула, предпочтительно биомаркер, комплексами, клеточными фракциями или клетками. Предпочтительно, молекула-мишень в контексте настоящего изобретения является нуклеиновой кислотой, например, молекулой ДНК или РНК, или олигонуклеотидом, таким как ДНК или РНК олигонуклеотид. Еще более предпочтительными являются молекулы-мишени, такие как пептид, полипептид или белок, фрагмент белка или полипептида или функциональный домен белка или полипептида, молекула лекарственного средства, маленькая молекула или витамин.
Молекула-мишень может быть непосредственно получена из образцов, как описано в данном документе выше. В других обстоятельствах образцы могут быть подвержены технологиям приготовления образцов, например, на основании стандартных протоколов, включая, к примеру, частичную очистку, которая делает молекулы-мишени более доступными для партнеров по связыванию, т.е. для аффинной молекулы, как определено в данном документе. К примеру, образцы крови могут быть отцентрифугированы для отделения фракций, включая целые клетки или мембраны из сыворотки, образцы экскрементов могут быть секционированы и гомогенизованы с физиологически приемлемым буфером и детергентом, образцы мокроты могут быть разжижены и фракционированы. Кроме того, антибиотики или бактерициды могут быть добавлены к образцам для предотвращения дополнительного роста любых представленных организмов. Целые клетки могут также быть удалены или могут быть лизированы для высвобождения их содержимого.
"Контейнер для образца", как это применяется в данном документе, относится к контейнеру, изготовленному из любого пригодного материала, подобного стеклу, любого прозрачного пластика или полупроводника, в которых измеряется образец. Магнитные частицы, как описано в данном документе, могут быть уже представлены в контейнере для образца, когда вводится образец, могут вводиться вместе с образцом или могут вводиться после того, как образец был введен в контейнер для образца. Контейнер для образца может дополнительно содержать сенсорную поверхность, содержащую вторую связывающую молекулу. Предпочтительно сенсорная поверхность расположена на дне контейнера для образца. Контейнер для образца мо