Способ получения нанопорошка феррита висмута
Иллюстрации
Показать всеИзобретение относится к получению однофазного нанокристаллического порошка феррита висмута BiFeO3 с ферромагнитными свойствами. Способ включает смешивание нитратов висмута Bi(NO3)3, нитратов железа Fe(NO3)3, глицерина и воды с получением раствора, выпаривание полученного раствора с образованием геля и нагрев его до температуры вспышки с образованием порошка. Упомянутые нитраты висмута и нитраты железа используют в расчетном количестве, необходимом для получения феррита висмута, а глицин - в количестве на 35-50% меньше расчетного количества, при этом выпаривание полученного раствора и нагрев до температуры образуемого геля ведут при непрерывном перемешивании, а полученный после вспышки порошок нагревают до 350-400°C в течение времени до 30 мин. Обеспечивается получение чистого, однородного по дисперсности порошка. 8 ил., 4 пр.
Реферат
Изобретение относится к способу получения нанопорошков на основе феррита висмута для создания функциональных материалов - наноструктурированных керамик и покрытий из него, необходимых при изготовлении компонентов электронной техники, которые могут найти широкое применение в микроэлектронике, в частности спиновой электронике (спинтронике); в сенсорной и СВЧ технике; в устройствах для записи, считывания и хранения информации и др.
Известны способы [1-11] получения нанопорошков на основе феррита висмута. Основными недостатками способов, описанных в [1-9], являются: высокие температуры синтеза, необходимость дополнительной обработки продуктов в ходе получения прекурсора и его сжигания, многофазность полученных порошков, наличие дефектов структуры нанокристаллов и необходимость дополнительных процедур для исключения этих недостатков после получения продукта в результате сжигания соответствующих прекурсоров. Из известных способов получения нанопорошков наиболее близкими по технической сущности являются методы, описанные в [10-12].
В [10] приводится технология получения нанопорошков на основе феррита висмута, суть которой в том, что водные растворы нитратов соответствующих металлов, полученные с добавлением азотной кислоты в качестве окислителя, осаждают добавлением винной кислоты, затем выпаривают. Высушенный осадок подвергают термической обработке при температурах 450-600°С в течение 2 часов. Затем подбираются среды и температуры отжига для получения однофазного поликристаллического порошка. Метод получения нанопорошка феррита висмута в [10] реализуется следующим способом: эквимолярные количества (0,01 М) Bi(NO3)3⋅5H2O и Fe(NO3)3-9H2O сначала растворяются в разбавленной азотной кислоте с образованием прозрачного раствора. В полученный раствор добавляется винная кислота в молярном соотношении 1:1 по отношению к нитратам металлов. Раствор, постоянно перемешивая, нагревают при 150-160°С до получения пушистого зеленого осадка. Полученный осадок фильтруют, сушат и нагревают при различных температурах (450-600°С) в течение 2 часов. Аморфный нанопорошок выдерживают длительное время при температурах ~ 600°С до его перехода полностью в нанокристаллическое состояние. Это важно, поскольку только нанокристаллическая фаза BiFeO3, наряду с сегнетоэлектрическими, обладает ферромагнитными свойствами. Для достижения однофазного состава BiFeO3 выдержку при этой температуре осуществляют в среде кислорода.
Суть технологии получения нанопорошков на основе феррита висмута, предложенного в [11] в том, что в водные растворы нитратов соответствующих металлов добавляют глицин в качестве топлива и подкисляют щавелевой либо уксусной кислотой, при получении BiFeO3 из предварительно смешанных оксидов Bi2O3 и Fe2O3 в соотношении 1:1 добавляется азотная кислота, для получения нитратов соответствующих металлов и дополнительно подкисляют уксусной кислотой. Растворы (предварительно смешивают, если они представляют собой водные растворы нитратов отдельных металлов) выпаривают на нагревателе мощностью 800 Вт до получения сухого прекурсора, нагревание которого в течение 10-20 секунд приводит к вспышке и образованию нанопорошка. Полученный порошок брикетируют и подвергают термообработке в микроволновой печи, а затем закалке, чтобы получить частицы чистого BiFeO3 одинакового размера.
Наиболее близким из выбранных аналогов является способ, описанный в [12]. Суть технологии получения однофазного нанокристаллического порошка феррита висмута BiFeO3 с ферромагнитными свойствами в [12] заключается в том, что изготавливается водный раствор из эквимолярной смеси нитрата висмута Bi(NO3)3 с глицином, нитрата железа Fe(NO3)3 с глицином и азотной кислоты, которая обеспечивает получение прозрачного раствора при смешивании. Полученный раствор выпаривается до плотности 1,14-1,16 г/см3, затем нагревая со скоростью 10-30 град/мин, доводится до температуры вспышки, в результате которой синтезируется соединение BiFeO3 в виде нанокристаллического порошка.
Недостатками метода [10] является то, что при осаждении раствора не может быть достигнута однородность из-за различной растворимости солей винной кислоты железа и висмута, необходимость выбора среды и температуры для термической обработки и многоэтапность этой обработки в целях получения однофазного порошка.
Недостатком метода [11] является то, что растворы подкисляются щавелевой или уксусной кислотой, при этом для формирования необходимо нанокристаллического порошка BiFeO3, полученный продукт после вспышки высушенного прекурсора подвергается брикетированию и термообработке (нагреванию и закалке), т.е. недостаток способа в многоэтапности процедуры в целях получения однофазного нанокристаллического порошка необходимого размера. Кроме того, дополнительно требуется оптимизация таких параметров, как скорость и время нагревания, а также максимальная температура продукта, содержащего соединение BiFeO3. Несоблюдение соответствующих оптимальных параметров может привести к рекристаллизации нанокристаллического порошка BiFeO3, снижая положительный эффект, достигаемый в результате получения BiFeO3 в виде наночастиц, обладающих ферромагнетизмом в отличие частиц дисперсностью выше 62 нм, обладающих антиферромагнетизмом.
Недостатком метода из [12] является то, что получение однофазного нанокристаллического порошка феррита висмута с ферромагнитными свойствами, необходимого для производства изделий из него, предполагает необходимость коррекции нескольких технологических параметров, это: количество кислоты для достижения прозрачности раствора; выбор значений плотности, до которой выпаривается раствор; значения скорости нагрева раствора, при котором достигается однофазность нанопорошка после вспышки. Наличие нескольких технологических параметров, требующих коррекции, усугубляет проблему масштабирования производства порошка.
Феррит висмута является неустойчивым химическим соединением, поэтому его получение в чистом виде, а тем более получение изделий из него, весьма проблематично. Нанодисперсность порошка предполагает наряду с кристаллической, наличие в нем рентгеноаморфной фазы, что усугубляет эту проблему, поскольку нанопорошки по сравнению с микрокристаллическими порошками разлагаются при более низких температурах. В связи с чем, общий недостаток всех методов [1-12] заключается в том, что в функциональных материалах и изделиях из них, изготавливаемых путем термообработки, в том числе после спекания напорошков BiFeCO3, получаемых этими методами, в результате разложения BiFeO3 неизбежно возникают фазы Bi25FeO39 и Bi2Fe4O9.
Задача предлагаемого изобретения - получение чистых, однородных по дисперсности нанокристаллических порошков на основе феррита висмута с возможностью производства нанопорошка в промышленных масштабах.
Техническим результатом изобретения является то, что он позволяет получать нанокристаллический порошок феррита висмута, обеспечивающий минимизацию содержания фаз разложения Bi25FeO39 и Bi2Fe4O9 соединения BiFeO3 при термообработке, в том числе его спекании для возможности получения наноструктурированной керамики и покрытий на основе феррита висмута со строгой стехиометрией, путем достижения оптимальной скорости сгорания, выбором количества глицина и интенсивного перемешивания раствора нитратов соответствующих металлов разной насыщенности. При этом синтезированный порошок нагревают до 350-400°С в течение времени до 30 мин для удаления органики и NO3 групп.
Способ получения однофазного нанокристаллического порошка феррита висмута BiFeO3 с ферромагнитными свойствами, включающий смешивание рассчитанных количеств нитрата висмута Bi(NO3)3, нитрата железа Fe(NO3)3, глицина и воды с получением раствора, выпаривание полученного раствора с образованием геля и нагрев до температуры вспышки с образованием порошка, отличающийся тем, что упомянутые нитраты висмута и железа используют в расчетном количестве, необходимом для получения феррита висмута, а глицин - в количестве на 35-50% меньше расчетного количества, при этом выпаривание полученного раствора и нагрев до температуры вспышки образуемого геля ведут при непрерывном перемешивании.
При снижении количества глицина от рассчитанного снижается интенсивность сгорания, а количество выделяемой теплоты в системе оказывается достаточным для разложения нитратов, в том числе нерастворенного дигидроксонитрата висмута (III). Корректировка снижаемого количества глицина в пределах 35-50% требуется для учета условий окружающей среды, особенностей посуды, мощности нагревателя, магнитной мешалки и др.
Способ получения чистых однородных по дисперсности нанокристаллических порошков и наноструктурированной керамики из них на основе феррита висмута осуществляется следующим образом:
1. Рассчитываются массы Bi(NO3)3 и Fe(NO3)3, необходимые для получения нанопорошка BiFeO3.
2. Рассчитывается масса глицина, необходимого для комплексообразования с Bi(NO3)3 и Fe(NO3)3 по реакции:
Bi(NO3)3+3NH2-СН2-СООН→Bi(OOCCH2NH2)3+3HNO3
Fe(NO3)3+3NH2-СН2-СООН→Fe(OOCCH2NH2)3+3HNO3
3. В рассчитанную массу нитрата висмута Bi(NO3)3 добавляют воду (выпадает белый осадок), раствор непрерывно перемешивается магнитной мешалкой. В этот раствор добавляется глицин на 35-50% меньше рассчитанного количества, затем добавляется нитрат железа Fe(NO3)3.
4. Непрерывно смешиваемый раствор выпаривается до вспышки образующегося геля.
5. Полученный после вспышки порошок прокаливается при 350-400°С в течение времени до 30 минут для удаления органики и NO3 групп.
В результате многократных проб был получен положительный результат - однородный по составу и дисперсности нанопорошок соединения BiFeO3 при соблюдении следующих технологических параметров:
Пример 1
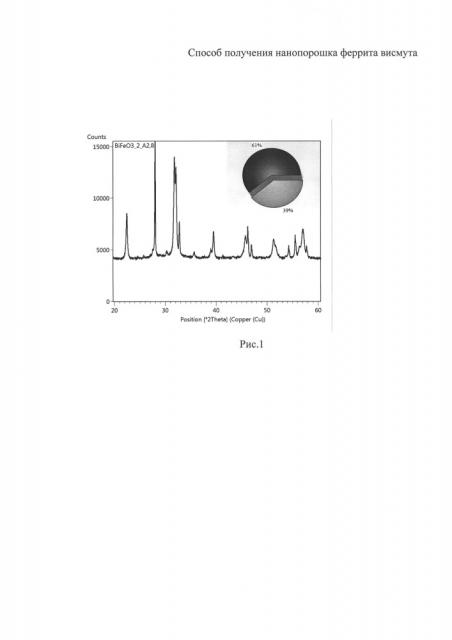
Для получения 10 граммов нанопорошка BiFeO3 в рассчитанную массу нитрата висмута Bi(NO3)3 - 15,45 г добавляется 100 мл воды (выпадает белый осадок), раствор непрерывно перемешивается магнитной мешалкой. В этот раствор добавляется азотная кислота 2,8 мл до получения прозрачного раствора, добавляется глицин 14,34 г - рассчитанное количество для комплексообразования, затем добавляется нитрат железа Fe(NO3)3 - 12,88 г. Непрерывно смешиваемый раствор выпаривается до вспышки, образующегося геля. Полученный в результате вспышки и горения порошок прокаливается при 400°С в течение 30 минут для удаления органики и NO3 групп.
На рис. 1 представлена дифрактограмма этого порошка и фазовая диаграмма с содержанием фаз из базы данных PAN-ICSD. Здесь кроме основной фазы Bi2O3 - 61%, содержится фаза богатая висмутом. Фаза, содержащая железо, находится в рентгеноаморфном состоянии.
Пример 2
В рассчитанную массу нитрата висмута Bi(NO)3 - 15,60 г добавляется 100 мл воды (выпадает белый осадок) раствор непрерывно перемешивается магнитной мешалкой. В этот раствор добавляется 6 г глицина (меньше рассчитанного количества 14,34 г), затем добавляется нитрат железа Fe(NO3)3 - 13,2 г. Непрерывно помешиваемый раствор, содержащий осадок, выпаривается до вспышки образующегося геля. Полученный в результате вспышки и горения порошок прокаливается при 400°С в течение 30 минут для удаления органики и NO3 групп.
На рис. 2 представлена дифрактограмма этого порошка и фазовая диаграмма с содержанием фаз из базы данных PAN-ICSD. Здесь кроме основной фазы Bi2O3 - 92%, содержится фаза, богатая висмутом. Фаза, содержащая железо, находится в рентгеноаморфном состоянии. Размер кристаллитов в среднем составляет 35 нм. В результате термообработки этого порошка при 600°С в течение 30 минут кристаллическая фаза, богатая висмутом, наблюдаемая на рис. 2, в результате взаимодействия с рентгеноаморфной фазой, богатой железом, образует Bi2O3. После такой термообработки (см. рис. 3) содержание феррита висмута в порошке возрастает до 100%. Размер кристаллитов взрастает и составляет примерно 50 нм.
Пример 3
В отличие от метода, приведенного в примере 2, при прочих равных условиях масса нитрата висмута - Bi(NO3)3 берется в количестве 15,60 г нитрат железа Fe(NO3)3 - 12,90 г.
На рис. 4 представлена дифрактограмма этого порошка и фазовая диаграмма с содержанием фаз из базы данных PAN-ICSD. Здесь кроме основной фазы Bi2O3 - 93%, содержится кристаллическая фаза, богатая висмутом (7%). Фаза, содержащая железо, находится в рентгеноаморфном состоянии. Размер кристаллитов составляет в среднем 50 нм. В результате термообработок этого порошка при 600°С и 650°С в течение 30 минут кристаллическая фаза, богатая висмутом, наблюдаемая на рис. 4, взаимодействуя с рентгеноаморфной фазой, богатой железом, образует Bi2O3. После таких термообработок (см. рис. 5 и 6) содержание феррита висмута в порошке возрастает до 96% и 98% соответственно, а размеры кристаллитов возрастают и в среднем составляют 70 нм и 80 нм соответственно, тем не менее эти порошки сохраняют ферромагнитные свойства.
Пример 4
В отличие от метода, приведенного в примере 2, при прочих равных условиях масса нитрата висмута - Bi(NO3)3 берется в количестве 15,39 г, глицин добавляется в количестве 5 г, нитрат железа - Fe(NO3)3 в количестве 12,90 г.
На рис. 7 представлена дифрактограмма этого порошка и фазовая диаграмма с содержанием фаз из базы данных PAN-ICSD. Здесь кроме основной фазы Bi2O3 - 94%, содержится фаза, богатая висмутом. Фаза, содержащая железо, находится в рентгеноаморфном состоянии. Здесь кроме основной фазы содержится кристаллическая фаза, богатая висмутом (6%). Фаза, содержащая железо, находится в рентгеноаморфном состоянии. Размер кристаллитов в среднем составляет 40 нм. В результате термообработки этого порошка при 600°С в течение 30 минут кристаллическая фаза, богатая висмутом, наблюдаемая на рис. 7, взаимодействуя с рентгеноаморфной фазой, богатой железом, образует Bi2O3. После такой термообработки (см. рис. 8) содержание феррита висмута в порошке возрастает до 96%. Размер кристаллитов возрастает и в среднем составляет 60 нм.
Преимуществами предложенного способа являются:
1. Одноэтапность получения однофазного феррита висмута в нанокристаллическом состоянии без необходимости дополнительной обработки промежуточных продуктов и необходимости корректировки нескольких технологических параметров: количество кислоты для достижения прозрачности раствора; выбор значений плотности, до которой выпаривается раствор; значения скорости и времени нагревания раствора.
2. Чистота, однородность и сохранение фазового состава при термообработке до температур 650°С и более.
3. Низкие температуры синтеза, при которых скорость рекристаллизации настолько мала, что размеры частиц в получаемом порошке в два и более раз меньше 62 нм. Частицы BiFeO3 c дисперсностью менее 62 нм наряду с сегнето- и пьезо- приобретают ферромагнитные свойства. Причем электрическое и магнитные поля в таких частицах связаны между собой линейной зависимостью.
Литература
1. Chen Z., Zhan G., HeXin, YangHu, WuHao (2011) Low-tem-peraturepreparationofbismuthferritemicrocrystals by a sol-gel-hydrothermal method. Cryst Res Technol 46: 309-314.
2. Cheng ZX, Li AH, Wang XL, Dou SX, Ozawa K, Kimura H, Zhang SJ, Shrout TR (2008) Structure, ferroelectric properties, and magnetic properties of the La-doped bismuth ferrite. J ApplPhys 103:07E507.
3. Ferri EAV, Santos IA, Radovanovic E., Bonzanini R., Girotto EM (2008) Chemical characterization of BiFeO3 obtained by Pechini method. J.
4. Kim JK, Kim SSu, Kim WJ (2005) Sol-gel synthesis and properties of multiferroic BiFeO3. Mater Lett 59: 4006-4009.
5. Kumar M.M., Palker V.R., Srinivas K., Suryanarayana S.V. (2000) Ferroelectricity in a pure BiFeO3 ceramics. ApplPhysLett 76:2764.
6. Luo W., Wang D., Wang F., Liu T., Cai J., Zhang L., Liu Y. (2009) Room-temperature simultaneously enhanced magnetization and electric.
7. Shetty S., Palkar V.R., Pinto R. (2002). Size effect study in mag-netoelectric BiFeO3 system. Pramana J Phys 58: 1027-1030.
8. CN 102627452 A (HARBIN INST TECHNOLOGY), 08.08.2012.
9. CN 102838356 A (SHANGHAI TITANOS INDASRY CO LTD), 26.12.2012.
10. Alina Manzoor, Hasanain S.K., Mumtaz A., Bertino M.F., Franzel L. Effects of size and oxygen annealing on the multiferroic behavior of bismuth ferrite nanoparticles // J Nanopart Res (2012) 14:1310.
11. CN 101269842 A (INST ELECTRICAL ING CAS), 24.09.2008.
12. Рабаданов М.Х., Палчаев Д.К., Ахмедов Ш.В., Фараджева М.П., Мурлиева Ж.Х., Каллаев С.Н., Садыков С.А. Способ получения однофазного нанопорошка феррита висмута // Патент №2556181. Бюл. №19, 10.07.2015.
Способ получения однофазного нанокристаллического порошка феррита висмута BiFeO3 с ферромагнитными свойствами, включающий смешивание нитратов висмута Bi(NO3)3, нитратов железа Fe(NO3)3, глицерина и воды с получением раствора, выпаривание полученного раствора с образованием геля и нагрев его до температуры вспышки с образованием порошка, отличающийся тем, что упомянутые нитраты висмута и нитраты железа используют в расчетном количестве, необходимом для получения феррита висмута, а глицин - в количестве на 35-50% меньше расчетного количества, при этом выпаривание полученного раствора и нагрев до температуры образуемого геля ведут при непрерывном перемешивании, а полученный после вспышки порошок нагревают до 350-400°C в течение времени до 30 мин.