Гетероциклильные пиримидиновые аналоги в качестве ингибиторов tук2
Иллюстрации
Показать всеНастоящее изобретение относится к новому соединению формулы (I) или его фармацевтически приемлемой соли, или его дейтерированному производному. Соединения обладают свойствами ингибитора нерепторной тирозинкиназы Tyk2 и селективным ингибирующим действием в отношении Янус киназ JAK1, JAK2, JAK3. Соединения могут найти применение в способе лечения или профилактики иммунологического, воспалительного, аутоиммунного, аллергического расстройства или заболевания отторжения трансплантата или заболевания "трансплантат-против-хозяина". В формуле (I)
R1 представляет собой Н; C1-6 алкил, где C1-6 алкил необязательно замещен одним или несколькими R3, которые являются одинаковыми или различными; при этом C1-6 алкил, содержащий гидроксигруппу, может быть дейтерирован; R3 представляет собой галоген; CN; С(О)OR4; OR4; C(O)R4; C(O)N(R4R4a); S(O)2R4; S(O)R4; или T1; R4, R4a, R4b независимо выбраны из группы, включающей Н; Т1; C1-6 алкил, где C1-6 алкил необязательно замещен одним или несколькими R5, которые являются одинаковыми или различными; R5 представляет собой галоген; CN; OR6; или Т1; R6 представляет собой Н; Т1 представляет собой С3-7 циклоалкил; 4-7-членный гетероциклил с 1-2 гетероатомами в цикле, выбранными из азота, кислорода или серы; или 7-8-членный гетеробициклил, возможно спироконденсированный, с двумя гетероатомами в цикле, выбранными из азота или азота и кислорода, где Т1 необязательно замещен одним или несколькими R7, которые являются одинаковыми или различными; R7 представляет собой галоген; CN; С(О)OR8; оксо (=O), где кольцо является, по крайней мере, частично, насыщенным; C1-6 алкил; R8 независимо выбраны из группы, включающей Н; C1-6 алкил; X1 представляет собой C(R11a) или N; X2 представляет собой C(R11b) или N; X3 представляет собой C(R11c) или N; X4 представляет собой C(R11d) или N; X5 представляет собой C(R11e) или N, при условии, что не более чем два из X1, X2, X3, X4, X5 представляют собой N; R11a, R11c, R11e независимо выбраны из группы, включающей Н; галоген; CN; OR12; С(О)N(R12R12a); S(О)2N(R12R12a); S(O)2R12; Т2; C1-6 алкил, где C1-6 алкил необязательно замещен одним или несколькими R13, которые являются одинаковыми или различными; R11b, R11d независимо выбраны из группы, включающей Н; галоген; CN; OR12; S(О)2N(R12R12a); S(O)R12; C1-6 алкил, где C1-6 алкил необязательно замещен одним или несколькими R13, которые являются одинаковыми или различными; R12, R12a независимо выбраны из группы, включающей Н и C1-6 алкил, где C1-6 алкил необязательно замещен одним или несколькими R13, которые являются одинаковыми или различными; Т2 представляет собой 5-членный гетероцикл с двумя атомами азота в цикле; R13 представляет собой галоген; CN; OR14; С(О)N(R14R14a); S(O)2N(R14R14a); S(O)2R14; S(O)R14; N(R14)S(О)2N(R14aR14b); N(R14)S(O)N(R14aR14b); SR14; N(R14R14a); NO2; OC(O)R14; N(R14)S(О)2R14a; R14, R14a, R14b независимо выбраны из группы, включающей Н или C1-6 алкил, где C1-6 алкил необязательно замещен одним или несколькими R15, которые являются одинаковыми или различными; R15 представляет собой галоген. 4 н. и 14 з.п. ф-лы, 13 табл., 480 пр.
Реферат
Настоящее изобретение относится к новому классу ингибиторов киназ, включая их фармацевтически приемлемые соли, пролекарства и метаболиты, которые используют для модуляции активности протеинкиназы для модуляции клеточной активности, например, сигнальной трансдукции, пролиферации и секреции цитокинов. Более конкретно, изобретение относится к соединениям, которые ингибируют, регулируют и/или модулируют активность TYK2 и пути сигнальной трансдукции, относящиеся к клеточной активности, как указано выше. Кроме того, настоящее изобретение относится к фармацевтическим композициям, содержащим указанные соединения, например, для лечения или профилактики иммунологического, воспалительного, аутоиммунного или аллергического расстройства или заболевания или отторжения трансплантата или заболевания “трансплантат-против-хозяина” и способам получения указанных соединений.
Киназы катализируют фосфорилирование белков, липидов, сахаров, нуклеозидов и других клеточных метаболитов и играют ключевую роль во всех аспектах физиологии эукариотической клетки. В частности, протеинкиназы и липидные киназы участвуют в сигнальных событиях, которые контролируют активацию, рост, дифференцировку и выживаемость клеток в ответ на внеклеточные медиаторы или стимулы, такие как факторы роста, цитокины или хемокины. В общем протеинкиназы разделены на две группы: протеинкиназы, которые, предпочтительно, фосфорилируют остатки тирозина, и протеинкиназы, которые, предпочтительно, фосфорилируют остатки серина и/или треонина. Тирозинкиназы включают трансмембранные рецепторы факторов роста, такие как рецептор эпидермального фактора роста (EGFR) и цитозольные нерецепторные киназы, такие как Янус-киназы (JAK).
Несоответственно высокая протеинкиназная активность вовлечена во многие заболевания, включая злокачественную опухоль, нарушения обмена веществ, аутоиммунные или воспалительные заболевания. Этот эффект может быть вызван, прямо или косвенно, нарушением механизмов контроля в результате мутации, сверхэкспрессии или несоответствующей активации фермента. Во всех этих случаях, селективное ингибирование киназы, как полагают, оказывает благоприятный эффект.
Одна группа киназ, на которой в последнее время сосредоточено внимание в области открытия лекарственных средств, представляет собой семейство Янус-киназ (JAK) нерецепторных тирозинкиназ. У млекопитающих, семейство включает четыре члена: JAK1, JAK2, JAK3 и тирозин-киназа 2 (TYK2). Каждый белок имеет киназный домен и каталитически неактивной псевдо-киназный домен. Белки JAK связываются с цитокиновыми рецепторами через их амино-терминальные домены FERM (Band-4,1, эзрин, радиксин, моезин). После связывания цитокинов с их рецепторами, JAK активируются и фосфорилируют рецепторы, тем самым создавая док-сайты для сигнальных молекул, в частности для членов семейства сигнальных трансдукторов и активаторов транскрипции (STAT) (Yamaoka et al, 2004. The Janus kinases (Jaks). Genome Biology 5(12): 253).
У млекопитающих, JAK1, JAK2 и TYK2 экспрессируются убиквитарно. В отличие от этого, экспрессия JAK3 происходит преимущественно в кроветворных клетках, и она строго регулируется клеточным развитием и активацией клеток (Musso et al, 1995. J. Exp. Med. 181(4): 1425-31).
Изучение JAK-дефицитных клеточных линий и мышей с направлено измененными генами, выявило существенные незаменимые функции JAK в сигнализации цитокинов. Мыши, нокаутные по JAK1, обладают перинатальным летальным фенотипом, связанным, вероятно, с неврологическими эффектами, которые нарушают у них сосательный рефлекс (Rodig et al, 1998. Cell 93(3):373-83). Делеция гена JAK2 приводит к смерти эмбриона на день 12,5 в результате дефекта в эритропоэзе (Neubauer et al, 1998. Cell 93(3):397-409). Интересно, что дефицит JAK3 был впервые выявлен у людей с аутосомно-рецессивной формой тяжелого комбинированного иммунодефицита (SCID) (Macchi et al, 1995. Nature 377(6544):65-68). Мыши, нокаутные по JAK3, также демонстрируют SCID, но не показывают неиммунные нарушения, указывая на то, что ингибитор JAK3, в качестве иммунодепрессанта, обладает ограничивающими эффектами in vivo и, следовательно, представляет собой перспективный препарат для иммуносупрессии (Papageorgiou и Wikman 2004, Trends in Pharmacological Sciences 25(11):558-62).
Роль TYK2 в биологической реакции на цитокины впервые была охарактеризована с использованием мутантной линии клеток человека, которая была резистентна к воздействию интерферонов типа I (IFN) и показала, что IFNα реактивность может быть восстановлена путем генетической комплементации TYK2 (Velazquez et al, 1992. Cell 70, 313-322). Дальнейшие in vitro исследования показали, что TYK2 в сигнальных путях многочисленных других цитокинов связан как с врожденным, так и приобретенным иммунитетом. Однако исследование TYK-2-/- мышей выявило менее значительные иммунологические дефекты, чем те, которые ожидались (Karaghiosoff et al, 2000. Immunity 13, 549-560; Shimoda et al, 2000. Immunity 13, 561-671). Удивительно, TYK2-дефицитные мыши показали лишь пониженную восприимчивость к IFNα/β и нормально реагировали на интерлейкин 6 (IL-6) и интерлейкин 10 (IL-10), оба которые активируют TYK2 in vitro. В отличие от этого, было показано, что TYK2 необходим для сигнализации IL-12 при отсутствии TYK2, приводя к активации дефектного STAT4 и нарушению способности Т-клеток этих мышей дифференцироваться в IFNγ-продуцирующие Th1-клетки. В соответствии с включением TYK2 в опосредование биологических эффектов IFN типа I и IL-12, TYK2-/- мыши были более восприимчивы к вирусным и бактериальным инфекциям.
До сих пор был описан только один пациент с аутосомно-рецессивным дефицитом TYK2 (Minegishi et al, 2006. Immunity 25, 745-755). Гомозиготная делеция четырех пар оснований (GCTT на нуклеотиде 550 в гене TYK2) и последующая мутация со сдвигом рамки считывания, кодирующей ДНК пациента, интродуцирует преждевременный стоп-кодон и приводит к процессированию белка TYK2 на аминокислоте 90. Фенотип этой нуль-мутации в клетках человека был значительно более серьезным, чем предполагаемый в исследованиях, выполняемых в мышиных клетках, лишенных TYK2. Пациент демонстрировал клинические симптомы, напоминающие первичный иммунодефицит - гипер-IgE синдром (HIES), включающий рецидивирующий абсцес кожи, атопический дерматит, крайне повышенные уровни IgE в сыворотке и восприимчивость к многочисленным оппортунистическим инфекциям. Вопреки сообщениям, было обнаружено, что у TYK2-/- мышей, посредством широкого ряда цитокинов, будет нарушена сигнализация, подчеркивая, таким образом, необходимую роль TYK2 для человека в зависимости от IFN типа I, IL-6, IL-10, IL-12 и IL-23. Также наблюдался дисбаланс в дифференциации Т-клеток-хелперов, при этом Т-клетки пациента демонстрировали чрезмерный сдвиг в сторону развития Th2 клеток, продуцирующих IL-4, и ослабление дифференциации Th1. Фактически, эти нарушения сигнализации цитокинов могут отвечать за многие описанные клинические проявления, например, атопический дерматит и повышенные уровни IgE (повышенное количество Th2), рост заболеваемости вирусными инфекциями (дефицит IFN), инфекции, вызываемые внутриклеточными бактериями (дефицит IL-12/Th1) и внеклеточными бактериями (дефицит IL-6 и IL-23/Th17).
Новые данные полногеномного поиска ассоциаций предполагает, что полиморфизм отдельных нуклеотидов (SNP) в гене TYK2 оказывает существенное влияние на восприимчивость к аутоиммунным заболеваниям. Менее эффективные варианты TYK2 ассоциированы с защитой от системной красной волчанки (SLE) (TYK2 rs2304256 и rs12720270, Sigurdsson et al, 2005. Am. J. Hum. Genet. 76, 528-537; Graham et al, 2007. Rheumatology 46, 927-930; Hellquist et al, 2009. J. Rheumatol. 36, 1631-1638; Jarvinen et al, 2010. Exp. Dermatol. 19, 123-131) и рассеянного склероза (MS) (rs34536443, Ban et al, 2009. Eur. J. Hum. Genet. 17, 1309-1313; Mero et al, 2009. Eur. J. Hum. Genet. 18, 502-504). Тогда как предполагаемая “мутация приобретения функции” повышает восприимчивость к воспалительному заболеванию кишечника (IBD) (rs280519 и rs2304256, Sato et al, 2009. J. Clin. Immunol. 29, 815-825). В подтверждение участия в TYK2 процессах иммунопатологических заболеваний, было показано, что мыши B10.D1, несущие миссенс-мутации в псевдокиназном домене TYK2, приводящих к недостатку кодируемого TYK2 белка, резистентны и к аутоиммунному артриту (CIA) и к экспериментальному аутоиммунному энцефаломиелиту (EAE) (Shaw et al., 2003. PNAS 100, 11594-11599; Spach et al, 2009. J. Immunol. 182, 7776-7783). Кроме того, недавнее исследование показало, что TYK2-/- мыши были полностью резистентны к MOG-индуцированному EAE (Oyamada et al, 2009. J. Immunol. 183, 7539-7546). У этих мышей резистентность сопровождалось недостатком CD4 Т-клеток, проникающих в спинной мозг, нарушением передачи сигнала через IL-12R и IL-23R и, следовательно, невозможностью повышающе регулировать энцефалитогенные уровни IFNγ и IL-17.
Нерецепторная тирозинкиназа TYK2 играет существенную роль как во врожденном, так и в приобретенном иммунитете. Недостаточная экспрессия TYK2 проявляется в ослабленной сигнализации нескольких противоспалительных цитокинов и сильном дисбалансе в дифференциации Т-клеток-хелперов. Кроме того, данные исследований генетической ассоциации подтверждают, что TYK2 является общим геном предрасположенности к аутоиммунному заболеванию. Взятые вместе, эти причины предусматривают TYK2 в качестве мишени для лечения воспалительных и аутоиммунных заболеваний.
В литературе были описаны некоторые ингибиторы семейства JAK, которые могут быть использованы в области медицины (Ghoreschi et al, 2009, Immunol Rev, 228: 273-287). Ожидается, что селективный ингибитор TYK2, который ингибирует TYK2 с большей эффективностью, чем JAK2, может обладать благоприятными терапевтическими свойствами, поскольку ингибирование JAK2 может вызвать анемию. (Ghoreschi et al, 2009. Nature Immunol. 4, 356-360).
Пиримидиновые производные, обладающие ингибирующей активностью в отношении киназ JAK3 и JAK2, описаны в WO-A 2008/009458. Пиримидиновые соединения для лечения состояний, в которых осуществляется модуляция пути JAK или ингибирование киназ JAK, в частности, JAK3, описаны в WO-A 2008/118822 и WO-2008/118823.
Фтор замещенные пиримидиновые соединения в качестве ингибиторов JAK3 описаны в WO-A 2010/118986. Гетероциклильные пиразолопиримидиновые аналоги в качестве ингибиторов JAK описаны в WO-A 2011/048082.
В WO-A 2008/129380 описаны сульфониламидные производные для лечения патологического роста клеток.
Ингибиторы TYK2 описаны в WO-A 2012/000970 и WO-A 2012062704.
Ингибиторы TYK2 также описаны в DE-A 102009001438, DE-102009015070, WO-A 2011/113802, WO-A 2012/035039 и WO-A 2012/000970.
Соответственно, соединения, которые ингибируют активность TYK2, являются лечебными, в частности, с селективностью в отношении JAK2. Такие соединения могут обеспечить фармакологический ответ, что оказывает лечебное воздействие на одно или несколько состояний, описанных в настоящем документе без излишних побочных эффектов, связанных с ингибированием JAK2.
Даже при том, что ингибиторы TYK2 известны, в этой области техники существует потребность в других ингибиторах, обладающих, по меньшей мере отчасти, более эффективными соответствующими фармацевтическими свойствами, такими как активность, селективность, в частности, в отношении киназы JAK2, и свойствами ADMET.
Таким образом, задачей настоящего изобретения является создание нового класса соединений в качестве ингибиторов TYK2, которые, предпочтительно, проявляют селективность по JAK2, и могут быть эффективными при лечении или профилактике расстройств, связанных с TYK2.
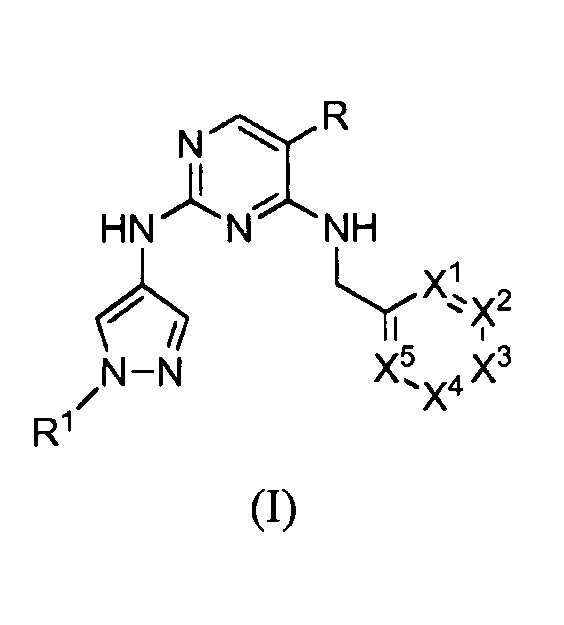
Таким образом, настоящее изобретение относится к соединениям формулы (I)
,
или их фармацевтически приемлемым солям или изотопным производным, где
R представляет собой Н; F; Cl; Br; или незамещенный C1-3 алкил;
R1 представляет собой H; C(O)OR2; C(O)R2; C(O)N(R2R2a); S(O)2N(R2R2a); S(O)N(R2R2a); S(O)2R2; S(O)R2; T1; C1-6 алкил; C2-6 алкенил; или C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R3, которые являются одинаковыми или различными;
R2, R2a независимо выбраны из группы, включающей H; T1; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R3, которые являются одинаковыми или различными;
R3 представляет собой галоген; CN; C(O)OR4; OR4; C(O)R4; C(O)N(R4R4a); S(O)2N(R4R4a); S(O)N(R4R4a); S(O)2R4; S(O)R4; N(R4)S(O)2N(R4aR4b); N(R4)S(O)N(R4aR4b); SR4; N(R4R4a); NO2; OC(O)R4; N(R4)C(O)R4a; N(R4)S(O)2R4a; N(R4)S(O)R4a; N(R4)C(O)N(R4aR4b); N(R4)C(O)OR4a; OC(O)N(R4R4a); или T1;
R4, R4a, R4b независимо выбраны из группы, включающей H; T1; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R5, которые являются одинаковыми или различными;
R5 представляет собой галоген; CN; C(O)OR6; OR6; C(O)R6; C(O)N(R6R6a); S(O)2N(R6R6a); S(O)N(R6R6a); S(O)2R6; S(O)R6; N(R6)S(O)2N(R6aR6b); N(R6)S(O)N(R6aR6b); SR6; N(R6R6a); NO2; OC(O)R6; N(R6)C(O)R6a; N(R6)S(O)2R6a; N(R6)S(O)R6a; N(R6)C(O)N(R6aR6b); N(R6)C(O)OR6a; OC(O)N(R6R6a); или T1;
R6, R6a, R6b независимо выбраны из группы, включающей H; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими атомами галогена, которые являются одинаковыми или различными;
T1 представляет собой фенил, C3-7 циклоалкил; 4-7-членный гетероциклил; или 7-11-членный гетеробициклил, где T1 необязательно замещен одним или несколькими R7, которые являются одинаковыми или различными;
R7 представляет собой галоген; CN; C(O)OR8; OR8; оксо (=O), где кольцо является, по крайней мере, частично, насыщенным; C(O)R8; C(O)N(R8R8a); S(O)2N(R8R8a); S(O)N(R8R8a); S(O)2R8; S(O)R8; N(R8)S(O)2N(R8aR8b); N(R8)S(O)N(R8aR8b); SR8; N(R8R8a); NO2; OC(O)R8; N(R8)C(O)R8a; N(R8)S(O)2R8a; N(R8)S(O)R8a; N(R8)C(O)N(R8aR8b); N(R8)C(O)OR8a; OC(O)N(R8R8a); C1-6 алкил; C2-6 алкенил; или C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R9, которые являются одинаковыми или различными;
R8, R8a, R8b независимо выбраны из группы, включающей H; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R9, которые являются одинаковыми или различными;
R9 представляет собой галоген; CN; C(O)OR10; OR10; C(O)R10; C(O)N(R10R10a); S(O)2N(R10R10a); S(O)N(R10R10a); S(O)2R10; S(O)R10; N(R10)S(O)2N(R10aR10b); N(R10)S(O)N(R10aR10b); SR10; N(R10R10a); NO2; OC(O)R10; N(R10)C(O)R10a; N(R10)S(O)2R10a; N(R10)S(O)R10a; N(R10)C(O)N(R10aR10b); N(R10)C(O)OR10a; или OC(O)N(R10R10a);
R10, R10a, R10b независимо выбраны из группы, включающей H; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими атомами галогена, которые являются одинаковыми или различными;
X1 представляет собой C(R11a) или N; X2 представляет собой C(R11b) или N; X3 представляет собой C(R11c) или N; X4 представляет собой C(R11d) или N; X5 представляет собой C(R11e) или N, при условии, что не более чем два из X1, X2, X3, X4, X5 представляют собой N;
R11a, R11c, R11e независимо выбраны из группы, включающей H; галоген; CN; C(O)OR12; OR12; C(O)R12; C(O)N(R12R12a); S(O)2N(R12R12a); S(O)N(R12R12a); S(O)2R12; S(O)R12; N(R12)S(O)2N(R12aR12b); N(R12)S(O)N(R12aR12b); SR12; N(R12R12a); NO2; OC(O)R12; N(R12)C(O)R12a; N(R12)C(O)N(R12aR12b); N(R12)C(O)OR12a; OC(O)N(R12R12a); T2; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R13, которые являются одинаковыми или различными;
R11b, R11d независимо выбраны из группы, включающей H; галоген; CN; C(O)OR12; OR12; C(O)R12; C(O)N(R12R12a); S(O)2N(R12R12a); S(O)N(R12R12a); S(O)2R12; S(O)R12; N(R12)S(O)2N(R12aR12b); N(R12)S(O)N(R12aR12b); SR12; N(R12R12a); NO2; OC(O)R12; N(R12)C(O)R12a; N(R12)C(O)N(R12aR12b); N(R12)C(O)OR12a; OC(O)N(R12R12a); C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R13, которые являются одинаковыми или различными;
R12, R12a, R12b независимо выбраны из группы, включающей H; T2; и C1-6 алкил, где C1-6 алкил; необязательно замещен одним или несколькими R13, которые являются одинаковыми или различными;
R13 представляет собой галоген; CN; C(O)OR14; OR14; C(O)R14; C(O)N(R14R14a); S(O)2N(R14R14a); S(O)N(R14R14a); S(O)2R14; S(O)R14; N(R14)S(O)2N(R14aR14b); N(R14)S(O)N(R14aR14b); SR14; N(R14R14a); NO2; OC(O)R14; N(R14)C(O)R14a; N(R14)S(O)2R14a; N(R14)S(O)R14a; N(R14)C(O)N(R14aR14b); N(R14)C(O)OR14a; OC(O)N(R14R14a); или T2;
R14, R14a, R14b независимо выбраны из группы, включающей H; T2; или C1-6 алкил, где C1-6 алкил необязательно замещен одним или несколькими R15, которые являются одинаковыми или различными;
R15 представляет собой галоген; CN; C(O)OR16; OR16; C(O)R16; C(O)N(R16R16a); S(O)2N(R16R16a); S(O)N(R16R16a); S(O)2R16; S(O)R16; N(R16)S(O)2N(R16aR16b); N(R16)S(O)N(R16aR16b); SR16; N(R16R16a); NO2; OC(O)R16; N(R16)C(O)R16a; N(R16)S(O)2R16a; N(R16)S(O)R16a; N(R16)C(O)N(R16aR16b); N(R16)C(O)OR16a; OC(O)N(R16R16a); или T2;
R16, R16a, R16b независимо выбраны из группы, включающей H; T2; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими атомами галогена, которые являются одинаковыми или различными;
T2 представляет собой фенил; нафтил; инденил; инданил; C3-7 циклоалкил; 4-7-членный гетероциклил; или 7-11-членный гетеробициклил, где T2 необязательно замещен одним или несколькими R17, которые являются одинаковыми или различными;
R17 представляет собой галоген; CN; C(O)OR18; OR18; оксо (=O), где кольцо является, по крайней мере, частично, насыщенным; C(O)R18; C(O)N(R18R18a); S(O)2N(R18R18a); S(O)N(R18R18a); S(O)2R18; S(O)R18; N(R18)S(O)2N(R18aR18b); N(R18)S(O)N(R18aR18b); SR18; N(R18R18a); NO2; OC(O)R18; N(R18)C(O)R18a; N(R18)S(O)2R18a; N(R18)S(O)R18a; N(R18)C(O)N(R18aR18b); N(R18)C(O)OR18a; OC(O)N(R18R18a); C1-6 алкил; C2-6 алкенил; или C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R19, которые являются одинаковыми или различными;
R18, R18a, R18b независимо выбраны из группы, включающей H; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими R19, которые являются одинаковыми или различными;
R19 представляет собой галоген; CN; C(O)OR20; OR20; C(O)R20; C(O)N(R20R20a); S(O)2N(R20R20a); S(O)N(R20R20a); S(O)2R20; S(O)R20; N(R20)S(O)2N(R20aR20b); N(R20)S(O)N(R20aR20b); SR20; N(R20R20a); NO2; OC(O)R20; N(R20)C(O)R20a; N(R20)S(O)2R20a; N(R20)S(O)R20a; N(R20)C(O)N(R20aR20b); N(R20)C(O)OR20a; или OC(O)N(R20R20a);
R20, R20a, R20b независимо выбраны из группы, включающей H; C1-6 алкил; C2-6 алкенил; и C2-6 алкинил, где C1-6 алкил; C2-6 алкенил; и C2-6 алкинил необязательно замещены одним или несколькими атомами галогена, которые являются одинаковыми или различными.
В случае если переменная или заместитель могут быть выбраны из группы различных вариантов, и такая переменная или заместитель встречаются более одного раза, соответствующие варианты могут быть одинаковыми или различными.
В контексте настоящего изобретения используются следующие термины:
Термин "необязательно замещенный" означает незамещенный или замещенный. В большинстве случаев (но ими не ограничиваясь) "один или несколько заместителей" означает один, два или три, предпочтительно, один или два и, более предпочтительно, один. Как правило, эти заместители могут быть одинаковыми или разными.
"Алкил" означает неразветвленную или разветвленную углеводородную цепь. Каждый атом водорода на атоме углероде алкильной группы может быть заменен заместителем, как указано далее в настоящем документе.
"Алкенил" означает прямую цепь или разветвленную углеводородную цепь, содержащую, по крайней мере, одну углерод-углерод двойную связь. Каждый атом водорода на атоме углерода алкенилной группы может быть заменен заместителем, как указано далее в настоящем документе.
"Алкинил" означает прямую цепь или разветвленную углеводородную цепь, содержащую, по крайней мере, одну углерод-углерод тройную связь. Каждый атом водорода на атоме углерода алкинильной группы может быть заменен заместителем, как указано далее в настоящем документе.
"C1-3-алкил" означает алкильную цепь, содержащую 1-3 атома углерода, например, если присутствуют на конце молекулы: метил, этил, н-пропил, изопропил, или, например, -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)-, -C(CH3)2-, когда два фрагменты молекулы связаны алкильной группой. Каждый атом водорода на атоме углерода C1-3 алкила может быть заменен заместителем, как указано далее в настоящем документе.
“C1-4 алкил” означает алкильную цепь, содержащую 1-4 атома углерода, например, если присутствуют на конце молекулы: C1-3 алкил, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, или например -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)-, -C(CH3)2-, когда два фрагмента молекулы связаны с алкильной группой. Каждый атом водорода на атоме углерода C1-4 алкильной группы может быть замещен заместителем, как указано далее в настоящем документе.
“C1-6 алкил” означает алкильную цепь, содержащую 1-6 атомов углерода, например, если присутствуют на конце молекулы: C1-3 алкил, C1-4 алкил, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил; трет-бутил, н-пентил, н-гексил, или например -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)-, -C(CH3)2-, когда два фрагмента молекулы связаны с алкильной группой. Каждый атом водорода на атоме углерода C1-6 алкильной группы может быть заменен заместителем, как указано далее в настоящем документе.
“C2-6 алкенил” означает алкенильную цепь, содержащую 2-6 атомов углерода, например, если присутствуют на конце молекулы: -CH=CH2, -CH=CH-CH3, -CH2-CH=CH2, -CH=CH-CH2-CH3, -CH=CH-CH=CH2, или например, -CH=CH-, когда два фрагмента в молекуле связаны посредством алкенильной группы. Каждый атом водорода на атоме углерода C2-6 алкенильной группы может быть заменен заместителем, как указано далее в настоящем документе.
“C2-6 алкинил” означает алкинильную цепь, содержащую 2-6 атомов углерода, например, если присутствуют на конце молекулы: -C≡CH, -CH2-C≡CH, CH2-CH2-C≡CH, CH2-C≡C-CH3 или например, -C≡C-, когда два фрагмента в молекуле связаны посредством алкинильной группы. Каждый атом водорода на атоме углерода C2-6 алкинильной группы может быть заменен заместителем, как указано далее в настоящем документе.
“C3-7 циклоалкил” или “C3-7 циклоалкильное кольцо” означает циклическую алкильную цепь, содержащую 3-7 атомов углерода, например циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил. Предпочтительно, циклоалкил относится к циклопропилу, циклобутилу, циклопентилу, циклогексилу или циклогептилу. Каждый атом водорода на атоме углерода циклоалкильной группе может быть заменен заместителем, как указано далее в настоящем документе. Термин “C3-5 циклоалкил” или “C3-5 циклоалкильное кольцо” определен соответственно.
“Галоген” означает фтор, хлор, бром или йод. Обычно предпочтительным является, когда галогеном является фтор или хлор.
“4-7-членный гетероциклил” или “4-7-членный гетероцикл” означает кольцо с 4, 5, 6 или 7 кольцевыми атомами, которое может содержать вплоть до максимального количества двойных связей (ароматическое или неароматическое кольцо, которое является полностью, частично или ненасыщенным), где, по меньшей мере, один из от одного до 4 кольцевых атомов заменены гетероатомом, выбранным из группы, включающей: серу (включая -S(O)-, -S(O)2-), кислород и азот (включая =N(O)-), и где кольцо связано с остальной частью молекулы через атом углерода или азота. Примерами 4-7-членных гетероциклов являются азетидин, оксетан, тиетан, фуран, тиофен, пиррол, пирролин, имидазол, имидазолин, пиридазол, пиразолин, оксазол, оксазолин, изоксазол, изоксазолин, тиазол, тиазолин, изотиазол, изотиазолин, тиадиазол, тиадиазолин, тетрагидрофуран, тетрагидротиофен, пирролидин, имидазолидин, пиразолидин, оксазолидин, изоксазолидин, тиазолидин, изотиазолидин, тиадиазолидин, сульфолан, пиран, дигидропиран, тетрагидропиран, имидазолидин, пиридин, пиридазин, пиразин, пиримидин, пиперазин, пиперидин, морфолин, тетразол, триазол, триазолидин, тетразолидин, диазепан, азепин или гомопиперазин. Термин “5-6-членный гетероциклил” или “5-6-членный гетероцикл” определен соответственно.
“Насыщенный 4-7-членный гетероциклил” или “насыщенный 4-7-членный гетероцикл” означает полностью насыщенный “4-7-членный гетероциклил” или “4-7-членный гетероцикл”.
“5-членный ароматический гетероциклил” или “5-членный ароматический гетероцикл” означает гетероцикл, полученный из циклопентадиенила, где, по крайней мере, один атом углерода заменен на гетероатом, выбранный из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-). Примерами таких гетероциклов являются фуран, тиофен, пиррол, имидазол, пиридазол, оксазол, изоксазол, тиазол, изотиазол, тиадиазол, триазол, тетразол.
"7-11-членный гетеробициклил" или "7-11-членный гетеробицикл" означает гетероциклическую систему из двух колец с 7-11 атомами в кольце, где, по крайней мере, один кольцевой атом является общим для обоих колец, и которая может содержать, вплоть до максимального количества, двойные связи (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично насыщенным или ненасыщенным) где, по крайней мере, от одного до 6 кольцевых атомов заменены гетероатомом, выбранным из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где кольцо связано с остальной частью молекулы через атом углерода или азота. Примерами 7-11-членного гетеробицикла являются индол, индолин, бензофуран, бензотиофен, бензоксазол, бензизоксазол, бензотиазол, бензизотиазол, бензимидазол, бензимидазолин, хинолин, хиназолин, дигидрохиназолин, хинолин, дигидрохинолин, тетрагидрохинолин, декагидрохинолин, изохинолин, декагидроизохинолин, тетрагидроизохинолин, дигидроизохинолин, бензазепин, пурин или птеридин. Термин 7-11-членный гетеробицикл также включает спиро структуры из двух колец, например, 1,4-диоса-8-азаспиро[4,5]декан 2-окса-6-азаспиро[3,3]гептан-6-ил или 2,6-диазаспиро[3,3]гептан-6-ил, или соединенные мостиковой связью гетероциклы, такие как 8-аза-бицикло[3,2,1]октан или 2,5-диазабицикло[2,2,2]октан-2-ил.
Предпочтительными соединениями формулы (I) являются соединения, в которых один или несколько остатков, содержащихся в них, имеют значения, указанные ниже, со всеми комбинациями предпочтительных определений заместителей, и они являются предметом настоящего изобретения. В отношении всех предпочтительных соединений формулы (I), настоящее изобретение также включает все таутомерные и стереоизомерные формы и их смеси во всех соотношениях, и их фармацевтически приемлемые соли.
В предпочтительных вариантах осуществления настоящего изобретения, заместители, указанные ниже, независимо друг от друга, имеют следующие значения. Следовательно, один или несколько из этих заместителей могут иметь предпочтительные или более предпочтительные значения, приведенные ниже.
Предпочтительно, R1 представляет собой незамещенный C1-4 алкил; или C1-4 алкил, замещенный одним или несколькими R3, которые являются одинаковыми или различными. Более предпочтительно, R1 представляет собой C1-4 алкил, замещенный одним или двумя R3.
Предпочтительно, R1 представляет собой H; или CH3.
Предпочтительно, R3 представляет собой галоген, OR4; C(O)N(R4R4a); C(O)T1; или T1. Более предпочтительно, R3 представляет собой C(O)N(R4R4a); C(O)T1; или T1.
Предпочтительно, R4, R4a независимо выбраны из группы, включающей H; T1; и C1-4 алкил, необязательно замещенный OR6. Более предпочтительно, R4 представляет собой изо-пропил, необязательно замещенный OH; или циклопропил.
Предпочтительно, T1 представляет собой морфолинил; пирролидинил; пиперидинил; тетрагидрофуранил; циклобутил; или циклопропил. Более предпочтительно, T1 представляет собой морфолинил; пирролидинил; тетрагидрофуранил; или циклопропил.
Предпочтительно, R1 представляет собой CH2C(O)NHCH(CH3)2; CH2C(O)NHCH(CH3)CH2OH; CH2C(O)NH(морфолин-4-ил); CH2C(O)NH(циклопропил); или CH2CH2(морфолин-4-ил).
Предпочтительно, R представляет собой H; F; Cl; или CH3;, более предпочтительно, R представляет собой H; или F; Еще, более предпочтительно, R представляет собой H.
Предпочтительно, группы R11a, R11b, R11c, R11d, R11e выбраны из группы, включающей H; галоген; CN; OR12; C(O)R12; C(O)N(R12R12a); S(O)2N(R12R12a); S(O)2R12; или C1-6 алкил, необязательно замещенный одним или несколькими галогенами. Более предпочтительно, группы R11a, R11b, R11c, R11d, R11e выбраны из группы, включающей H; F; Cl; CN; OCH3; OCHF2; C(O)NH2; SO2NH2; CH3; или CF3.
Предпочтительно, R11a, R11b представляют собой, независимо, F; или Cl.
Предпочтительно, оба R11a и R11e представляют собой Cl.
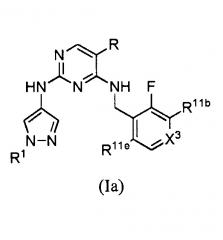
Предпочтительные сочетания заместителей определяются формулой (Ia):
,
где R представляет собой H или F;
X3 представляет собой N; или C(R11c);
R11b представляет собой H; F; Cl; CH3; CN; или OCH3;
R11c представляет собой H; F; Cl; CH3; CN; OCH3; SO2NH2; или C(O)N(R12R12a);
R11e представляет собой F; Cl; или CH3;
и где R1, R12, R12a имеют указанные выше значения;
при условии, что, по крайней мере, один или оба R11b, R11c представляют собой H.
Предпочтительно X1, X2, X4, X5 являются иными, чем N.
Предпочтительно, R представляет собой H.
Соединения формулы (I), в которой некоторые или все из вышеуказанных групп имеют предпочтительные значения, также являются объектом настоящего изобретения.
Другие предпочтительные соединения по настоящему изобретению выбраны из группы, включающей:
2-(4-((4-((4-циано-2,6-дифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-изопропилацетамид;
(S)-2-(4-((4-((2,6-дихлорбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-(1-гидроксипропан-2-ил)ацетамид;
N-циклопропил-2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамид;
N-(1-цианоэтил)-2-(4-((4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамид;
N-этил-2-(4-((4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамид;
3,5-дифтор-N,N-диметил-4-(((2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)метил)бензамид;
4-(((2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)метил)бензолсульфонамид;
4-(((5-фтор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)метил)бензолсульфонамид;
2-(4-((5-хлор-4-((4-сульфамоилбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-циклопропилацетамид;
4-(((5-фтор-2-((1-(2-морфолинo-2-оксоэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)метил)бензолсульфонамид;
2-(4-((4-((2,6-дифтор-3-метоксибензил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамид;
2-(4-((4-((2,6-дифтор-3-метоксибензил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N,N-диметилацетамид;
2-(4-((4-((3-(дифторметокси)бензил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N,N-диметилацетамид;
2-(4-((5-хлор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)этанол;
2-(4-((5-хлор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N,N-диметилацетамид;
2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)этанол;
2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N,N-диметилацетамид;
N,N-диметил-2-(4-((5-метил-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамид;
2-(4-((4-((2,6-дифтор-3-метоксибензил)амино)-5-метилпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N,N-диметилацетамид;
2-(4-((5-метил-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолинoэтанон;
2-(4-((4-((2,6-дифтор-3-метоксибензил)амино)-5-метилпиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолинoэтанон;
2-(4-((4-((3-(дифторметокси)бензил)амино)-5-метилпиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолинoэтанон;
2-(4-((4-((2,6-дифтор-3-метоксибензил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолинoэтанон;
2-(4-((4-((3-бром-2-фторбензил)амино)-5-хлорпиримидин-2-ил)амино)-1H-пиразол-1-ил)этанол;
2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолинoэтанон;
1-морфолинo-2-(4-((4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)этанон;
2-(4-((4-((2,6-дифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолинoэтанон;
2-(4-((4-((2,6-дифтор-4-метоксибензил)амино)-5-метилпиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолинoэтанон;
4-(((5-фтор-2-((1-(2-оксо-2-(пиперидин-1-ил)этил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)метил)бензолсульфонамид;
3,5-дифтор-4-(((5-фтор-2-((1-(2-оксо-2-(пиперидин-1-ил)этил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)метил)бензолсульфонамид;
N-изопропил-2-(4-((5-метил-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамид;
N-циклобутил-2-(4-((5-метил-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамид;
1-(2,2-диметилморфолинo)-2-(4-((5-метил-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)этанон;
(R)-N-(1-гидроксипропан-2-ил)-2-(4-((5-метил-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамид;
(S)-N-(1-гидроксипропан-2-ил)-2-(4-((5-метил-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамид;
2-(4-((5-метил-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-(тетрагидрофуран-3-ил)ацетамид;
2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-изопропилацетамид;
1-(2,2-диметилморфолинo)-2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)этанон;
(R)-2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-(3-метилморфолинo)этанон;
(R)-2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-(1-гидроксипропан-2-ил)ацетамид;
(S)-2-(4-((5-фтор-4-((2,4,6-трифторбензил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-(1-гидроксипропан-2-ил)ацетамид;
3,5-дифтор-4-(((5-метил-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)метил)бензолсульфонамид;
2-(4-((4-((3-(дифторметокси)бензил)амино)-5-фторпиримидин-2-