Композиция и способ лечения болезни глаз, связанной с нуклеиновыми кислотами
Иллюстрации
Показать всеГруппа изобретений относится к области медицины, а именно к офтальмологии, и предназначена для лечения синдрома сухости глаз. Композиция для лечения синдрома сухости глаз, связанного с нуклеиновыми кислотами, который развивается в результате выработки/образования нуклеиновых кислот вместе с образованием глазных мукоидных пленок и/или биопленок, содержит дезоксирибонуклеазу I (ДНКазу I) и офтальмологическое вспомогательное вещество, и не содержит антибиотик. Композицию наносят на поверхность глаза для удаления нуклеиновой кислоты с поверхности глаза. Также обеспечивается способ лечения указанного синдрома сухости глаз, предусматривающий введение указанной композиции в глаз в эффективном количестве. Использование группы изобретений позволяет повысить эффективность лечения синдрома сухости глаз, связанного с нуклеиновыми кислотами, который развивается в результате выработки/образования нуклеиновых кислот вместе с образованием глазных мукоидных пленок и/или биопленок. 2 н. и 11 з.п. ф-лы, 16 ил., 7 пр.
Реферат
Перекрестная ссылка на родственные заявки
Настоящая заявка устанавливает приоритет согласно предварительной патентной заявке на патент США №61/600,377, поданной 17 февраля 2012 г., и предварительной патентной заявке №61/569,604, поданной 12 декабря 2011 г., содержание которых полностью включено в настоящую заявку посредством ссылки.
Краткое описание списка последовательностей
Настоящая заявка включает список последовательностей, соответствующий 37 Своду федеральных правил §§ 1.821-1.825. Список последовательностей находится в файле с названием «11738468_1.txt» (790 бит, созданный 14 августа 2012 г.), включенном в настоящую заявку посредством ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к композиции и способу лечения болезни глаз, связанной с нуклеиновыми кислотами.
Предшествующий уровень техники
Эпителий поверхности глаза подвергается постоянному динамическому обмену, что является частью нормального процесса отшелушивания. Данный обмен происходит более интенсивно у пациентов, страдающих различными формами болезней глаз, связанных с нуклеиновыми кислотами, такими как синдром сухих глаз (ССГ). Поверхностные клетки роговицы отшелушиваются в прекорнеальную слезную пленку. Процесс отшелушивания эпителиальных клеток роговицы, или десквамация, регулируется апоптотическими механизмами. Мертвые и умирающие клетки выделяют нуклеиновые кислоты, представляющие собой один из видов появляющихся в очаге поражения молекул, которые могут стимулировать систему врожденного иммунитета и связывают ее с системой приобретенного иммунитета. Например, внеклеточные цепи ДНК были обнаружены в корнеальных филаментах, которые часто присутствуют в роговице пациентов с ССГ. Отшелушенные клетки в прекорнеальной слезной пленке представляют собой потенциальный источник внеклеточной ДНК. Слезная жидкость содержит некоторые компоненты нейтрофильной внеклеточной ловушки (НВЛ). Нейтрофилы неактивно привлекаются к поверхности глаза, и множество нейтрофилов присутствует в слезной пленке при воспалении поверхности глаза, что играет важную роль в развитии и усилении симптомов. Эластаза нейтрофилов и гистоновые белки также были обнаружены в слезной жидкости. Эти сообщения описывают присутствие внеклеточной ДНК, гистонов, эластазы нейтрофилов и нуклеаз в слезной жидкости и предлагают возможные объяснения механизмов, обеспечивающих постоянное образование и удаление внеклеточной ДНК в слезной пленке.
Внеклеточная ДНК в слезной пленке, такой как глазной биопленке и мукоидной пленке, может играть роль в развитии патологии, ассоциированной с болезнью глаз, связанной с нуклеиновыми кислотами. Болезни глаз, связанные с нуклеиновыми кислотами, которые могут быть ассоциированы с образованием глазных мукоидных пленок и/или биопленок, представляют собой потенциально инвалидизирующие состояния, оказывающие негативное воздействие на качество жизни, связанное со зрением. Они могут приводить к развитию дискомфорта в глазах и/или к ухудшению зрительного восприятия, в том числе скорости чтения и контрастной чувствительности.
Несмотря на высокую частоту болезней глаз, связанных с нуклеиновыми кислотами, в настоящее время не существует достаточно эффективного лечения данных состояний. Так, поскольку гиперосмолярность и воспаление традиционно считаются основными причинами синдрома сухих глаз, современные способы лечения сосредоточены на применении гигиенических средств для век, местных антибиотиков, пероральных тетрациклинов, противовоспалительных препаратов и/или кортикостероидов. Такие способы лечения часто неэффективны или нестабильно эффективны. Соответственно, существует необходимость в новых терапевтических способах лечения болезней глаз, связанных с нуклеиновыми кислотами, таких как ССГ, которые развиваются, например, в результате выработки/образования нуклеиновых кислот вместе с образованием глазных мукоидных пленок и/или биопленок.
Краткое описание изобретения
В настоящем изобретении представлена композиция для лечения болезней глаз, связанных с нуклеиновыми кислотами. Данные заболевания могут быть связаны с низким качеством слезной жидкости, которое может быть обусловлено образованием биопленки нуклеиновых кислот/мукоидной пленки на поверхности глаза или внутри глаза. Нуклеиновая кислота может быть внеклеточной. Одним из таких заболеваний является синдром сухих глаз (ССГ). Композиция может включать нуклеазу и офтальмологическое вспомогательное вещество. Нуклеаза может представлять собой ДНКазу или РНКазу или их комбинацию. Нуклеаза может быть эндонуклеазой и экзонуклеазой. ДНКаза может быть дезоксирибонуклеазой I (ДНКазой I), дезоксирибонуклеазой II (ДНКазой II), дезоксирибонуклеазой III или микрококковой нуклеазой. РНКаза может быть рибонуклеазой А (РНКазой А), рибонуклеазой Н (РНКазой Н), рибонуклеазой I (РНКазой I), рибонуклеазой II (РНКазой II), рибонуклеазой III (РНКазой III), рибонуклеазой D (РНКазой D), рибонуклеазой L (РНКазой L), рибонуклеазой Р (РНКазой Р), рибонуклеазой PH (РНКазой PH), рибонуклеазой PhyM (РНКазой PhyM), рибонуклеазой R (РНКазой R), рибонуклеазой T (РНКазой T), рибонуклеазой T1 (РНКазой T1), рибонуклеазой T2 (РНКазой T2), рибонуклеазой U2 (РНКазой U2), рибонуклеазой V1 (РНКазой V1), рибонуклеазой V (РНКазой V), олигрибонуклеазой, экзорибонуклеазой I или экзорибонуклеазой II. ДНКаза или РНКаза могут быть рекомбинантными. Композиция может содержать также антагонист или ингибитор. Антагонист или ингибитор может быть выбран из группы, содержащей антибиотик, антагонист Toll-подобного рецептора, антагонист интерферона типа 1, ингибитор кателицидина, ингибитор MyD88, стероид, противоаллергическое вещество, ингибитор эластазы нейтрофилов и их комбинации.
Также в настоящем изобретении приведен способ лечения болезни глаз, связанной с нуклеазой. Способ может включать введение описанных выше композиций нуклеаз с офтальмологическим вспомогательным веществом в глаз в количестве, эффективном для лечения болезни глаз. Поверхность глаза может содержать слезную пленку, которая может быть представлена биопленкой или мукоидной пленкой. Биопленка или мукоидная пленка могут содержать нуклеиновую кислоту. Нуклеиновая кислота может быть представлена ДНК, РНК или их комбинацией. Слезная пленка может содержать менее 0,05 единиц Куница нуклеазной активности перед введением композиции. Эффективное количество композиции может содержать от 5 нг/мл до 3 мг/мл нуклеазы. Эффективное количество композиции может содержать от 100 нг/мл до 200 нг/мл нуклеазы.
Болезнь глаз, связанная с нуклеиновыми кислотами, может быть ССГ, диффузным ламеллярным кератитом, кератитом, связанным с применением контактных линз, эндофтальмитом или инфекционной кератопатией хрусталика, рубцовым пемфигоидом глаза, сухим кератоконъюнктивитом, синдромом Шегрена, сухим кератоконъюнктивитом, ассоциированным с синдромом Шегрена, сухим кератоконъюнктивитом, не связанным с синдромом Шегрена, офтальмосклерозом, сухим кератитом, ксерофтальмией, нарушением слезной пленки, пониженным уровнем слезообразования, недостаточностью слезной жидкости или дисфункцией мейбомиевых желез. ССГ может быть аутоиммунным ССГ или ССГ, ассоциированным с синдромом Шегрена, например, ССГ может быть вызван одной или несколькими перечисленными ниже причинами: старением, использованием контактных линз и применением лекарственных препаратов. Лекарственные препараты могут включать ампициллин, амоксициллин/клавуланат, метронидазол, клиндамицин, эритромицин, гентамицин, ванкомицин, ципрофлаксин, клиндамицин, тетрациклин, анксиолитик или их комбинацию. Антагонистом Toll-подобного рецептора может быть олигонуклеотид, содержащий последовательность TTAGGG. Олигонуклеотид может содержать последовательность TTAGGGTTAGGGTTAGGGTTAGGG (SEQ ID NO: 1). Антагонистом интерферона типа 1 может быть соединение, которое антагонизирует или конкурентно ингибирует интерферон типа 1, связываясь с его рецептором, например с субъединицами рецептора IFNAR-1 и/или IFNR-2. Соединение может быть антителом к интерферону α (IFNα). Ингибитором кателицидина может быть бактериальный экзополисахарид. Ингибитором эластазы нейтрофилов может быть вещество, выбранное из группы, состоящей из ONO-5046, MR-889, L-694,458, CE-1037, GW-311616 TEI-8362, ONO-6818, AE-3763, FK-706, ICI-200, 880, ZD-0892 и ZD-8321.
Также в настоящем изобретении приведен способ определения наличия у пациента болезни глаз, связанной с нуклеазой. Способ может включать сбор образца слезной жидкости у пациента. Данный образец можно проинкубировать с красителем, который связывает ДНК, например, с красителем picogreen. Кроме того, образец можно проинкубировать с ДНКазой и после этого с красителем. Интенсивность окрашивания можно измерить и сравнить с интенсивностью флуоресценции красителя в нормальном контрольном образце. Повышенный по сравнению с контролем уровень интенсивности флуоресценции в образце может указывать на существование синдрома сухих глаз.
Также в настоящем изобретении приведен способ лечения бактериальной инфекции глаз. Способ включает введение композиции, содержащей нуклеазу, в глаз в количестве, которое эффективно для лечения инфекции. Композиция может быть инъецирована в глаз.
Краткое описание чертежей
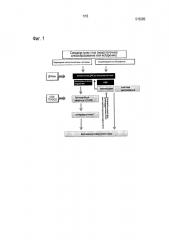
Фигура 1 показывает схему биологии ССГ. Внеклеточная ДНК обнаруживается на поверхности глаз пациентов с ССГ. Данная внеклеточная ДНК может происходить из двух основных источников: из нейтрофилов и из клеток конъюнктивы и из других клеток роговицы. Внеклеточная ДНК нейтрофилов образует нейтрофильные внеклеточные ловушки (НВЛ). Данные НВЛ содержат воспалительные и ангиогенные молекулы, такие как кателицидин, эластазу нейтрофилов, ассоциированный с ними гистон. Внеклеточная ДНК из клеток конъюнктивы, также как и из НВЛ, действует как «молекулы из очага поражения». Молекулы из очага поражения запускают и поддерживают воспаление. ДНК молекул из очага поражения действует через Toll-подобный рецептор 9 (TLR9), повышая уровень интерферонов типа 1, увеличивая уровень нескольких медиаторов воспаления.
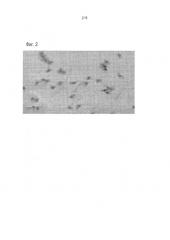
Фигура 2 показывает клетки, перенесенные на покрытые силаном адгезивные стекла, окрашенные гематоксилином и эозином. Ядра и цепи окрашены гематоксилином, что указывает на присутствие внутриклеточной и внеклеточной ДНК, соответственно, свидетельствуя о присутствии НВЛ.
Фигура 3 представляет собой конфокальное изображение (63х) непрямой флуоресценции при окрашивании красителем DAPI для выявления нуклеиновой кислоты. Краситель проникает в клеточное ядро, а также во внеклеточные цепи ДНК. Фигура 3 показывает наличие внеклеточной ДНК, которая важна для формирования НВЛ.
Фигура 4 показывает наличие нейтрофилов и нитей, выходящих из клеток в виде внеклеточной ДНК. Клетки сначала были окрашены с помощью непрямой флуоресценции. (В) показывает внеклеточные нитевидные структуры, выявляя ядерную и внеклеточную ДНК. Затем клетки отмывали и окрашивали гематоксилином и эозином, чтобы подтвердить наличие нейтрофилов и цепей, выходящих из клеток, указывающих на наличие НВЛ.
Фигура 5 представляет собой конфокальное изображение клеток, окрашенных с помощью непрямой флуоресценции первичными антителами к эластазе нейтрофилов, гистону и DAPI. Гранулярное окрашивание эластазы нейтрофилов колокализуется с гистоном и нуклеиновой кислотой.
Фигура 6 показывает наличие НВЛ на поверхности глаза (А). После обработки ДНКазой нитевидная внеклеточная ДНК исчезает, при этом целостность клетки сохраняется (В). Два образца (А) и (В) отбирали у одного и того же пациента. Образец А обрабатывали фосфатно-солевым буфером в течение 20 минут, после чего окрашивали DAPI. Образец В обрабатывали ДНКазой (100 МЕ/мл) в течение 20 минут и окрашивали DAPI.
Фигура 7 подтверждает наличие НВЛ и дифференцирует их от слизи на поверхности глаза. Образец слизи с поверхности конъюнктивы окрашивали DAPI. Окрашивалось ядро, однако слизь не окрашивалась.
Фигура 8 дополнительно подтверждает наличие слизи у того же пациента, образец которого проанализирован на фигуре 7. Данный образец окрашивали реактивом Шиффа. Окрашивание показывает наличие нитей слизи.
Фигура 9 показывает график, построенный для сухих глаз (проба Ширмера <5) по сравнению с нормальным слезообразованием (проба Ширмера >5), с указанием стандартного отклонения. Наблюдается достоверное отличие оптической плотности внеклеточной ДНК при синдроме сухих глаз по сравнению с нормальным слезообразованием. Оптическая плотность в случае синдрома сухих глаз выше (17834,14), чем в случае нормального слезообразования (12609,86). Таким образом, при синдроме сухих глаз количество внеклеточной ДНК, полученной на фильтровальной бумаге в тесте Ширмера, выше, чем при нормальном слезообразовании.
Фигура 10 показывает данные количественной ПЦР в реальном времени об уровне генов интерферона альфа 1, интерферона бета, Toll-подобного рецептора TLR-9 и Myd88 у людей с тяжелой формой синдрома сухих глаз по сравнению с людьми с нормальным слезообразованием (без синдрома сухих глаз). Уровни этих генов повышены в несколько раз в конъюнктиве пациентов с синдромом сухих глаз и угнетенным слезообразованием. Эти пути (TLR-9 и Myd88) стимулируются внеклеточной ДНК, таким образом, данными о рецепторе и транскрипции подтверждается, что воспаление поверхности глаза стимулируется внеклеточной ДНК. Уровень участвующих в последующих стадиях медиаторов воспаления (интерферонов альфа и бета) также повышен у пациентов с синдромом сухих глаз.
Фигура 11 показывает материал, полученный при получении отпечатков полосок пробы Ширмера. (А1, А2): Импрессионная цитология с использованием полосок пробы Ширмера (А1, стрелка) и покрытых силаном стекол (А2). (В): Окрашивание гематоксилином и эозином, показывающее отшелушенные поверхностные клетки. (С): Изображение, полученное с помощью широкопольной флуоресцентной микроскопии после окрашивания DAPI материала оттисков конъюнктивы, показывает наличие коротких и редких цепей внеклеточных ДНК (внДНК) (стрелки) у нормальных индивидов (С1) и многочисленные цепи внеклеточной ДНК (С2) у пациентов с ССГ (стрелки). (D): Изображение, полученное с помощью конфокальной иммунофлуоресцентной микроскопии после окрашивания DAPI, показывает наличие многочисленных нитей (стрелки) и нейтрофилов с многолопастным ядром. (Е): Изображение, полученное с помощью конфокальной иммунофлуоресцентной микроскопии, показывает, что гистоны (Е1, зеленый), эластаза нейтрофилов (Е2, красный) и внДНК (Е3, синий) являются молекулярными компонентами НВЛ (Е4, наложение). Стрелка указывает на нить НВЛ. Вставка на Е2 показывает нейтрофилы с окрашенным DAPI многолопастным ядром. Масштабная линейка: В, С1, С2 и D (50 мкм); Е1 и Е2 вставка (10 мкм).
Фигура 12 показывает внеклеточную ДНК и нейтрофильные внеклеточные ловушки (НВЛ) в мукоидных пленках. (А): Клинические фотографии глаз пациентов с тяжелой формой угнетения слезообразования при ССГ. Стрелка указывает на мукоидную пленку на роговице и бульбарной конъюнктиве (А1), и на нижнем своде (А2). На вставке показано увеличенное изображение мукоидных пленок. (В): цитологическое исследование мукоидных пленок. (В1): окрашивание гематоксилином и эозином показывает поверхностные клетки эпителия и многочисленные нейтрофилы. (В2): окрашивание DAPI показывает наличие цепей внДНК (стрелка) и многолопастного ядра нейтрофилов. (В3): Иммуноокрашивание эластазы нейтрофилов (красный) подтверждает наличие нейтрофилов. (С): Конфокальное изображение, полученное после иммунофлуоресцентного окрашивания, показывает, что эластаза нейтрофилов (С1, красный), гистоны (С2, зеленый) и внДНК (С3, синий) являются компонентами НВЛ (С4, наложение). Стрелка указывает на нить НВЛ. (D): Лазерную захватывающую микродиссекцию проводили с окрашенными DAPI нитями для подтверждения наличия ДНК в них. На D1 стрелки указывают на цепь внДНК. На D2 звездочка занимает площадь нити после лазерной захватывающей микродиссекции. (03): ПЦР-продукт глицеральдегидфосфатдегидрогеназы (ГАФДГ) на дорожке с внДНК подтверждает наличие ДНК. Масштабная линейка: В1, В2 и В3 (20 мкм); С, D1 и D2 (50 мкм).
Фигура 13 показывает нейтрофилы (А1-А4): кателицидин (зеленый) присутствует в мукоидных пленках (А1, стрелка) и цепях внДНК (А1, острие стрелки). Кателицидин колокализуется с эластазой нейтрофилов (А2, красный) и окрашенным DAPI ядром (А3, синий). (В1-В4): Кателицидин (зеленый) присутствует в нейтрофилах (В1, стрелка) и колокализуется с эластазой нейтрофилов (В2, красный) и DAPI (В3, синий). (С1-С4): Кателицидин (С1, стрелка) и окрашенный DAPI материла ядра (С3, острие стрелки) выходят из нейтрофилов, образуя НВЛ. Масштабная линейка: 10 мкм.
Фигура 14 показывает экспрессию генов у пациентов с ССГ и в контроле. (А): Средний уровень образования слезной жидкости, измеренный с помощью пробы Ширмера I, был достоверно ниже у пациентов с ССГ. (В): Длину внДНК измеряли после отпечатывания полосок пробы Ширмера на стекле. Длина внДНК была достоверно выше у пациентов с ССГ. (С): Количество внДНК на полосках пробы Ширмера измеряли с помощью окрашивания красителем picogreen. У пациентов с ССГ количество внДНК было существенно выше. (D): Гены пути передачи сигнала от внДНК экспрессировались на повышенном уровне в отшелушенных клетках конъюнктивы пациентов с ССГ. (Е): Экспрессия генов воспаления также была существенно увеличена у пациентов с ССГ. * p<0,05.
Фигура 15 показывает наличие нуклеаз и ДНКазы I в слезной жидкости (А1-А6): Изображение, полученное с помощью иммунофлуоресцентной микроскопии, показывает наличие ДНКазы I в слезных железах человека (А1-А3, красный). Специфичность окрашивания была подтверждена с помощью конкурентного пептида (А4-А6) и изотипического контроля (данные не показаны). (В): нуклеазная активность в слезах нормальных индивидов. Твердофазный иммуноферментный анализ ДНКазы I показал, что ее концентрация в нормальной слезной жидкости составляет 3,14 нг/мл. При использовании набора реактивов для определения ДНКазы нормальная слезная жидкость вызывала полную деградацию ДНК (дорожка «слезная жидкость»). Таким образом, нуклеазная активность слезной жидкости выше 0,05 единиц Куница. (С): Нуклеазную активность слезной жидкости количественно оценивали с помощью метода резонансного переноса энергии флуоресценции (FRET). Типичный график сравнения нуклеазной активности у пациентов с ССГ (синий) и здоровых индивидов (зеленый) показывает, что нуклеазная активность у пациентов с ССГ снижена. (D): Нуклеазная активность у пациентов с ССГ была достоверно ниже, чем у здоровых индивидов. * p<0,05, масштабная линейка: 20 мкм.
Фигура 16 показывает мукоидные пленки, размещенные на плашках с бактериальной культурой. У пациентов с тяжелой формой угнетенного слезообразования при синдроме сухих глаз могут образовываться мукоидные пленки на поверхности глаза. Мукоидные пленки снимали с поверхности глаза с помощью стерильной палочки с тампоном eSwab. Был обнаружен рост грамположительных кокков, идентифицированных как не обладающие коагулазной активностью виды стафилококка. (А): Рост на культуральной чашке с кровяным агаром показал наличие бактериальных колоний размером с булавочную головку. (В): Окрашивание с помощью набора реактивов Baclight live/dead мазков культивируемых колоний показало наличие живых кокков (зеленый) одновременно с мертвыми кокками (красный). Данные эксперименты подтверждают, что бактерии присутствуют в мукоидных пленках на поверхности глаза пациентов с синдромом сухих глаз.
Подробное описание изобретения
Изобретатели сделали неожиданное открытие, свидетельствующее о том, что болезни глаз связаны с нуклеиновыми кислотами, такие как ССГ и связанные с ССГ состояния, можно лечить нуклеазой и офтальмологическим вспомогательным веществом в присутствии или в отсутствие антибиотика. Основой настоящего открытия является наличие нейтрофильных внеклеточных ловушек (НВЛ) на поверхности глаз(а) пациентов, страдающих болезнью глаз, связанной с нуклеиновыми кислотами, такой как ССГ. НВЛ представляют собой внеклеточные структуры, состоящие из хроматина, который включает нуклеиновую кислоту, такую как ДНК, эластазы нейтрофилов, гистона и белков гранул. НВЛ могут создавать повышенную концентрацию антимикробной активности и, соответственно, доминируют в очагах воспаления.
1. Определения
Терминология, используемая в настоящем изобретении, применяется только с целью описания частных случаев применения изобретения и не является единственно возможной. Как применяется в спецификации и прилагаемых формулах изобретения, формы единственного числа, союз «и», определенные и неопределенные артикли включают множественные ссылки, если иное четко не следует из контекста.
а. Контроль
«Контроль» при использовании в настоящем изобретении может обозначать композицию или образец, для которого известно отсутствие синдрома сухих глаз или бактериального заражения (отрицательный контроль). Положительный контроль может обозначать образец, который относится к случаю болезни глаз, связанной с нуклеиновыми кислотами, или бактериальной инфекции. Любой контроль может содержать известное количество внеклеточной ДНК.
При указании интервалов значений в настоящем изобретении подразумевается существование всех чисел одного уровня точности внутри интервала. Например, для интервала 6-9 числа 7 и 8 подразумеваются в дополнение к 6 и 9, а для интервала 6,0-7,0 подразумеваются числа 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9 и 7,0.
2. Композиция на основе нуклеаз
В настоящем изобретении представлена композиция на основе нуклеаз («нуклеазная композиция»), способная удалить нуклеиновую кислоту с поверхности глаза или внутри глаза. Нуклеиновая кислота может быть внеклеточной. Нуклеазная композиция может содержать одну или несколько нуклеаз. Нуклеаза может представлять собой ДНКазу или РНКазу. Нуклеазная композиция может также содержать офтальмологическое вспомогательное вещество. Кроме того, нуклеазная композиция может содержать один или несколько антибиотиков, противовирусное соединение, противовоспалительное вещество, антагонист Toll-подобного рецептора, антагонист интерферона типа 1, ингибитор кателицидина, ингибитор MyD88, стероид, противоаллергическое вещество и/или ингибитор эластазы нейтрофилов. Кроме того, нуклеазная композиция может не содержать любой из антибиотиков, противовирусных соединений, противовоспалительных веществ, антагонист Toll-подобного рецептора, антагонист интерферона типа 1, ингибитор кателицидина, ингибитор MyD88, стероид, противоаллергическое вещество и/или ингибитор эластазы нейтрофилов, но может использоваться в сочетании с одним или несколькими антибиотиками, антагонистами Toll-подобного рецептора, антагонистами интерферона типа 1, ингибиторами кателицидина и/или ингибиторами эластазы нейтрофилов.
Уровень рН и/или осмолярности нуклеазной композиции может быть доведен до необходимого перед использованием. Уровень рН нуклеазной композиции может варьировать в интервале от 4 до 9, от 5 до 8, от 6 до 7 или от 6,5 до 7,5. Уровень рН нуклеазной композиции может быть равен 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9, 5,0, 5,1, 5,2, 5,3, 5,4, 5,5, 5,6, 5,7, 5,8, 5,9, 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9, 7,0, 7,1, 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8, 7,9, 8,0, 8,1, 8,2, 8,3, 8,4, 8,5, 8,6, 8,7, 8,8, 8,9 или 9,0. Уровень рН нуклеазы может быть равен 7,4.
Осмолярность нуклеазной композиции может быть гипоосмолярной и гиперосмолярной. Например, осмолярность ДНКазной композиции может быть между 100 мОсм/л и 500 мОсм/л, 150 мОсм/л и 450 мОсм/л, 200 мОсм/л и 400 мОсм/л, 250 мОсм/л и 350 мОсм/л, 275 мОсм/л и 325 мОсм/л, 100 мОсм/л и 150 мОсм/л, 150 мОсм/л и 200 мОсм/л, 150 мОсм/л и 300 мОсм/л, 200 мОсм/л и 300 мОсм/л, 0 мОсм/л и 100 мОсм/л, 25 мОсм/л и 75 мОсм/л, 50 мОсм/л и 125 мОсм/л, 0 мОсм/л и 50 мОсм/л.
а. Нуклеаза
Нуклеазы, предполагаемые настоящим изобретением, включают ДНКазы и РНКазы.
ДНКаза может быть ферментом, который катализирует гидролитическое расщепление фосфодиэфирных связей в остове ДНК. Одним из таких ферментов является дезоксирибонуклеаза. Примеры дезоксирибонуклеаз включают следующие, но не ограничиваются ими: дезоксирибонуклеазу I (ДНКазу I), дезоксирибонуклеазу II (ДНКазу II) и микрококковую нуклеазу. ДНКаза может быть рекомбинантной человеческой ДНКазой, ДНКазой животного происхождения (напр., бычьей) или микрококкового происхождения. Рекомбинантная ДНКаза I может быть дорназой альфа, доступной под торговым названием PULMOZYME® компании Genetech Inc. Вариант ДНКазы может быть получен путем модификации ее генетического состава, например, путем удаления сигнального пептида, мутации сайтов связывания субстрата или внесения аминокислотных замен для создания гиперактивных вариантов или более стабильных вариантов. Например, может быть использована ДНКаза II или ДНКаза I-, II- или III-подобные варианты, в сочетании друг с другом или по отдельности.
РНКаза может быть ферментом, который катализирует гидролитическое расщепление фосфодиэфирных связей в остове РНК. Одним из таких ферментов является рибонуклеаза. Примеры рибонуклеаз включают следующие, но не ограничиваются ими: рибонуклеазу А (РНКазу А), рибонуклеазу Н (РНКазу Н), рибонуклеазу I (РНКазу I), рибонуклеазу II (РНКазу II), рибонуклеазу III (РНКазу III), рибонуклеазу D (РНКазу D), рибонуклеазу L (РНКазу L), рибонуклеаза Р (РНКазой Р), рибонуклеазу PH (РНКазу PH), рибонуклеазу PhyM (РНКазу PhyM), рибонуклеазу R (РНКазу R), рибонуклеазу T (РНКазу T), рибонуклеазу T1 (РНКазу T1), рибонуклеазу T2 (РНКазу T2), рибонуклеазу U2 (РНКазу U2), рибонуклеазу V1 (РНКазу V1), рибонуклеазу V (РНКазу V), олигорибонуклеазу, экзорибонуклеазу I или экзорибонуклеазу II. РНКаза может быть рекомбинантной человеческой РНКазой или РНКазой животного происхождения (напр., бычьей). Вариант РНКазы может быть получен путем модификации ее генетического состава, например, путем удаления сигнального пептида, мутации сайтов связывания субстрата или внесения аминокислотных замен для создания гиперактивных вариантов или более стабильных вариантов.
Нуклеаза может отрезать основания на концах молекул нуклеиновых кислот (экзодезоксирибонуклеазы или экзорибонуклеазы, типы экзонуклеаз). Нуклеаза может быть эндонуклеазой, которая может использоваться в индивидуальном виде или в сочетании с другой нуклеазой. Примерами эндонуклеаз являются липокалин и РНКаза А. Нуклеаза может вносить разрыв в любое место цепи (экзодезоксирибонуклеазы или экзорибонуклеазы, типы экзонуклеаз). Нуклеаза может быть неспецифичной к последовательности ДНК, которую она разрезает. Нуклеаза может быть специфичной к последовательности. Нуклеаза может разрезать только двухцепочечную нуклеиновую кислоту, только одноцепочечную нуклеиновую кислоту или как двухцепочечную, так и одноцепочечную нуклеиновую кислоту.
Дозировка нуклеазы может быть определена, например, врачом без ненужного экспериментирования. Дозировка может быть скорректирована в зависимости от противопоказаний, переносимости или похожих состояний. Специалисты в данной области могут без труда оценить такие факторы и на основании имеющейся информации определить точную эффективную концентрацию нуклеазы, которую следует применять, как описано здесь. Нуклеаза может содержаться в нуклеазной композиции в интервале между 5 нг/мл и 3 мг/мл, между 1 мг/мл и 3 мг/мл, между 2 мг/мл и 3 мг/мл, между 10 нг/мл и 900 нг/мл, между 20 нг/мл и 800 нг/мл, между 30 нг/мл и 700 нг/мл, между 40 нг/мл и 600 нг/мл, между 50 нг/мл и 600 нг/мл, между 60 нг/мл и 500 нг/мл, между 70 нг/мл и 400 нг/мл, между 80 нг/мл и 300 нг/мл, между 90 нг/мл и 200 нг/мл, между 50 нг/мл и 250 нг/мл, между 100 нг/мл и 200 нг/мл, между 150 нг/мл и 250 нг/мл, между 100 нг/мл и 150 нг/мл, между 90 нг/мл и 100 нг/мл. Нуклеаза может содержаться в нуклеазной композиции в количестве 10 нг/мл, 20 нг/мл, 30 нг/мл, 40 нг/мл, 50 нг/мл, 60 нг/мл, 70 нг/мл, 80 нг/мл, 90 нг/мл, 100 нг/мл, 110 нг/мл, 150 нг/мл, 200 нг/мл, 250 нг/мл, 300 нг/мл, 350 нг/мл, 400 нг/мл, 450 нг/мл, 500 нг/мл, 550 нг/мл, 600 нг/мл, 650 нг/мл, 700 нг/мл, 750 нг/мл, 800 нг/мл, 850 нг/мл, 900 нг/мл, 950 нг/мл, 1 мг/мл, 2 мг/мл или 3 мг/мл. Как подробнее описано здесь, композиция может быть вручную введена в глаз в соответствующей дозировке, например в виде глазных капель, или введена с помощью микрокапельного или аэрозольного прибора, позволяющего ввести определенную дозу лекарственного препарата.
(1) Офтальмологическое вспомогательное вещество
Офтальмологическим вспомогательным веществом может быть любое офтальмологическое вспомогательное вещество. Офтальмологическим вспомогательным веществом может быть буфер, регулятор тоничности, увлажняющее средство и/или антиоксидант. Буфер может быть борной и/или фосфорной кислотой. Буфер может минимизировать изменения рН нуклеазной композиции. Регулятор тоничности может создавать изотоническую среду и может включать хлорид натрия, хлорид калия, хлорид магния и/или борную кислоту. Антиоксиданты включают метабисульфит натрия и ЭДТА, например, антиоксиданты можно использовать для стабилизации нуклеазной композиции. Увлажняющие средства, которые включают поливиниловый спирт и полисорбат 80, позволяют нуклеазной композиции распределяться по поверхности глаза. Другие офтальмологические вспомогательные вещества включают хлорид бензалкония, этилендиаминтетрауксусную кислоту (ЭДТА), пурит, хлорбутанол, перборат натрия и сорбиновую кислоту, перборат натрия, пурит, полиолы, глицерин, полисорбат 80, декстран 70, пропиленгликоль и полиэтиленгликоли, такие как ПЭГ-400. Офтальмологическим вспомогательным веществом может быть мазь, такая как минеральное масло, белый вазелин, белая мазь или ланолин. Также как жидкие носители, вазелин и минеральное масло могут использоваться в качестве носителей в препаратах, выпускающихся в форме мази, для увеличения времени контакта с глазом. Данные ингредиенты способствуют образованию окклюзивной пленки на поверхности глазного яблока и улучшают состав слезной пленки, укрепляя слизистый и водный слои. Офтальмологическое вспомогательное вещество может обеспечивать слизеподобные свойства и/или снижать потерю водного слоя вследствие испарения. Офтальмологическое вспомогательное вещество может работать в качестве носителя, такого так фармацевтически приемлемый носитель, как описано ниже.
(2) Антибиотик
Антибиотиком может быть любой антибиотик. Антибиотиком может быть ампициллин, амоксициллин/клавуланат, метронидазол, клиндамицин, эритромицин, гентамицин, ванкомицин, ципрофлаксин, клиндамицин, тетрациклин, анксиолитик, амикацин, канамицин, неомицин, нетилмицин, стрептомицин, тобрамицин, тейкопланин, ванкомицин, азитромицин, кларитромицин, кларитромицин, диритромицин, эритромицин, рокситромицин, тролеандомицин, амоксициллин, ампициллин, азлоциллин, карбенициллин, клозациллин, диклоксациллин, флукозациллин, мезлоциллин, нафциллин, пенициллин, пиперациллин, тикарциллин, бацитрацин, колистин, полимиксин В, ципрофлоксацин, эноксацин, гатифлоксацин, левофлоксацин, ломефлоксацин, моксифлоксацин, норфлоксацин, офлазацин, тровафлоксацин, мафенид, сульфацетамид, сульфаметизол, сульфасалазин, сульфизоксазол, триметроприм, котримоксазол, демеклоциклин, соксициклин, миноциклин, доксициклин или окситетрациклин. Антибиотик может быть офтальмологически приемлемым антибиотиком.
(3) Противовирусные соединения
Противовирусным веществом может быть любое противовирусное соединение. Противовирусным соединением может быть абакавир, ацикловир, адефовир, амантадин, ампренавир, амплиген, арбидол, атазанавир, атрипла, боцепревир, цидофовир, дарунавир, делавирдин, диданозин, докозанол, эдоксудин, эфавиренц, эмтрицитабин, энфувиртид, энтекавир, фамцикловир, фомивирсен, фозампренавир, ганцикловир, ибацитабин, имуновир, идоксуридин, имихимод, индинавир, ламивудин, лопанавир, ловирид, маравирок, мороксидин, пенцикловир, перемивир, плеконарил, рибавирин, ритонавир, саквинавир, телапревир, тенофувир, трувада, валацикловир, валганцикловир или занамивир. Противовирусное соединение может быть офтальмологически приемлемым противовирусным соединением.
(4) Противовоспалительное соединение
Противовоспалительное соединение может быть нестероидным или стероидным противовоспалительным. Противовоспалительное соединение может быть циклоспорином или циклоспорином А. Циклоспорин А может быть 0,05% циклоспорином А (например, рестазис, RESTASIS®). Противовоспалительное соединение может быть офтальмологически приемлемым противовоспалительным.
(5) Антагонист Toll-подобного рецептора-9
Toll-подобный рецептор 9 (TLR9) узнает специфические неметилированные CpG олигонуклеотидные последовательности (ОДН, олигодезоксинуклеотиды), которые отличают микробную ДНК от ДНК млекопитающих. Антагонистом Toll-подобного рецептора может быть любой олигонуклеотид, который нейтрализует стимулирующий эффект CpG ОДН. Такие олигонуклеотиды могут характеризоваться наличием трех последовательно расположенных G после С или А. Более того, добавление четвертого G (G-тетрады) может усиливать ингибирующую способность ОДН. Последовательности, обладающие наибольшей ингибирующей способностью, содержат TTAGGG, например (TTAGGG)4 (SEQ ID NO: 1). На фигуре 1 приведен пример. Антагонистический олигонуклеотид может действовать, нарушая колокализацию CpG ОДН и TLR9, например, в эндосомных везикулах. Антагонист Toll-подобного рецептора 9 может быть офтальмологически приемлемым антагонистом Toll-подобного рецептора 9.
(6) Антагонист интерферона типа 1
Интерферон типа 1 является частью защитной реакции на вирусные инфекции и некоторые внутриклеточные паразиты. В то время как данные белки применяются для терапии некоторых вирусных заболеваний, рака и множественного склероза, выработка интерферонов типа 1 может быть нарушена при некоторых заболеваниях.
Антагонистом интерферона типа 1 может быть любое соединение, которое антагонизирует или конкурентно ингибирует интерферон типа 1. Соединение может быть антителом к интерферону α, например, соединение может антагонизировать или ингибировать интерферон типа 1, связываясь с его рецептором. Соединение может антагонизировать или ингибировать интерферон типа 1, связываясь с субъединицами его рецептора, IFNAE-1 или IFNR-2. Антагонист или конкурентный ингибитор может блокировать биологическую активность нативного интерферона. Антагонист интерферона типа 1 может быть офтальмологически приемлемым антагонистом интерферона типа 1.
(7) Ингибитор кателицидина
Ингибитором кателицидина может быть любой ингибитор, способный блокировать или снижать биологическую активность кателицидина, который стабилизирует внеклеточную ДНК на поверхности глаза. Примером ингибитора кателицидина является бактериальный экзополисахарид. Ингибитор кателицидина может быть офтальмологически приемлемым ингибитором кателицидина.
(8) Ингибитор MyD88
Ингибитором MyD88 может быть любое соединение, способное ингибировать или снижать биологическую активность или экспрессию MyD88. Ингибитор MyD88 может быть пептидом или малой молекулой, которая ингибирует гомодимеризацию MyD88, такой как ST2825 (Sigma Tau, Помеция, Италия), синтетическим олигопептидом IMG2205 (Imgenex Corporation, Сан-Диего, Калифорния) и/или ингибирующим MyD88 пептидом. Ингибитор MyD88 может ингибировать связывание MyD88 с партнерами по передаче сигнала. Ингибитором MyD88 может быть доминантно-негативный белок MyD88. Ингибитором MyD88 может быть антисмысловая, киРНК (короткая интерферирующая РНК) или кшРНК (короткая шпилечная РНК), которая ингибирует экспрессию MyD88.
(9) Ингибитор эластазы нейтрофилов
Ингибитором эластазы нейтрофилов может быть любое соединение, способное ингибировать или снижать биологическую активность эластазы нейтрофилов, представляющей собой сериновую протеазу, секретируемую нейтрофилами во время воспаления. Так ингибитор может быть синтетическим, естественным, обратимым или необратимым. Например, ингибитором эластазы нейтрофилом может быть ONO-5046, MR-889, L-694,458, CE-1037, GW-311616 или TEI-8362. Ингибитором эластазы нейтрофилом может быть ONO-6818, AE-3763, FK-706, ICI-200,880, ZD-0892 или ZD-8321. См. примеры в Expert Opinion on Investigational Drugs, July 2002, Vol. 11, No. 7: Pages 965-980 (Neutrophil elastase inhibitors as treatment for COPD, by Hiroyuki Ohbayashi). Ингибитор эластазы нейтрофилов может быть офтальмологически приемлемым ингибитором эластазы нейтрофилов.
б. Фармацевтически приемлемый носитель
Нуклеаза может быть включена в фармацевтические составы, подходящие для введения индивиду (например, пациенту, который может быть человеком или нет). Обычно нуклеазная композиция содержит фармацевтически приемлемый носитель, подход