Бор-содержащие малые молекулы в качестве противовоспалительных средств
Иллюстрации
Показать всеИзобретение относится к медицине и касается применения 5-(4-цианофенокси)-1,3-дигидро-1-гидрокси-2,1-бензоксаборола или его фармацевтически приемлемой соли для изготовления лекарственного средства для лечения или профилактики связанного с воспалением заболевания, выбранного из акне и волчанки, у человека. Применение данного вещества позволяет лечить заболевания кожи, связанные с аутоиммунным компонентом. 3 ил., 20 пр.
Реферат
Перекрестная ссылка на родственные заявки
Настоящая заявка заявляет приоритет на основании Временных Патентных Заявок США, имеющих серийный № 60/823888, подана 29 августа 2006 года, и 60/774532, подана 16 февраля 2006 года, которые включены в настоящую заявку посредством ссылки во всей полноте для всех целей.
Предпосылки изобретения
Иррегулярное воспаление является основным компонентом широкого ряда заболеваний человека. В крови людей, страдающих дегенеративными расстройствами, часто наблюдаются чрезмерные уровни провоспалительных регуляторов. Одним типом таких провоспалительных регуляторов являются цитокины, включающие IL-1α, β, IL-2, IL-3, IL-6, IL-7, IL-9, IL-12, IL-17, IL-18, IL-23, TNF-α, LT, LIF, Онкостатин и IFNc1α, β, γ.
Неограничивающий перечень обычных медицинских проблем, которые непосредственно вызваны воспалительными цитокинами, включают: артрит, где воспалительные цитокины могут привести к патологическим изменениям в синовиальной мембране и деструкции хрящей суставов и кости; почечную недостаточность, где воспалительные цитокины препятствуют циркуляции и повреждают нефроны; обыкновенную волчанку, где воспалительные цитокины усиливают ослабление и повреждение иммунного комплекса; астму, где воспалительные цитокины закрывают дыхательные пути; псориаз, где воспалительные цитокины индуцируют дерматит; панкреатит, где воспалительные цитокины индуцируют повреждение клеток поджелудочной железы; аллергию, где воспалительные цитокины индуцируют проницаемость сосудов и гиперемию; фиброз, где воспалительные цитокины атакуют поврежденную ткань; осложнения после хирургических операций, где воспалительные цитокины препятствуют заживлению; анемию, где воспалительные цитокины оказывают разрушающее действие на продукцию эритропоэтина; и фибромиалгию, где у пациентов с фибромиалгией повышен уровень воспалительных цитокинов.
Другие заболевания, связанные с хроническим воспалением, включают рак; сердечный приступ, где хроническое воспаление способствует коронарному атеросклерозу; болезнь Альцгеймера, где хроническое воспаление разрушает клетки головного мозга; застойную сердечную недостаточность, где хроническое воспаление вызывает атрофию сердечной мышцы; удар, где хроническое воспаление стимулирует тромбоэмболические явления; и стеноз клапана аорты, где хроническое воспаление повреждает сердечные клапаны. Артериосклероз, остеопороз, болезнь Паркинсона, инфекция, воспалительное заболевание кишечника, включающее болезнь Крона и язвенный колит, а также рассеянный склероз (типичное заболевание, связанное с аутоиммунным воспалением) также связаны с воспалением (Bebo, B.F., Jr., J Neurosci Res, 45: 340-348, (1996); Mennicken, F., Trends Pharmacol Sci, 20: 73-78, (1999); Watanabe, T, Int J Cardiol, 66 Suppl 1: S45-53; discussion S55, (1998); Sullivan, G.W., J Leukoc Biol, 67: 591-602, (2000); Franceschi, C, Ann NY Acad Sci, 908: 244-254, (2000); Rogers, J, Ann N Y Acad Sci, 924: 132-135, (2000); Li, Y.J., Hum Mol Genet, 12: 3259-3267, (2003); Maccarrone, M., Curr Drug Targets Inflamm Allergy, 1: 53-63, (2002); Lindsberg, P.J., Stroke, 34: 2518-2532, (2003); DeGraba, T.J., Adv Neurol, 92: 29-42, (2003);. Ito, H., Curr Drug Targets Inflamm Allergy, 2: 125-130, (2003); von der Thusen, J.H., Pharmacol Rev, 55: 133-166, (2003); Schmidt, M.I.,. Clin Chem Lab Med, 41: 1120-1130, (2003); Virdis, A., Curr Opin Nephrol Hypertens, 12: 181-187, (2003); Tracy, R.P., Int J Clin Pract, Suppl 10-17, (2003); Haugeberg, G., Curr Opin Rheumatol, 15: 469-475, (2003); Tanaka, Y., J Bone Miner Metab, 21: 61-66, (2003); Williams, J.D., Clin Exp Dermatol, 27: 585-590, (2002)). Некоторые заболевания на стадиях их прогрессирования могут угрожать жизни. Существуют некоторые методики для лечения таких воспалительных заболеваний; однако результаты, в основном, неудовлетворительные, о чем свидетельствует недостаточная эффективность и связанные с лекарственным средством побочные эффекты.
Воспалительное заболевание кишечника
Воспалительное заболевание кишечника (IBD) включает болезнь Крона (CD) и язвенный колит (UC), оба этих идиопатических хронических заболеваний все чаще возникают во многих частях мира. В США каждый год наблюдается 600000 случаев возникновения этих заболеваний. IBD может поражать тонкий кишечник, толстый кишечник, либо оба. CD может поражать любую часть желудочно-кишечного тракта, но наиболее часто поражает периферический тонкий кишечник и толстую кишку. Это заболевание либо распространяется на прямую кишку, либо вызывает воспаление или инфекцию с дренированием вокруг прямой кишки. UC обычно вызывает язвы в нижней части толстого кишечника, часто начиная с прямой кишки. Симптомы бывают разными, но могут включать диарею, лихорадку и боль. Пациенты с продолжительным UC имеют повышенный риск развития рака толстой кишки. В настоящее время нет никакого успешного лечения, поскольку причина IBD остается неясной, хотя были предположения об инфекционном и иммунологическом механизмах. Лечение IBD направлено на контроль воспалительных симптомов, традиционно с использованием кортикостероидов, аминосалицилатов и стандартных иммуносупрессивных средств, таких как азатиоприн (6-меркаптопурин), метотрексат и циклоспорин. Из них единственными модифицирующими заболевание терапевтическими средствами являются иммуносупрессивные средства азатиоприн и метотрексат, оба они обладают замедленным началом действия и лишь умеренной эффективностью. Длительная терапия может вызвать поражение печени (фиброз или цирроз) и супрессию костного мозга. Также пациенты часто становятся невосприимчивыми к такому лечению. Другие терапевтические схемы просто направлены на симптомы (Rutgeerts, P.A, J Gastroenterol Hepatol, 17 Suppl: S 176-185 (2002); Rutgeerts, P., Aliment Pharmacol Ther, 17: 185-192 (2003)).
Псориаз
Псориаз является одним из наиболее распространенных иммуноопосредованных хронических кожных заболеваний, которое возникает в различных формах и с различной степенью тяжести, поражающее примерно 2% населения или более 4,5 миллиона людей с США, из которых 1,5 миллиона, как считают, страдают формой заболевания от умеренной до тяжелой. У десяти-тридцати процентов пациентов с псориазом также наблюдается развитие формы артрита - псориатического артрита, который повреждает кость и соединительную ткань вокруг суставов. Псориаз возникает в виде пятен припухлой красной кожи, покрытых скоплением белых чешуек. Они могут также быть в виде узелков (пустулярный псориаз) или ожогов (эритродермический). Псориаз также может вызывать сильный зуд и жжение. Пациенты страдают психологически, а также физически. В настоящее время существуют некоторые способы лечения псориаза, включающие местное лечение, фототерапию и системное лечение. Однако они, в основном, считаются только подавляющими заболевание и модифицирующими заболевание; ни один из них не является излечивающим. Более того, многие виды лечения являются либо косметически нежелательными, неудобными для длительного применения или связаны с существенной токсичностью.
С ростом понимания биологических особенностей псориаза за последние два десятилетия стали доступными биологические методы лечения, нацеленные на активность Т-лимфоцитов и цитокинов, ответственных за воспалительный характер этого заболевания. В настоящее время лекарственные средства, выписываемые от псориаза, включают ингибиторы TNF-α, изначально применяемые для лечения ревматоидного артрита (RA), ENBREL® (этанерсепт), REMICADE® (инфликсимаб) и HUMIRA® (адалимумаб), а также ингибитор Т-клеток AMEVIVE® (алефасепт) от фирмы Biogen, одобренный в 2002 году, и RAPTIVA® (эфализумаб) от фирмы Genentech/Xoma, одобренный в 2003 году (Weinberg, J.M., J Drugs Dermatol, 1: 303-310, (2002)). AMEVIVE ALEFACEPT® представляет собой иммуноглобулиновый гибридный белок, состоящий из первого внеклеточного домена LFA-3 человека, гибридизованного с шарнирными C(H)2 и C(H)3 областями IgG(1) человека. Он ингибирует Т-клеточную пролиферацию через NK-клетки (Cooper, J.C, Eur J Immunol, 33: 666-675, (2003)). RAPTIVA® также известен как анти-CD11a, гуманизированное моноклональное антитело, которое нацелено на молекулы Т-клеточной адгезии, антиген-1 функции лейкоцитов (LFA-1). Предотвращение связывания LFA-1 с его лигандом (ICAM-1, молекула-1 межклеточной адгезии) ингибирует активацию и миграцию лимфоцитов, приводя к уменьшению инфильтрации лимфоцитов, ограничивая, таким образом, каскад событий, приводящих в результате к признакам и симптомам псориаза (Cather, J.C, Expert Opin Biol Ther, 3: 361-370, (2003)). Однако потенциальные побочные эффекты для существующих в настоящее время ингибиторов TNF-α, известных из уровня техники, являются тяжелыми, включая развитие лимфомы (Brown, S.L., Arthritis Rheum, 46: 3151-3158, (2002)), осложнение застойной сердечной недостаточности, приводящее к серьезным инфекциям и сепсису, и обострения рассеянного склероза и расстройств центральной нервной системы (Weisman, M.H.,. J Rheumatol Suppl, 65: 33-38, (2002); Antoni, C, Clin Exp Rheumatol, 20: S152-157, (2002)). Хотя побочные эффекты Т-клеточного ингибитора AMEVIVE®/RAPTIVA® могут быть лучше переносимыми при лечении псориаза, RAPTIVA® является иммуносупрессивным средством. Иммуносупрессивные средства могут повышать риск инфекции, реактивировать латентные, хронические инфекции или повышать риск развития рака.
Хотя за последние два десятилетия были различные продвижения в понимании биологических особенностей псориаза, и появились нетрадиционные методы лечения псориаза, как описано выше, в основном не существует способов, адекватно устраняющих страдания, причиняемые этим заболеванием. Наблюдение за 40000 пациентами с псориазом в США, осуществленное National Psoriasis Foundation в 1998 году, показало, что 79% более молодых пациентов испытывали неудовлетворенность в связи с неэффективностью их лечения. Из числа пациентов с тяжелым заболеванием, 32% чувствовали, что их лечение было недостаточно оперативным (Mendonca, C.O., Pharmacol Ther, 99: 133-147, (2003); Schon, M.P., J Invest Dermatol, 112: 405-410, (1999)).
Ревматоидный артрит
Ревматоидный артрит (RA) представляет собой еще один пример причиняющего беспокойство воспалительного расстройства. Это широко распространенное хроническое, связанное с воспалением заболевание, характеризующееся хроническим воспалением мембранной выстилки (синовиальная оболочка) суставов и/или других внутренних органов. Воспалительные клетки также могут распространяться и повреждать кость и хрящ. Пораженный сустав может потерять правильную форму и положение, что приводит к потере двигательной способности. Пациенты с RA испытывают боль, тугоподвижность, повышенное тепло, покраснение и разбухание в суставах и другие системные симптомы, такие как лихорадка, слабость и анемия. В настоящее время примерно 1% населения или 2,1 миллиона в США страдают этой болезнью, из них больше женщин (1,5 миллиона), чем мужчин (0,6 миллиона). Патология RA не до конца понятна, хотя теоретически было предположено, что механизмом этого процесса является каскад неправильных иммунологических реакций. Традиционное лечение, к сожалению, является недостаточным при RA (Bessis, N., J Gene Med, 4: 581-591, (2002)) (29). Это заболевание полностью не отвечает на симптоматическое лечение, включающее кортикостероиды и нестероидные противовоспалительные лекарственные средства (NSAID), используемые с 1950-х. Также такое лечение связано с риском серьезных неблагоприятных эффектов. Терапевтические эффекты модифицирующих заболевание противоревматоидных лекарственных средств (DMARD), таких как Метотрексат (MTX), часто являются несоответствующими и кратковременными.
Недавно был разработан новый класс биологических DMARD (модифицирующих заболевание противоревматоидных лекарственных средств) для лечения RA на основании понимания роли цитокинов, TNF-α и IL-1, в воспалительном процессе. FDA одобрены некоторые такие DMARD, включающие ENBREL® (этанерсепт) от фирмы Immunex/Amgen Inc. в 1998, REMICADE® (инфликсимаб) от фирмы Centocor/Johnson & Johnson, HUMIRA® (адалимумаб) от фирмы Abbott Laboratories Inc. в 2002, и KINERET® (анакинра) от фирмы Amgen в 2001. ENBREL® представляет собой рекомбинантный белок растворимого рецептора TNF (TNFR). REMICADE® представляет собой гуманизированное мышиное (химерное) анти-TNF-α моноклональное антитело. HUMIRA® представляет собой полностью человеческое анти-TNF моноклональное антитело, созданное с использованием метода отображения информации о фагах, что дает антитело с вариабельными областями тяжелой и легкой цепи человека и константными областями IgG1:k человека. Все эти 3 лекарственных средства на основе белка нацелены на TNF-α и связываются с ним, блокируя эффекты TNF-α. KINERET® представляет собой антагонист рекомбинантного рецептора IL-1, который является подобным природному IL-1Ra человека, за исключением добавления одного метионинового остатка по его аминоконцу. KINERET® блокирует биологическую активность IL-1 путем конкурентного ингибирования связывания IL-1 с рецептором IL-1 типа I (IL-1RI) и, следовательно, снижает провоспалительные эффекты IL-1.
Лечение этими биологическими DMARD облегчает симптомы, ингибирует развитие структурных повреждений и улучшает физическую деятельность у пациентов с умеренной до тяжелой формы активного RA. Эти три имеющиеся в настоящее время на рынке блокирующих TNF-α средства обладают одинаковой эффективностью при их сочетании с MTX, широко применяемым DMARD, при лечении пациентов с RA (Hochberg, M.C, Ann Rheum Dis, 62 Suppl 2: iiU13-16, (2003)). При том, что они обеспечивают существенную эффективность и хороший общий профиль безопасности за короткий и средний срок у многих пациентов с RA, эти биологические виды лечения могут создавать серьезные проблемы и длительные побочные эффекты, например, в области печени, и все еще нуждаются в оценке. Были вызывающие беспокойство сообщения о связи между использованием обоих этих средств ENBREL® или REMICADE® и развитием лимфомы (S.L., Артрит Rheum, 46: 3151-3158, (2002)). Как описано выше, некоторые сообщения показали, что у пациентов, которых лечили ENBREL® или REMICADE®, обострялась застойная сердечная недостаточность и развивались серьезные инфекции и сепсис, а также наблюдалось еще большее обострение рассеянного склероза и других проблем центральной нервной системы (Antoni, C, Clin Exp Rheumatol, 20: S152-157, (2002); Mendonca, C.O., Pharmacol Ther, 99: 133-147, (2003)).
Рассеянный склероз
Рассеянный склероз (MS) представляет собой аутоиммунное заболевание, которое диагностировано у от 350000 до 500000 человек в США. Множественные области воспаления и потери миелина в головном мозге и спинном мозге являются показателями этого заболевания. У пациентов с MS наблюдаются неврологические нарушения различной степени, в зависимости от локализации и степени потери миелина. Обычные симптомы MS включают усталость, слабость, мышечную спастичность, проблемы с равновесием, проблемы с мочевым пузырем и кишечником, онемение, потерю зрения, тремор и депрессию. Существующие в настоящее время виды лечения MS только смягчают симптомы или откладывают потерю трудоспособности, и некоторые новые виды лечения MS, включающие трансплантацию стволовых клеток и генную терапию, являются консервативными (Fassas, A., Blood Rev, 17: 233-240, (2003); Furlan, R., Curr Pharm Des, 9: 2002-2008, (2003)). Хотя анти-TNF антитела показали защитный эффект в экспериментальном аутоиммунном энцефаломиелите (EAE), они осложняют заболевание у пациентов с MS, это говорит о том, что только лишь ингибирование TNF-α не является достаточным (Ghezzi, P., Neuroimmunomodulation, 9: 178-182, (2001)).
Нейродегенеративные расстройства
Болезнь Альцгеймера (AD) и болезнь Паркинсона (PK) представляют собой два наиболее распространенных нейродегенеративных расстройства. AD серьезно влияет на способность человека к обычной повседневной деятельности. Она затрагивает те части головного мозга, которые контролируют мышление, память и язык. Считается, что около 4 миллионов американцев, обычно после 60 лет, страдают AD.
PK представляет собой прогрессивное расстройство центральной нервной системы, поражающее более 1,5 миллиона человек в США. Клинически, это заболевание характеризуется уменьшением спонтанных движений, трудностями при ходьбе, постуральной нестабильностью, оцепенелостью, обусловленной напряжением мышц, и тремором. PK развивается в результате дегенерации пигментированных нейронов в черном веществе головного мозга, приводя к снижению доступности допамина. Причина этих нейродегенеративных расстройств неизвестна, и в настоящее время нет никакого эффективного лечения этих заболеваний.
Таким образом, необходимы новые подходы для лечения указанных выше и других связанных с воспалением заболеваний. Хотя механизмы связанных с воспалением заболеваний остаются неясными и часто отличаются друг от друга, было показано, что дисфункция иммунной системы, вызванная дерегуляцией цитокинов, играет важную роль в инициации и развитии воспаления (Schon, M.P., J Invest Dermatol, 112: 405-410, (1999); Andreakos, E.T., Cytokine Growth Factor Rev, 13: 299-313, (2002); Najarian, D.J., J Am Acad Dermatol, 48: 805-821, (2003)).
Цитокины, в основном, можно классифицировать на 3 типа: провоспалительные (IL-1α, β, IL-2, IL-3, IL-6, IL-7, IL-9, IL-12, IL-17, IL-18, IL-23, TNF-α, LT, LIF, Онкостатин, и IFNc1α, β, γ); противовоспалительные (IL-4, IL-10, IL-11, W-13 и TGF-β); и хемокины (IL-8, Gro-α, MIP-1, MCP-1, ENA-78 и RANTES).
Оказалось, что во многих воспалительных состояниях провоспалительные цитокины, особенно TNF-α, IL-1β и IL-6, а также противовоспалительный цитокин IL-10 играют важную роль в патогенезе различных связанных с воспалением заболеваний и поэтому могут служить в качестве потенциальных терапевтических мишеней. Например, повышенные уровни некоторых провоспалительных цитокинов (TNF-α, IFNγ, IL-1, IL-2, IL-6 и IL-12) и хемокинов (IL-8, MCP-1 и RANTES) наблюдались при некоторых связанных с воспалением заболеваниях, таких как CD, псориаз, RA, болезнь Grave и тироидит Хашимото (Andreakos, E.T., Cytokine Growth Factor Rev, 13: 299-313, (2002)), что идет параллельно с повышением уровня растворимых рецепторов TNF, антагонистов рецептора IL-1 и противовоспалительного цитокина IL-10 (Noguchi, M., Gut, 43: 203-209, (1998); Autschbach, F., Am J Pathol, 153: 121-130, (1998)). Было показано, что IL-10 подавляет повышение продукции провоспалительных цитокинов как in vitro в культурах LPMC, так и in vivo у пациентов (Schreiber, S., Gastroenterology, 108: 1434-1444, (1995)). Положительный ответ CD пациентов, которых лечили при помощи IL-10, демонстрирует, что может также иметь место дисбаланс между продукцией провоспалительных и противовоспалительных цитокинов при CD.
Обобщая вышесказанное, за последние годы подход к лечению связанных с воспалением заболеваний претерпел эволюционное изменение частично в связи с растущим беспокойством, связанным с тяжестью этих заболеваний, и частично в связи со значительным прогрессом в понимании важной роли цитокинов в иммунопатогенезе этих заболеваний. Основные усилия были сфокусированы на нацеливание на TNF-α и IL-1 (Baugh, J.A., Curr Opin Drug Discov Devel, 4: 635-650, (2001)), и в настоящее время некоторые продукты (ингибиторы TNF-α: инфликсимаб, моноклональное анти-TNF-α антитело; и этанерсепт, рецептор p75 TNF-α) для лечения RA, псориаза и IBD, как указано выше, имеются на рынке или находятся в стадии клинических испытаний. Некоторые другие средства-кандидаты или стратегии, нацеленные на IL-1 (Gabay, C, Curr Opin Investig Drugs, 4: 593-597, (2003)), IL-6 или IL-10, находятся в стадии разработки (Gabay, C, Curr Opin Investig Drugs, 4: 593-597, (2003); Palladino, M.A., Nat Rev Drug Discov, 2: 736-746, (2003); Girolomoni, G., Curr Opin Investig Drugs, 3: 1590-1595, (2002)). Эти биологические виды лечения обеспечивают существенную эффективность в течение короткого и среднего периода времени у многих пациентов с RA (Elliott, M.J., Lancet, 344: 1125-1127, (1994); Moreland, L.W., N Engl J Med, 3377: 141-147, (1997); Campion, G.V., Artritis Rheum, 39: 1092-1101, (1996); Feldmann, M., Nat Immunоl, 2: 771-773, (2001)). Хотя эти лекарственные средства хорошо переносятся и обладают хорошим общим профилем безопасности, в данной области остается необходимость в дополнительных лекарственных средствах, которые могут ингибировать провоспалительные цитокины или стимулировать противовоспалительные цитокины.
На основании этой концепции, авторами настоящего изобретения были исследованы некоторые типы малых молекул для оценки их способности к регуляции различных цитокинов и изучены потенциальные клинические применения для лечения различных связанных с воспалением заболеваний.
Краткое описание изобретения
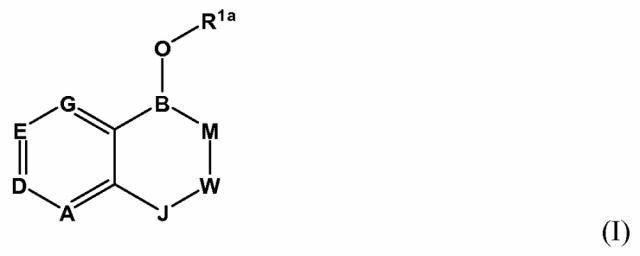
В первом аспекте настоящее изобретение обеспечивает способ лечения или профилактики связанного с воспалением заболевания у человека или животного, при этом указанный способ включает введение человеку или животному терапевтически эффективного количества соединения, описанного в настоящей заявке. В иллюстративном варианте воплощения соединение является представителем, выбранным из C1-C100. В иллюстративном варианте воплощения соединение имеет структуру, соответствующую формуле I:
,
где B представляет собой бор. R1a является представителем, выбранным из группы, включающей отрицательный заряд, противоион соли, H, циано, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. M является представителем, выбранным из кислорода, серы и NR2a. R2a является представителем, выбранным из группы, включающей H, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. J является представителем, выбранным из (CR3aR4a)n1 и CR5a. R3a, R4a и R5a являются представителями, независимо выбранными из группы, включающей H, циано, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. Индекс n1 означает целое число, выбранное из 0-2. W является представителем, выбранным из C=O(карбонил), (CR6aR7a)m1 и CR8a. R6a, R7a и R8a являются представителями, независимо выбранными из группы, включающей H, циано, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. Индекс m1 означает целое число, выбранное из 0 и 1. A является представителем, выбранным из CR9a и N. D является представителем, выбранным из CR10a и N. E является представителем, выбранным из CR11a и N. G является представителем, выбранным из CR12a и N. R9a, R10a, R11a и R12a являются представителями, независимо выбранными из группы, включающей H, OR*, NR*R**, SR*, -S(O)R*, -S(O)2R*,-S(O)2NR*R**, -C(O)R*, -C(O)OR*, -C(О)NR*R**, нитро, галоген, циано, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. Каждый R* и R** являются представителями, независимо выбранными из группы, включающей H, нитро, галоген, циано, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. Сочетание атомов азота (A+D+E+G) означает целое число, выбранное из 0-3. Представитель, выбранный из R3a, R4a и R5a, и представитель, выбранный из R6a, R7a и R8a, вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R3a и R4a, вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R6a и R7a, вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R9a и R10a, вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R10a и R11a, вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R11a и R12a, вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца.
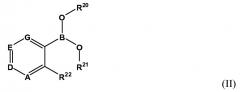
Во втором аспекте настоящее изобретение обеспечивает способ лечения или профилактики связанного с воспалением заболевания у человека или животного, при этом указанный способ включает введение человеку или животному терапевтически эффективного количества соединения, имеющего структуру, соответствующую формуле II:
,
где B представляет собой бор. R20, R21 и R22 являются представителями, независимо выбранными из группы, включающей отрицательный заряд, противоион соли, H, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. A является представителем, выбранным из CR9a и N. D является представителем, выбранным из CR10a и N. E является представителем, выбранным из CR11a и N. G является представителем, выбранным из CR12a и N. R9a, R10a, R11a и R12a являются представителями, независимо выбранными из группы, включающей H, OR*, NR*R**, SR*, -S(O)R*, -S(O)2R*, -S(O)2NR*R**, -C(O)R*, -C(O)OR*, -C(О)NR*R**, нитро, галоген, циано, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. Каждый R* и R** являются представителями, независимо выбранными из группы, включающей H, нитро, галоген, циано, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил и замещенный или незамещенный гетероарил. Сочетание атомов азота (A+D+E+G) означает целое число, выбранное из 0-3. Представитель, выбранный из R3a, R4a и R5a, и представитель, выбранный из R6a, R7a и R8a, вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R3a и R4a вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R6a и R7a вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R9a и R10a вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R10a и R11a вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца. R11a и R12a вместе с атомами, с которыми они связаны, необязательно объединяются с образованием 4-7-членного кольца.
Изобретение также обеспечивает дополнительные способы использования соединений и фармацевтических композиций соединений, описанных в настоящей заявке.
Краткое описание чертежей
Фиг.1 показывает степень ингибирования соединениями по настоящему изобретению каждого из четырех цитокинов: TNF-α, IL-1β, IFN-γ и IL-4.
Фиг.2 представляет иллюстративные соединения по настоящему изобретению.
Фиг.3 представляет иллюстративные соединения по настоящему изобретению.
Подробное описание изобретения
I. Определения и аббревиатуры
Аббревиатуры, используемые в настоящей заявке, в основном, имеют их традиционное значение, принятое в области химии и биологии.
"Соединение по настоящему изобретению", как этот термин используется в настоящей заявке, относится к соединениям, обсуждаемым в настоящей заявке, фармацевтически приемлемым солям и пролекарствам этих соединений.
"Ингибирование" и "блокирование" используются в настоящей заявке взаимозаменяемо и относятся к частичной или полной блокаде экспрессии провоспалительных цитокинов при помощи способа по настоящему изобретению, что приводит к снижению количества цитокина у субъекта или пациента.
Когда группы заместителей определены при помощи их традиционных химических формул, которые написаны слева направо, они равным образом охватывают химически идентичные заместители, получаемые при написании структурной формулы справа налево, например, -CH2O- также может означать -OCH2-.
Термин "поли", как он используется в настоящей заявке, означает по меньшей мере 2. Например, поливалентный металлический ион означает ион металла, имеющий валентность по меньшей мере 2.
"Фрагмент" относится к радикалу молекулы, который присоединен к еще одному фрагменту.
Символ , независимо от того, используется ли он как связь или расположен перпендикулярно к связи, указывает местоположение, в котором представленный фрагмент присоединен к остальной части молекулы.
Термин "алкил", как таковой или как часть еще одного заместителя, означает, если не указано иное, линейный или разветвленный, или циклический углеводородный радикал, или их сочетание, который может быть полностью насыщенным, моно- или полиненасыщенным, и может включать ди- и поливалентные радикалы, имеющие указанное количество атомов углерода (т.е. C1-C10 означает один-десять атомов углерода). Примеры насыщенных углеводородных радикалов включают, но не ограничиваются этим, группы, такие как метил, этил, н-пропил, изопропил, н-бутил, трет-бутил, изобутил, втор-бутил, циклогексил, (циклогексил)метил, циклопропилметил, гомологи и изомеры, например, н-пентил, н-гексил, н-гептил, н-октил, и т.п. Ненасыщенная алкильная группа представляет собой группу, содержащую одну или несколько двойных связей или тройных связей. Примеры ненасыщенных алкильных групп включают, но не ограничиваются этим, винил, 2-пропенил, кротил, 2-изопентенил, 2-(бутадиенил), 2,4-пентадиенил, 3-(1,4-пентадиенил), этинил, 1- и 3-пропинил, 3-бутинил и высшие гомологи и изомеры. Термин "алкил", если не указано иное, также включает производные алкила, более подробно описанные ниже, такие как "гетероалкил". Алкильные группы, которые ограничены углеводородными группами, указаны как "гомоалкил".
Термин "алкилен", как таковой или как часть еще одного заместителя, означает двухвалентный радикал, производный от алкана, представленный, но не ограничивающийся этим, формулой -CH2CH2CH2CH2-, и, кроме того, включает группы, которые описаны ниже как "гетероалкилен". Типично, алкильная (или алкиленовая) группа содержит от 1 до 24 атомов углерода, при этом группы, содержащие 10 или меньше атомов углерода, являются предпочтительными в настоящем изобретении. "Низший алкил" или "низший алкилен" представляет собой алкильную или алкиленовую группу с более короткой цепью, в основном, содержащую восемь или меньше атомов углерода.
Термины "алкокси", "алкиламино" и "алкилтио" (или тиоалкокси) используются в их традиционном значении и относятся к алкильным группам, которые присоединены к остальной части молекулы через атом кислорода, аминогруппу или атом серы, соответственно.
Термин "гетероалкил", как таковой или в сочетании с еще одним термином, означает, если не указано иное, стабильный линейный или разветвленный, или циклический углеводородный радикал, или их сочетания, включающий указанное количество атомов углерода и, по меньшей мере, один гетероатом. В иллюстративном варианте воплощения гетероатомы могут быть выбраны из группы, включающей B, O, N и S, и при этом атомы азота и серы необязательно могут быть окислены, а гетероатом азота необязательно может быть кватернизирован. Гетероатом(ы) B, O, N и S могут находиться в любом положении внутри гетероалкильной группы или в положении, в котором алкильная группа присоединена к остальной части молекулы. Примеры включают, но не ограничиваются этим, -CH2-CH2-O-CH3, -CH2-CH2-NH-CH3, -CH2-CH2-N(CH3)-CH3, -CH2-S-CH2-CH3, -CH2-CH2, -S(O)-CH3, -CH2-CH2-S(O)2-CH3, -CH=CH-O-CH3, -CH2-CH=N-OCH3 и -CH=CH-N(CH3)-CH3. Вплоть до двух гетероатомов могут быть последовательно расположены, например, -CH2-NH-OCH3. Подобным образом, термин "гетероалкилен", как таковой или как часть еще одного заместителя, означает двухвалентный радикал, производный от гетероалкила, представленный, но не ограничивающийся этим, -CH2-CH2-S-CH2-CH2- и -CH2-S-CH2-CH2-NH-CH2-. Что касается гетероалкиленовых групп, гетероатомы также могут быть расположены на любом или общих концах цепи (например, алкиленокси, алкилендиокси, алкиленамино, алкилендиамино и т.п.). Также, что касается алкиленовых и гетероалкиленовых связывающих групп, направление, в котором записана формула связывающей группы, не предполагает никакой ориентации связывающей группы. Например, формула -C(O)2R'- представляет как -C(O)2R'-, так и -R'C(O)2-.
Термины "циклоалкил" и "гетероциклоалкил", как таковые или в сочетании с другими терминами, означают, если не указано иное, циклические варианты "алкила" и "гетероалкила", соответственно. Также, что касается гетероциклоалкила, гетероатом может находиться в положении, в котором гетероцикл присоединен к остальной части молекулы. Примеры циклоалкила включают, но не ограничиваются этим, циклопентил, циклогексил, 1-циклогексенил, 3-циклогексенил, циклогептил и т.п. Примеры гетероциклоалкила включают, но не ограничиваются этим, 1-(1,2,5,6-тетрагидропиридил), 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 4-морфолинил, 3-морфолинил, тетрагидрофуран-2-ил, тетрагидрофуран-3-ил, тетрагидротиен-2-ил, тетрагидротиен-3-ил, 1-пиперазинил, 2-пиперазинил и т.п.
Термины "гало" или "галоген", как таковые или как часть еще одного заместителя, означают, если не указано иное, атом фтора, хлора, брома или йода. Кроме того, такие термины, как "галогеналкил", включают моногалогеналкил и полигалогеналкил. Например, термин "галоген(C1-C4)алкил" включает, но не ограничивается этим, трифторметил, 2,2,2-трифторэтил, 4-хлорбутил, 3-бромпропил и т.п.
Термин "арил" означает, если не указано иное, полиненасыщенный, ароматический заместитель, который может представлять собой одно кольцо или несколько колец (предпочтительно от 1 до 3 колец), которые конденсированы вместе или связаны ковалентно. Термин "гетероарил" относится к арильным группам (или кольцам), которые содержат от одного до четырех гетероатомов. В иллюстративном варианте воплощения гетероатом выбран из B, N, O и S, где атомы азота и серы необязательно являются окисленными, а атом(ы) азота необязательно кватернизирован(ы). Гетероарильная группа может быть присоединена к остальной части молекулы через гетероатом. Неограничивающие примеры арильной и гетероарильной групп включают фенил, 1-нафтил, 2-нафтил, 4-бифенил, 1-пирролил, 2-пирролил, 3-пирролил, 3-пиразолил, 2-имидазолил, 4-имидазолил, пиразинил, 2-оксазолил, 4-оксазолил, 2-фенил-4-оксазолил, 5-оксазолил, 3-изоксазолил, 4-изоксазолил, 5-изоксазолил, 2-тиазолил, 4-тиазолил, 5-тиазолил, 2-фурил, 3-фурил, 2-тиенил, 3-тиенил, 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидил, 4-пиримидил, 5-бензотиазолил, пуринил, 2-бензимидазолил, 5-индолил, 1-изохинолил, 5-изохинолил, 2-хиноксалинил, 5-хиноксалинил, 3-хинолил и 6-хинолил. Заместители для каждой из указанных выше арильной и гетероарильной кольцевых систем выбраны из групп приемлемых заместителей, описанных ниже.
Для краткости, термин "арил" при использовании в сочетании с другими терминами (например, арилокси, арилтиокси, арилалкил) включает как арильные, так и гетероарильные кольца, определенные выше. Таким образом, термин "арилалкил" включает такие радикалы, в которых арильная группа присоединена к алкильной группе (например, бензил, фенетил, пиридилметил и т.п.), включая такие алкильные группы, в которых атом углерода (например, метиленовая группа) был замещен, например, атомом кислорода (например, феноксиметил, 2-пиридилоксиметил, 3-(1-нафтилокси)пропил и т.п.).
Каждый из описанных выше терминов (например, "алкил", "гетероалкил", "арил" и "гетероарил") включают как замещенные, так и незамещенные формы указанных радикалов. Предпочтительные заместители для каждого типа радикала представлены ниже.
Заместители для алкильных и гетероалкильных радикалов (включая такие группы, которые часто указывают как алкилен, алкенил, гетероалкилен, гетероалкенил, алкинил, циклоалкил, гетероциклоалкил, циклоалкенил и гетероциклоалкенил) в общем виде указаны как "заместители алкильной группы", и они могут представлять собой одну или несколько из многочисленных групп, выбранных, но не ограничиваясь этим, из следующих: -OR', =О, =NR', =N-ОR', -NR'R", -SR', -галоген, -OC(O)R', -C(O)R', -CO2R', -CONR'R", -ОC(О)NR'R", -NR"C(O)R', -NR'-C(О)NR"R"', -NR"C(О)2R', -NR-C(NR'R"R'")=NR"", -NR-C(NR'R")=NR'", -S(O)R', -S(O)2