Терапия болезни паркинсона с применением комбинации с фиксированными дозами
Иллюстрации
Показать всеГруппа изобретений относится к химико-фармацевтической промышленности и представляет собой фармацевтическую композицию для применения для лечения болезни Паркинсона, содержащую фармацевтически приемлемый носитель и комбинацию прамипексола и разагилина с фиксированными дозами; и способ получения состава с пролонгированным высвобождением, содержащего комбинацию прамипексола и разагилина или их фармацевтически приемлемых солей с фиксированными их дозами, причем указанная комбинация с фиксированными дозами содержит от 0,05 до 1,0 мг прамипексола и от 0,055 до 1,0 мг разагилина. Группа изобретений позволяет снизить количество побочных эффектов при сохранении высокой эффективности фармацевтической композиции путем снижения дозы прамипексола и сохранения высокой дозы разагилина. 2 н. и 17 з.п. ф-лы, 4 ил., 6 табл., 4 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к области нейродегенеративных заболеваний и, в частности, относится к композициям и способам лечения болезни Паркинсона.
УРОВЕНЬ ТЕХНИКИ
[0002] Для лечения болезни Паркинсона традиционно применяют агонисты дофамина; тем не менее, их использование может быть ограничено нежелательными явлениями различной степени тяжести. Введение агонистов дофамина, как правило, связано с тошнотой, рвотой и ортостатической гипотензией. Указанные побочные эффекты становятся более выраженными при использовании более высоких доз, но, как правило, их можно уменьшать при использовании схемы с замедленным и комплексным титрованием. Прамипексол (а также несколько других агонистов дофамина (DA)) также связывают с расстройствами побуждений, периферическими отеками, психозом и седативными эффектами, которые трудно контролировать, что тем самым ограничивает возможность использования этого лекарственного средства. Разагилин, другое лекарственное средство, применяемое для лечения болезни Паркинсона, в целом хорошо переносится, но также имеет несколько проблем, связанных с безопасностью, в частности риск сырного эффекта (гипертонический криз) при употреблении пищи, богатой тирамином, и серотонинового эффекта (избыточной активности серотонина) при использовании в комбинации с селективными ингибиторами обратного захвата серотонина и другими антидепрессантами, которые традиционно назначают при болезни Паркинсона. Если рассматривать оба этих лекарственных средства, то более высокие дозы прамипексола, как правило, связывают с повышенным риском тяжелых нежелательных эффектов, и, таким образом, лечащим врачам важно знать стратегии лечения, которые обеспечивают максимальную эффективность при борьбе с симптомами PD (болезни Паркинсона) и при этом минимизируют осложнения, связанные с двигательной активностью, и нежелательные явления, вызванные DA.
[0003] В компании Pharma Two В обнаружили, что объединение агентов со взаимодополняющими механизмами действия (т.е. двух различных активных агентов, обладающих симптоматическим или нейрозащитным действием) обеспечивает увеличенную эффективность борьбы с болезнью Паркинсона по сравнению с той, которую можно достичь при использовании увеличенных доз каждого из агентов по отдельности (международная заявка на патент WO 2009147681). Данные доклинических испытаний, полученные ранее в Pharma Two В, позволяют предположить, что ингибитор МАО-В разагилин и агонист дофамина прамипексол в низких дозах обладают синергическим действием, выражающимся в увеличении эффективности указанных лекарственных средств. С учетом того, что начало лечения с использованием агонистов дофамина связано с профилем относительно тяжелых нежелательных явлений, существующие в настоящее время способы лечения включают схему титрования с использованием низких доз, которые, по ожиданиям, не оказывают терапевтического действия, но минимизируют побочные эффекты, вызываемые немедленным началом введения эффективных доз. Кроме того, нежелательные эффекты связывают с долгосрочным лечением с использованием увеличенных доз агониста дофамина. Таким образом, вариант применения комбинации, содержащей низкие дозы агониста дофамина, является предпочтительным для многих пациентов и может обеспечивать высокоактивное терапевтическое действие, сопровождающееся минимальными побочными эффектами.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0004] Согласно некоторым аспектам в настоящем изобретении предложена фармацевтическая композиция для применения для лечения болезни Паркинсона, содержащая фармацевтически приемлемый носитель и комбинацию прамипексола и разагилина с фиксированными их дозами, причем указанная комбинация с фиксированными дозами содержит субтерапевтическую дозу прамипексола и субтерапевтическую дозу разагилина, при этом доза прамипексола ниже или равна дозе разагилина.
[0005] Согласно другому аспекту в настоящем изобретении предложены способы получения состава с пролонгированным высвобождением (ER) комбинации прамипексола и разагилина или их фармацевтически приемлемых солей с фиксированными их дозами, включающие стадии:
(i) растворения активного агента, содержащего прамипексол, разагилин или оба указанных вещества, необязательно подходящим образом смешанного со связывающим агентом и/или агентом, способствующим скольжению, в подходящей системе растворителей с получением однородной суспензии;
(ii) нанесения покрытия суспензии, полученной на стадии (i), на инертные пеллеты, такие как инертные зерна нонпарель;
(iii) необязательно, нанесения изолирующего/защитного подпокровного слоя на пеллеты, содержащие разагилин, пеллеты, содержащие прамипексол, или пеллеты, содержащие прамипексол и разагилин, полученные на стадии (ii);
(iv) нанесения на пеллеты, полученные на стадии (ii) или (iii), слоя покрытия с пролонгированным высвобождением, который обеспечивает пролонгированное высвобождение указанных прамипексола и разагилина, с получением тем самым указанного состава с пролонгированным высвобождением;
(v) необязательно, смешения пеллет с покрытием, полученных на стадии (iv), с подходящим вспомогательным веществом; и
(vi) заполнения капсул указанным составом с пролонгированным высвобождением или прессования указанного состава с пролонгированным высвобождением в таблетки, где указанные капсулы или таблетки имеют желаемое отношение пеллет, содержащих прамипексол, к пеллетам, содержащим разагилин; или указанные капсулы или таблетки содержат пеллеты, содержащие прамипексол и разагилин;
с получением тем самым состава с пролонгированным высвобождением, содержащего комбинацию прамипексола и разагилина с фиксированными их дозами.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0006] На фиг. 1 показан профиль растворения комбинированного продукта.
[0007] На фиг. 2 показано зависящее от дозы синергическое действие прамипексола, разагилина и их комбинации на уровень дофамина в мозге мышей.
[0008] На фиг. 3А-В изображены результаты исследования фармакокинетики Р2 В001 (FDC (комбинация с фиксированными дозами), содержащая 1 мг разагилина и 0,75 мг прамипексола) и их сравнение с соответствующими коммерческими лекарственными средствами, Азилектом (1 мг разагилина) и Мирапексом ER (0,75 мг прамипексола), которые вводили отдельно или в комбинации. Приведены концентрации в плазме (пг/мл) прамипексола и разагилина.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0009] Настоящее изобретение основано на том факте, что существует возможность использования комбинации очень низких доз агониста дофамина, в частности таких доз, которые в настоящее время, как правило, не используют для монотерапии, но используют для титрования, с различными дозами ингибитора моноаминоксидазы В (МАОВ), разагилина, при этом можно добиваться высокой эффективности за счет синергии механизмов действия этих двух лекарственных средств.
[0010] Этот факт позволяет уменьшать дозу прамипексола и таким образом предотвращает риск появления нежелательных явлений, вызванных агонистом дофамина (DA), и при этом поддерживает сравнимую с более высокими дозами эффективность у пациентов. Таким образом, существует возможность более точного определения наилучших доз разагилина и прамипексола для использования в комбинации, которые связаны со значительным действием в отношении болезни Паркинсона и хорошим профилем безопасности.
[0011] Таким образом, согласно настоящему изобретению комбинация с фиксированными дозами, содержащая субтерапевтические дозы прамипексола и разагилина или их фармацевтически приемлемых солей, т.е. дозу прамипексола, которая при его отдельном введении не оказывает существенное терапевтическое действие, и дозу разагилина, которая при его отдельном введении не оказывает существенное терапевтическое действие, где доза прамипексола ниже или равна дозе разагилина, является эффективной для лечения болезни Паркинсона.
[0012] Термин «комбинация с фиксированными дозами», используемый в настоящем описании, относится к единому составу, содержащему два различных лекарственных средства, в указанном случае, разагилин и прамипексол, в точном отношении, а именно в конкретных фиксированных дозах.
[0013] Термин «субтерапевтическая доза», используемый в настоящем описании, относится к дозе ниже эффективного уровня дозировки, традиционно используемого при монотерапии для лечения заболевания, или к дозе, которую на настоящее время, как правило, не используют при эффективной монотерапии, т.е. в случае прамипексола и разагилина примерно 1 мг/день.
[0014] В частности, мольное отношение прамипексола к разагилину выбрано из диапазона от 1:1 до 1:20, от 1:1 до 1:10, от 1:1 до 1:5, от 1:1 до 1:3 или от 1:1 до 1:2.
[0015] В конкретных вариантах реализации мольное отношение прамипексола к разагилину выбрано из диапазона от 1:1,1 до 1:20, от 1:1,1 до 1:10, от 1:1,1 до 1:5, от 1:1,1 до 1:3 или от 1:1,1 до 1:2. В частности это отношение выбрано из группы, состоящей из 1:1,1, 1:1,2, 1:1,3, 1:1,4, 1:1,5, 1:1,6, 1:1,7, 1:1,8, 1;1,9, 1:2,0, 1:2,1, 1:2,2, 1:2,3, 1:2,4, 1:2,5, 1:2,6, 1:2,7, 1:2,8, 1:2,9 и 1:3,0.
[0016] В конкретных вариантах реализации комбинация с фиксированными дозами содержит от 0,05 мг до 1,0 мг прамипексола и от 0,05 мг до 1,0 мг разагилина при условии, что доза прамипексола ниже или равна дозе разагилина, как определено выше.
[0017] В конкретных вариантах реализации комбинация с фиксированными дозами содержит от 0,1 до 0,6 мг прамипексола и от 0,1 до 0,75 мг разагилина.
[0018] В конкретных вариантах реализации комбинация с фиксированными дозами может содержать 0,05, 0,055, 0,06, 0,065, 0,07, 0,075, 0,08, 0,085, 0,09, 0,095, 0,1, 0,105, 0,11, 0,115, 0,12, 0,125, 0,13, 0,135, 0,14, 0,145, 0,15, 0,155, 0,16, 0,165, 0,17, 0,175, 0,18, 0,185, 0,19, 0,195, 0,2, 0,205, 0,21, 0,215, 0,22, 0,225, 0,23, 0,235, 0,24, 0,245, 0,25, 0,255, 0,26, 0,265, 0,27, 0,275, 0,28, 0,285, 0,29, 0,295, 0,3, 0,305, 0,31, 0,315, 0,32, 0,325, 0,33, 0,335, 0,34, 0,345, 0,35, 0,355, 0,36, 0,365, 0,37, 0,375, 0,38, 0,385, 0,39, 0,395, 0,4, 0,405, 0,41, 0,415, 0,42, 0,425, 0,43, 0,435, 0,44, 0,445, 0,45, 0,455, 0,46, 0,465, 0,47, 0,475, 0,48, 0,485, 0,49, 0,495, 0,5, 0,505, 0,51, 0,515,0,52, 0,525, 0,53,0,535, 0,54, 0,545, 0,55,0,555, 0,56, 0,565, 0,57,0,575, 0,58, 0,585, 0,59, 0,595, 0,6, 0,605, 0,61, 0,615, 0,62, 0,625, 0,63, 0,635, 0,64, 0,645, 0,65, 0,655, 0,66, 0,665, 0,67, 0,675, 0,68, 0,685, 0,69, 0,695, 0,7, 0,705, 0,71, 0,715, 0,72, 0,725, 0,73, 0,735, 0,74, 0,745, 0,75, 0,755, 0,76, 0,765, 0,77, 0,775, 0,78, 0,785, 0,79, 0,795, 0,8, 0,805, 0,81, 0,815, 0,82, 0,825, 0,83, 0,835, 0,84, 0,845, 0,85, 0,855, 0,86, 0,865, 0,87, 0,875, 0,88, 0,885, 0,89, 0,895, 0,9, 0,905, 0,91, 0,915, 0,92, 0,925, 0,93, 0,935, 0,94, 0,945, 0,95,0,955, 0,96, 0,965, 0,97,0,975, 0,98, 0,985, 0,99, 0,995 или 1 мг прамипексола и 0,05, 0,055, 0,06, 0,065, 0,07, 0,075, 0,08, 0,085, 0,09, 0,095, 0,1, 0,105, 0,11, 0,115, 0,12, 0,125, 0,13, 0,135, 0,14, 0,145, 0,15, 0,155, 0,16, 0,165, 0,17, 0,175, 0,18, 0,185, 0,19, 0,195, 0,2, 0,205, 0,21, 0,215, 0,22, 0,225, 0,23, 0,235, 0,24, 0,245, 0,25, 0,255, 0,26, 0,265, 0,27, 0,275, 0,28, 0,285, 0,29, 0,295, 0,3, 0,305, 0,31, 0,315, 0,32, 0,325, 0,33, 0,335, 0,34, 0,345, 0,35, 0,355, 0,36, 0,365, 0,37, 0,375, 0,38, 0,385, 0,39, 0,395, 0,4, 0,405, 0,41, 0,415, 0,42, 0,425, 0,43, 0,435, 0,44, 0,445, 0,45, 0,455,0,46, 0,465, 0,47, 0,475,0,48, 0,485, 0,49, 0,495, 0,5, 0,505, 0,51, 0,515, 0,52, 0,525, 0,53, 0,535, 0,54, 0,545, 0,55, 0,555, 0,56, 0,565, 0,57, 0,575, 0,58, 0,585, 0,59, 0,595, 0,6, 0,605, 0,61, 0,615, 0,62, 0,625, 0,63, 0,635, 0,64, 0,645, 0,65, 0,655, 0,66, 0,665, 0,67, 0,675, 0,68, 0,685, 0,69, 0,695, 0,7, 0,705, 0,71, 0,715, 0,72, 0,725, 0,73, 0,735, 0,74, 0,745, 0,75, 0,755, 0,76, 0,765, 0,77, 0,775, 0,78, 0,785, 0,79, 0,795, 0,8, 0,805, 0,81, 0,815, 0,82, 0,825, 0,83, 0,835,0,84, 0,845, 0,85, 0,855, 0,86, 0,865, 0,87, 0,875, 0,88, 0,885, 0,89, 0,895, 0,9, 0,905, 0,91, 0,915, 0,92, 0,925, 0,93, 0,935, 0,94, 0,945, 0,95, 0,955, 0,96, 0,965, 0,97, 0,975, 0,98, 0,985, 0,99, 0,995 или 1 мг разагилина при условии, что доза прамипексола ниже или равна дозе разагилина, что определено выше.
[0019] Для большей ясности, но не ограничения объема предложенного изобретения, если не указано иное, следует понимать, что все числовые значения, выражающие количество, процентное содержание или долю, а также другие числовые значения, указанные в настоящем описании, во всех случаях используются вместе с термином «примерно». Соответственно, числовые параметры, приведенные в настоящем описании, являются приблизительными и могут изменяться в зависимости от желаемого конечного результата. Например, каждый числовой параметр можно рассматривать с учетом числа указанных значащих цифр, а также использования привычных правил округления.
[0020] Следует понимать, что любые диапазоны доз, диапазоны количеств, диапазоны концентраций, диапазоны процентного содержания или диапазоны отношений, приведенные в настоящем описании, включают дозы, концентрации, процентное содержание или отношения, имеющие любое значение, не выходящее за рамки этого диапазона, а также выходящее за его границы, но не более чем на одну десятую от значения верхнего или нижнего предела указанного диапазона, или долю от указанного значения, такую как одна десятая и одна сотая от числового значения, если не указано иное.
[0021] В других вариантах реализации прамипексол и разагилин вводят в состав с пролонгированным высвобождением (ER). Термин «пролонгированное высвобождение» используют в настоящем описании взаимозаменяемо с терминами «долгосрочное действие», «повторяющееся действие», «контролируемое высвобождение» и «замедленное высвобождение», и он относится к высвобождению активного агента с предварительно определенными интервалами или к постепенному высвобождению, таким образом, что содержащийся активный агент является доступным в течение продленного периода времени после приема внутрь.
[0022] В конкретных вариантах реализации постепенное высвобождение всего или практически всего количества прамипексола и разагилина, входящих в состав комбинации с фиксированными дозами, из состава с пролонгированным высвобождением происходит в течение 24 часов.
[0023] Фармацевтическая композиция может иметь вид монолитной матрицы; таблетки, предпочтительно двух- или многослойной таблетки, матричной таблетки, распадающейся таблетки, растворимой таблетки или жевательной таблетки; капсулы или саше, предпочтительно заполненных гранулами, зернами, шариками или пеллетами; или системы депо на основе биоразлагаемого полимера, такого как поли(D,L-лактид) (ПЛА), полигликолид (ПГА) и сополимер D,L-лактида и гликолида (ПЛГА), и она может быть приготовлена для перорального введения.
[0024] Активный агент можно подходящим образом смешивать со связывающим агентом и/или агентом, способствующим скольжению, в подходящей системе растворителей с получением однородной суспензии, и далее полученную суспензию можно наносить на инертные пеллеты с получением тонкого покрытия. Согласно настоящему изобретению разагилин и прамипексол можно растворять в отдельных растворителях и по отдельности распылять на различные пеллеты с получением пеллет, содержащих разагилин, и пеллет, содержащих прамипексол; или каждый отдельный раствор можно распылять на одни и те же пеллеты с получением пеллет, содержащих разагилин и прамипексол. В качестве альтернативы разагилин и прамипексол можно растворять в общем растворителе с получением общего однородного раствора, или с получением общего однородного раствора можно смешивать отдельные растворы, после этого общий однородный раствор можно распылять на пеллеты с получением пеллет, содержащих разагилин и прамипексол.
[0025] На следующей стадии, которая является необязательной, на пеллеты, содержащие разагилин, пеллеты, содержащие прамипексол, или пеллеты, содержащие разагилин и прамипексол, наносят покрытие изолирующего/защитного подпокровного слоя, после чего на пеллеты наносят слой покрытия с пролонгированным высвобождением, что обеспечивает пролонгированное высвобождение разагилина и прамипексола, таким образом получают указанный состав с пролонгированным высвобождением. Пеллеты с покрытием затем можно смешивать с подходящим вспомогательным веществом и, наконец, составом с пролонгированным высвобождением заполняют капсулы или состав прессуют в таблетки, где указанные капсулы или таблетки имеют желаемое отношение пеллет, содержащих разагилин, к пеллетам, содержащим прамипексол; или указанные капсулы или таблетки содержат пеллеты, содержащие разагилин и прамипексол.
[0026] Желаемое отношение, такое как определено выше в настоящем описании, можно получать при помощи любого способа, который обеспечивает желаемый результат, такого как, не ограничиваясь ими, взвешивание, измерение объема или подсчет количества пеллет, содержащих разагилин, и пеллет, содержащих прамипексол, по отдельности и заполнение ими капсулы, или прессование таблетки, имеющей желаемую массу, объем или количество пеллет, содержащих каждый активный агент. Предпочтительно пеллеты взвешивают по отдельности и заполняют в желаемом отношении капсулы или прессуют в таблетки или взвешивают вместе в предварительно определенном отношении, после чего смесь взвешивают и заполняют капсулу. В случае пеллет, содержащих разагилин и прамипексол, отношение определяют на стадии нанесения покрытия на инертные пеллеты, на которой раствор с желаемым отношением двух агентов распыляют на инертные пеллеты, или два отдельных раствора распыляют послойно на инертные пеллеты в желаемом отношении.
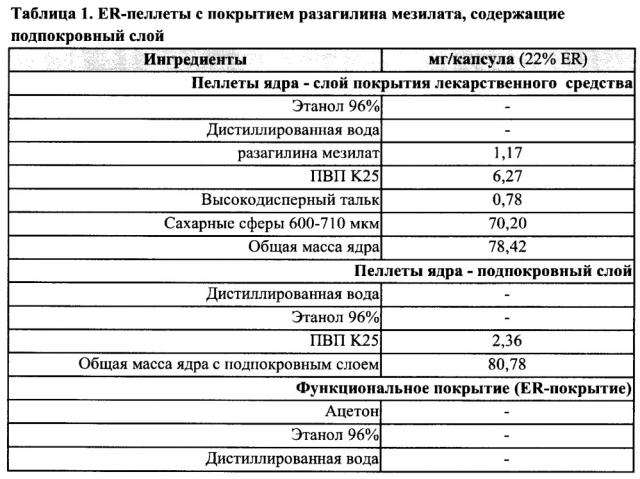
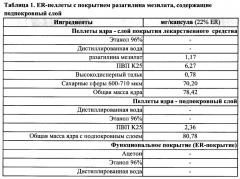
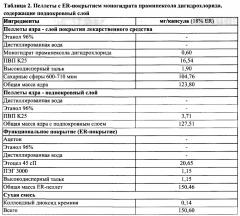
[0027] Таким образом, в конкретных вариантах реализации фармацевтическая композиция согласно настоящему изобретению содержит пеллеты с пролонгированным высвобождением, содержащие (i) инертное ядро пеллеты; (ii) слой лекарственного средства, покрывающий указанное ядро пеллеты, причем указанный слой лекарственного средства содержит активный агент, содержащий разагилин, прамипексол, или оба указанных вещества, или их фармацевтически приемлемые соли, необязательно подходящим образом смешанный со связывающим веществом и/или пленкообразующим полимером и дополнительно необязательно смешанный с агентом, способствующим скольжению; (iii) необязательно изолирующий/защитный подпокровный слой, покрывающий указанный слой лекарственного средства; и (iv) слой с пролонгированным высвобождением, покрывающий указанный подпокровный слой, если его используют, или покрывающий указанный слой лекарственного средства.
[0028] ER-пеллета согласно настоящему изобретению необязательно может содержать изолирующий/защитный подпокровный слой, покрывающий указанный слой лекарственного средства. Задачей указанного подпокровного слоя является изоляция слоя активного вещества от внешнего ER-покрытия и защита от возможного взаимодействия с участием активного агента, которое может влиять на его стабильность и приводить к образованию продуктов разложения активного фармацевтического ингредиента (АФИ). В конкретных вариантах реализации подпокровный слой содержит пленкообразующий полимер и, необязательно, агент, способствующий скольжению.
[0029] ER-пеллета согласно настоящему изобретению содержит внешний слой ER-покрытия, также называемый в настоящем описании «функциональный слой», покрывающий подпокровный слой, если он присутствует, или покрывающий слой лекарственного средства.
[0030] В конкретных вариантах реализации слой ER-покрытия содержит по меньшей мере один рН-независимый полимер, т.е. набухающий в воде/не растворимый в воде/гидрофобный полимер, и, необязательно, порообразующий агент, причем пеллета с пролонгированным высвобождением имеет не зависящие от рН характеристики высвобождения in vitro. В других вариантах реализации функциональный слой содержит рН-независимый полимер, гидрофильный полимер-модулятор высвобождения, выступающий в качестве порообразующего агента, и, необязательно, гидрофобный или гидрофильный пластификатор и/или агент, способствующий скольжению. В дополнительных конкретных вариантах реализации слой ER-покрытия содержит смесь рН-зависимого полимера кишечнорастворимого покрытия и рН-независимого полимера, причем пеллета с пролонгированным высвобождением имеет характеристики высвобождения in vitro примерно нулевого порядка при кислом или физиологическом значении рН, т.е. при значениях рН не более 7,4.
[0031] Связывающие агенты для фармацевтического применения представляют собой гидрофильные вещества, такие как сахара и природные и синтетические полимеры, используемые для получения твердых лекарственных форм благодаря своим адгезионным и когезионным свойствам. Задачей связывающих агентов является способствование увеличению размера за счет увеличения когезионной способности порошков, что тем самым обеспечивает пеллеты и таблетки с необходимой прочностью сцепления. Несмотря на то, что связывающие агенты улучшают внешний вид, твердость и прочность на истирание указанных препаратов, они не влияют на скорость распада таблетки или скорость растворения активных веществ. Связывающие агенты природного происхождения, которые традиционно использовали в прошлом, включают аравийскую камедь, желатин, крахмал и гидролизованный крахмал. Указанные вещества были заменены на связывающие агенты синтетического происхождения, наиболее важными из которых являются повидон и различные производные целлюлозы. Примеры связывающих агентов, которые можно смешивать с активным агентом в слое покрытия лекарственного средства ER-пеллеты согласно настоящему изобретению включают, но не ограничиваются ими, поливинилпирролидон (ПВП), гидроксипропилметилцеллюлозу (ГПМЦ), гидроксипропилцеллюлозу (ГПЦ), микрокристаллическую целлюлозу и их комбинации.
Связывающий агент можно содержаться в количестве от 0,5% до 20%, предпочтительно от 0,5% до 10% по массе от общей массы пеллеты.
[0032] Термин «пленкообразующий полимер», используемый в настоящем описании, относится к полимерам, способным отверждаться с образованием адгезивных пленок. Кроме того, физическим свойством указанных полимеров, которое является существенным для их использования в качестве покрытия, является способность образовывать пленки или придавать определенные адгезионные свойства материалу, на который их наносят. Примеры пленкообразующих полимеров включают без ограничений ПВП, ГПМЦ, ГПЦ, микрокристаллическую целлюлозу и их комбинации. Пленкообразующий полимер, если он содержится в слое лекарственного средства, может присутствовать в количестве до 90% по массе от общей массы слоя лекарственного средства, предпочтительно от 0,5% до 20% по массе от общей массы пеллеты. Количество пленкообразующего полимера в подпокровном слое может составлять до 100% по массе от общей массы подпокровного слоя, предпочтительно от 0,5% до 10% по массе от общей массы пеллеты.
[0033] Для увеличения текучести гранулятов и порошков за счет уменьшения трения и поверхностного заряда в фармацевтические композиции, как правило, добавляют агенты, способствующие скольжению. Кроме того, их используют в качестве агентов, препятствующих слипанию, во время процесса нанесения покрытия. Конкретные агенты, способствующие скольжению, такие как тальк и глицерилмоностеарат, традиционно используют в составах с покрытием в качестве агентов, препятствующих слипанию, которые уменьшают склонность к слипанию при уменьшении температуры продукта. Другие агенты, способствующие скольжению, такие как коллоидный диоксид кремния, обеспечивают желаемые характеристики текучести, которые используют для улучшения свойств текучести сухих порошков в ряде процессов, таких как получение таблеток и капсул, вследствие небольшого размера частиц и большой удельной площади поверхности. Неограничивающие примеры агентов, способствующих скольжению, включают тальк, в частности высокодисперсный тальк, коллоидный диоксид кремния, глицерилмоностеарат и их комбинации.
[0034] Агенты, способствующие скольжению, если они содержатся в слое лекарственного средства, могут присутствовать в количестве до 30% по массе от общей массы слоя лекарственного средства, предпочтительно от 0,5% до 5% по массе от общей массы пеллеты. Количество агента, способствующего скольжению, если он содержится в подпокровном слое, может составлять до 10% по массе от общей массы подпокровного слоя, предпочтительно от 0,5% до 5% по массе от общей массы пеллеты.
[0035] Примеры рН-независимых полимеров, которые могут содержаться в ER-пеллете согласно настоящему изобретению, включают, но не ограничиваются ими, этилцеллюлозу, Сурелиз (Surelease®), сополимеры сложных эфиров акриловой и метакриловой кислот, такие как Эудрагит RL (Eudragit® RL) (поли(этилакрилат, метилметакрилат, хлорид триметиламмонийэтилметакрилата), 1:2:0,2), Эудрагит RS (Eudragit® RS) (поли(этилакрилат, метилметакрилат, хлорид триметиламмонийэтилметакрилата), 1:2:0,1), Эудрагит NE (Eudragit® NE) (поли(этилакрилат, метилметакрилат), 2:1) и их комбинации. рН-независимый полимер может содержаться в количестве от 10% до 50%, предпочтительно от 10% до 30% по массе от общей массы пеллеты.
[0036] Примеры рН-зависимых полимеров кишечнорастворимого покрытия, которые могут содержаться в ER-пеллете согласно настоящему изобретению, включают без ограничений Эудрагит S (Eudragit® S) (поли(метакриловая кислота, метилметакрилат), 1:2), Эудрагит L 55 (Eudragit® L 55) (поли(метакриловая кислота, этилакрилат), 1:1), Колликоат (Kollicoat®) (графт сополимер полиэтиленгликоля с поливиниловым спиртом), 1:1), фталат гидроксипропилметилцеллюлозы (ФГПМЦ), альгинаты, карбоксиметилцеллюлозу и их комбинации. рН-зависимый полимер кишечнорастворимого покрытия может содержаться в количестве от 10% до 50%, предпочтительно от 10% до 30% по массе от общей массы пеллеты.
[0037] Термин «порообразующий агент», используемый в настоящем описании, относится к веществу, которое растворяется в среде организма и, таким образом, образует в матрице открытые поры, что увеличивает скорость диффузии активного агента через слой покрытия. Размер получаемых пор до некоторой степени можно контролировать при помощи размера используемого твердого дисперсного материала. Для однородности пор дисперсный материал можно просеивать через сита со все более мелким размером ячеек с получением частиц, имеющих размер, находящийся в желаемом диапазоне. Порообразующий агент, который может содержаться в ER-пеллетах согласно настоящему изобретению, представляет собой неорганическое или органическое вещество, включая, например, поливинилпирролидон (ПВП), полиэтиленгликоль (ПЭГ), ГПМЦ, ГПЦ, метилцеллюлозу, 1,2-пропиленгликоль, лактозу, сахарозу, тальк, в частности высокодисперсный тальк, и их комбинации. Порообразующий агент может содержаться в количестве от 0,1% до 20%, предпочтительно от 0,1% до 10% по массе от общей массы пеллеты.
[0038] Термин «гидрофильный полимер-модулятор высвобождения», используемый в настоящем описании, относится к водорастворимому полимеру, контролирующему высвобождением активного агента. Тем не менее, в конкретных вариантах реализации гидрофильный полимер-модулятор высвобождения, содержащийся в слое ER-покрытия ER-пеллеты согласно настоящему изобретению, фактически выступает в качестве порообразующего агента. Примеры гидрофильных полимеров-модуляторов высвобождения включают, но не ограничиваются ими, ПВП, ПЭГ, ГПМЦ, ГПЦ и их комбинации. Гидрофильный полимер-модулятор высвобождения может содержаться в количестве от 0,1% до 20%, предпочтительно от 0,1% до 10% по массе от общей массы пеллеты.
[0039] Термин «пластификатор», используемый в настоящем описании, включает любые соединения или комбинации соединений, способные придавать пластичность или размягчать полимер, используемый в ER-пеллете согласно настоящему изобретению. При получении слоя ER-покрытия пластификатор может уменьшать температуру плавления или температуру стеклования (температуру размягчения) используемого полимера или комбинации полимеров; может расширять диапазон средней молекулярной массы указанного полимера или комбинации полимеров и может дополнительно уменьшать вязкость указанного полимера или комбинации полимеров для более удобной обработки раствора покрытия. Неограничивающие примеры пластификаторов включают дибутилсебакат, дибутилфталат, сложные эфиры лимонной кислоты, такие как триэтилцитрат и триацетин; пропиленгликоль; низкомолекулярные поли(алкиленоксиды), такие как ПЭГ, поли(пропиленгликоли) и поли(этилен-/пропиленгликоли); и их комбинации. Пластификаторы могут содержаться в количестве от 0,1% до 20%, предпочтительно от 0,1% до 10% по массе от общей массы пеллеты.
[0040] ER-пеллета согласно настоящему изобретению может дополнительно содержать неактивные ингредиенты, такие как регулятор осмотического давления/тоничности. Указанные агенты традиционно используют для регулируемого по времени распадания, если требуется пульсирующая доставка лекарственного средства. Примеры подходящих вспомогательных веществ, регулирующих осмотическое давление/тоничность, которые можно применять для получения ER-пеллет, включают, но не ограничиваются ими, хлорид натрия и маннит. Регулятор осмотического давления/тоничности, если он содержится в ER-пеллете, может присутствовать в количестве до 20%, предпочтительно от 0,5% до 10% по массе от общей массы пеллеты.
[0041] В конкретном варианте реализации, предложенном в настоящем описании, ER-пеллеты, предложенные в настоящем описании, содержат инертное ядро пеллеты; слой лекарственного средства, содержащий активный агент в смеси с ПВП, используемым в качестве пленкообразующего полимера/связывающего агента, и высокодисперным тальком, используемым в качестве агента, способствующего скольжению; и слой ER-покрытия, содержащий этилцеллюлозу в качестве рН-независимого полимера и ПЭГ в качестве порообразующего агента, причем количество указанного пленкообразующего полимера/связывающего агента составляет до 90% по массе от общей массы слоя лекарственного средства или от 0,5% до 20% по массе от общей массы пеллеты; количество указанного агента, способствующего скольжению, составляет до 30% по массе от общей массы слоя лекарственного средства или от 0,1% до 10% по массе от общей массы пеллеты; количество указанного рН-независимого полимера составляет от 50% до 90% по массе от общей массы слоя ER-покрытия или от 10% до 30% по массе от общей массы пеллеты; а количество указанного порообразующего агента составляет от 1% до 20% по массе от общей массы слоя ER-покрытия или от 0,1% до 10% по массе от общей массы пеллеты.
[0042] В других конкретных вариантах реализации, предложенных в настоящем описании, ER-пеллета согласно настоящему изобретению содержит инертное ядро пеллеты; слой лекарственного средства, содержащий указанный активный агент в смеси с ПВП, используемым в качестве пленкообразующего полимера/связывающего агента, и высокодисперным тальком, используемым в качестве агента, способствующего скольжению; изолирующий/защитный подпокровный слой, содержащий ПВП в качестве пленкообразующего полимера; и слой ER-покрытия, содержащий этилцеллюлозу в качестве рН-независимого полимера, ПЭГ в качестве порообразующего агента и высокодисперный тальк в качестве агента, способствующего скольжению, причем количество указанного пленкообразующего полимера/связывающего агента, входящего в состав указанного слоя лекарственного средства составляет до 90% по массе от общей массы слоя лекарственного средства или от 0,5% до 20% по массе от общей массы пеллеты; количество указанного агента, способствующего скольжению, входящего в состав указанного слоя лекарственного средства, составляет до 30% по массе от общей массы слоя лекарственного средства или от 0,1% до 10% по массе от общей массы пеллеты; количество указанного пленкообразующего полимера, входящего в состав указанного подпокровного слоя, составляет до 100% по массе от общей массы подпокровного слоя или от 0,5% до 20% по массе от общей массы пеллеты; количество указанного рН-независимого полимера составляет от 50% до 90% по массе от общей массы слоя ER-покрытия или от 10% до 30% по массе от общей массы пеллеты; количество указанного порообразующего агента составляет от 1% до 20% по массе от общей массы слоя ER-покрытия или от 0,1% до 10% по массе от общей массы пеллеты; а количество указанного агента, способствующего скольжению, входящего в состав указанного слоя ER-покрытия, составляет от 0,1% до 20% по массе от общей массы слоя ER-покрытия или от 0,1% до 10% по массе от общей массы пеллеты.
[0043] В конкретных вариантах реализации пеллеты с пролонгированным высвобождением смешивают с одним или более подходящими вспомогательными веществами и либо помещают в капсулы, либо прессуют в таблетки, причем указанные капсулы или таблетки содержат пеллеты с пролонгированным высвобождением, содержащие пеллеты с пролонгированным высвобождением, содержащие разагилин, и пеллеты с пролонгированным высвобождением, содержащие прамипексол, или пеллеты с пролонгированным высвобождением, содержащие разагилин и прамипексол.
[0044] Указанные капсулы или таблетки можно получать с использованием любой подходящей технологии, известной в данной области техники.
[0045] Примеры подходящих вспомогательных веществ, которые можно применять для получения пероральной фармацевтической композиции, включают, но не ограничиваются ими, диоксиды кремния, а также другие агенты, способствующие скольжению, известные в данной области техники, такие как определено выше.
[0046] Наполнители таблеток дополняют объем таблетки или капсулы, что делает целесообразным их получение на практике, а также удобным использование потребителем. За счет увеличения общего объема наполнители обеспечивают объем конечного продукта, подходящий для использования пациентом. Хороший наполнитель должен быть инертным, совместимым с другими компонентами состава, негигроскопичным, относительно дешевым, поддающимся уплотнению и предпочтительно безвкусным или имеющим приятный вкус. Растительная целлюлоза (чистые растительные волокна) является популярным наполнителем таблеток или твердых желатиновых капсул. Двухосновный фосфат кальция является другим популярным наполнителем для таблеток. В мягких желатиновых капсулах можно применять разнообразные растительные жиры и масла. Наполнители таблеток включают, например, лактозу, маннит/Parteck®, сорбит, крахмал и их комбинации.
[0047] Разрыхлитель расширяется и растворяется во влажном состоянии, что приводит к распаданию таблетки в пищеварительном тракте и высвобождению активных ингредиентов для их всасывания. Типы разрыхлителей включают вещества, способствующие обратному захвату воды и промоторы распадания таблетки. Эти вещества обеспечивают быстрое разрушение таблетки на более мелкие фрагменты при приведении ее в контакт с водой, что способствует растворению. Неограничивающие примеры разрыхлителей включают перекрестно сшитый поливинилпирролидон (кросповидон), карбоксиметилцеллюлозу натрия/кальция (CMC), кроскармеллозу натрия, гидроксипропилцеллюлозу с низкой степенью замещения, бикарбонат натрия, крахмал, натрия крахмал гликолят и их комбинации.
[0048] Для улучшения определенных технологических характеристик в составы в виде таблетки или капсулы добавляют небольшие количества смазывающих веществ. Более конкретно, указанные агенты предотвращают слипание ингредиентов друг с другом, а также их прилипание к пуансону, используемому для получения таблеток, или к частям машины, наполняющей капсулы. Смазывающие вещества также обеспечивают низкое трение между твердым веществом и стенками формы при получении таблеток и их извлечении из формы. Примеры смазывающих веществ включают без ограничений глицерилбегенат, стеариновую кислоту, тальк, стеарат цинка, стеарат кальция и их комбинации.
[0049] Согласно другому аспекту настоящее изобретение относится к способу лечения болезни Паркинсона, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества фармацевтической композиции для применения для лечения болезни Паркинсона, содержащей фармацевтически приемлемый носитель и комбинацию прамипексола и разагилина с фиксированными их дозами, причем указанная комбинация с фиксированными дозами содержит субтерапевтическую дозу прамипексола и субтерапевтическую дозу разагилина, при этом доза прамипексола ниже или равна дозе разагилина.
[0050] Термины «излечивать», «лечение» и «обеспечивает существенное терапевтическое действие», которые используют взаимозаменяемо в настоящем описании, относятся к прекращению, замедлению, уменьшению степени тяжести или минимизации нейродегенеративного процесса в нигростриарных нейронах (нейрозащитная терапия), устранению или уменьшению биохимического дисбаланса, увеличению синтеза дофамина, стимуляции активности дофаминовых рецепторов и высвобождению дофамина из пресинаптического пространства и/или ингибированию повторного захвата дофамина пресинаптическими рецепторами и катаболизма дофамина. Указанные термины также могут относиться к улучшению или замедлению ухудшения симптомов болезни Паркинсона, таких как тремор, замедленность движений (брадикинезия), синдром беспокойных ног, мышечная ригидность, нарушение осанки и равновесия, расстройство автоматических движений, изменения речи, нарушение сна и/или нарушение качества жизни (QOL), к устранению или у