Применение наноалмазов для генерации свободных радикалов для терапевтических целей при облучении
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к использованию наноалмазов в качестве лекарственных средств, генерирующих свободные радикалы, в частности для лечения опухолей. Изобретение основано на генерации свободных радикалов на поверхности наноалмазов, когда их подвергают облучению, например ионизирующему излучению. Для повышения эффективности наноалмазов можно получать комплексы наноалмазов с радиосенсибилизирующим средством, таким как химическая молекула или интерферирующая РНК, направленная на репарирующий ген. Осуществление изобретения позволяет получить композицию, предназначенную для радиосенсибилизации опухолевых клеток. 2 н. и 26 з.п. ф-лы, 18 ил., 1 табл., 6 пр.
Реферат
Изобретение относится к области лучевой терапии. В частности его целью является применение конкретных наночастиц алмаза (или наноалмазов) для локальной генерации свободных радикалов.
Лучевая терапия представляет собой общепринятый способ лечения злокачественных опухолей, используемый приблизительно в 50% случаев. Он заключается в создании свободных радикалов в клетке путем локального облучения; такие свободные радикалы вызывают разрывы ДНК облученных клеток, приводя к их гибели. В настоящее время эффективность видов лечения на основе лучевой терапии ограничена резистентностью определенных опухолей к ионизирующему облучению по сравнению со здоровыми клетками. Избирательная и эффективная радиосенсибилизация опухолевых клеток позволила бы значительно улучшить эффективность таких видов лечения и снизить побочные эффекты на здоровые ткани.
Для этой цели были описаны различные подходы, такие как использование наночастиц, способных локально генерировать свободные радикалы, или использование радиосенсибилизирующих средств.
Первый подход заключается в локальной генерации свободных радикалов в опухоли с использованием наночастиц. Описанные к настоящему времени способы этого типа основаны на физических свойствах, связанных с наночастицами, позволяющими эффективно генерировать свободнорадикальные частицы на их поверхности при облучении. Используемые наночастицы, как правило, состоят из атомов с большим атомным числом (Z) для более эффективного поглощения рентгеновских лучей, но, как правило, они являются дорогостоящими веществами (золото, платина, редкоземельные элементы) и/или могут вызывать токсичность, и/или являются не очень стабильными в биологической среде. В качестве примера можно упомянуть патентную заявку US 2008/0003183 (Ting Guo), в которой предлагают использовать наночастицы, состоящие из тяжелых элементов, таких как золото, способных локально испускать электроны Оже при облучении. Такую генерацию электронов можно индуцировать с использованием рентгеновских лучей с энергией, которую только слабо поглощают молекулы воды, для генерации свободных радикалов в непосредственной близости к наночастицам. Однако для улучшения коллоидной стабильности и биосовместимости таких наночастиц часто необходимой является прививание молекул, которые могут снижать дозу вторичных электронов или электронов Оже, передаваемых в среду наночастицы, и, таким образом, снижать дозу генерируемых свободных радикалов.
Согласно второму подходу, указанному выше, в настоящее время исследуют новые радиосенсибилизирующие молекулы, целью которых является направленное воздействие на механизмы биологической защиты, специфической для опухолевых клеток (C. Begg et al., 2011). К сожалению, эти молекулы не всегда могут быть доставлены в опухолевые клетки in vivo, что ограничивает их терапевтическое применение. В частности, это является случаем с интерферирующими РНК POLQ, для которых недавно была продемонстрирована высокая избирательность при радиосенсибилизации опухолевых клеток in vitro (Higgins et al., 2010). Использование таких интерферирующих РНК in vivo без средств векторизации может вызывать затруднения, так как их биодоступность является ограниченной.
В настоящее время известны различные биотехнологические применения наноалмазов, такие как векторизация и доставка лекарственных средств и интерферирующих РНК в опухолевые клетки. В этих применениях наноалмазы используют только в качестве пассивных векторов. В качестве примера можно упомянуть патентную заявку US 2010/0305309 (Ho et al.), относящуюся к различным способам доставки лекарственных средств наноалмазами. В этом конкретном случае поверхность наноалмазов, используемых в качестве векторов, является окисленной, что обеспечивает им отрицательный заряд поверхности и вызывает необходимость добавления полимеров для обеспечения векторизации цепей ДНК или РНК, которые также имеют отрицательный заряд. Такие полимеры могут вызывать дополнительную токсичность и значительно увеличивать размер наноалмазов, что может вызывать большее удерживание в органах, таких как печень или почки, при применениях in vivo.
Настоящее изобретение основано на демонстрации авторами изобретения свойств наноалмазов, которые до настоящего времени были неизвестны. В настоящем описании термин "наноалмаз" означает любую наночастицу, в основном состоящую из sp3-гибридизованных атомов углерода, размером менее 250 нм. Эти наночастицы в числе прочего можно синтезировать измельчением синтетического алмаза или посредством детонации. В последнем случае размер наноалмазов, как правило, составляет менее 10 нм. Термин "наноалмаз" также означает агрегаты с размером наночастиц, состоящие из первичных наночастиц алмаза. Авторы изобретения наблюдали, что наноалмазы обладают конкретными физическими свойствами, которые позволяют им эффективно генерировать свободные радикалы при облучении, в частности при ионизирующем облучении. Наноалмазы фактически состоят из атомов углерода в очень большой концентрации (1,8×1023 атомов/см3), что обеспечивает эффективное поглощение излучения по сравнению с окружающими биологическими тканями, несмотря на одинаковый атомный номер. Кроме того, наноалмазы обладают очень хорошей коллоидной стабильностью, даже без функционализации, которая может уменьшать перенос образуемых электронов в их среду. Наконец, прекрасная теплопроводность алмаза обеспечивает очень эффективное высвобождение тепла в результате облучения (например, ионизирующего облучения) на поверхности наноалмазов. Таким образом, наноалмазы обеспечивают эффективную генерацию свободных радикалов в опухолевых клетках и/или тепло, при этом используя вещество на основе углерода, которое не является дорогостоящим, является биосовместимым и стабильным в биологической среде без необходимости функционализации.
Таким образом, настоящее изобретение относится, во-первых, к использованию наноалмаза для генерации свободных радикалов для терапевтических и/или диагностических целей. Согласно одной из конкретных реализаций изобретения продукция тепла связана с продукцией свободных радикалов. Использование наноалмаза в качестве лекарственного средства и/или в качестве диагностического средства, генерирующего свободные радикалы, следует из свойств, продемонстрированных авторами изобретения и описанными выше.
В контексте настоящего изобретения терапевтическое действие наноалмазов обусловлено повреждением, вызываемым непосредственно или опосредованно свободными радикалами, генерируемыми на поверхности наноалмазов, молекул, располагаемых непосредственно вокруг наночастиц и, в частности, менее 10 нм от поверхности наночастиц. В применениях, целью которых является разрушение клетки, таким образом, предпочтительно наночастицы проникают в клетки, для того чтобы свободные радикалы вызывали повреждение нуклеиновых кислот клетки (ядерной ДНК и РНК и/или цитоплазматических РНК, и/или митохондриальной ДНК и т. д.). Для этого наноалмазы, средний диаметр которых составляет менее 100 нм, или даже менее 50 нм, или даже менее 10 нм, являются предпочтительными для осуществления изобретения.
Авторы изобретения наблюдали, что особенно эффективными являются наноалмазы, которые подвергали конкретной обработке поверхности для получения функциональных групп CHx (x=1, 2 или 3) и/или углерода в форме графита на поверхности (например, посредством водородной плазмы, высокотемпературного обжига в вакууме или в атмосфере водорода). В настоящем описании выражение "графитизированный наноалмаз" означает любой наноалмаз, содержащий на поверхности sp2-гибридизованные атомы углерода. Очевидно, что присутствие sp2-гибридизованных атомов углерода на поверхности наноалмаза не исключает присутствия других химических групп на поверхности таких наноалмазов. Аналогично выражение "гидрогенизированный наноалмаз" означает любой наноалмаз, содержащий функциональные группы типа C-H, CH2 или CH3 на поверхности. Когда наноалмазы, поверхность которых (частично или полностью) графитизировали и/или гидрогенизировали, подвергают воздействию воздуха или диспергируют в водной среде, они проявляют свойства проводимости на поверхности, которые обеспечивают им отрицательную электронную аффинность. Вместе с этим их поверхность становится благоприятной для предпочтительной адсорбции молекул, которые являются предшественниками свободных радикалов в биологической среде (в основном H2O, O2 и NO2), таким образом обеспечивая перенос электронов от наноалмаза к этим молекулам, которые возникают спонтанно. Под действием ионизирующего облучения такой перенос электронов увеличивается и особенно эффективно порождает свободные радикалы. Кроме того, предпочтительная адсорбция молекул, таких как H2O, O2 и NO2 на поверхности таких модифицированных наноалмазов, в результате введения этих молекул в клетки обеспечивает решение проблемы одной из основных причин радиорезистентности опухолевых клеток, которая заключается в отсутствии кислорода в этих клетках (гипоксия), ограничении образования содержащих кислород свободных радикалов.
Кроме того, наноалмазы, содержащие функциональные группы CHx и/или углерод в форме графита на поверхности, обладают очень высокой диэлектрической проницаемостью, что обеспечивает возможность их использования в качестве источника тепла под действием электромагнитного поля, колеблющегося с частотой от 100 до 106 Гц (Batsanov et al., 2012). Эти наноалмазы также обладают свойствами поглощения инфракрасного излучения, как другие наноматериалы на основе углерода, которые также индуцируют выделение тепла (Yang et al., 2010). Для получения продукции тепла наноалмазами предпочтительно используют инфракрасное излечение с длиной волны от 600 до 1400 нм, где этот диапазон соответствует инфракрасному излучению, поглощаемому биологическими тканями. Таким образом, свойства генерировать свободные радикалы могут быть связаны с гипертермией.
Таким образом, согласно одной из предпочтительных реализаций настоящее изобретение относится к наноалмазу, поверхность которого по меньшей мере частично графитизировали и/или гидрогенизировали, для использования для генерации свободных радикалов для терапевтических и/или диагностических целей, необязательно связанных с теплом. В частности, настоящее изобретение относится к наноалмазу для использования в сочетании с облучением в качестве лекарственного средства и/или в качестве диагностического средства, генерирующего свободные радикалы.
В числе излучений, способных вызывать образование свободных радикалов на поверхности частиц наноалмазов, можно упомянуть ионизирующее излучение, в числе которых электромагнитные волны, такие как рентгеновские лучи, гамма-лучи и ультрафиолетовые лучи, а также корпускулярное излучение, в частности излучение, состоящее из протонов, адронов или бета-частиц (β+ или β-). Таким образом, согласно одному из предпочтительных вариантов осуществления настоящее изобретение относится к наноалмазу, такому как описанные выше наноалмазы, для использования в сочетании с ионизирующим облучением, в качестве лекарственного средства и/или в качестве диагностического средства.
Специалисты в данной области адаптируют параметры применяемого облучения (природу, энергию, силу и время облучения) в зависимости от глубины ткани, которой необходимо достигнуть, и от других клинических и технических параметров. Только в качестве обозначения некоторые значения приведены в таблице 1 ниже.
Однако можно использовать другие виды облучения вместо указанных выше видов облучения или в сочетании с ними. Среди этих видов облучения различной природы можно упомянуть видимое, инфракрасное, микроволновое или нейтронное излучение, в частности для получения продукции тепла. Виды облучения могут быть множественными как в отношении природы используемого излучения, так и в отношении применения нескольких периодов времени облучения.
| Таблица 1 | ||||
| Природа излучения | Энергия | Время | Проникновение | Органы |
| УФ | 3-120 эВ | несколько минут | поверхностное | Кожа и полости (пример: мочевой пузырь) |
| Рентгеновские лучи | от 20 до 150 кэВ | несколько минут | несколько миллиметров | Кожа и полости (пример: мочевой пузырь) |
| Рентгеновские лучи (ортовольтажное) | от 200 до 500 кэВ | несколько минут | до 6 см | Поверхностные органы, мышцы |
| Рентгеновские лучи (мегавольтажные) | от 1000 кэВ до 25000 кэВ | несколько минут | весь организм | Глубокие органы (пример: предстательная железа) |
Согласно одной из конкретных реализаций изобретения по меньшей мере некоторые из генерируемых свободных радикалов представляют собой содержащие кислород свободные радикалы. Авторы изобретения также продемонстрировали, что азот может адсорбироваться на поверхности наноалмазов. Таким образом, согласно одной из конкретных реализаций изобретения по меньшей мере некоторые из генерируемых свободных радикалов представляют собой содержащие азот свободные радикалы.
Вследствие того, что свободные радикалы вызывают повреждения ДНК, описанные выше наноалмазы находят полезное применение при разрушении клеток-мишени, таких как злокачественные клетки. Таким образом, согласно одному из предпочтительных вариантов осуществления настоящее изобретение относится к использованию наноалмаза, как описано выше, для лечения солидной опухоли, где указанное использование основано на природном свойстве наноалмаза генерировать свободные радикалы при облучении.
Согласно одной из конкретных реализаций изобретения частицы наноалмаза являются функционализованными. В частности, наноалмаз по изобретению может быть связан с молекулой, обеспечивающей направленную доставку, ковалентной или нековалентной связью. В известном уровне техники было описано несколько способов прививания молекул на поверхность наноалмазов, и специалисты в данной области могут выбирать, в частности, в зависимости от типа молекулы, обеспечивающей направленную доставку, способ, который является наиболее подходящим. В качестве неограничивающих примеров способов приведения молекул, обеспечивающих направленную доставку, к поверхности наноалмазов можно привести:
- связывание пептида путем образования амидной или сложноэфирной функциональной группы между наноалмазом и молекулой, обеспечивающей направленную доставку (Huang and Chang, 2004),
- прямое связывание молекулы, обеспечивающей направленную доставку, с наноалмазом посредством создания связи C-C между двумя соединениями (Girard et al., 2011),
- связывание по типу циклоприсоединения с использованием присутствия атомов углерода в состоянии sp2- или sp-гибридизации на наноалмазе и/или на молекуле, обеспечивающей направленную доставку (Jarre et al., 2011),
- связывание по типу силанизации за счет присутствия силановых функциональных групп на поверхности наноалмаза и/или на молекуле, обеспечивающей направленную доставку (Krüger et al., 2006),
- нековалентное связывание на основе электростатического взаимодействия и/или образования водородных связей между наноалмазом и молекулой, обеспечивающей направленную доставку (Chen et al., 2010).
Эти типы связывания можно проводить непосредственно на поверхности наноалмазов или посредством молекул, предварительно привитых или адсорбированных на поверхности наноалмазов. Для гидрогенизированных наноалмазов наиболее эффективным является прямое связывание путем создания связи C-C. Для графитизированных наноалмазов наиболее подходящим является связывание путем циклоприсоединения.
Согласно одному из предпочтительных вариантов осуществления наноалмазов, используемых для направленной доставки, по изобретению направленная доставка обеспечивается по меньшей мере одним биологическим лигандом, распознаваемым рецептором, сверхэкспрессированным на поверхности определенных клеток. Биологические лиганды, обеспечивающие возможность специфической направленной доставки в определенные клетки, могут представлять собой:
- пептиды, например пептид RGD, или их производные, или их аналоги (например, пептид - аналог соматостатина октреотат, аналог бомбезина, аналог нейротензина, EGF, VIP и т. д.),
- белки, антитела или их производные, или их аналоги,
- сахара, в частности моносахариды (например, глюкозу, галактозу, глюкозамин или галактозамин), олигосахариды, полисахариды или их производные или их аналоги,
- олигонуклеотиды, ДНК, РНК или их производные, или их аналоги,
- органические молекулы (такие, как фолат или бисфосфонат памидронат),
- органометаллические комплексы.
Их активность направленной доставки обусловлена молекулярным распознаванием этих лигандов рецепторами, сверхэкспрессированными на поверхности клеток, в представляющей интерес области.
Лиганды, которые являются особенно предпочтительными для осуществления изобретения, представляют собой молекулы лигандов, которые часто являются сверхэкспрессированными на поверхности опухолевых клеток. Например, преимущественно можно использовать пептиды, содержащие мотив RGD, такие как цикло(RGDfK), цикло(RGDyK) или цикло(RGDfV). Эти пептиды распознают интегрин aγβ3, который сверхэкспрессирован на поверхности опухолевых клеток и эндотелиальных клеток во время неоангиогенеза опухоли. Таким образом, использование этих лигандов в наноалмазах по изобретению обеспечивает направленную доставку в опухоли и в участки их васкуляризации с целью их уничтожения посредством образования свободных радикалов, необязательно связанной с образованием тепла. Другой предпочтительный лиганд, например, представляет собой пептид, содержащий мотив NGR, описанный Curnis et al. (2002), который также направленно воздействует на новообразованные сосуды.
Очевидно, что другие молекулы можно прививать на поверхность наноалмазов, используемых в контексте настоящего изобретения, например, для увеличения их стабильности в биологической среде или для их мечения (флуорофор, радиоактивная метка и т. д.) (фигура 17).
Преимущественно за наноалмазами по настоящему изобретению можно наблюдать способами визуализации с использованием характерной люминесценции окрашенных центров в наноалмазах (центров N-V или т. п.) (Chang et al., 2008). Также можно использовать способы спектроскопии, в частности романовскую спектроскопию (Chao et al., 2007). Таким образом, практикующий врач может подтверждать наличие наноалмазов в области-мишени, например, в солидной опухоли, перед тем как подвергать эту область облучению, которое приведет к генерации свободных радикалов. Это обеспечивает дополнительное снижение побочных эффектов лечения.
Как указано выше, наноалмазы известны благодаря их способности векторизовать молекулы. Согласно одному конкретному варианту осуществления в настоящем изобретении предлагают использовать наноалмазы как из-за их свойств векторизации (пассивная функция), так и из-за их свойств генерации свободных радикалов при облучении (активная функция). Принцип функционирования этого аспекта изобретения продемонстрирован на фигуре 18. Сочетание свойств векторизации наноалмазов с их свойствами генерации свободных радикалов является особенно эффективным в отношении мультимодальных комплексов наноалмаз/радиосенсибилизирующее средство. Это обусловлено тем, что радиосенсибилизирующие средства обеспечивают избирательный ответ, оказывая действие на биологические пути, специфические для опухолевых клеток, тогда как наноалмазы увеличивают количество генерируемых свободных радикалов. Комбинация этих двух компонентов позволяет значительно увеличивать эффективность и избиртаельность по сравнению с отдельным использованием наночастиц или радиосенсибилизирующих молекул: с одной стороны, использование наноалмазов позволяет транспортировать радиосенсибилизирующие средства в опухолевые клетки направленным образом и постепенно высвобождать их в этих клетках таким образом, что улучшается биодоступность радиосенсибилизирующих средств, и с другой стороны, радиосенсибилизирующие средства инактивируют защитные механизмы опухолевых клеток, и, таким образом, генерируемые наноалмазами радикалы будут вызывать больше разрывов ДНК в опухолевых клетках. Такое сочетание позволяет априори увеличивать концентрации радиосенсибилизирующих средств, доставляемых в опухолевые клетки, и снижать дозу облучения, необходимого для элиминации этих клеток.
Согласно этому подходу настоящее изобретение относится к композиции, содержащей наноалмаз, как описано выше, необязательно функционализированный молекулой, обеспечивающей направленную доставку, а также радиосенсибилизирующей молекулой. Такая радиосенсибилизирующая молекула может быть связана с указанным наноалмазом ковалентной связью или являться просто адсорбированной на его поверхности.
Были описаны различные типы радиосенсибилизирующих молекул, также называемые "радиосенсибилизирующие средства", и их можно использовать для осуществления настоящего изобретения. В частности, в этом отношении можно упомянуть радиосенсибилизирующие средства химического типа, неполный список которых включает мисонидазол, метронидазол, этанидазол, пимонидазол, фенилпропаноиды и монойодуксусную кислоту. Эти молекулы можно ковалентно связывать с наноалмазами необязательно посредством плеча, которое является расщепляемым в клеточной среде, обеспечивая высвобождение этих молекул после интернализации наноалмаза. В качестве примера расщепляемого плеча можно привести полимер PEG/полилизин, плечо на основе пептида, расщепляемое ферментом, сверхэкспрессированным в типе опухоли-мишени (например, MMP2 или катепсином D), или еще плечо, содержащее дисульфидный мостик, который будет расщепляться тиоредоксинами в лизосомах и эндосомах клеток. Альтернативно химическое радиосенсибилизирующее средство может быть связано с наноалмазом посредством слабых связей (электростатической адсорбции, которая является прямым или опосредованным полимером с зарядом).
Как указано выше, новое направление исследования в области радиосенсибилизации относится к использованию нуклеиновых кислот, способных модулировать экспрессию определенных белков, участвующих в репарации ДНК. Таким образом, настоящее изобретение также относится к композиции, содержащей наноалмаз, как описано выше, и к радиосенсибилизирующей молекуле, состоящей из молекулы нуклеиновой кислоты, адсорбированной на поверхности наноалмаза. Нуклеиновые кислоты, которые являются предпочтительными для реализации этого аспекта изобретения, представляют собой интерферирующие РНК, способные ингибировать экспрессию гена, ответственного за репарацию ДНК, как, например, интерферирующая РНК, которая ингибирует экспрессию гена POLQ.
Очевидно, что композиции по изобретению преимущественно будут использовать в сочетании с облучением, в частности в качестве лекарственного средства против злокачественной опухоли, и предпочтительно в таких условиях, что облучение индуцирует на поверхности наноалмазов продукцию свободных радикалов и/или тепла. Термин "в сочетании" означает, что желаемое действие получают, когда представляющие интерес клетки, ткани или органы, в которые частично ввели наночастицы по изобретению, возбуждают облучением. Тем не менее, необязательно, чтобы частицы и лучи вводили одновременно или согласно одному и тому же протоколу.
Другая конкретная цель изобретения относится к способу индукции или вызывания лизиса, или разрушения злокачественных клеток in vitro, ex vivo или in vivo, который включает приведение злокачественных клеток в контакт с одним или несколькими наноалмазами или композициями, как описано ранее, в течение периода времени, достаточного для обеспечения их проникновения в злокачественные клетки и при необходимости для обеспечения высвобождения радиосенсибилизирующих средств, а затем воздействие на клетки лучами, как определено выше, где указанное воздействие индуцирует образование свободных радикалов и/или тепла на поверхности наноалмазов и вызывает лизис или гибель указанных клеток. При необходимости промежуточный этап детекции наноалмазов, например романовской спектроскопией, проводят перед этапом воздействия лучами для контроля расположения наноалмазов.
Изобретение также относится к способу лечения злокачественной опухоли, включающей введение пациенту, страдающему злокачественной опухолью, композиции, содержащей наноалмазы, как определено ранее, предпочтительно функционализированных молекулой, обеспечивающей направленную доставку, в условиях, позволяющих наноалмазам или агрегатам в форме наночастиц проникать в злокачественные клетки, и последующее лечение пациента в присутствии источника возбуждения, например, выбранного из рентгеновских лучей, гамма-лучей, УФ-лучей, протонов и адронов, приводящих к модификации, разрушению или нарушению функций злокачественных клеток у пациента, таким образом обеспечивая лечение злокачественной опухоли.
В настоящем описании термин "лечение" означает любое улучшение клинических признаков, в частности таких, как уменьшение размера или развитие опухоли или площади патологической ткани, подавление или разрушение патологических клеток или тканей, замедление прогрессирования патологического состояния, уменьшение образования метастазов, регрессия или полная ремиссия и т. д. Наноалмазы и композиции по изобретению также можно использовать in vitro или ex vivo.
Изобретение является пригодным для лечения любого типа злокачественной опухоли, в частности метастазировавших или неметастазировавших солидных опухолей, например, выбранных из злокачественных опухолей легкого, печени, почки, мочевого пузыря, молочной железы, головы и шеи, головного мозга, яичника, предстательной железы, кожи, желудочно-кишечного тракта, толстой кишки и т. д. Лучи можно применять в любой момент времени после введения частиц один или несколько раз с использованием любой системы лучевой терапии или радиографии, доступной в настоящее время. Наноалмазы и композиции по изобретению можно вводить различными путями, предпочтительно посредством системной, или местной инъекции, или перорально. При необходимости могут быть предусмотрены повторные инъекции или введения.
Следующие ниже примеры и прилагаемые чертежи иллюстрируют изобретение, однако не ограничивая его объем.
Условные обозначения к чертежам
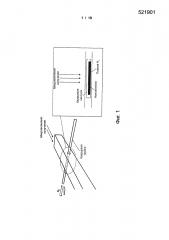
Фигура 1: Схема подготовки гидрирования наноалмазов (ND) водородной (H2) плазмой при воздействии микроволнового излучения.
Фигура 2: Снимки трансмиссионной электронной микроскопии высокого разрешения (HRTEM) исходных ND (a) и ND через 1 час (b) и 8 часов (c) обжига в вакууме при 750ºC. Плоскости алмаза (111) и плоскости графита (001) обозначены белыми и серыми линиями соответственно. Реконструкции поверхностей графита обозначены белыми стрелками. Линейный масштаб составляет 5 нм.
Фигура 3: Спектры фотоэлектронной рентгеновской спектроскопии (XPS) уровня ядра углерода (C1s) исходных ND (ND-исходный) и ND через 1 час (ND-1 час), 5 часов (ND-5 часов) и 8 часов (ND-8 часов) обжига в вакууме при 750ºC.
Фигура 4: Изменение дзета-потенциала ND-1 часа, ND-5 часов, ND-8 часов и гидрогенизированных ND (ND-H) в ультрачистой воде в зависимости от pH.
Фигура 5: Распределение размера белков среды DMEM+10% эмбриональная телячья сыворотка (ЭТС) (черный) и ND-5 часов в деионизованной воде (синий) и в MEM сразу после добавления (зеленый) и через 5 часов (красный). Измерения проводят при 37ºC.
Фигура 6: Снимки HRTEM наноалмазов, поверхность которых является гидрогенизированной (a) и графитизированной (b). На плоскости выделены плоскости (111) алмаза и графитовые перестройки поверхности указаны белыми стрелками. Линейный масштаб составляет 5 нм.
Фигура 7: Спектры XPS уровня ядра углерода (C1s) гидрогенизированных наноалмазов после диспергирования в воде (a) и через 1 час обжига в вакууме при 400ºC (b).
Фигура 8: Спектры инфракрасной спектроскопии с преобразованием Фурье исходных ND (ND-исходный) и ND-G через 1 час (ND-1 час) и 8 часов (ND-8 часов) обжига в вакууме.
Фигура 9: Клеточный ответ линии Caki-1 после экспозиции ND-COOH без облучения.
Фигура 10: Клеточный ответ линии Caki-1 после экспозиции ND-COOH после облучения 4 Гр.
Фигура 11: Клеточный ответ линии Caki-1 после экспозиции ND-H без облучения.
Фигура 12: Клеточный ответ линии Caki-1 после экспозиции ND-H после облучения 4 Гр.
Фигура 13: Оценка клеток Caki-1 после экспозиции ND-COOH и ND-H без облучения.
Фигура 14: Оценка клеток Caki-1 после экспозиции ND-COOH и ND-H после облучения 4 Гр.
Фигура 15: Окислительный стресс, индуцируемый ND-H при облучении или без него. Контроль без зонда иллюстрирует фоновое значение люминесценции, которая не связана со свободными радикалами. Другой контроль подвергали экспозиции флуоресцентным зондом, но не ND-H. Серые столбики отражают интенсивность окислительного стресса в необлученных клетках, и белые столбики отражают интенсивность окислительного стресса в клетках, подвергнутых облучению 4 Гр через один час после облучения.
Фигура 16: Интернализация зонда нуклеиновой кислоты пептида, меченного флуорофором Cy3 (ANP-Cy3), адсорбируемого на поверхности ND-H. Наблюдения проводили через 24 часа (A) или 72 часа (B) после инкубации клеток Caki в присутствии смеси ND-H/ANP-Cy3. Ядра клеток метили бисбензимидом Hoechst 33342.
Фигура 17: Комплекс наночастица алмаза/радиосенсибилизирующее средство.
Фигура 18: Принцип функционирования: a) введение комплекса наноалмаз (NP)/радиосенсибилизирующее средство в клетку; b) выделение радиосенсибилизирующих средств и ингибирование защитных механизмов клетки: c) генерация электронов и образование свободных радикалов при облучении.
ПРИМЕРЫ
Пример 1: Получение наноалмазов (ND) с графитовыми перестройками поверхности или гидрогенизированными функциональными группами на поверхности
ND, обладающие свойствами, пригодными для радиосенсибилизации опухолевых клеток, модифицировали с использованием конкретных видов обработки, обеспечивающих образование графитовых перестроек (графитизация) или гидрогенизированных функциональных групп типа CHx с x=1, 2 или 3 (гидрирование). В контексте настоящего изобретения также можно использовать ND, содержащие комбинацию этих двух типов концевых групп поверхности. Описанные ниже способы представляют собой способы, используемые авторами изобретения для гидрирования (водородной плазмой при микроволновом облучении) и графитизации (обжигом в вакууме при высокой температуре или при воздействии микроволнами в вакууме гидрогенизированных ND), но эти конкретные концевые группы поверхности также можно априори получать другими способами. Следует отметить, что указанные условия следует адаптировать в зависимости от химии исходной поверхности ND, которые могут изменяться у различных поставщиков. Виды обработки, описываемые в настоящем описании, оптимизируют для детонации ND, получаемых Nanocarbon Institute в Японии (профессор Eiji Osawa).
1.1. Гидрирование водородной плазмой при микроволновом облучении
1.1.1. Способ
Способ, используемый для обеспечения гидрогенизированных концевых групп на ND, описан в ссылке Girard et al., 2010. ND (приблизительно 50-100 мг) вводят сухим способом в кварцевый картридж или непосредственно в кварцевую трубку, которую вставляют перпендикулярно в волновод, соединенный с 2,45 ГГц микроволновым генератором (Sairem), как представлено на фигуре 1. Волновод охлаждают водой и трубку охлаждают сжатым воздухом. Эта трубка соединена с устройством для первичной подачи насосом и для подачи газообразных водорода высокой степени чистоты N9,0 и аргона.
Сначала проводили серию первичных чисток посредством первичной подачи насосом в трубку (давление <0,1 мбар) и восстановление давления водородом высокой степени чистоты, затем вводили водород высокой степени чистоты до тех пор, пока стабилизированное давление не достигало 12 мбар. Такое давление также поддерживали на всем протяжении процесса гидрирования посредством изоляции трубы (статический режим) или поддерживали посредством комбинации непрерывного потока водорода и клапана регуляции давления согласно инструкции (динамический режим). Для индукции образования плазмы в трубке используют мощность микроволнового излучения 300 Вт. Геометрию микроволнового излучения в волноводе регулируют таким образом, чтобы получать максимальную мощность, поглощаемую плазмой, и отраженную мощность, равную нулю, на уровне генератора. Трубку периодически поворачивают и перемещают в ручном режиме для обеспечения того, чтобы большинство ND подвергались действию плазмы. Обычное время экспозиции составляет 20-30 минут. Для получения полного гидрирования важно проводить чистку через 5 минут обработки для удаления окисленных частиц, выделяющихся с поверхности ND; после прекращения микроволнового излучения трубку подвергали откачке в начальном вакууме, а затем в трубку повторно вводили чистый водород, чтобы вновь инициировать образование плазмы. Такая промежуточная чистка не является необходимой в случае гидрирования при динамическом потоке водорода. В конце обработки трубку охлаждают под водородом до тех пор, пока она не достигает температуры окружающей среды, а затем откачивают насосом остаточный газ. Трубку снова помещают в условия давления окружающей среды введением аргона, затем можно выделять ND.
1.1.2. Характеризация
Были опубликованы подробные характеристики свойств поверхности получаемых таким образом гидрогенизированных ND (Girard et al., 2010; Girard et al., 2011; Arnault et al., 2011). В них изучали химию поверхности электронной спектроскопией (XPS), инфракрасной спектроскопией (FTIR) и романовской спектроскопией. Кроме того, на такие гидрогенизированные наноалмазы наносили три привитых соединения, селективность которых известна; демонстрировали эквивалентную селективность по отношению к наличию гидрогенизированных концевых групп наноалмазов. В частности, это демонстрирует, что такие ND обладают свойствами отрицательной электронной аффинности (Girard et al., 2011). Эти свойства обуславливают их применение для генерации свободных радикалов в воде (см. пример 2).
1.2. Графитизация гидрогенизированных ND воздействием микроволнового излучения
ND, гидрогенизированные описанным выше способом, можно графитизировать после их гидрирования in situ путем простого повторного воздействия микроволновым излучением в начальном вакууме. Это обусловлено тем, что авторы изобретения наблюдали, что гидрогенизированные ND обладают способностью поглощать микроволновое излучение в вакууме. Таким образом, при регуляции геометрии микроволнового резонатора большая часть микроволной мощности (авторы изобретения использовали 300 Вт для 100 мг ND) поглощается ND и преобразуется в тепло. Воздействие в течение нескольких секунд является достаточным для обеспечения очень быстрого повышения температуры ND, индуцирующей образование графитовых перестроек на поверхности, как происходит в общепринятом способе графитизации посредством высокотемпературного обжига (см. ниже). С другой стороны, воздействие в течение более чем одной минуты приводит к образованию полностью графитных наночастиц, в которых полностью исчезает алмазное ядро. Этот способ может являться ал