Способ продуцирования с2-оксигенатов путем ферментации с использованием серы с высокой степенью окисления
Иллюстрации
Показать всеИзобретение относится к области биохимии. Предложен способ продуцирования С2-оксигенатов путем анаэробной ферментации с использованием микробной культуры карбоксидотрофного микроорганизма. Способ включает получение серной добавки, контактирование микробной культуры микроорганизма с содержащим монооксид углерода субстратом, поддерживание микробной культуры при рН менее 5,3 в водной сбраживаемой среде, содержащей серную добавку, и выделение одного или более С2-оксигенатов из водной сбраживаемой среды. Причем серная добавка содержит способствующее в водной сбраживаемой среде образованию оксоанионов серы неорганическое соединение серы S(II)-S(IV). Изобретение обеспечивает достижение в зоне ферментации высоких титров этанола, а также необязательное присутствие цистеина в зоне ферментации. 15 з.п. ф-лы, 22 ил., 6 табл., 12 пр.
Реферат
Область, к которой относится изобретение
Изобретение относится к способу продуцирования этанола и/или ацетата из субстратов монооксида углерода и/или диоксида углерода и водорода посредством анаэробной ферментации с использованием карбоксидотрофных микроорганизмов. Более конкретно изобретение относится к использованию специфических источников неорганической сферы для обеспечения потребности микроорганизмов в биологическом соединении серы с применением способа, который является экономически более эффективным и предпочтительным для такого продуцирования этанола и ацетата.
Предшествующий уровень техники
Производство биотоплива для его использования в качестве жидкого моторного топлива или для смешивания со стандартным бензином или с дизельным моторным топливом находит все большее применение во всем мире. Таким биотопливом является, например, этанол и н-бутанол. Одним из главных стимулов для производства биотоплива является то, что оно может быть получено из возобновляемых ресурсов методами ферментации и биотехнологии. Обычно биотопливо получают из легко поддающихся ферментации углеводов, таких как сахара и крахмалы. Поскольку такие сырьевые источники конкурируют с источниками получения пищевых продуктов для человека, то в последнее время, основное внимание ученых было направлено на альтернативные источники для получения биотоплива и других химических соединений.
Одним из альтернативных источников питания микроорганизмов является лигноцеллюлозные сырьевые продукты, такие как остатки при рубке леса, деревья лесных насаждений, солома, трава и другие отходы сельскохозяйственного производства. Однако в высокой степени гетерогенная природа лигноцеллюлозных материалов, которые служат в качестве механического каркаса структуры растений и деревьев, делает их, по существу, не поддающимися биоконверсии. Кроме того, эти материалы содержат преимущественно отдельные компоненты трех классов, которые служат в качестве структурных элементов, такие как целлюлоза (сахарные С6-полимеры), гемицеллюлоза (различные сахарные C5- и C6-полимеры) и лигнин (ароматические гетерополимеры и гетерополимеры, связанные эфирными связями). Затем, с применением других хорошо известных методов такая лигноцеллюлозная сырьевая биомасса может быть впоследствии превращена в синтез-газ (также известный как синтетический газ, состоящий, главным образом, из смеси CO, H2 и CО2 с другими компонентами, такими как CH4, N2, NH3, H2S, и другими газами в следовых количествах). Впоследствии такой синтез-газ подвергают ферментации с использованием анаэробных микроорганизмов, в результате чего получают биотопливо, такое как этанол, н-бутанол или другие химические соединения, такие как уксусная кислота, масляная кислота и т.п. В патенте США 7285402, описание которого вводится в настоящее описание посредством ссылки, описаны методы превращения монооксида углерода, диоксида углерода и водорода в уксусную кислоту и этанол путем ферментации с использованием анаэробных бактерий.
Для анаэробной ферментации, осуществляемой в целях получения биотоплива и других химических соединений, могут быть использованы любые газообразные субстраты, которые продуцируют монооксид углерода, диоксид углерода и водород из различных источников. Так, например, в публикации заявки на патент США 2011/0300593 описаны источники, такие как отходящий газ, образующийся из отходов сталеплавильного производства, а именно источник монооксида углерода, и содержание этой публикации вводится в настоящее описание посредством ссылки. Могут быть также использованы и многие другие источники субстратов. Так, например, синтез-газ может быть получен из множества других углеродных источников, таких как природный газ; газ, полученный путем перегонки; торфяной газ; газ, полученный из нефтяного кокса, угля, твердых отходов и органических отходов.
Этанол может быть продуцирован из CO, CО2 и H2 с использованием различных анаэробных бактерий, в частности бактерий, принадлежащих к роду Clostridium. Так, например, в литературе описаны различные штаммы бактерий, которые продуцируют этанол из газов, и такими бактериями являются Clostridium ljungdahlii, Clostridium autoethanogenum и Clostridium coskatii, которые также описаны в настоящей заявке.
Продуцирование этанола и других продуктов анаэробными микроорганизмами зависит от многих рабочих условий в зоне ферментации (см. патенты США NN 5173429, 5593886 и 6368819, WO 98/00558 и WO 02/08438). Два главных условия, влияющих на продуктивность микроорганизмов, являются pH и окислительно-восстановительный потенциал (ОВП) зоны ферментации. В WO 2009/022925 описано влияние pH и ОВП на превращение газообразных субстратов в продукты.
Микроорганизмам, участвующим в процессах метаболизма, необходимы питательные элементы и микроэлементы, и соответствующая подача конкретных питательных элементов может оказывать большое влияние на рост и жизнеспособность микроорганизмов. Фактически эти питательные вещества могут потребоваться для обеспечения потребления микроорганизмами монооксида углерода в качестве источника энергии. Так, например, для такого микроорганизма может потребоваться присутствие кофакторов металлов для обеспечения метаболических функций монооксид углерода-дегидрогеназы (CODH) и ацетил-CoA-синтазы (ACS). Важно отметить, что все необходимые питательные элементы должны присутствовать в нужном количестве и в биологически доступной форме.
Другим необходимым питательным элементом является источник восстановленной серы, которая обычно присутствует в форме органического сульфида, такого как цистеин. Цистеин представляет собой источник серы, необходимый для осуществления ферментативных процессов в микробной культуре. Хорошо известно, что микроорганизмам для осуществления ими ферментативных процессов требуется сера. Действительно, медиатор переноса электронов, ферредоксин, а также ферменты пути Вуда-Льюнгдала, такие как ацетил-CoA-синтаза и монооксид углерода-дегидрогеназа содержат серу. Поэтому важно, чтобы сера была добавлена в биологически доступной форме и в количестве, достаточном для предотвращения ингибирования роста микроорганизмов или продуцирования продуктов этими микроорганизмами.
Во многих случаях альтернативой цистеину является сульфид водорода, который служит источником восстановленной серы, необходимой для осуществления метаболических процессов данными микроорганизмами. В обычной сбраживаемой среде источник серы, такой как сульфид, находится в равновесии с сульфидом водорода. Хотя сульфид водорода является менее дорогостоящим, чем цистеин, однако он является токсичным, а поэтому требует специальных условий транспортировки, и представляет особую опасность при его использовании в чистом виде. Подача в ферментер серы в форме сульфидной соли, такой как сульфид натрия, способствует образованию сульфида водорода в концентрации, которая может со временем снижаться из-за испарения. Кроме того, сульфид водорода имеет ограниченную растворимость в среде. Сульфид водорода может становиться в высокой степени летучим в определенных условиях, что может оказаться желательным в зоне ферментации и будет приводить к повышению его потребления в качестве источника серы. В результате ограниченной растворимости сульфида водорода в воде концентрация серы в растворе может значительно снижаться в зависимости от условий в сбраживаемой среде. В соответствии с этим идентификация улучшенных или альтернативных источников серы для продуцирования спирта микроорганизмами, необходимых в системах ферментации с использованием таких газов, как монооксид углерода или водород и диоксид углерода, в качестве сырьевых материалов, позволит повысить производительность и рентабельность такой технологи производства спирта.
В соответствии с этим способы производства этанола или ацетата путем анаэробной ферментации были бы более эффективными, если будут обнаружены такие соединения серы, которые могут быть применены для рентабельного производства биологической серы, необходимой микроорганизмам для ее утилизации в благоприятных условиях ферментации, что позволило бы решить проблемы, связанные с использованием сульфида водорода в качестве источника серы.
В публикации патентной заявки США 20110300593 описано применение альтернативных источников серы. В этом документе описаны, в частности, только полисульфиды, элементарная и коллоидная сера, как неорганические соединения серы, используемые в качестве альтернативного источника серы. Еще более важно отметить, что в этом документе описано использование этих конкретных соединений серы, как средства для получения сульфида водорода в виде активных молекул в сбраживаемой среде. Таким образом, в цитируемой работе не сообщается о каких-либо серных добавках, которые при их использовании вместо сульфида водорода позволили бы продуцировать другие соединения серы в биологически доступной форме, а поэтому, в указанной работе не представлено каких-либо решений проблем, связанных с высокой летучестью сульфида водорода.
Таким образом, необходимо разработать экономически рентабельные способы ферментации синтетического газа для продуцирования окисленных C2-органических соединений, где подача микроэлементов серы может быть осуществлена в «необходимых» количествах с применением эффективной и недорогостоящей технологии.
Описание сущности изобретения
Изобретение относится к способам биоконверсии синтетического газа (синтез-газа) в окисленные C2-органические соединения, такие как этанол и ацетат, где подача микроэлементов серы обеспечивается серной добавкой, которая поставляет в жидкую питательную среду оксианионы серы или оксианионы сероводорода в форме, необходимой для осуществления микроорганизмами метаболических процессов и при этом облегчающей такие процессы в зоне ферментации при pH, ингибирующем рост примесных микроорганизмов. Было обнаружено, что такие соединения могут обеспечивать потребности карбоксидотрофных микроорганизмов в микроэлементе серы, необходимом для продуцирования этанола и ацетата из субстратов CO, CO2 и H2. Соединения этого класса включают бисульфиты, которые обычно используются в качестве антимикробных агентов в различных пищевых продуктах. При этом обычно предполагается, что такие соединения будут негативно влиять на рост и жизнеспособность микроорганизмов. Таким образом, было обнаружено, что такие соединения могут быть с успехом использованы для получения молекул серы, которые будут удовлетворять потребности микроорганизмов в метаболизме и позволят решить проблему, связанную с летучестью сульфида водорода при низких pH в зоне ферментации.
В своем широком аспекте изобретение относится к способу получения C2-оксигенатов с использованием этанол-продуцирующих карбоксидотрофных микроорганизмов путем доставки серы в сбраживаемую среду в биологически доступной и в высокой степени растворимой форме. Поддерживание pH ниже 5,3, а более предпочтительно ниже 5,1 является в высокой степени эффективным для ингибирования роста примесных микроорганизмов в зоне ферментации. Типичными примесями, которые могут влиять на процесс ферментации или нарушать этот процесс, являются микроорганизмы, которые продуцируют бутираты, и могут снижать селективность процесса получения более желательных этаноловых продуктов.
В изобретении для подачи серы с более высокой степенью окисления используются микроорганизмы, способствующие снижению степени окисления серы до приемлемых уровней. Было высказано предположение, что благодаря такому процессу микроорганизм продуцирует гидросульфид (HS-), который ассимилируется в используемой клетке. Это способствует снижению уровня HS- в жидкой питательной среде и минимизации любого сульфида в равновесной концентрации с сульфидом водорода, которая вносит свой вклад в выделение сульфида водорода из сбраживаемой среды.
В своих конкретных вариантах изобретение относится к способу продуцирования C2-оксигенатов путем анаэробной ферментации с использованием этанол-продуцирующего карбоксидотрофного микроорганизма. Этот способ включает получение серной добавки, включающей неорганическое соединение серы S(II)-S(IV), которое способствует образованию анионов серы, содержащих атомы кислорода и/или атомы кислорода и водорода в водной сбраживаемой среде; контактирование микробной культуры микроорганизма с субстратом, содержащим монооксид углерода; поддерживание микробной культуры в сбраживаемой среде, включающей серную добавку, при pH менее 5,3; и выделение одного или более C2-оксигенатов из сбраживаемой среды. В другом варианте осуществления изобретения указанная серная добавка включает неорганическое соединение серы S(III)-S(IV).
В конкретном варианте осуществления изобретения серной добавкой является сернистая кислота, бисульфит, метабисульфит, дитионит, тиосульфат или их комбинации. В предпочтительном варианте осуществления изобретения серной добавкой является сернистая кислота, бисульфит, метабисульфит или их комбинации. В других вариантах осуществления изобретения серной добавкой могут быть бисульфит натрия, метабисульфит натрия.
В конкретном варианте осуществления изобретения серная добавка присутствует в сбраживаемой среде в концентрации по меньшей мере 0,1, обычно в пределах от 0,1 до 10, а предпочтительно в пределах от 0,5 до 2 ммоль серы на грамм сухой клеточной массы микроорганизма.
В конкретном варианте осуществления изобретения контактирование микроорганизмов с серной добавкой происходит в присутствии дополнительного органического источника серы, и концентрация органической серы в сбраживаемой среде со временем снижается. В предпочтительном варианте осуществления изобретения концентрация органической серы в сбраживаемой среде составляет менее чем 0,3 ммоль органической серы на грамм сухой клеточной массы микроорганизма, а более предпочтительно менее чем 0,1 ммоль органической серы на грамм сухой клеточной массы микроорганизма.
В другом своем аспекте изобретение относится к способу удаления цистеина, используемого в качестве аминокислоты и источника серы, из жидкой питательной сбраживаемой среды. В конкретном варианте осуществления изобретения концентрация цистеина в сбраживаемой среде может быть значительно снижена, а предпочтительно снижена до менее чем 0,3 ммоль на грамм сухой клеточной массы микроорганизма. В конкретном варианте осуществления изобретения добавление цистеина в сбраживаемую среду может быть полностью прекращено.
В другом аспекте изобретения pH сбраживаемой среды поддерживают в пределах от 4,3 до 5,1, а предпочтительно ниже 4,9.
В другом аспекте изобретения указанный способ включает добавление хелатообразующего агента в сбраживаемую среду. В предпочтительном варианте осуществления изобретения в качестве хелатообразующего агента используют этилендиаминтетрауксусную кислоту, диэтилентриаминпентауксусную кислоту, нитрилотриуксусную кислоту, цитрат натрия и их смеси.
Вообще говоря, этанол является предпочтительным метаболитом, продуцируемым микроорганизмами. Другие метаболиты продуцируются в большинстве случаев вместе с ацетатом при ферментации субстрата. Было обнаружено, что способы согласно изобретению позволяют увеличить отношение спиртового продукта к кислотному продукту. Было обнаружено, что отношение этанола к ацетату составляет в пределах от более чем 5:1 до более чем 10:1, причем отношение спирта к ацетату может быть увеличено до 20:1 или более.
Изобретение применяется в случае, когда источник органической серы, такой как цистеин, находится в первом сосуде, используемом для роста микробной культуры, а затем эту микробную культуру переносят во второй сосуд. Первый сосуд, если это необходимо, может также содержать серную добавку. Контактирование микробной культуры, выращенной в первом сосуде с субстратом, может быть затем осуществлено во втором отдельном сосуде. Второй сосуд может содержать сбраживаемую среду с небольшим количеством цистеина или без цистеина. В конкретных вариантах осуществления изобретения второй сосуд для ферментации может иметь больший объем, как это практически используется при последовательном пассировании в целях переноса микробной культуры в сосуды большого объема для промышленного производства. Такое пассирование микробной культуры может продолжаться до переноса в третью зону ферментации и в дополнительные зоны ферментации большего объема. В предпочтительном варианте осуществления изобретения концентрация органической серы, такой как цистеин, будет снижаться по мере увеличения объема зоны ферментации. В другом варианте осуществления изобретения добавление цистеина в зону ферментации можно продолжить только в те зоны ферментации, которые имеют объем менее чем 40000 л, а более предпочтительно менее чем 4000 л.
В соответствии с другим своим вариантом изобретение относится к способу снижения уровня цистеина при продуцировании этанола или ацетата посредством анаэробной ферментации. Указанный способ включает контактирование микробной культуры карбоксидотрофного микроорганизма с субстратом, содержащим монооксид углерода, и культивирование микробной культуры в анаэробных условиях в первой зоне ферментации, содержащей цистеин в первой концентрации, с получением выращенной на цистеине микробной культуры в первой зоне ферментации. Некоторые или все выращенные на цистеине микробные культуры переносят во вторую зону ферментации, содержащую серную добавку, включающую неорганическое соединение серы, имеющее степень окисления от +2 до +4 (S(II)-S(IV)), так чтобы во второй зоне ферментации образовывались анионы, состоящие из атомов серы в комбинации с атомами кислорода и/или водорода. Субстрат, содержащий (i) монооксид углерода, (ii) диоксид углерода и водород или (iii) смеси компонентов (i) и (ii), добавляют во вторую зону ферментации для превращения субстрата в C2-оксигенаты. Из второй зоны ферментации выделяют один или более C2-оксигенатов.
Краткое описание графического материала
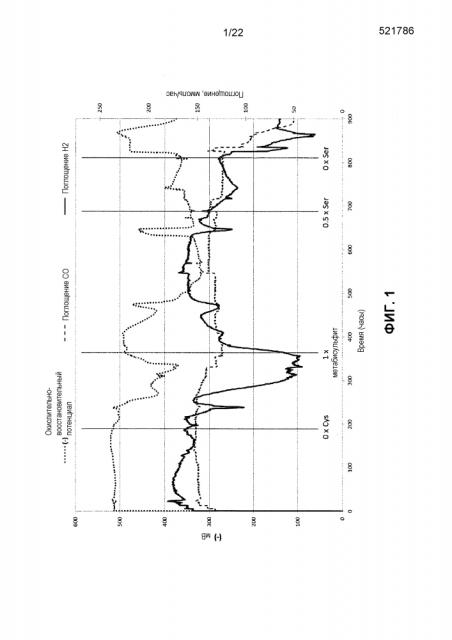
На фиг. 1-22 представлены графики ферментации, на которых указаны данные поглощения газа и продуцирования продукта при проведении непрерывной серии реакций ферментации с использованием серной добавки согласно изобретению.
Определения
«Биореактор» представляет собой любой аппарат для ферментации, имеющий по меньшей мере один сосуд для сохранения микроорганизмов в присутствии сбраживаемой среды, где термин «сосуд» означает устройство любой конфигурации, включающее трубы, колонки, мембраны, экран и другие подобные устройства, которые представляют собой реакторы непрерывного или периодического действия и могут включать барботирующий колоночный биореактор (BCBR), проточный реактор непрерывного действия, снабженный мешалкой (CSTR), реактор с иммобилизованными клетками (ICR), такой как биореактор, снабженный мембраной (MSBR), эжекторные циркуляционные реакторы, реакторы со струйным течением жидкости, трубные реакторы или любое другое устройство, которое обеспечивает контактирование микроорганизмов с субстратом в газо-жидкостной среде. Ферментеры, используемые в изобретении, могут иметь любую подходящую конфигурацию, однако предпочтительно, чтобы их конфигурация и режим работы обеспечивали высокий уровень превращения монооксида углерода и водорода в окисленное органическое соединение.
Термин «C2-оксигенат» означает любую молекулу, содержащую 2 атома углерода, атомы водорода и по меньшей мере один атом кислорода. При этом предпочтительно, чтобы С2-оксигенаты содержали этанол, уксусную кислоту и анионы ацетата.
Термин «микробная культура» означает смесь микроорганизмов с жидкой сбраживаемой средой, где микроорганизмы присутствуют в виде взвеси, суспензии или фиксированных колоний. Микробная культура включает микроорганизмы, суспендированные на подвижной среде-носителе, такой как трубчатые кольца или биочипы, или фиксированные на среде-носителе, такой как мембраны или другие пористые или полупористые среды. Термин «микробная культура» включает культуры, приготовленные из одного штамма микроорганизма или множества штаммов микроорганизмов.
Термин «сбраживаемая среда» означает водную жидкость, которая контактирует с микроорганизмами и содержит питательные элементы, такие как витамины, микроэлементы, аминокислоты и т.п., необходимые микроорганизму для сохранения своих биологических функций, а также продукты метаболизма, которые продуцируются микроорганизмами и выделяются из сбраживаемой среды. Сбраживаемая среда может поддерживать микроорганизмы, суспендированные в виде планктона, либо она может служить в качестве суспензионной среды для сохранения материала-носителя, на котором растут микроорганизмы, либо она может служить для подачи микробной культуры или ее выведения через носитель, такой как мембрана. В сбраживаемую среду может быть непосредственно добавлен газообразный субстрат, и такая среда будет служить средством для подачи субстрата к микроорганизмам.
Термин «сбраживание» или «ферментация» означает любое превращение субстрата под действием микроорганизма независимо от того, находится ли данный микроорганизм в фазе первичного роста или в фазе первоначального продуцирования продуктов-метаболитов.
Термин «среднее время удерживания клеток» при непрерывной ферментации означает общую массу клеток в ферментере, деленную на скорость истощения биомассы в ферментере.
Термин «питательная жидкость» означает водную жидкость, содержащую один или более питательных элементов, таких как витамины, микроэлементы или аминокислоты, необходимые микроорганизму для сохранения или улучшения своих биологических функций, где указанная водная жидкость может быть добавлена в сбраживаемую среду, либо она может непосредственно контактировать с микробной культурой.
Термин «органическая сера» означает любое сероорганическое соединение, определяемое как любое производное серы, имеющее по меньшей мере одну алкильную или арильную группу.
Термин «окислительно-восстановительный потенциал» или «ОВП» при его количественном определении означает величину разности потенциалов между водным раствором и электродом типа Ag/Ag-Cl, измеряемую с использованием солевого мостика, содержащего 3,8M электролита KCl.
Термины «S(II)», «S(III)» и «S(IV)» означают атомы серы в соединении серы, имеющие степень окисления «+2», «+3» и «+4» соответственно.
Термин «субстрат(ы)» означает газ или газы, которые представляют собой первичный источник углерода и энергии для микроорганизмов и включают по меньшей мере один из таких компонентов, как монооксид углерода или смесь диоксида углерода и водорода.
Подробное описание изобретения
В изобретении используются неорганические соединения серы уникального класса, которые обеспечивают доставку серы, необходимую для осуществления ферментации в целях продуцирования С2-оксигенатов из газообразных субстратов, содержащих один или более из таких компонентов, как монооксид углерода и/или смесь диоксида углерода и водорода. В большинстве случаев главное преимущество такого способа заключается в том, что присутствие цистеина в зоне ферментации не является необходимым. В некоторых вариантах осуществления изобретения цистеин может быть удален в начале реакции ферментации, либо количество цистеина может быть снижено, и/или цистеин может быть полностью удален по мере прохождения реакции ферментации. Это означает, что количество цистеина может быть снижено до значительно более низких уровней, чем это может потребоваться в случае, когда цистеин представляет собой первичный источник биологически доступной серы, либо это означает, что цистеин может быть удален во время непрерывного процесса ферментации не только как источник серы, но и как прямой источник аминокислоты. Было обнаружено, что неорганические серные добавки согласно изобретению обеспечивают поддерживание высокого уровня серы в зоне ферментации, а также позволяют микроорганизму размножаться на фазах роста и продуцирования, так чтобы в зоне ферментации могли достигаться высокие титры этанола.
Главной целью изобретения является получение серной добавки конкретного типа. Такая серная добавка, которая может быть использована в изобретении, может содержать соединения серы, имеющее атомы серы со степенью окисления от +2 до +4 (S(II)-S(IV)). Эти добавки могут представлять собой соединения серы любого типа, содержащие оксоанионы серы и/или оксоанионы сероводорода. Конкретными анионными формами такой добавки являются сульфит, бисульфит, метабисульфит, диоксид серы, дитионит и тиосульфат. Такая добавка может быть получена путем добавления различных соединений серы, таких как сернистая кислота, бисульфит натрия, метабисульфит натрия, метабисульфит калия, дитионовая кислота, дитионит натрия, тиосульфат натрия.
Серная добавка после ее диспергирования в водную жидкость сбраживаемой среды может присутствовать в активной анионной форме. Оксоанионы серы и оксоанионы сероводорода, которые являются эффективными для осуществления изобретения, содержат сульфитную форму SО32- и форму сульфита водорода НSО3- (бисульфитную форму). Не претендуя на какую-либо конкретную теорию, авторы изобретения лишь указывают на способность микроорганизмов переносить эти оксоанионы серы через мембрану клеточной структуры. После переноса оксианионов вовнутрь клеток микроорганизмы восстанавливают эти оксианионы до HS-. Реакции протекают в следующей последовательности: SO3-2=>H2S под действием сульфит-редуктазы, а затем HS-+O-ацетилсерин => цистеин под действием O-ацетилсерин-сульфгидрилазы. Под действием воды соединения серы диссоциируют с образованием равновесных смесей аниона сульфита и других положительно заряженных или нейтральных молекул. Так, например, с использованием раствора сернистой кислоты в воде в качестве добавки может быть достигнуто равновесие диоксида серы и иона бисульфита в соответствии со следующей формулой:
H2SO3+H2OHSO3-+H+
с константой диссоциации
Κa=1,38×l0-2; pΚa=1,86.
Аналогичным образом, водный диоксид серы будет связываться с водой и подвергаться депротонированию в соответствии с общей формулой и pKa
SO2+H2OHSO3-+H+
с константой диссоциации
Κa=1,54×l0-2; pΚa=1,81.
Сульфит водорода также находится в равновесии с ионом сульфита в соответствии с формулой
HSO3-SO32-+H+
и представляет собой слабую кислоту с pΚa=6,97.
Используемый в изобретении анион дитионита ([S2O4]2-) представляет собой другой оксоанион серы, который может быть получен из дитионовой кислоты и H2S2O4, и который после гидролиза образует равновесную смесь тиосульфата и бисульфита в соответствии с формулой
2S2O4-2+H2O→S2O3-2+2HSO3-1
Подходящие серные добавки могут быть получены в различных формах широкого ряда, которые обеспечивают утилизацию серных добавок и оксоанионов серы микроорганизмами. Специалистам известно, что для получения серных добавок согласно изобретению могут быть использованы подходящие неорганические соли серы. Обычно используемые формы добавок включают бисульфит натрия, метабисульфит натрия, сернистую кислоту, метабисульфит калия, бисульфит калия или любую другую комбинацию катиона-оксоаниона-серы. Особенно предпочтительно, чтобы соединение серы было, по существу, растворимым в сбраживаемой среде и нетоксичным для микробной культуры в эффективной концентрации серной добавки на любой стадии роста микробной культуры.
Изобретение позволяет сохранять серную добавку на предварительно определенном или более высоком уровне. Серная добавка может быть введена в количестве, достаточном для того, чтобы все это количество серы или ее части удовлетворяло биологическим потребностям микроорганизмов. Серную добавку обычно вводят в количестве, достаточном для того, чтобы отдельные атомы серы удовлетворяли биологическим потребностям микроорганизмов. Для создания стационарных условий ферментации, при которых все количество серы будет удовлетворять биологическим потребностям микроорганизмов, серу обычно добавляют в концентрации, составляющей по меньшей мере 0,25 ммоль серной добавки на грамм сухой клеточной массы микроорганизма в случае ионов одноатомной серы, причем такое количество может быть скорректировано для ионов многоатомной серы. Предпочтительная концентрация добавленной серы составляет в пределах от 0,67 до 2 ммоль серы на грамм сухой клеточной массы микроорганизма.
Серная добавка может включать различные источники неорганической серы, которые могут разлагаться и/или высвобождаться с образованием биологически доступных молекул серы согласно изобретению в различных количествах в зависимости от таких параметров, как pH, температура, давление и т.п. Может оказаться необходимым, чтобы со временем добавление серной добавки варьировалось в зависимости от скорости разложения и диссоциации конкретно используемой серной добавки. Такое изменение типа и/или количества добавляемой серной добавки может оказаться необходимым для поддержания роста и/или продуктивности микробной культуры. Поэтому эффективность ферментации может быть повышена посредством увеличения концентрации молекул серы нужного вида путем добавления большего количества серной добавки или изменения типа серной добавки в различные периоды времени и на различных стадиях ферментации.
В конкретных вариантах осуществления изобретения одно или более неорганических соединений серы представляют собой раствор бисульфитного соединения, такого как бисульфит натрия, приготовленный в форме предпочтительно 5-молярного раствора бисульфита и разведенный с получением маточного раствора в предпочтительной концентрации приблизительно 1,2 мМ. Концентрация бисульфита в растворе зависит от различных факторов, включая pH и растворимость.
В другом варианте осуществления изобретения было обнаружено, что карбоксидотрофные микроорганизмы могут выживать в культуральной среде, которая не содержит каких-либо дополнительных аминокислот, включая цистеин, и источником серы для этих микроорганизмов является сернистая кислота (H2SO3). Атомы серы сернистой кислоты и метабисульфита имеют степень окисления +4. Известно, что метабисульфит, сернистая кислота, сульфит, диоксид серы и бисульфит могут присутствовать в воде в равновесном состоянии. T. Fazio & C.R. Warner. 1990. A Review of Sulphites in Foods: analytical methodology and findings. Food Addit. Contam. 7:433-454.
В этом конкретном варианте осуществления изобретения рост микробной культуры может быть инициирован цистеином, используемым в качестве серной добавки, с последующим снижением концентрации цистеина (наряду с пропорциональным увеличением количества серной добавки) и небольшой постоянной коррекцией поглощения водорода. При необходимости для регуляции переноса газовой массы могут быть изменены режим перемешивания и скорость потока газа. Удовлетворительные результаты могут быть получены даже в том случае, когда питательная жидкость абсолютно не содержит метабисульфита и цистеина в течение 800 ч, а в качестве источника серы остается только сернистая кислота, поставляемая с питательной жидкостью для ее утилизации микроорганизмами. (Анионы сульфата присутствуют в среде, однако стандартные микроорганизмы, используемые в изобретении, не утилизуют сульфат ни по механизму ассимиляции, ни по механизму диссимиляции). В некоторых случаях может быть также добавлен серин.
В некоторых случаях добавление избыточного количества соединений S(IV) может несмотря на изменение KLa приводить к снижению уровня поглощения водорода. Это может быть обусловлено известным действием соединений S(IV), используемых в качестве ингибиторов роста микробов. Поэтому изобретение может иметь то преимущество, что оно позволяет проводить мониторинг количества полученного соединения S(IV), которое должно быть достаточным для предотвращения каких-либо побочных эффектов, обусловленных присутствием слишком малого количества биологически доступной серы, а также токсических эффектов, обусловленных слишком большим количеством соединения S(IV). И в этом случае добавление избыточного количества серы может также приводить к высвобождению микробной культурой больших количеств сульфида водорода, которые представляют определенную опасность и удаление которых требует значительных материальных затрат.
Предложенный метод ассимиляции сернистой кислоты в клетках инициируется сульфит-редуктазой. При рН рабочей культуры 4,5-5,3 сернистая кислота будет подвергаться химическому депротонированию с образованием, главным образом, формы HSO3-, где величины двух pΚa составляют 7,2 и 1,9. Затем этот бисульфит подвергается биологическому превращению в H2S под действием указанного фермента, и на этой стадии, очевидно, происходит ассимиляция цистеина посредством связывания ацетилсерина. Хотя неизвестно, присутствует ли ген O-ацетилсерин-сульфгидролазы, используемой в этой реакции, в геноме карбоксидотрофных микроорганизмов согласно изобретению, однако известно, что в геноме карбоксидотрофных микроорганизмов согласно изобретению присутствует ген сульфит-редуктазы. Кроме того, присутствие сульфида водорода в отходящем газе ферментера, хотя этот сульфид водорода и не подавался в ферментер с питательной жидкостью, а также способность микроорганизмов выживать на соединении S(IV) указывают на наличие гена O-ацетилсерин-сульфгидролазы.
Сера может быть добавлена в сбраживаемую среду любым подходящим способом. В соответствии с изобретением серная добавка может быть добавлена любым методом, обеспечивающим биологическую доступность нужных молекул серы для микроорганизма в предварительно определенных количествах и в определенное время проведения ферментации. Эту добавку предпочтительно вводят непосредственно в сбраживаемую среду в процессе добавления питательной жидкости, которая обеспечивает микробную культуру другими микроэлементами. Таким образом, серная добавка может быть введена периодически или непрерывно в виде смесей в концентрации, которая может варьироваться в процессе ферментации. Серная добавка может подаваться в различные участки микробной культуры, например, во множество различных отделений биореактора, снабженного сосудом для ферментации, в котором микроорганизмы суспендированы в форме планктона. Подачу серной добавки обычно осуществляют после инокуляции биореактора микробной культурой, и такая подача может быть увеличена по мере роста культуры и по мере повышения потребности в метаболическом соединении серы в процессе ферментации. Подачу серной добавки обычно регулируют для поддержания предварительно определенной концентрации одного или более оксоанионов сероводорода или серы на уровне, достаточном для их утилизации микроорганизмами в биореакторе.
Для определения концентрации серной добавки в растворе может быть применен любой подходящий метод. Подача серной добавки может регулироваться в зависимости от присутствия сульфида в отходящем газе зоны ферментации. При ферментации сульфид обычно высвобождается в область «хэд-спейса» или в газовую фазу, расположенные выше сбраживаемой среды. Этот сульфид может образовываться из сульфида, присутствующего в сбраживаемой среде, и никогда не усваивается микроорганизмом (внеклеточный сульфид), либо он может образовываться из сульфида, высвобождаемого микроорганизмом (внутриклеточный сульфид). Преимуществом изобретения является возможность минимизации любого образования внеклеточного сульфида, а присутствие и высвобождение сульфида является показателем переизбытка серной добавки в сбраживаемой среде. Поэтому мониторинг концентрации сульф