Получение дгк и других дц-пнжк в растениях
Иллюстрации
Показать всеИзобретение относится к области биохимии, в частности к генетически модифицированной клетке растения сои, продуцирующей масло, содержащее 0,36-8,00% ДГК от общего количества жирных кислот и 0,30-3,98% ДПК(n-6) от общего количества жирных кислот, а также к способу ее получения. Также раскрыты генетически модифицированные растение и семя сои для получения масла сои, содержащего 0,36-8,00% ДГК от общего количества жирных кислот и 0,30-3,98% ДПК(n-6) от общего количества жирных кислот. Изобретение также относится к маслу сои, содержащему 0,36-8,00% ДГК от общего количества жирных кислот и 0,30-3,98% ДПК(n-6) от общего количества жирных кислот, а также к способу его получения. Изобретение позволяет эффективно получать масло сои, содержащее 0,36-8,00% ДГК от общего количества жирных кислот и 0,30-3,98% ДПК(n-6) от общего количества жирных кислот. 6 н. и 12 з.п. ф-лы, 39 ил., 14 табл., 12 пр.
Реферат
УРОВЕНЬ ТЕХНИКИ
Область техники, к которой относится изобретение
Настоящее изобретение, в общем, относится к рекомбинантным организмам-хозяевам (например, растениям), генетически модифицированным системой синтазы полиненасыщенных жирных кислот (ПНЖК) и одним или несколькими вспомогательными белками, которые обеспечивают возможность и/или улучшают продуцирование ПНЖК в организме-хозяине. Настоящее изобретение также относится к способам получения и применения таких организмов (например, для получения ПНЖК), а также продуктам, получаемым из таких организмов (например, маслу и семени).
Уровень техники
Полиненасыщенные жирные кислоты (ПНЖК) считаются полезными для применений в пищевых продуктах, фармацевтических применений, промышленных применений и других целей. Однако, в настоящее время обеспечение ПНЖК за счет природных источников (например, рыбьего жира) и химического синтеза не достаточно для долгосрочных коммерческих нужд.
Растительные масла, получаемые из растений (например, масличных культур), относительно недороги и не имеют проблем, связанных с загрязнением, как в случае рыбьего жира. Однако ПНЖК, обнаруженные во внедренных для коммерческих целей растениях и растительных маслах, обычно не содержат более насыщенные или длинноцепочечные ПНЖК и обычно содержат только такие жирные кислоты, как линолевая кислота (восемнадцать атомов углерода с 2 двойными связями в дельта 9- и 12-положениях - 18:2 дельта 9,12) и линолевая кислота (18:3 дельта 9,12,15).
Было описано получение более ненасыщенных или длинноцепочечных ПНЖК в растениях с использованием модификации жирных кислот, эндогенно продуцируемых растениями. Например, было описано, что генетическая модификация растений различными отдельными генами, кодирующими элонгазы и/или десатуразы жирных кислот, приводит к образованию листьев и семян, содержащих значительные уровни длинноцепочечных и более ненасыщенных ПНЖК, таких как эйкозапентаеновая кислота (ЭПК), а также содержащих значительные уровни смешанных имеющих более короткие цепи и менее ненасыщенных ПНЖК
публикация заявки на выдачу патента США № 2004/0172682, заявка на выдачу патента США № 61/345537, поданная 17 мая 2010).
Fabaceae (или Leguminosae) представляют собой большое и экономически важное семейство цветковых растений, которые обычно известны как семейство бобовых (фасоль, горох, бобы или зернобобовые). Род Glycine является родом в семействе Fabaceae и включает, например, Glycine albicans, Glycine aphyonota, Glycine arenari, Glycine argyrea, Glycine canescens, Glycine clandestine, Glycine curvata, Glycine cyrtoloba, Glycine falcate, Glycine gracei, Glycine hirticaulis, Glycine hirticaulis подвид leptosa, Glycine lactovirens, Glycine latifolia, Glycine latrobeana, Glycine microphylla, Glycine montis-douglas, Glycine peratosa, Glycine pescadrensis, Glycine pindanica, Gycine pullenii, Glycine rubiginosa, Glycine stenophita, Glycine syndetika, Glycine tabacina, Glycine tomentella, Glycine soja и Glycine max (соя). Семейство Fabaceae также включает арахис, фасоль (Phaseolus vulgaris), кормовые бобы (Vicia faba) или горох (Pisum sativum).
Большая часть соевого масла производится в форме растительных масел, получаемых для потребления человеком. Также растет рынок, обеспечивающий применение соевого масла в промышленности.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В данной области существует потребность в относительно недорогом способе рационального и эффективного получения определенных количеств (например, коммерческих количеств) длинноцепочечных или более ненасыщенных ПНЖК в растениях, семенах растений или растительном масле, а также определенных количеств липидов (например, триацилглицерина (ТАГ) и фосфолипида (ФЛ)), которыми обогащают ПНЖК в растениях, семенах растений или растительном масле. Система получения и улучшения продуцирования ПНЖК в организмах-хозяевах (например, растениях) в результате получения рекомбинантных организмов-хозяев, генетически модифицированных синтазой полиненасыщенных жирных кислот (ПНЖК) и одним или несколькими вспомогательными белками, которые описаны в настоящей публикации, является значимой альтернативой способам, известным в данной области.
Настоящее изобретение относится к генетически модифицированным растениям (например, растениям семейства Fabaceae или рода Glycine, таким как соя), потомкам, семенам, клеткам, тканям или их частям, содержащим (i) последовательность нуклеиновой кислоты, кодирующую синтазу полиненасыщенных жирных кислот (ПНЖК) (например, ПНЖК-синтазу водорослей), которая продуцирует, по меньшей мере, одну ПНЖК; и (ii) последовательность нуклеиновой кислоты, кодирующую фосфопантетеинилтрансферазу (PPT-азу), которая переносит кофактор фосфопантетеинил на АПБ-домен системы ПНЖК-синтазы (например, системы ПНЖК-синтазы водорослей).
В некоторых вариантах осуществления настоящего изобретения ПНЖК-синтаза содержит аминокислотную последовательность, которая на 80-99% идентична аминокислотной последовательности SEQ ID NO: 1 или содержит аминокислотную последовательность SEQ ID NO: 1. В некоторых вариантах последовательность нуклеиновой кислоты, кодирующая ПНЖК-синтазу, содержит последовательность нуклеиновой кислоты, идентичную на 80-99% последовательности нуклеиновой кислоты SEQ ID NO: 6, или содержит последовательность нуклеиновой кислоты SEQ ID NO: 6. В некоторых вариантах ПНЖК-синтаза содержит аминокислотную последовательность, которая на 80-99% идентична аминокислотной последовательности SEQ ID NO: 2 или содержит аминокислотную последовательность SEQ ID NO: 2. В некоторых вариантах последовательность нуклеиновой кислоты, кодирующая ПНЖК-синтазу, содержит последовательность нуклеиновой кислоты, идентичную на 80-99% последовательности нуклеиновой кислоты SEQ ID NO: 7, или содержит последовательность нуклеиновой кислоты SEQ ID NO: 7. В некоторых вариантах ПНЖК-синтаза содержит аминокислотную последовательность, которая на 80-99% идентична аминокислотной последовательности SEQ ID NO: 3, или содержит аминокислотную последовательность SEQ ID NO: 3. В некоторых вариантах последовательность нуклеиновой кислоты, кодирующая ПНЖК-синтазу, содержит последовательность нуклеиновой кислоты, которая на 80-99% идентична последовательности нуклеиновой кислоты SEQ ID NO: 8, или содержит последовательность нуклеиновой кислоты SEQ ID NO: 8. В некоторых вариантах ПНЖК-синтаза содержит аминокислотную последовательность SEQ ID NO: 1, 2 или 3 или любое их сочетание. В некоторых вариантах последовательность нуклеиновой кислоты, кодирующая ПНЖК-синтазу, содержит последовательность нуклеиновой кислоты SEQ ID NO: 6, 7 или 8, или любое их сочетание.
В некоторых вариантах PPT-аза содержит аминокислотную последовательность, которая на 80-99% идентична последовательности SEQ ID NO: 5, или содержит аминокислотную последовательность SEQ ID NO: 5. В некоторых вариантах последовательность нуклеиновой кислоты, кодирующая PPT-азу, на 80-99% идентична последовательности нуклеиновой кислоты SEQ ID NO: 10 или содержит последовательность нуклеиновой кислоты SEQ ID NO: 10.
В некоторых вариантах последовательности нуклеиновых кислот (i) и (ii) находятся в одном рекомбинантном экспрессирующем векторе. В некоторых вариантах последовательности нуклеиновых кислот (i) и (ii) находятся в разных рекомбинантных экспрессирующих векторах. В некоторых вариантах последовательности нуклеиновой кислоты (i) и/или (ii) оперативно связаны со специфичным для семян промотором. В некоторых вариантах последовательности нуклеиновой кислоты (i) и/или (ii) оперативно связаны с промотором, выбранным из PvDlec2, PvPhaseolin, LfKCS3, FAE 1, BoACP и BnaNapinC. В некоторых вариантах последовательности нуклеиновой кислоты (i) и/или (ii) оперативно связаны со специфичным для листьев промотором. В некоторых вариантах последовательности нуклеиновой кислоты (i) и/или (ii) оперативно связаны с промотором убиквитина или CsVMV.
В некоторых вариантах генетически модифицированное растение, его потомок, семя, клетка, ткань или часть дополнительно содержит (iii) последовательность нуклеиновой кислоты, кодирующую ацил-CoA-синтетазу (ACoAS), которая катализирует превращение свободных жирных кислот длинноцепочечных ПНЖК (ПСЖК), в ацил-CoA. В некоторых вариантах ACoAS содержит аминокислотную последовательность, которая на 80-99% идентична последовательности SEQ ID NO: 4, или содержит аминокислотную последовательность SEQ ID NO: 4. В некоторых вариантах ACoAS содержит последовательность нуклеиновой кислоты, которая на 80-99% идентична последовательности нуклеиновой кислоты SEQ ID NO: 9, или содержит последовательность нуклеиновой кислоты SEQ ID NO: 9. В некоторых вариантах последовательность нуклеиновой кислоты, кодирующая ACoAS, содержит последовательность нуклеиновой кислоты SEQ ID NO: 34. В некоторых вариантах последовательности нуклеиновых кислот (i), (ii) и/или (iii) находятся в одном рекомбинантном экспрессирующем векторе. В некоторых вариантах последовательности нуклеиновых кислот (i), (ii) и (iii) находятся в разных рекомбинантных экспрессирующих векторах. В некоторых вариантах последовательности нуклеиновых кислот (i) и (ii) находятся в одном рекомбинантном экспрессирующем векторе, а последовательность нуклеиновой кислоты (iii) находится в другом рекомбинантном экспрессирующем векторе. В некоторых вариантах последовательности нуклеиновых кислоты (i) и (iii) находятся в одном рекомбинантном экспрессирующем векторе, а последовательность нуклеиновой кислоты (ii) находится в другом рекомбинантном экспрессирующем векторе. В некоторых вариантах последовательности нуклеиновых кислот (ii) и (iii) находятся в одном рекомбинантном экспрессирующем векторе, а последовательность нуклеиновой кислоты (i) находится в другом рекомбинантном экспрессирующем векторе. В некоторых вариантах последовательности нуклеиновых кислот (i), (ii) и/или (iii) оперативно связаны со специфичным для семян промотором. В некоторых вариантах последовательности нуклеиновых кислот (i), (ii) и/или (iii) оперативно связаны с промотором, выбранным из PvDlec2, LfKCS3, FAE 1, BoACP и BnaNapinC. В некоторых вариантах последовательности нуклеиновых кислот (i), (ii) и/или (iii) оперативно связаны со специфичным для листьев промотором. В некоторых вариантах последовательности нуклеиновых кислот (i), (ii) и/или (iii) оперативно связаны с промотором убиквитина или CsVMV.
В некоторых вариантах генетически модифицированное растение, его потомок, клетка, ткань или часть дополнительно содержит последовательность нуклеиновой кислоты, кодирующую ацетил-CoA-карбоксилазу (ACC-азу), и/или последовательность нуклеиновой кислоты, кодирующую диацилглицеринацилтрансферазу типа 2 (DGAT2).
В некоторых вариантах генетически модифицированное растение, его потомок, клетка, ткань, семя или часть содержит, по меньшей мере, одну из плазмид pDAB7361, pDAB7362, pDAB7363, pDAB7368, pDAB7369, pDAB7370, pDAB100518, pDAB101476, pDAB101477, pDAB9166, pDAB9167, pDAB7379, pDAB7380, pDAB9323, pDAB9330, pDAB9337, pDAB9338, pDAB9344, pDAB9396, pDAB101412, pDAB7733, pDAB7734, pDAB101493, pDAB109507, pDAB109508, pDAB109509, pDAB9151, pDAB108207, pDAB108208, pDAB108209, pDAB9159, pDAB9147, pDAB108224 и pDAB108225.
В некоторых вариантах генетически модифицированное растение, его потомок, клетка, ткань, семя или часть или масло (например, масло из семян), полученное из генетически модифицированного растения, его потомка, семени, клетки, ткани или части, содержит регистрируемые количества ДГК (докозагексаеновой кислоты (C22:6, n-3)), ДПК(n-6) (докозапентаеновой кислоты (C22:5, n-6)) и/или ЭПК (эйкозапентаеновой кислоты (C20:5, n-3)). В некоторых вариантах генетически модифицированное растение, его потомок, клетка, ткань, семя или часть или масло (например, масло из семян), полученное из генетически модифицированного растения, его потомка, семени, клетки, ткани или части, содержит от 0,01% до 15% масс. ДГК от общего количества жирных кислот, от 0,05% до 10% масс. ДГК от общего количества жирных кислот или от 0,05% до 5% масс. ДГК от общего количества жирных кислот. В некоторых вариантах генетически модифицированное растение, его потомок, клетка, ткань, семя или часть или масло (например, масло из семян), полученное из генетически модифицированного растения, его потомка, семени, клетки, ткани или части, содержит от 0,01% до 10% масс. ЭПК от общего количества жирных кислот, от 0,05% до 5% масс. ЭПК от общего количества жирных кислот или от 0,05% до 1% масс. ЭПК от общего количества жирных кислот. В некоторых вариантах генетически модифицированное растение, его потомок, клетка, ткань, семя или часть или масло (например, масло из семян), полученного из генетически модифицированного растения, его потомка, семени, клетки, ткани или части, содержит от 0,01% до 10% масс. ДПК(n-6) от общего количества жирных кислот, от 0,01% до 5% масс. ДПК(n-6) от общего количества жирных кислот или от 0,01% до 1% масс. ДПК(n-6) от общего количества жирных кислот. В некоторых вариантах генетически модифицированное растение, его потомок, клетка, ткань, семя или часть или масло (например, масло из семян), полученное из генетически модифицированного растения, его потомка, семени, клетки, ткани или части, содержит соотношение ЭПК:ДГК от 1:1 до 1:30 или от 1:1 до 1:3 по массе в общей массе жирных кислот. В некоторых вариантах генетически модифицированное растение, его потомок, клетка, ткань, семя или часть или масло (например, масло из семян), полученное из генетически модифицированного растения, его потомка, семени, клетки, ткани или части, содержит соотношение ДПК(n-6):ДГК от 1:1 до 1:10 или от 1:1 до 1:3 по массе в общей массе жирных кислот. В некоторых вариантах масло (например, масло из семян), полученное из генетически модифицированного растения, его потомка, клетки, ткани, семени или части, содержит от 70% до 99% масс. триглицеридов от общей массы масла.
В некоторых вариантах регистрируемые количества ДГК, ДПК(n-6) и/или ЭПК также выявляют в зерне и/или муке, полученной из генетически модифицированного растения, его потомка, ткани, семени или части.
Настоящее изобретение относится к маслу (например, масло из семян) или семени, полученным из генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации. Настоящее изобретение относится к продукту питания, содержащему масло (например, масло из семян), полученное из генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации. Настоящее изобретение также относится к функциональному пищевому продукту, содержащему масло (например, масло из семян), или семя, полученное из генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации. Настоящее изобретение относится к фармацевтическому продукту, содержащему масло (например, масло из семян) или семя, полученное из генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации.
Настоящее изобретение относится к способу получения масла, содержащего, по меньшей мере, одну ДЦ-ПНЖК, включающему в себя извлечение масла из генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации, или семени генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации. Настоящее изобретение также относится к способу получения масла, содержащего, по меньшей мере, одну ДЦ-ПНЖК, включающему в себя выращивание генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации. Настоящее изобретение также относится к способу получения, по меньшей мере, одной ДЦ-ПНЖК в масле из семян, включающему в себя извлечение масла из семени генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации.
Настоящее изобретение относится к способу получения, по меньшей мере, одной ПНЖК в масле из семян, включающему в себя выращивание генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации. Настоящее изобретение также относится к способу предоставления индивидууму добавки или терапевтического продукта, содержащего, по меньшей мере, одну ПНЖК, включающему в себя предоставление индивидууму генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации, масла, описанного в настоящей публикации, семени, описанного в настоящей публикации, продукта питания, описанного в настоящей публикации, функционального продукта питания, описанного в настоящей публикации, или фармацевтического продукта, описанного в настоящей публикации. В некоторых вариантах ПНЖК, входящей в состав указанных вариантов, является ДГК, ДПК(n-6) и/или ЭПК.
Настоящее изобретение относится к способу получения генетически модифицированного растения (например, сои), его потомка, клетки, ткани или части, описанных в настоящей публикации, включающему в себя трансформацию растения или растительной клетки (i) последовательностью нуклеиновой кислоты, кодирующей синтазу ПНЖК (например, ПНЖК-синтазу водорослей), которая продуцирует, по меньшей мере, одну полиненасыщенную жирную кислоту (ПНЖК); и (ii) последовательностью нуклеиновой кислоты, кодирующей фосфопантетеинилтрансферазу (PPT-азу), которая переносит кофактор фосфопантетеинил на АПБ-домен системы ПНЖК-синтазы (например, системы ПНЖК-синтазы водорослей). В некоторых вариантах способ дополнительно включает в себя трансформацию растения или растительной клетки (iii) последовательностью нуклеиновой кислоты, кодирующей ацил-CoA-синтетазу (ACoAS), которая катализирует превращение свободных жирных кислот (СЖК) длинноцепочечных ПНЖК в ацил-CoA.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Различные варианты осуществления изобретения можно более полно понять из следующего подробного описания, фигур и прилагаемого описания последовательностей, которые составляют часть настоящей заявки.
На фиг. 1 изображены выравнивания Clustal W (выравнивания в векторе NTI) реконструированных последовательностей ДНК, кодирующих каждый из 9 повторяющихся доменов PUFA OrfA.
Фиг. 2 представляет собой карту плазмиды pDAB7362.
Фиг. 3 представляет собой карту плазмиды pDAB7361.
Фиг. 4 представляет собой карту плазмиды pDAB7363.
Фиг. 5 представляет собой карту плазмиды pDAB7365.
Фиг. 6 представляет собой карту плазмиды pDAB7368.
Фиг. 7 представляет собой карту плазмиды pDAB7369.
Фиг. 8 представляет собой карту плазмиды pDAB7370.
Фиг. 9 представляет собой карту плазмиды pDAB100518.
Фиг. 10 представляет собой карту плазмиды pDAB101476.
Фиг. 11 представляет собой карту плазмиды pDAB101477.
На фиг. 12 показано содержание ДГК и ДЦ-ПНЖК в отдельных семенах сои T2 от растений T1, полученных в результате двух событий трансформации сои с использованием pDAB7362.
На фиг. 13 показано выявление на Вестерн-блотах ПНЖК-синтазы OrfA, ПНЖК-синтазы OrfB и химерной ПНЖК-синтазы OrfC в экстрактах белков семян сои T2.
Фиг. 14 представляет собой карту плазмиды pDAB9166.
Фиг. 15 представляет собой карту плазмиды pDAB9167.
Фиг. 16 представляет собой карту плазмиды pDAB7379.
Фиг. 17 представляет собой карту плазмиды pDAB7380.
Фиг. 18 представляет собой карту плазмиды pDAB9323.
Фиг. 19 представляет собой карту плазмиды pDAB9330.
Фиг. 20 представляет собой карту плазмиды pDAB9337.
Фиг. 21 представляет собой карту плазмиды pDAB9338.
Фиг. 22 представляет собой карту плазмиды pDAB9344.
Фиг. 23 представляет собой карту плазмиды pDAB9396.
Фиг. 24 представляет собой карту плазмиды pDAB101412.
Фиг. 25 представляет собой карту плазмиды pDAB7733.
Фиг. 26 представляет собой карту плазмиды pDAB7734.
Фиг. 27 представляет собой карту плазмиды pDAB101493.
Фиг. 28 представляет собой карту плазмиды pDAB109507.
Фиг. 29 представляет собой карту плазмиды pDAB109508.
Фиг. 30 представляет собой карту плазмиды pDAB109509.
Фиг. 31 представляет собой карту плазмиды pDAB9151.
Фиг. 32 представляет собой карту плазмиды pDAB108207.
Фиг. 33 представляет собой карту плазмиды pDAB108208.
Фиг. 34 представляет собой карту плазмиды pDAB108209.
Фиг. 35 представляет собой карту плазмиды pDAB9159.
Фиг. 36 представляет собой карту плазмиды pDAB9147.
Фиг. 37 представляет собой карту плазмиды pDAB108224.
Фиг. 38 представляет собой карту плазмиды pDAB108225.
На фиг. 39 показано содержание ДГК и ДЦ-ПНЖК в семенах T2 от отдельных трансгенных растений Arabidopsis, полученных в результате событий трансформации с использованием pDAB101493, pDAB7362, pDAB7369, pDAB101412 или pDAB7380.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Термин «полиненасыщенная жирная кислота» или «ПНЖК» в используемом в настоящем описании смысле относится к жирным кислотам с длиной углеродной цепи, составляющей по меньшей мере, 16 атомов углерода, по меньшей мере, 18 атомов углерода, по меньшей мере, 20 атомов углерода или 22 или больше атомов углерода, по меньшей мере, с 3 или большим количеством двойных связей, 4 или большим количеством двойных связей, 5 или большим количеством двойных связей или 6 или большим количеством двойных связей, при этом все двойные связи находятся в цис-конфигурации.
Термин «длинноцепочечные полиненасыщенные жирные кислоты» или «ДЦ-ПНЖК» в используемом в настоящем описании смысле относится к жирным кислотам с длиной цепи 20 и больше атомов углерода, содержащим 3 или больше двойных связей, или 22 или больше атомов углерода, по меньшей мере, с 3 или большим количеством двойных связей, 4 или большим количеством двойных связей, 5 или большим количеством двойных связей или 6 или большим количеством двойных связей. ДЦ-ПНЖК из ряда омега-6 включают без ограничения дигомо-гамма-линоленовую кислоту (C20:3n-6), арахидоновую кислоту (C20:4n-6), адреновую кислоту (также называемую докозатетраеновой кислотой или ДТК) (C22:4n-6) и докозапентаеновую кислоту (C22:5n-6). ДЦ-ПНЖК из ряда омега-3 включают без ограничения эйкозатриеновую кислоту (C20:3n-3), эйкозатетраеновую кислоту (C20:4n-3), эйкозапентаеновую кислоту (C20:5n-3), докозапентаеновую кислоту (C22:5n-3) и докозагексаеновую кислоту (C22:6n-3). ДЦ-ПНЖК также включают жирные кислоты более чем с 22 атомами углерода и 4 или большим количеством двойных связей включая без ограничения C28:8(n-3).
Термин «ПНЖК-синтаза» в используемом в настоящем описании смысле относится к ферменту, который продуцирует полиненасыщенные жирные кислоты (ПНЖК), и в частности, длинноцепочечные ПНЖК (ДЦ-ПНЖК), а также к любому домену такого фермента в комплексе. Термин ПНЖК-синтаза включает без ограничения PKS-системы ПНЖК или PKS-подобные системы для получения ПНЖК. Некоторые конкретные ПНЖК-синтазы указаны в настоящем описании с использованием дополнительного обозначения, например, «SzPUFA»-синтаза или «hSzThPUFA»-синтаза, как определено в настоящей заявке. Термин «система ПНЖК-синтазы» включает ПНЖК-синтазу и любые вспомогательные ферменты, которые могут влиять на функцию ПНЖК-синтазы при экспрессии в гетерологичном организме (например, PPT-азу или ACS).
Термины «фосфопантетеинилтрансфераза» и «PPT-аза» в используемом в настоящем описании смысле относятся к ферменту, который активирует ПНЖК-синтазу в результате переноса кофактора (например, 4-фосфопантетеина) от кофермента A (CoA) на один или несколько доменов АПБ, присутствующих в ПНЖК-синтазе. Одним примером PPT-азы, которая может активировать один или несколько доменов ПНЖК-синтазы, описанной в настоящей публикации, является белок Het I вида Nostoc PCC 7120 (ранее называемого Anabaena sp. PCC 7120), обозначаемый в настоящем описании «NoHetI».
Термины «ацил-CoA-синтетаза», «ACoAS» и «ACS» в используемом в настоящем описании смысле относятся к ферменту, который катализирует превращение длинноцепочечных полиненасыщенных свободных жирных кислот (СЖК) в ацил-CoA. Некоторые конкретные ацил-CoA-синтетазы названы в настоящем описании с использованием дополнительного обозначения, например, «SzACS-2», как определено в настоящей заявке.
Термин «растение» в используемом в настоящем описании смысле включает любого его потомка, клетку, ткань, семя, масло из семян или часть.
«Нутрицевтик» означает продукт, выделенный, очищенный, сконцентрированный или полученный из растений, который полезен с физиологической точки зрения или обеспечивает защиту от заболевания, включая обработанные продукты питания с добавлением таких продуктов, а также продукты питания, полученные из культур, которые были генетически сконструированы так, чтобы они содержали повышенные уровни физиологически активных компонентов.
«Функциональный продукт питания» означает продукт питания, который (a) сходен по виду или может представлять собой обычный продукт питания, который потребляют в виде части обычной диеты и (b) обладает повышенной пищевой ценностью и/или специфической пищевой ценностью в результате модификации соотношения компонентов, которые обычно присутствуют в немодифицированном пищевом продукте.
Подразумевается, что термины «полинуклеотид» и «нуклеиновая кислота» охватывают одну нуклеиновую кислоту, а также множество нуклеиновых кислот, молекулу нуклеиновой кислоты или ее фрагмент, вариант или производное, или конструкцию, например, матричную РНК (мРНК) или плазмидную ДНК (пДНК). Полинуклеотид или нуклеиновая кислота может содержать нуклеотидную последовательность полноразмерной последовательности кДНК или ее фрагмент, включая нетранслируемые 5'- и 3'-последовательности и кодирующие последовательности. Полинуклеотид или нуклеиновая кислота могут состоять из любого полирибонуклеотида или полидезоксирибонуклеотида, которые могут представлять собой немодифицированную РНК или ДНК или модифицированную РНК или ДНК. Например, полинуклеотид или нуклеиновая кислота может состоять из однонитевой и двунитевой ДНК, из ДНК, которая является смесью однонитевых и двунитевых областей, одно- и двунитевой РНК и РНК, которая является смесью одно- и двунитевых областей, гибридных молекул, содержащих ДНК и РНК, которые могут быть однонитевыми или чаще двунитевыми, или смесью одно- и двунитевых областей. Указанные термины также охватывают химически, ферментативно или метаболически модифицированные формы полинуклеотида или нуклеиновой кислоты.
Полинуклеотид или последовательность нуклеиновой кислоты могут быть названы «изолированными», при этом они извлечены из своего природного окружения. Например, гетерологичный полинуклеотид или нуклеиновая кислота, кодирующая полипептид или полипептидный фрагмент, обладающий активностью дегидратазы дигидроксикислоты, находящаяся в векторе, считается изолированной в целях настоящего изобретения. Дополнительные примеры изолированного полинуклеотида или нуклеиновой кислоты включают рекомбинантные полинуклеотиды, находящиеся в гетерологичных клетках-хозяевах, или очищенный (частично или по существу) полинуклеотид или нуклеиновую кислоту в растворе. Изолированный полинуклеотид или нуклеиновая кислота согласно настоящему изобретению дополнительно включают такие молекулы, полученные в результате синтеза. Изолированный полинуклеотид или нуклеиновая кислота в форме полимера ДНК может состоять одного или нескольких участков кДНК, геномной ДНК или синтетической ДНК.
Термин «ген» относится к нуклеиновой кислоте или ее фрагменту, который способен экспрессироваться, давая конкретный белок, и необязательно содержит регуляторные последовательности, предшествующие (5'-некодирующие последовательности) и следующие (3'-некодирующие последовательности) за кодирующей последовательностью.
В используемом в настоящем описании смысле термин «кодирующая область» относится к последовательности ДНК, которая кодирует конкретную аминокислотную последовательность. «Подходящие регуляторные последовательности» относятся к нуклеотидным последовательностям, расположенным выше (5'-некодирующие последовательности), в пределах или ниже (3'-некодирующие последовательности) кодирующей последовательности, которые влияют на транскрипцию, процессинг или стабильность РНК или на трансляцию ассоциированной кодирующей последовательности. Регуляторные последовательности могут включать промоторы, лидерные последовательности трансляции, интроны, последовательности распознавания для полиаденилирования, участки процессинга РНК, участок связывания эффектора и структуру стебель-петля.
В используемом в настоящем описании смысле подразумевается, что термин «полипептид» охватывает отдельный «полипептид», а также множество «полипептидов» и их фрагменты, и относится к молекуле, состоящей из мономеров (аминокислот), линейно связанных амидными связями (также известными как пептидные связи). Термин «полипептид» относится к любой цепи или цепям из двух или более аминокислот и не относится к конкретной длине продукта. Таким образом, пептиды, дипептиды, трипептиды, олигопептиды, белок, цепь аминокислот или любой другой термин, используемый по отношению к цепи или цепям из двух или более аминокислот, включены в определение «полипептид», и термин «полипептид» может быть использован вместе или взаимозаменяемо с любым из указанных терминов. Полипептид может быть получен из природного биологического источника или может быть получен основанным на рекомбинации способом, но не обязательно транслирован с определенной последовательности нуклеиновой кислоты. Он может быть создан любым способом, включая химический синтез.
Под «изолированным» полипептидом или его фрагментом, вариантом или производным подразумевают полипептид, который не находится в своей природной среде. При этом не требуется конкретного уровня очистки. Например, изолированный полипептид может быть извлечен из нативного или природного окружения. Рекомбинантно полученные полипептиды и белки, экспрессированные в клетках-хозяевах, считают изолированными в целях настоящего изобретения, также как нативные или рекомбинантные полипептиды, которые были отделены, фракционированы или частично или по существу полностью очищены любым подходящим способом.
В используемом в настоящем описании смысле «нативный» относится к форме полинуклеотида, гена или полипептида, которые встречаются в природе, с их собственными регуляторными последовательностями, если таковые присутствуют.
В используемом в настоящем описании смысле «эндогенный» относится к нативной форме полинуклеотида, гена или полипептида в его природном окружении в организме или в геноме организма. «Эндогенный полинуклеотид» включает нативный полинуклеотид в его природном положении в геноме организма. «Эндогенный ген» включает нативный ген в его природном положении в геноме организма. «Эндогенный полипептид» включает нативный полипептид в его природном положении в организме.
В используемом в настоящем описании смысле «гетерологичный» относится к полинуклеотиду, гену или полипептиду, в норме не встречающемуся в организме хозяина, но который введен в организм хозяина. «Гетерологичный полинуклеотид» включает нативную кодирующую область или ее часть, которую повторно вводят в исходный организм в форме, которая отличается от соответствующего нативного полинуклеотида. «Гетерологичный ген» включает нативную кодирующую область или ее часть, которую повторно вводят в исходный организм в форме, которая отличается от соответствующего нативного гена. Например, гетерологичный ген может включать нативную кодирующую область, которая представляет собой часть химерного гена, включая ненативные регуляторные области, который повторно вводят в нативного хозяина. «Гетерологичный полипептид» включает нативный полипептид, который повторно вводят в исходный организм в форме, которая отличается от соответствующего нативного полипептида.
В используемом в настоящем описании смысле термин «модификация» относится к изменению полинуклеотида, раскрытого в настоящем описании, которое приводит к пониженной, по существу исключенной или исключенной активности полипептида, кодируемого полинуклеотидом, а также к изменению полипептида, раскрытого в настоящем описании, которое приводит к пониженной, по существу исключенной или исключенной активности полипептида. Такие изменения могут быть осуществлены способами, хорошо известными в данной области, включая без ограничения делецию, мутацию (например, спонтанный мутагенез, случайный мутагенез, мутагенез, вызываемый генами-мутаторами, или мутагенез, вызванный транспозонами), замену, инсерцию, понижающую регуляцию, изменение положения в клетке, изменение состояния полинуклеотида или полипептида (например, метилирование, фосфорилирование или убиквитинилирование), удаление кофактора, введение антисмысловой РНК/ДНК, введение интерферирующей РНК/ДНК, химическую модификацию, ковалентную модификацию, облучение УФ или рентгеновским излучением, гомологичную рекомбинацию, митотическую рекомбинацию, способы замены промоторов и/или сочетания указанных способов. Принципы определения того, какие нуклеотиды или аминокислотные остатки могут быть модифицированы, можно установить посредством сравнения последовательности конкретного полинуклеотида или полипептида с последовательностью гомологичных полинуклеотидов или полипептидов, например, дрожжевых или бактериальных, и максимизации количества модификаций, осуществляемых в областях с высокой гомологией (консервативных областях) или консенсусных последовательностях.
Термин «производное» в используемом в настоящем описании смысле относится к модификации последовательности, раскрытой в настоящем изобретении. Иллюстративными примерами таких модификаций могут быть замена, инсерция и/или делеция одного или нескольких оснований по сравнению с последовательностью нуклеиновой кислоты кодирующей последовательности, раскрытой в настоящем описании, которые сохраняют, в небольшой степени изменяют или повышают функцию кодирующей последовательности, раскрытой в настоящем описании, в данном виде масличной культуры. Такие производные легко могут быть определены специалистом в данной области, например, с использованием способов компьютерного моделирования для прогнозирования и оптимизации структуры последовательности. Термин «производное» также охватывает последовательности нуклеиновой кислоты, имеющие высокую гомологию последовательности с раскрытыми в настоящем описании кодирующими последовательностями, так чтобы они были способны выполнять описанные функции с целью применения для получения ДЦ-ПНЖК согласно настоящему изобретению.
В используемом в настоящем описании смысле термин «вариант» относится к полипептиду, отличающемуся от конкретно указанного полипептида согласно изобретению инсерциями, делециями, мутациями и заменами аминокислот, созданному с использованием, например, методики рекомбинантной ДНК, такой как мутагенез. Принципы определения того, какие аминокислотные остатки могут быть заменены, добавлены или делетированы без нарушения представляющих интерес активностей, можно установить посредством сравнения последовательности конкретного полипептида с последовательностью гомологичных полипептидов и максимизации количества аминокислотных изменений, осуществляемых в областях с высокой гомологией (консервативных областях), или замены аминокислот консенсусными последовательностями.
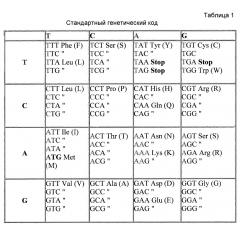
Альтернативно рекомбинантные варианты полинуклеотида, кодирующие такие же или сходные полипептиды, могут быть синтезированы или отобраны с использованием «вырожденности» генетического кода. Могут быть введены различные замены кодонов, такие как молчащие изменения, которые приводят к появлению различных сайтов рестрикции, чтобы оптимизировать клонирование в плазмидном или вирусном векторе для экспрессии. Мутации в полинуклеотидной последовательности могут быть отражены в виде добавления к полипептиду другого полипептида или доменов других пептидов, чтобы модифицировать свойства любой части полипептида.
Аминокислотные «замены» могут быть результатом замены одной аминокислоты другой аминокислотой, имеющей сходные структурные и/или химические свойства, т.е. результатом консервативных аминокислотных замен, или они могут быть результатом замены одной аминокислоты аминокислотой, имеющей другие структурные и/или химические свойства, т.е. результатом неконсервативных аминокислотных замен. «Консервативные» аминокислотные замены могут быть осуществлены на основе сходства полярности, заряда, растворимости, гидрофобности, гидрофильности или амфипатической природы используемых остатков. Например, неполярные (гидрофобные) аминокислоты включают аланин, лейцин, изолейцин, валин, пролин, фенилаланин, триптофан и метионин; полярны