Универсальная питательная среда для изолирования микобактериоподобных микроорганизмов
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Универсальная питательная среда для культивирования коринебакетрий, нокардий и родококков содержит панкреатический гидролизат кильки, Д- глюкозу, KH2PO4, MgSO4, водный голубой, натрий углекислый, агар микробиологический, геотермальная вода, стерильная деффибринированная кровь животных и парафин в заданном соотношении компонентов. Изобретение позволяет повысить дифференцирующие и ингибирующие свойства питательной среды. 2 табл.
Реферат
Изобретение рекомендуется использовать в бактериологических лабораториях для культивирования микобактериоподобных микроорганизмов, в частности коринебактерий, нокардий и родококов, сенсибилизирующих по многочисленным данным организм животных к туберкулину.
Накопленные на сегодняшний день данные по лабораторному выявлению указанных микроорганизмов не позволяют определить универсальную, простую в изготовлении, доступную и эффективную питательную среду для культивирования, поэтому для повышения результативности приходиться пользоваться несколькими средами. Нередко при выборе сред исходят из лабораторных возможностей, доступности сред, пренебрегая при этом диагностическими свойствами [1, 5, 7].
Для изолирования коринебактерий используют питательные среды: нитритный агар по Виноградскому, среда Сотона, кровяной агар, кровяно-теллуритовый агар, среда Клауберг II, среда Бучина [1, 7], для нокардий и родококков, среда Мюнца, УМ-агар, среда с овсяной мукой, декстрозный агар, питательный бульон [5, 6].
Нитритный агар по Виноградскому [2] с н-алканами (гексодекан C16H34) в количестве 2% и синтетическая среда Сотона с добавлением 2%-ой смеси углеводородов имеют существенные недостатки. Углеводороды имеют разные температурные параметры кипения, в связи с чем стерилизовать в термостате их приходиться по отдельности при разных температурных режимах, что создает определенные трудности при их подготовке. Кроме того, среды отличаются слабыми ростовыми свойствами.
Кровяной агар, состоящий из расплавленного и охлажденного до 45-50°С питательного агара и 5-10% дефибринированной или цельной свежи взятой крови животного, имеет низкие ингибирующие свойства по отношению к сопутствующей микрофлоре.
Указанные недостатки относятся и к кровяно-теллуритовому агару, отличающемуся от кровяного агара наличием 2 мл 2% раствора теллурита калия (K2TeO3).
Среда Клауберг II, отличается сложностью в изготовлении. Химически чистый глицерин, требуемый для приготовления глицериновой смеси, необходимо стерилизовать при 110°С в течение 30 минут. Изготовление среды осложняется еще и тем, что нужно предварительно приготовить лаковую кровь из дистиллированной воды и дефибринированной крови животного, что сопряжено с дополнительными расходами и временем. Видимые колонии на данной среде появляются не раньше 48 ч.
Сывороточный агар, состоящий из питательной среды с 10-15% лошадиной или бычьей стерильной сывороткой, имеет низкие дифференцирующие свойства на фоне обильного роста сопутствующей микрофлоры.
Сухая хинозольная среда Бучина [4], характеризуется низкой высеваемостью. Среда содержит 2 вида минеральных солей, что по нашему мнению недостаточно для качественного обеспечения углеводородокисляющих микроорганизмов необходимыми факторами роста а также микро- и макроэлементами [1, 6].
Среда Мюнца для выделения и выращивания нокардий и родококков, с добавлением парафиновой приманки, обладает слабыми ростовыми свойствами.
Низкими ингибирующими свойствами характеризуются среды УМ-агар и питательный бульон.
Среда с овсяной мукой и декстрозный агар не отличаются диагностической ценностью из-за низкой высеваемости, а также обильным ростом посторонней микрофлоры.
С учетом вышесказанного, при конструировании универсальной питательной среды мы исходили из содержания в среде пластического материала (азот, углерод, водород, кислород) для построения тела микробных клеток, источника энергий (Д-глюкоза), а также минимального количество микроэлементов, участвующих в образовании коферментов. Кроме основных компонентов (пластических и энергетических) для нормального развития микроорганизмам необходим «фактор роста», которыми являются парафин, агар микробиологический и дефибринированная кровь животных.
Воду (дистиллированную), как основной растворитель питательных веществ, мы заменили на геотермальную (с минерализацией 5,02 г/л), в том числе и в целях расширения солевого состава среды, что позволить качественно обеспечить среду минеральными солями, анионами, катионами и тд.
Расширенный лабораторный анализ геотермальной воды (фотометрия, потенциометрия, атомно-абсорбционная спектрометрия, комплексометрия и тд.) показал качественное и количественное отличие данной воды от дистиллированной по микро- и макроэлементам. Суммарное значение составляло: анионов - 1,6771 г/л (NH4, Na, K, Mg, Са, Sr, Fe, Mn, Zn, Cu, Ni), катионов - 3,4732 г/л (Cl, Br, I, SO4, HCO3, HPO4, NO3). Кроме того, в геотермальной воде содержится нейтральные и кислые битумы (2,5 мг/л), гумусовые вещества (7,1 мг/л) как источник углеводородов. Для углеводородокисляющих микроорганизмов, к которым относятся коринебактерий, нокардий и родококки, такой источник является стимулом повышения ростовых свойств, предлагаемой среды [3, 5, 6, 7].
Наиболее близким к заявляемой среде являются:
- для выделения коринебактериии, сухая хинозольная среда Бучина (панкреатический гидролизат кильки - 30,6 г; натрия хлорид - 5,0±0,05 г; д-глюкоза - 15,0 г; водный голубой - 0,25 г; натрий углекислый - 0,4±0,05 г; агар микробиологический - 8,0±1,0 г (PH 7,4±0,2); дистиллированная вода - до 1 литра; 5% стерильная дефибринированая кровь человека или животных).
- для нокардий и родококков, среда Мюнца (KNO3 - 1 г, MgSO4 - 0,1 г, Na2HPO4 - 0,6 г, KH2PO4 - 0,14 г, NaCl - 1,0 г, водопроводная вода - 0,5 л, вода дистиллированная - 0,5 л, рН - (6,8-7) - подводят кислотой.
К недостаткам данных сред относятся слабые ростовые и низкие ингибирующие постороннюю микрофлору свойства.
Цель изобретения: разработка универсальной питательной среды для культивирования коринебактерий, нокардии и родококов, характеризующейся диагностической ценностью и практической значимостью.
Для достижения поставленной цели взяли панкреатический гидролизат кильки - 31,7 г, д-глюкозу - 16,0 г, KH2PO4 - 0,17 г, MgSO4 - 0,2 г, водный голубой - 0,28 г, натрий углекислый - 0,3 г ± 0,05, агар микробиологический - 8,1 г ± 1,0 (рН 7,4±0,2), добавили геотермальную воду до 1 л и стерильную дефибринированную кровь животных - 5%. В процессе размешивания, не допуская образования пены, вносили 4-5 капель парафина, разлили в чашки Петри. После застывания среду слегка подсушили в термостате при температуре 37±1°С в течение 40-60 мин. Цвет готовой среды темно-синий. Хранили в холодильнике, использовали в течение 3-4 сут.
Сопоставительный анализ с прототипами позволяет сделать вывод, что заявляемый состав среды отличается от известных, подбором минимального количество компонентов для построения тела углеводородокисляющими микроорганизмами (азот, углерод, водород, кислород) - пластический материал, парафин - фактор роста, (д-глюкоза) - источник энергий, кроме того, заменой дистиллированной воды геотермальной и расширением солевого состава за счет большего содержания микро- и макроэлементов в геотермальной воде. Таким образом, заявляемое техническое решение соответствует критерию «новизна».
При экспериментальной проверке были испытаны среды, наиболее часто используемые для культивирования коринебактерий, нокардий и родококков. Среды готовили по прописи авторов [2].
Оценку сред проводили посевом тест-штаммов и свежевыделенных культур коринебактерий, нокардий и родококков. В качестве музейного штамма использовали Corynebacterium xerosis N1911, N. asteroides ВКМ Ac 1077 и R. bronchialis ИМВ Ac 737. а нативным материалом служили лабораторные штаммы, выделенные из объектов внешней среды (почва, корма, навоз и кровь крупного рогатого скота).
Культуру каждого штамма высевали в 8 чашках Петри каждой среды. Коринебактерии на нитритный агар по Виноградскому, среду Сотона, кровяной агар, кровяно-теллуритовый агар, среду Клауберг II, среду Бучина и на универсальную среду. Нокардии и родококки - среду Мюнца, УМ-агар, среду с овсяной мукой, дакстрозный агар, питательный бульон, универсальная среда.
Для соблюдения равнозначности опыта материал высевали равными дозами (500 клеток в 0,1 мл). При учете результатов провели сравнительный анализ эффективности сред изучаемых образцов с предлагаемым по скорости и интенсивности роста, по величине колоний и ингибирующим к сопутствующей микрофлоре свойствам. Результаты учитывали через 24 и 48 ч. Опыты повторялись двукратно.
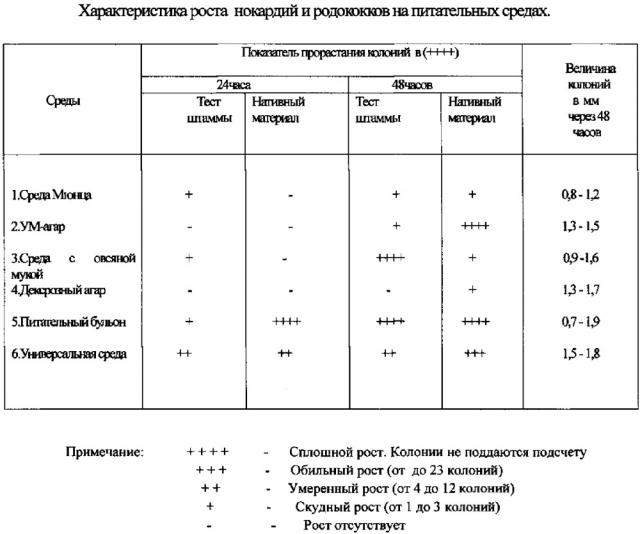
По результатам проведенных исследований, среда Мюнца и декстрозный агар показали низкие ростовые свойства 1-2 колонии. Низкие ингибирующие постороннюю микрофлору свойства обнаружили на среде с овсяной мукой, аналогичная картина на УМ-агаре, на фоне слабых ростовых свойств (Табл. 1)
На питательном бульоне колонии не поддаются подсчету из-за обильного роста посторонней микрофлоры.
На универсальной среде обнаружили умеренный рост на первые сутки с тест-штаммами и с нативным материалом - до 12 колонии, на вторые сутки - до 23 колонии в чашках с нативным материалом, но фоне хороших ингибирующих постороннюю микрофлору свойств.
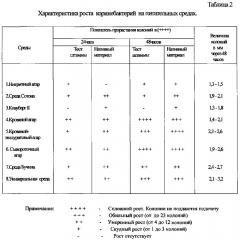
Рост колоний на среде Бучина формировался на первые сутки от 1 до 3 колоний с тест-штаммами и умеренным ростом с нативным материалом от 4 до 12 колоний (Табл. 2). На вторые сутки количество колоний в чашках с тест-штаммами увеличилось до 12 колоний.
По ростовым свойствам кровяной и кровяно-теллуритовые агары не уступают среде Бучина, но рост колоний формировался на фоне низких ингибирующих свойств по отношению к сопутствующей микрофлоре.
Низкими дифференцирующими свойствами обладает и сывороточный агар, где обнаружили обильный рост сопутствующей микрофлоры на вторые сутки.
Эффективность нитритного агара и Клауберг II была самой низкой. Слегка заметный рост обнаружили на средах через 48 ч.
Слегка заметное помутнение обнаружили на среде Сатона, на вторые сутки картина практически не изменилось.
Предлагаемая среда показала высокие дифференцирующие и ингибирующие свойства. Колонии появились на первые сутки в количестве от 4 до 12 в чашках с тест-штаммами и с нативным материалом. На вторые сутки обнаружили обильный рост в обеих чашках до 23 колонии, без сопутствующей микрофлоры, что является показателем высокой ингибирующей активности. Рост отличался не только числом, но и характером и размером колонии.
Выводы. Таким образом, проведенные исследования показали, что универсальная среда (М-10), для микобактериоподобных микроорганизмов обладает хорошими ростовыми свойствами на фоне высокой активности ингибирующей постороннюю микрофлору свойств. Кроме того, среда отличается от остальных вариантов по массивности выросших колоний, что в конечном итоге является показателем диагностической ценности и практической значимости универсальной среды.
Литература
1. Баратов М.О. Сравнительное изучение наиболее часто используемых сред для выделения коринебактерий / М.О. Баратов, М.М. Ахмедов О.П. Сакидибиров // Материалы Всероссийской науч.-практ. конф. « Повышение продуктивности с/х. животных и птицы на основе инновационных достижений». - 2009 г. - Новочеркасск – С. 64-67.
2. Биргер М.О. Справочник по микробиологическим и вирусологическим методам исследования / М.О. Биргер, Е.А. Ведьмина, В.В. Влодавец // - М: Медицина, 1985. - 261 с.
3. Высоцкий В.В. Сравнительное электронно-микроскопическое изучение 8 представителей рода Corynebacterium, выращенных на твердой питательной среде в стационарной фазе развития / В.В. Высоцкий, И.К. Мазурова, Е.А. Шмелева // Микробиология. - 1976. - №7. - С. 121-125.
4. Меджидов М.М. Сухие микробиологические питательные среды / Меджидов М.М. и др. // - Каталог. - Махачкала, 1998, 78 с.
5. Нуратинов Р.А. Кислотоустойчивые микроорганизмы - микобактерии, нокардии, родококки: химический состав, биологические свойства, антигенная структура / Р.А. Нуратинов и др. // Проблемы туберкулеза. - 2001. - №5. - С. 54-58.
6. Нестеренко O.A. Нокардиоподобные и коринеподобные бактерии / О.А. Нестеренко // - Киев: Наукова Думка, 1985. С. 320-333.
7. Шапелева Р.Г. Сравнительное изучение питательных сред для выделения коринебактерий / Р.Г. Шапелева, З.Г. Андреева, Г.П. Сокольникова // Журнал микробиология. - 1989. - №5. – С. 62-64.
Универсальная питательная среда для культивирования коринебактерий, нокардий и родококков, содержащая панкреатический гидролизат кильки, Д-глюкозу, KH2PO4, MgSO4; водный голубой, натрий углекислый, агар микробиологический, геотермальную воду, стерильную дефибринированую кровь животных и парафин, при следующем соотношении компонентов:
| Панкреатический гидролизат кильки | 31,7 г |
| Д-глюкоза | 16,0 г |
| KH2PO4 | 0,17 г |
| MgSO4 | 0,2 г |
| Водный голубой | 0,28 г |
| Натрий углекислый | 0,3 г ± 0,05 |
| Агар микробиологический | 8,1 г ± 1,0 (рН 7,4±0,2) |
| Геотермальная вода | до 1 литра |
| стерильная дефибринированная кровь животных | 5% |
| Парафин | 4-5 капель |