Способы гликоконъюгирования и композиции
Иллюстрации
Показать всеГруппа изобретений относится к медицине, в частности к области вакционопрофилактики, и раскрывает способ получения гликоконъюгата, содержащего бактериальный капсульный полисахарид, конъюгированный с белком-носителем через (2-((2-оксоэтил)тио)этил)карбаматный (еТЕС) спейсер, гликоконъюгат, полученный указанным способом, и иммуногенную композицию, содержащую указанный гликоконъюгат. Изобретения позволяют получать соответствующим образом блокированные конъюгаты на основе белка-носителя, у которых поддерживаются функциональные свойства носителя и сам конъюгат сохраняет способность вызывать желаемый иммунный ответ. 3 н. и 13 з.п. ф-лы, 15 табл., 9 пр., 8 ил.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение в целом относится к гликоконъюгатам, содержащим сахарид, ковалентно конъюгированный с белком-носителем через (2-((2-оксоэтил)тио)этил)карбаматный (еТЕС) спейсер, к иммуногенным композициям, содержащим такие гликоконъюгаты, и к способам получения и применения таких гликоконъюгатов и иммуногенных композиций.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Подход к повышению иммуногенности слабо иммуногенных молекул посредством конъюгирования этих молекул с молекулами «носителя» успешно используется на протяжении нескольких десятилетий (см., например, Goebel et al. (1939) J. Exp. Med. 69:53). Например, описаны многие иммуногенные композиции, в которых очищенные капсульные полимеры были конъюгированы с белками-носителями для создания более эффективных иммуногенных композиций с использованием этого «эффекта носителя» (Schneerson et al. (1984) Infect. Immun. 45: 582-591). Также было показано, что конъюгирование позволяет обойти слабый антительный ответ, обычно наблюдаемый у младенцев при иммунизации свободным полисахаридом (Anderson et al. (1985) J. Pediatr. 107: 346; Insel etal. (1986) J. Exp. Med. 158: 294).
Успешно получены конъюгаты с использованием различных сшивающих агентов или агентов сочетания, таких как гомобифункциональные, гетеробифункциональные сшивающие агенты или сшивающие агенты «нулевой длины». В настоящее время известно много способов сочетания иммуногенных молекул, таких как сахариды, белки и пептиды, с пептидными или белковыми носителями. В большинстве способов создаются аминные, амидные, уретановые, изотиомочевинные или дисульфидные связи или в некоторых случаях простые тиоэфирные связи. Недостатком использования сшивающих агентов или агентов сочетания, при котором в боковые цепи реакционно-способных молекул аминокислот носителя и/или иммуногенных молекул вводятся реакционно-способные сайты, является то, что реакционно-способные сайты, если они не нейтрализованы, могут свободно реагировать с любой нежелательной молекулой либо in vitro (возможно негативно влияя, таким образом, на функциональные свойства или стабильность конъюгатов), либо in vivo (обуславливая, таким образом, возможный риск побочных эффектов у лиц или животных, иммунизированных данными препаратами). Такой избыток реакционно-способных сайтов может быть модифицирован или «блокирован (capped)» с целью инактивации этих сайтов с использованием различных известных химических реакций, но сами эти реакции могут оказаться по иным причинам разрушительными для функциональных свойств конъюгатов. Это может быть особенно проблематичным при попытке создания конъюгата путем введения реакционно-способных сайтов в молекулу носителя, поскольку ее более существенный размер и более сложная структура (по сравнению с иммуногенной молекулой) может делать ее более уязвимой к разрушительным последствиям химической обработки. Таким образом, сохраняется необходимость в новых способах получения соответствующим образом блокированных конъюгатов на основе белка-носителя, у которых поддерживаются функциональные свойства носителя и сам конъюгат сохраняет способность вызывать желаемый иммунный ответ.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на способы получения гликоконъюгатов, содержащих сахарид, ковалентно конъюгированный с белком-носителем через бивалентный гетеробифункциональный линкер, называемый в данном описании как (2-((2-оксоэтил)тио)этил)карбаматный (еТЕС) спейсер. Этот еТЕС спейсер представляет собой структуру, линейная часть которой состоит из семи атомов (т.е. -C(O)NH(CH2)2SCH2C(O)-), и обеспечивает образование стабильной тиоэфирной и амидной связей между сахаридом и белком-носителем. Согласно изобретению также предложены соединенные через еТЕС гликоконъюгаты (еТЕС linked glycoconjugates), иммуногенные композиции, содержащие их, и способы применения таких гликоконъюгатов и иммуногенных композиций.
В одном из аспектов изобретения предложен гликоконъюгат, содержащий сахарид, конъюгированный с белком-носителем через еТЕС спейсер, при этом сахарид ковалентно связан с еТЕС спейсером через карбаматную связь, а белок-носитель ковалентно связан с еТЕС спейсером через амидную связь.
В некоторых воплощениях сахарид представляет собой полисахарид, такой как капсульный полисахарид, имеющий происхождение из бактерий, в частности из патогенных бактерий. В других воплощениях сахарид представляет собой олигосахарид или моносахарид.
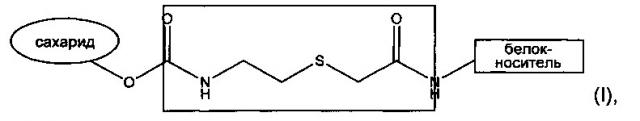
Соединенные через еТЕС гликоконъюгаты по изобретению могут быть представлены общей формулой (I):
где атомы, составляющие еТЕС спейсер, помещены в центральный блок.
Белки-носители, введенные в гликоконъюгаты по изобретению, выбраны из группы белков-носителей, обычно подходящих для таких целей, которые описаны далее в данном изобретении или известны специалистам в данной области техники. В конкретных воплощениях белок-носитель представляет собой CRM197 (перекрестно-реагирующий материал (cross-reactive material; CRM)).
В другом аспекте изобретения предложен способ получения гликоконъюгата, содержащего сахарид, конъюгированный с белком-носителем через еТЕС спейсер, включающий стадии: а) приведения во взаимодействие сахарида с производным угольной кислоты в органическом растворителе с получением активированного сахарида; б) приведения во взаимодействие активированного сахарида с цистамином или цистеамином либо их солью с получением тиолированного сахарида; в) приведения во взаимодействие тиолированного сахарида с восстанавливающим агентом с получением активированного тиолированного сахарида, содержащего один или более свободных сульфгидрильных остатков; г) приведения во взаимодействие активированного тиолированного сахарида с активированным белком-носителем, содержащим одну или более α-галогенацетамидных групп, с получением конъюгата (тиолированный сахарид)-(белок-носитель); и д) приведения во взаимодействие конъюгата (тиолированный сахарид)-(белок-носитель) с (1) первым блокирующим реагентом, способным блокировать неконъюгированные α-галогенацетамидные группы активированного белка-носителя; и/или (2) вторым блокирующим реагентом, способным блокировать неконъюгированные свободные сульфгидрильные остатки активированного тиолированного сахарида; с образованием таким образом соединенного через еТЕС гликоконъюгата.
Во многих воплощениях производное угольной кислоты представляет собой 1,1'-карбонил-ди-(1,2,4-триазол) (CDT) или 1,1'-карбонилдиимидазол (CDI). Предпочтительно производное угольной кислоты представляет собой CDT, а органический растворитель представляет собой полярный апротонный растворитель, такой как диметилсульфоксид (DMSO). В предпочтительных воплощениях тиолированный сахарид получают путем взаимодействия активированного сахарида с бифункциональным симметричным тиоалкиламинным реагентом цистамином или его солью. Альтернативно, тиолированный сахарид может быть получен путем взаимодействия активированного сахарида с цистеамином или его солью. Соединенные через еТЕС гликоконъюгаты, полученные способами по изобретению, могут быть представлены общей формулой (I).
Во многих воплощениях первым блокирующим реагентом является N-ацетил-L-цистеин, который взаимодействует с неконъюгированными α-галогенацетамидными группами на остатках лизина белка-носителя с образованием остатка S-карбоксиметилцистеина (CMC), ковалентно связанного с активированным остатком лизина посредством тиоэфирной связи. В других воплощениях вторым блокирующим реагентом является йодоацетамид (IAA), который взаимодействует с неконъюгированными свободными сульфгидрильными группами активированного тиолированного сахарида с получением блокированного тиоацетамида. Часто стадия д) включает блокирование с использованием как первого блокирующего реагента, так и второго блокирующего реагента. В некоторых воплощениях стадия д) включает блокирование с применением N-ацетил-L-цистеина в качестве первого блокирующего реагента и IAA в качестве второго блокирующего реагента.
В некоторых воплощениях стадия блокирования д) дополнительно включает взаимодействие с восстанавливающим агентом, например, DTT (дитиотреитол), ТСЕР (трис(2-карбоксиэтил)фосфин) или меркаптоэтанолом, после взаимодействия с первым и/или вторым блокирующим реагентом.
В некоторых воплощениях стадия г) дополнительно включает получение активированного белка-носителя, содержащего одну или более α-галогенацетамидных групп, с последующим приведением во взаимодействие активированного тиолированного сахарида с активированным белком-носителем. Во многих воплощениях активированный белок-носитель содержит одну или более α-бромацетамидных групп.
В другом аспекте изобретения предложен соединенный через еТЕС гликоконъюгат, содержащий сахарид, конъюгированный с белком-носителем через еТЕС спейсер, полученный в соответствии с любым из способов, раскрытых в данном описании.
Для каждого из аспектов изобретения, в конкретных воплощениях способов и композиций, изложенных в данном описании, соединенный через еТЕС гликоконъюгат содержит сахарид, который представляет собой бактериальный капсульный полисахарид, в частности капсульный полисахарид, имеющий происхождение из патогенных бактерий.
В некоторых таких воплощениях соединенный через еТЕС гликоконъюгат содержит пневмококковый (Pn) капсульный полисахарид, имеющий происхождение из Streptococcus pneumoniae. В конкретных воплощениях данный Pn капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Pn-серотипов 1, 3, 4, 5, 6А, 6В, 7F, 8, 9V, 10А, 11А, 12F, 14, 15В, 18С, 19А, 19F, 22F, 23F и 33F.
В других таких воплощениях соединенный через еТЕС гликоконъюгат содержит менингококковый (Mn) капсульный полисахарид, имеющий происхождение из Neisseria meningitidis. В конкретных воплощениях данный Mn капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Mn-серотипов А, С, W135 и Y.
В особо предпочтительных воплощениях сахарид представляет собой бактериальный капсульный полисахарид, такой как Pn или Mn капсульный полисахарид, ковалентно конъюгированный с CRM197 через еТЕС спейсер.
Композиции и способы, изложенные в данном описании, полезны для различных приложений. Например, гликоконъюгаты по изобретению можно использовать для получения иммуногенных композиций, содержащих соединенный через еТЕС гликоконъюгат. Такие иммуногенные композиции можно использовать для защиты реципиентов от бактериальных инфекций, например, вызываемых патогенными бактериями, такими как S. pneumoniae или N. meningitidis.
Таким образом, в другом аспекте изобретения предложена иммуногенная композиция, содержащая соединенный через еТЕС гликоконъюгат и фармацевтически приемлемый эксципиент, носитель или разбавитель, при этом гликоконъюгат содержит сахарид, ковалентно конъюгированный с белком-носителем через еТЕС спейсер, как изложено в данном описании.
Во многих воплощениях иммуногенная композиция содержит соединенный через еТЕС гликоконъюгат и фармацевтически приемлемый эксципиент, носитель или разбавитель, при этом гликоконъюгат содержит бактериальный капсульный полисахарид.
В некоторых таких воплощениях иммуногенная композиция содержит соединенный через еТЕС гликоконъюгат, который содержит Pn капсульный полисахарид, имеющий происхождение из S. pneumoniae. В некоторых конкретных воплощениях данный Pn капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Pn-серотипов 1, 3, 4, 5, 6А, 6В, 7F, 8, 9V, 10А, 11А, 12F, 14, 15В, 18С, 19А, 19F, 22F, 23F и 33F.
В других таких воплощениях иммуногенная композиция содержит соединенный через еТЕС гликоконъюгат, который содержит Mn капсульный полисахарид, имеющий происхождение из N. meningitidis. В некоторых конкретных воплощениях данный Mn капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Mn-серотипов А, С, W135 и Y.
В предпочтительных воплощениях иммуногенная композиция содержит соединенный через еТЕС гликоконъюгат, который содержит бактериальный капсульный полисахарид, такой как Pn или Mn капсульный полисахарид, ковалентно конъюгированный с CRM197 через еТЕС спейсер.
В некоторых воплощениях иммуногенные композиции содержат адъювант. В некоторых таких воплощениях адъювант представляет собой адъювант на основе алюминия, выбранный из группы, состоящей из фосфата алюминия, сульфата алюминия и гидроксида алюминия. В одном воплощении иммуногенные композиции, изложенные в данном описании, содержат в качестве адъюванта фосфат алюминия.
В другом аспекте изобретения предложен способ предупреждения, лечения или уменьшения интенсивности бактериальной инфекции, заболевания или состояния у субъекта, включающий введение субъекту иммунологически эффективного количества иммуногенной композиции по изобретению, которая содержит соединенный через еТЕС гликоконъюгат, содержащий бактериальный антиген, такой как бактериальный капсульный полисахарид.
В одном воплощении инфекция, заболевание или состояние ассоциированы с бактериями S. pneumoniae, и гликоконъюгат содержит Pn капсульный полисахарид. В другом воплощении инфекция, заболевание или состояние ассоциированы с бактериями N. meningitidis, и гликоконъюгат содержит Mn капсульный полисахарид.
В других аспектах изобретения предложен способ индуцирования иммунного ответа против патогенных бактерий; способ предупреждения, лечения или уменьшения интенсивности заболевания или состояния, вызванного патогенными бактериями; и способ снижения тяжести по меньшей мере одного симптома инфекции, заболевания или состояния, вызванного патогенными бактериями, в каждом случае путем введения субъекту иммунологически эффективного количества иммуногенной композиции, содержащей соединенный через еТЕС гликоконъюгат и фармацевтически приемлемый эксципиент, носитель или разбавитель, при этом гликоконъюгат содержит бактериальный антиген, такой как бактериальный капсульный полисахарид, имеющий происхождение из патогенных бактерий.
В другом аспекте изобретения предложен способ индуцирования иммунного ответа у субъекта, включающий введение субъекту иммунологически эффективного количества иммуногенной композиции, содержащей соединенный через еТЕС гликоконъюгат и фармацевтически приемлемый эксципиент, носитель или разбавитель, при этом гликоконъюгат содержит бактериальный антиген, такой как бактериальный капсульный полисахарид. В предпочтительных воплощениях способ включает вызывание защитного иммунного ответа у субъекта, как далее изложено в данном описании.
В другом аспекте изобретения предложен способ введения субъекту иммунологически эффективного количества иммуногенной композиции, содержащей соединенный через еТЕС гликоконъюгат, для вызывания защитного иммунного ответа у субъекта, как далее изложено в данном описании.
В следующем аспекте изобретения предложено антитело, выработанное в ответ на соединенный через еТЕС гликоконъюгат по настоящему изобретению или на иммуногенную композицию, содержащую такой гликоконъюгат. Подобные антитела можно использовать в исследованиях и клинических лабораторных анализах, таких как обнаружение и серотипирование бактерий, или можно использовать для придания пассивного иммунитета субъекту.
В еще одном аспекте изобретения предложена иммуногенная композиция, содержащая соединенный через еТЕС гликоконъюгат по настоящему изобретению, для применения в предупреждении, лечении или уменьшении интенсивности бактериальной инфекции, например инфекции, вызванной S. pneumoniae или N. meningitidis.
В другом аспекте изобретения предложено применение иммуногенной композиции, содержащей соединенный через еТЕС гликоконъюгат по настоящему изобретению, для изготовления лекарственного средства для предупреждения, лечения или уменьшения интенсивности бактериальной инфекции, например инфекции, вызванной S. pneumoniae или N. meningitidis.
В некоторых предпочтительных воплощениях терапевтических и/или профилактических способов и применений, описанных выше, иммуногенная композиция содержит соединенный через еТЕС гликоконъюгат, содержащий бактериальный капсульный полисахарид, ковалентно связанный с белком-носителем через еТЕС спейсер. Во многих воплощениях способов и применений, изложенных в данном описании, бактериальный капсульный полисахарид представляет собой Pn капсульный полисахарид или Mn капсульный полисахарид. В некоторых таких воплощениях Pn капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Pn-серотипов 1, 3, 4, 5, 6А, 6В, 7F, 8, 9V, 10А, 11А, 12F, 14, 15В, 18С, 19А, 19F, 22F, 23F и 33F. В других таких воплощениях Mn капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Mn-серотипов А, С, W135 и Y.
В некоторых предпочтительных воплощениях белок-носитель представляет собой CRM197. В особо предпочтительных воплощениях иммуногенная композиция содержит соединенный через еТЕС гликоконъюгат, содержащий бактериальный капсульный полисахарид, такой как Pn или Mn капсульный полисахарид, ковалентно конъюгированный с CRM197 через еТЕС спейсер.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 показана общая схема получения соединенных через еТЕС гликоконъюгатов по изобретению для гликоконъюгата, содержащего полисахарид, ковалентно конъюгированный с CRM197.
На Фиг. 2 показана повторяющаяся полисахаридная структура капсульного полисахарида S. pneumoniae серотипа 33F (Pn-33F).
На Фиг. 3 показана повторяющаяся полисахаридная структура капсульного полисахарида S. pneumoniae серотипа 22F (Pn-22F).
На Фиг. 4 показана повторяющаяся полисахаридная структура капсульного полисахарида S. pneumoniae серотипа 10А (Pn-10А).
На Фиг. 5 повторяющаяся полисахаридная структура капсульного полисахарида S. pneumoniae серотипа 11А (Pn-11А).
На Фиг. 6 показана репрезентативная структура гликоконъюгата Pn-33F, в состав которого входит еТЕС линкер (А) и возможно блокированные и неблокированные свободные сульфгидрильные сайты (Б).
На Фиг. 7 показана блок-схема репрезентативных способов для процессов активации (А) и конъюгирования (Б), использованных при получении гликоконъюгата Pn-33F с CRM197.
На Фиг. 8 показан уровень тиолирования капсульного полисахарида Pn-33F как функция числа молярных эквивалентов CDT, использованного на стадии активации.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретение может быть более легко понято со ссылкой на следующее далее подробное описание предпочтительных воплощений изобретения и примеров, включенных в данное описание. Если не указано иное, все технические и научные термины, использованные в данном описании, имеют значение, обычно понимаемое средним специалистом в области техники, к которой данное изобретение относится. Хотя при практическом применении или тестировании настоящего изобретения можно использовать любые способы и материалы, аналогичные или эквивалентные изложенным в данном описании, некоторые предпочтительные способы и материалы приведены в данном описании. При описании воплощений и составлении формулы изобретения будет использована определенная терминология в соответствии с изложенными ниже определениями.
Как использовано в данном описании, формы единственного числа включают ссылки на множественное число, если не указано иное. Так, например, ссылки на «способ» включают в себя один или более способов и/или стадий изложенного в данном описании типа, а ссылки на «еТЕС спейсер» относятся к одному или более чем одному еТЕС спейсеру, как будет очевидно среднему специалисту в данной области техники после прочтения данного описания.
Использованный в данном описании термин «примерно» означает нахождение в пределах статистически значимого диапазона величины, такой как установленный диапазон концентраций, период времени, молекулярная масса, температура или рН. Такой диапазон по порядку величины может находиться в типичном случае в пределах 20%, в более типичном случае в пределах 10% и в еще более типичном случае в пределах 5% указанной величины или диапазона. В некоторых случаях такой диапазон может находиться в пределах экспериментальной ошибки, типичной для стандартных методов, используемых для измерения и/или определения заданной величины или диапазона. Допустимое отклонение, охватываемое термином «примерно», будет зависеть от конкретной исследуемой системы и может быть легко оценено специалистом средней квалификации в данной области техники. В тех случаях, когда в данной заявке приводится диапазон, каждое целое число в пределах данного диапазона также рассматривается как воплощение изобретения.
Следует отметить, что использованные в данном описании такие термины, как «содержит», «содержал», «содержащий», «включает», «включающий» и им подобные, могут иметь значение, приписываемое им в патентном законе США; например, они могут означать «включает в себя», «включал в себя», «включающий в себя» и тому подобное. Такие термины подразумевают включение конкретных ингредиентов или набора ингредиентов без исключения любых других ингредиентов. Такие термины, как «состоящий по существу из» и «состоит по существу из», имеют значение, приписываемое им в патентном законе США; например, они позволяют включение дополнительных ингредиентов или стадий, которые не умаляют новые или основные характеристики изобретения, т.е. они исключают дополнительные неперечисленные ингредиенты или стадии, которые умаляют новые или основные характеристики изобретения. Термины «состоит из» и «состоящий из» имеют значение, приписываемое им в патентном законе США; а именно то, что эти термины являются закрытыми. Соответственно эти термины подразумевают включение конкретного ингредиента или набора ингредиентов и исключение всех других ингредиентов.
Термин «сахарид», использованный в данном описании, может относиться к полисахариду, олигосахариду или моносахариду. Часто ссылки на сахарид относятся к бактериальному капсульному полисахариду, в частности к капсульным полисахаридам, имеющим происхождение из патогенных бактерий, таких как S. pneumoniae или N. meningitidis.
Термины «конъюгат» или «гликоконъюгат» используются взаимозаменяемо в данном описании и относятся к сахариду, ковалентно конъюгированному с белком-носителем. Гликоконъюгаты по настоящему изобретению в некоторых случаях обозначены в данном описании как «соединенные через еТЕС» гликоконъюгаты, которые содержат сахарид, ковалентно конъюгированный с белком-носителем по меньшей мере через один еТЕС спейсер. Соединенные через еТЕС гликоконъюгаты по изобретению и иммуногенные композиции, содержащие их, могут содержать некоторое количество свободного сахарида.
Термин «свободный сахарид», как он использован в данном описании, означает сахарид, который не конъюгирован ковалентно с белком-носителем, или сахарид, который соединен ковалентно с очень небольшим числом белков-носителей, присоединенных при большом соотношении сахарид/белок (больше 5:1), но тем не менее присутствует в составе гликоконъюгата. Этот свободный сахарид может быть нековалентно ассоциированным с гликоконъюгатом (т.е. нековалентно связанным с гликоконъюгатом, адсорбированным на гликоконъюгате или заключенным в гликоконъюгат либо захваченным гликоконъюгатом) (конъюгированный сахарид)-(белок-носитель). Термины «свободный полисахарид» и «свободный капсульный полисахарид» могут быть использованы в данном описании для передачи одного и того же значения в отношении гликоконъюгатов, в которых сахарид представляет собой полисахарид или капсульный полисахарид соответственно.
Как использовано в данном описании, термины «конъюгировать», «конъюгированный» и «конъюгирование» относятся к способу, при котором сахарид, например бактериальный капсульный полисахарид, ковалентно присоединяют к молекуле-носителю или белку-носителю. В способах по настоящему изобретению сахарид ковалентно конъюгирован с белком-носителем по меньшей мере через один еТЕС спейсер. Конъюгирование может быть осуществлено способами, описанными ниже, или другими способами, известными в данной области техники. Конъюгирование с белком-носителем повышает иммуногенность бактериального капсульного полисахарида.
Гликоконъюгаты
Настоящее изобретение относится к гликоконъюгатам, содержащим сахарид, ковалентно конъюгированный с белком-носителем через один или более еТЕС спейсеров, при этом сахарид ковалентно конъюгирован с еТЕС спейсером через карбаматную связь, и белок-носитель ковалентно конъюгирован с еТЕС спейсером через амидную связь.
В дополнение к наличию одного или более еТЕС спейсеров, новые признаки гликоконъюгатов по настоящему изобретению включают профили молекулярных масс сахаридов и конечных соединенных через еТЕС гликоконъюгатов, соотношение числа конъюгированных остатков лизина на одну молекулу белка-носителя и числа остатков лизина, ковалентно связанных с полисахаридом через еТЕС спейсер(ы), число ковалентных связей между белком-носителем и сахаридом как функцию от числа повторяющихся единиц сахарида и относительное количество свободного сахарида в сравнении с общим количеством сахарида.
Соединенные через еТЕС гликоконъюгаты по изобретению могут быть представлены общей формулой (I):
Этот еТЕС спейсер представляет собой структуру, линейная часть которой состоит из семи атомов (т.е. -C(O)NH(CH2)2SCH2C(O)-) и обеспечивает образование стабильной тиоэфирной и амидной связей между сахаридом и белком-носителем. Синтез соединенного через еТЕС гликоконъюгата включает в себя взаимодействие активированной гидроксильной группы сахарида с аминогруппой тиоалкиламинного реагента, например, цистамина или цистеинамина либо их соли, образование карбаматной связи с сахаридом с получением тиолированного сахарида. Образование одной или более свободных сульфгидрильных групп происходит в реакции с восстанавливающим агентом с получением активированного тиолированного сахарида. В результате взаимодействия этих свободных сульфгидрильных групп активированного тиолированного сахарида с активированным белком-носителем, имеющим одну или более α-галогенацетамидных групп на остатках, содержащих аминогруппу, образуется тиоэфирная связь с получением конъюгата, при этом белок-носитель присоединяется к еТЕС спейсеру через амидную связь.
В гликоконъюгатах по изобретению сахарид может быть полисахаридом, олигосахаридом или моносахаридом, а белок-носитель может быть выбран из любого подходящего носителя, как в дальнейшем изложено в данном описании, или известного специалистам в данной области техники. Во многих воплощениях сахарид представляет собой бактериальный капсульный полисахарид. В некоторых таких воплощениях белок-носитель представляет собой CRM197.
В некоторых таких воплощениях соединенный через еТЕС гликоконъюгат содержит Pn капсульный полисахарид, имеющий происхождение из Streptococcus pneumoniae. В конкретных воплощениях данный Pn капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Pn-серотипов 1, 3, 4, 5, 6А, 6В, 7F, 8, 9V, 10А, 11А, 12F, 14, 15В, 18С, 19А, 19F, 22F, 23F и 33F. В других воплощениях капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Pn-серотипов 10А, 11A, 22F и 33F. В одном из таких воплощений капсульный полисахарид представляет собой капсульный полисахарид Pn-33F. В другом таком воплощении капсульный полисахарид представляет собой капсульный полисахарид Pn-22F. В другом таком воплощении капсульный полисахарид представляет собой капсульный полисахарид Pn-10А. Еще в одном таком воплощении капсульный полисахарид представляет собой капсульный полисахарид Pn-11А.
В других воплощениях соединенный через еТЕС гликоконъюгат содержит Mn капсульный полисахарид, имеющий происхождение из N. meningitidis. В конкретных воплощениях данный Mn капсульный полисахарид выбран из группы, состоящей из капсульных полисахаридов Mn-серотипов А, С, W135 и Y. В одном из таких воплощений капсульный полисахарид представляет собой капсульный полисахарид Mn-А. В другом таком воплощении капсульный полисахарид представляет собой капсульный полисахарид Mn-С. В другом таком воплощении капсульный полисахарид представляет собой капсульный полисахарид Mn-W135. Еще в одном таком воплощении капсульный полисахарид представляет собой капсульный полисахарид Mn-Y.
В особо предпочтительных воплощениях соединенный через еТЕС гликоконъюгат содержит Pn или Mn бактериальный капсульный полисахарид, такой как капсульный полисахарид Pn-серотипа 1, 3, 4, 5, 6А, 6В, 7F, 8, 9V, 10А, 11А, 12F, 14, 15В, 18С, 19А, 19F, 22F, 23F или 33F, или капсульный полисахарид Mn-серотипа А, С, W135 или Y, который ковалентно конъюгирован с CRM197 через еТЕС спейсер.
В некоторых воплощениях соединенные через еТЕС гликоконъюгаты по настоящему изобретению содержат сахарид, ковалентно конъюгированный с белком-носителем через еТЕС спейсер, при этом сахарид имеет молекулярную массу в диапазоне от 10 кДа до 2000 кДа. В других таких воплощениях сахарид имеет молекулярную массу в диапазоне от 50 кДа до 2000 кДа. В других таких воплощениях сахарид имеет молекулярную массу в диапазоне от 50 кДа до 1750 кДа; от 50 кДа до 1500 кДа; от 50 кДа до 1250 кДа; от 50 кДа до 1000 кДа; от 50 кДа до 750 кДа; от 50 кДа до 500 кДа; от 100 кДа до 2000 кДа; от 100 кДа до 1750 кДа; от 100 кДа до 1500 кДа; от 100 кДа до 1250 кДа; от 100 кДа до 1000 кДа; от 100 кДа до 750 кДа; от 100 кДа до 500 кДа; от 200 кДа до 2000 кДа; от 200 кДа до 1750 кДа; от 200 кДа до 1500 кДа; от 200 кДа до 1250 кДа; от 200 кДа до 1000 кДа; от 200 кДа до 750 кДа; или от 200 кДа до 500 кДа. В некоторых таких воплощениях сахарид представляет собой бактериальный капсульный полисахарид, такой как капсульный полисахарид Pn-серотипа 1,3,4, 5, 6А, 6В, 7F, 8, 9V, 10А, 11A, 12F, 14, 15В, 18С, 19А, 19F, 22F, 23F или 33F, или капсульный полисахарид Mn-серотипа А, С, W135 или Y, при этом данный капсульный полисахарид имеет молекулярную массу, лежащую в пределах любого из описанных диапазонов молекулярных масс.
В некоторых воплощениях соединенный через еТЕС гликоконъюгат по изобретению имеет молекулярную массу в диапазоне от 50 кДа до 20000 кДа. В других воплощениях соединенный через еТЕС гликоконъюгат имеет молекулярную массу в диапазоне от 500 кДа до 10000 кДа. В других воплощениях соединенный через еТЕС гликоконъюгат имеет молекулярную массу в диапазоне от 200 кДа до 10000 кДа. В еще одних воплощениях соединенный через еТЕС гликоконъюгат имеет молекулярную массу в диапазоне от 1000 кДа до 3000 кДа.
В следующих воплощениях соединенный через еТЕС гликоконъюгат по изобретению имеет молекулярную массу в диапазоне от 200 кДа до 20000 кДа; от 200 кДа до 15000 кДа; от 200 кДа до 10000 кДа; от 200 кДа до 7500 кДа; от 200 кДа до 5000 кДа; от 200 кДа до 3000 кДа; от 200 кДа до 1000 кДа; от 500 кДа до 20000 кДа; от 500 кДа до 15000 кДа; от 500 кДа до 12500 кДа; от 500 кДа до 10000 кДа; от 500 кДа до 7500 кДа; от 500 кДа до 6000 кДа; от 500 кДа до 5000 кДа; от 500 кДа до 4000 кДа; от 500 кДа до 3000 кДа; от 500 кДа до 2000 кДа; от 500 кДа до 1500 кДа; от 500 кДа до 1000 кДа; от 750 кДа до 20000 кДа; от 750 кДа до 15000 кДа; от 750 кДа до 12500 кДа; от 750 кДа до 10000 кДа; от 750 кДа до 7500 кДа; от 750 кДа до 6000 кДа; от 750 кДа до 5000 кДа; от 750 кДа до 4000 кДа; от 750 кДа до 3000 кДа; от 750 кДа до 2000 кДа; от 750 кДа до 1500 кДа; от 1000 кДа до 15000 кДа; от 1000 кДа до 12500 кДа; от 1000 кДа до 10000 кДа; от 1000 кДа до 7500 кДа; от 1000 кДа до 6000 кДа; от 1000 кДа до 5000 кДа; от 1000 кДа до 4000 кДа; от 1000 кДа до 2500 кДа; от 2000 кДа до 15000 кДа; от 2000 кДа до 12500 кДа; от 2000 кДа до 10000 кДа; от 2000 кДа до 7500 кДа; от 2000 кДа до 6000 кДа; от 2000 кДа до 5000 кДа; от 2000 кДа до 4000 кДа; или от 2000 кДа до 3000 кДа.
Другой характеристикой соединенных через еТЕС гликоконъюгатов по изобретению является число остатков лизина в белке-носителе, подвергнутых конъюгированию с сахаридом через еТЕС спейсер, которое можно охарактеризовать в виде диапазона конъюгированных остатков лизина.
Во многих воплощениях белок-носитель ковалентно конъюгирован с еТЕС спейсером через амидную связь с одной или более ε-аминогруппами остатков лизина на белке-носителе. В некоторых таких воплощениях белок-носитель содержит от 2 до 20 остатков лизина, ковалентно конъюгированных с сахаридом. В других таких воплощениях белок-носитель содержит от 4 до 16 остатков лизина, ковалентно конъюгированных с сахаридом.
В предпочтительном воплощении белок-носитель содержит CRM197, который содержит 39 остатков лизина. В некоторых таких воплощениях CRM197 может содержать от 4 до 16 остатков лизина, ковалентно связанных с сахаридом, из 39. Другой способ выражения этого параметра состоит в том, что от примерно 10% до примерно 41% остатков лизина CRM197 являются ковалентно связанными с сахаридом. В другом таком воплощении CRM197 может содержать от 2 до 20 остатков лизина, ковалентно связанных с сахаридом, из 39. Другой способ выражения этого параметра состоит в том, что от примерно 5% до примерно 50% остатков лизина CRM197 являются ковалентно связанными с сахаридом.
Соединенные через еТЕС гликоконъюгаты по изобретению также могут быть охарактеризованы соотношением (масса/масса) сахарида к белку-носителю. В некоторых воплощениях соотношение сахарид:(белок-носитель) (масс./масс.) находится в диапазоне от 0,2 до 4. В других воплощениях соотношение сахарид:(белок-носитель) (масс./масс.) находится в диапазоне от 1,0 до 2,5. В следующих воплощениях соотношение сахарид:(белок-носитель) (масс./масс.) находится в диапазоне от 0,4 до 1,7. В некоторых таких воплощениях сахарид представляет собой бактериальный капсульный полисахарид и/или белок-носитель представляет собой CRM197.
Гликоконъюгаты также могут быть охарактеризованы числом ковалентных связей между белком-носителем и сахаридом в зависимости от числа повторяющихся единиц сахарида. В одном воплощении гликоконъюгат по изобретению содержит по меньшей мере одну ковалентную связь между белком-носителем и полисахаридом на каждые 4 повторяющиеся сахаридные единицы полисахарида. В другом воплощении ковалентная связь между белком-носителем и полисахаридом встречается по меньшей мере один раз на каждые 10 повторяющихся сахаридных единиц полисахарида. В другом воплощении ковалентная связь между белком-носителем и полисахаридом встречается по меньшей мере один раз на каждые 15 повторяющихся сахаридных единиц полисахарида. В следующем воплощении ковалентная связь между белком-носителем и полисахаридом встречается по меньшей мере один раз на каждые 25 повторяющихся сахаридных единиц полисахарида.
Во многих воплощениях белок-носитель представляет собой CRM197, а ковалентная связь через еТЕС спейсер между CRM197 и полисахаридом встречается по меньшей мере один раз на каждые 4, 10, 15 или 25 повторяющихся сахаридных единиц полисахарида.
Важным фактором при образовании конъюгата является разработка условий, позволяющих сохранить потенциально чувствительные несахаридные функциональные группы заместителей отдельных компонентов, такие как О-ацильные, фосфатные или глицеролфосфатные боковые цепи, которые могут образовывать часть эпитопа сахарида.
В одном воплощении гликоконъюгат содержит сахарид, имеющий степень О-ацетилирования в диапазоне 10-100%. В некоторых таких воплощениях сахарид имеет степень О-ацетилирования в диапазоне 50-100%. В других таких воплощениях сахарид имеет степень О-ацетилирования в диапазоне 75-100%. В следующих воплощениях сахарид имеет степень О-ацетилирования больше 70% или ровно 70% (не менее 70%).
Соединенные через еТЕС гликоконъюгаты и иммуногенные композиции по изобретению могут содержать свободный сахарид, который не конъюгирован ковалентно с белком-носителем, но тем не менее присутствует в составе гликоконъюгата. Этот свободный сахарид может быть нековалентно ассоциированным с гликоконъюгатом (т.е. нековалентно связанным с гликоконъюгатом, адсорбированным на гликоконъюгате или заключенным в гликоконъюгат либо захваченным гликоконъюгатом).
В некоторых воплощениях соединенный через еТЕС гликоконъюгат содержит менее чем примерно 45% свободного сахарида, менее чем примерно 40% свободного сахарида, менее чем примерно 35% свободного сахарида, менее чем примерно 30% свободного сахарида, менее чем примерно 25% свободного сахарида, менее чем примерно 20% свободного сахарида, менее чем примерно 15% свободного сахарида, менее чем примерно 10% свободного сахарида или менее чем примерно 5% свободного сахарида относительно общего количества сах