Раствор электролита для устройств хранения электроэнергии, таких как батареи и конденсаторы, содержащий соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом, способ получения упомянутого раствора электролита, а также конденсатор, включающий в себя упомянутый раствор электролита
Иллюстрации
Показать всеИзобретение относится к раствору электролита. Раствор электролита содержит соль, катион которой является щелочным металлом, и органический растворитель с гетероэлементом, причем удовлетворяется по меньшей мере одно из условий 1-3. Условие 1: в отношении интенсивности пика, получаемого от органического растворителя в спектре колебательной спектроскопии раствора электролита, удовлетворяется условие Is>Io, где интенсивность исходного пика органического растворителя обозначается как Io, а интенсивность пика, получающегося в результате сдвига исходного пика, обозначается как Is. Условие 2: «d/c», получаемое путем деления плотности d (г/см3) раствора электролита на концентрацию с соли (моль/л) в растворе электролита, удовлетворяет условию 0,15≤d/c≤0,71. Условие 3: вязкость η (мПа·с) раствора электролита удовлетворяет условию 10<η<500, а ионная проводимость σ (мСм/см) раствора электролита удовлетворяет условию 1≤σ<10. Химическая структура аниона соли представлена нижеприведенной общей формулой (7), PF6 или BF4:
13SO2)(R14SO2)N Общая формула (7),
где R13 и R14, каждый, независимо представляют собой CnFb; n и b, каждое, независимо являются целым числом, большим или равным 0, и удовлетворяют условию 2n+1=b. Органический растворитель выбран из: нитрилов; простых эфиров, выбранных из 1,2-диметоксиэтана, 1,2-диэтоксиэтана, тетрагидрофурана, 1,2-диоксана, 1,3-диоксана, 1,4-диоксана, 2,2-диметил-1,3-диоксолана, 2-метилтетрагидропирана или 2-метилтетрагидрофурана; этиленкарбоната; пропиленкарбоната; амидов; сложных эфиров; сульфонов; сульфоксидов; сложных эфиров фосфорной кислоты или линейного карбоната, причем карбонат представлен нижеприведенной общей формулой (10):
19OCOOR20 Общая формула (10),
где R19 и R20, каждый, независимо выбраны из CnHaFb, то есть линейного алкила, n является целым числом не меньше 1, a и b, каждое, независимо являются целым числом не меньше 0 и удовлетворяют условию 2n+1=a+b. Также предложены конденсатор и способ получения раствора электролита. Изобретение позволяет улучшить характеристики батареи. 3 н. и 13 з.п. ф-лы, 70 ил., 22 табл., 99 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение относится: к раствору электролита (электролитическому раствору) для устройств хранения электроэнергии, таких как батареи и конденсаторы, содержащему соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом; к способу получения этого раствора электролита; а также к конденсатору, включающему в себя этот раствор электролита.
УРОВЕНЬ ТЕХНИКИ
[0002] Обычно батарея включает в себя в качестве главных компонентов положительный электрод, отрицательный электрод и раствор электролита. В растворе электролита подходящий электролит добавляется в подходящем диапазоне концентраций. Например, в растворе электролита литий-ионной аккумуляторной батареи в качестве электролита обычно добавляется соль лития, такая как LiClO4, LiAsF6, LiPF6, LiBF4, CF3SO3Li и (CF3SO2)2NLi, и концентрация соли лития в растворе электролита обычно устанавливается на уровне примерно 1 моль/л.
[0003] Фактически, патентный документ 1 раскрывает литий-ионную аккумуляторную батарею, использующую раствор электролита, содержащий LiPF6 в концентрации 1 моль/л. Кроме того, патентный документ 2 раскрывает литий-ионную аккумуляторную батарею, использующую раствор электролита, содержащий (CF3SO2)2NLi в концентрации 1 моль/л. Вязкость растворов электролита, раскрытых в патентных документах 1 и 2, составляет не более, чем примерно 5 мПа·с.
[0004] В дополнение к этому, с целью улучшения характеристик батарей активно проводятся исследования различных присадок для добавления к раствору электролита, содержащему соль лития.
[0005] Например, патентный документ 3 описывает раствор электролита, полученный путем добавления к раствору электролита, содержащему LiPF6 в концентрации 1 моль/л, небольшого количества конкретной добавки, а также раскрывает литий-ионную аккумуляторную батарею, использующую этот раствор электролита. В дополнение к этому, патентный документ 4 также описывает раствор электролита, полученный путем добавления к раствору электролита, содержащему LiPF6 в концентрации 1 моль/л, небольшого количества фенилглицидилового эфира, а также раскрывает литий-ионную аккумуляторную батарею, использующую этот раствор электролита. Вязкости растворов электролита, раскрытых в патентных документах 3 и 4, составляют не более, чем примерно 5 мПа·с.
[0006] Конденсатор обычно относится к электрическому конденсатору, который отдает или накапливает заряд в соответствии с его емкостью. Механизм действия заряда и разряда электричеством конденсатора основан на адсорбции и десорбции заряда на электроде. Так как этот механизм действия не сопровождается электрохимическими реакциями, конденсатор является весьма устойчивым, и перенос заряда в конденсаторе происходит быстро.
[0007] Некоторые из конденсаторов включают в себя раствор электролита, и в качестве их примеров известны конденсаторы с двойным электрическим слоем. Когда между электродами в конденсаторе с двойным электрическим слоем образуется разность электрических потенциалов, на положительном электроде анионы раствора электролита выстраиваются в слой на границе раздела между положительным электродом и раствором электролита, а на отрицательном электроде катионы раствора электролита выстраиваются в слой на границе раздела между отрицательным электродом и раствором электролита. Такое «слоеное» состояние обладает емкостью, и это состояние является заряженным состоянием конденсатора с двойным электрическим слоем.
[0008] В качестве конденсатора, включающего в себя раствор электролита и отличающегося от конденсатора с двойным электрическим слоем, известен литий-ионный конденсатор, имеющий улучшенное рабочее напряжение. Литий-ионный конденсатор относится к конденсатору, положительный электрод которого является электродом, подобным электроду конденсатора с двойным электрическим слоем, отрицательный электрод которого является электродом, сформированным из материала, подобного отрицательному электроду литий-ионной аккумуляторной батареи, и раствор электролита которого является обычным раствором электролита для литий-ионных аккумуляторных батарей. Поскольку потенциал отрицательного электрода литий-ионного конденсатора понижается посредством предварительного легирования, при котором отрицательный электрод предварительно легируется ионами лития, литий-ионный конденсатор демонстрирует высокую электрическую емкость.
[0009] Во время заряда и разряда литий-ионного конденсатора отрицательный электрод обратимо легируется и делегируется, то есть присоединяет и отщепляет часть ионов лития, которыми был предварительно легирован отрицательный электрод. Таким образом, полагают, что между раствором электролита и отрицательным электродом литий-ионного конденсатора протекает электрохимическая реакция (реакция в ячейке), идентичная той, что происходит в литий-ионной аккумуляторной батарее. С другой стороны, между раствором электролита и положительным электродом происходят адсорбция и десорбция заряда, которые характерны для конденсаторов.
[0010] Электрическая емкость (J), которая может использоваться конденсатором, определяется как (Емкость электрода)×(Напряжение)×(Напряжение)/2. С целью увеличения электрической емкости рассмотрены использование материала с большой удельной площадью поверхности электрода, использование содержащего органический растворитель раствора электролита в качестве раствора электролита и т.п.
[0011] Конкретным примером описанных выше мер является активно предпринимаемая попытка увеличения емкости электрода путем увеличения удельной площади поверхности углеродного материала, используемого для электрода, с тем, чтобы увеличить количество мест адсорбирования заряда.
[0012] В качестве конкретных мер, фокусирующихся на растворе электролита, в патентных документах 5-9 раскрываются конденсаторы, использующие ионные жидкости в качестве растворов электролита. Как раскрыто в патентных документах 10 и 11, в качестве растворов электролита обычных конденсаторов и литий-ионных конденсаторов обычно используются растворы, полученные путем растворения LiPF6 или (C2H5)4NBF4 в растворителе, таком как пропиленкарбонат, с концентрацией примерно 1 моль/л.
СПИСОК ЛИТЕРАТУРЫ
ПАТЕНТНАЯ ЛИТЕРАТУРА
[0013] Патентный документ 1: JP2013149477 (A)
Патентный документ 2: JP2013134922 (A)
Патентный документ 3: JP2013145724 (A)
Патентный документ 4: JP2013137873 (A)
Патентный документ 5: JP2004111294 (A)
Патентный документ 6: JP2008010613 (A)
Патентный документ 7: WO2004019356 (A1)
Патентный документ 8: WO2004027789 (A1)
Патентный документ 9: WO2005076299 (A1)
Патентный документ 10: JPH1131637 (A)
Патентный документ 11: JPH1027733 (A)
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКАЯ ПРОБЛЕМА
[0014] Как описано в патентных документах 1-4, обычно в растворе электролита, используемом в литий-ионной аккумуляторной батарее, технически общепринято использовать соль лития в концентрации примерно 1 моль/л. В дополнение, как описано в патентных документах 3 и 4, были проведены исследования по улучшению растворов электролита с фокусом на добавках, которые являются отдельными от соли лития.
[0015] Вопреки таким обычным техническим общеизвестным сведениям, один вариант настоящего изобретения фокусируется на соотношении (взаимозависимости) между солью металла и растворителем в растворе электролита, и цель этого варианта состоит в том, чтобы предложить раствор электролита, в котором соль металла и растворитель существуют в новом состоянии, а также способ получения этого раствора электролита.
[0016] В отличие от фокуса специалистов в данной области техники до настоящего времени, один вариант настоящего изобретения фокусируется на соотношении между плотностью и концентрацией в растворе электролита, и цель этого варианта состоит в том, чтобы предложить группу подходящих растворов электролита.
[0017] Один вариант настоящего изобретения фокусируется на вязкости самого раствора электролита, и цель этого варианта состоит в том, чтобы предложить раствор электролита, вязкость которого находится в диапазоне, который традиционно не использовался.
[0018] Ионная жидкость состоит из катиона с большим ионным радиусом и аниона с большим ионным радиусом и находится в жидком состоянии при обычной температуре. Так как раствор электролита, образованный из ионной жидкости, состоит только из ионов, он имеет высокую концентрацию ионов по сравнению с раствором электролита с тем же самым объемом. Хотя ионная жидкость имеет большой радиус ионов, так как концентрация ионов в растворе электролита является высокой, электрическая емкость конденсатора, включающего в себя раствор электролита, образованный из ионной жидкости, является сопоставимой с электрической емкостью конденсатора, включающего в себя обычный раствор электролита.
[0019] Однако у электрической емкости конденсатора, включающего в себя образованный из ионной жидкости раствор электролита, также есть пределы. Таким образом, был выполнен поиск нового средства, способного улучшить электрическую емкость конденсатора.
[0020] Один вариант настоящего изобретения был создан с учетом таких обстоятельств, и цель этого варианта состоит в том, чтобы предложить конденсатор, включающий в себя раствор электролита, в котором соль металла и растворитель существуют в новом состоянии.
РЕШЕНИЕ ПРОБЛЕМЫ
[0021] Авторы настоящего изобретения провели тщательное исследование методом проб и ошибок. В результате авторы настоящего изобретения обнаружили, что вопреки общеизвестным техническим сведениям раствор электролита с добавленной к нему в качестве электролита солью лития в количестве большем, чем обычно используемое, сохраняет состояние раствора. В дополнение к этому, авторы настоящего изобретения нашли, что такой раствор электролита подходящим образом действует в качестве раствора электролита батареи. После выполнения анализа этого раствора электролита авторы настоящего изобретения обнаружили, что раствор электролита, в котором существует конкретное соотношение в пиках, наблюдаемых в инфракрасном (ИК) спектре или рамановском спектре, является особенно выгодным в качестве раствора электролита батареи, и пришли к одному варианту настоящего изобретения.
[0022] Раствор электролита, который представляет собой один вариант настоящего изобретения, является раствором электролита, содержащим соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом, и при этом в отношении интенсивности пика, получаемого от органического растворителя в спектре колебательной спектроскопии раствора электролита, удовлетворяется условие Is>Io, когда интенсивность исходного пика органического растворителя обозначается как Io, а интенсивность пика, получаемого в результате сдвига исходного пика органического растворителя, обозначается как Is.
[0023] Способ получения раствора электролита, который представляет собой один вариант настоящего изобретения, включает в себя: первую стадию растворения с приготовлением первого раствора электролита путем смешивания органического растворителя с гетероэлементом и соли, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, для растворения этой соли; вторую стадию растворения с приготовлением второго раствора электролита в перенасыщенном состоянии путем добавления этой соли к упомянутому первому раствору электролита при условиях перемешивания и/или нагревания для растворения этой соли; и третью стадию растворения с приготовлением третьего раствора электролита путем добавления этой соли к упомянутому второму раствору электролита при условиях перемешивания и/или нагревания для растворения этой соли.
[0024] Авторы настоящего изобретения провели тщательное исследование, не ограничиваясь общеизвестными техническими сведениями, методом проб и ошибок. В результате авторы настоящего изобретения обнаружили среди растворов электролита, включающих в себя соль металла и органический растворитель, большое число подходящих растворов электролита, особенно подходящих в качестве растворов электролита для литий-ионных аккумуляторных батарей. Что касается зависимости между подходящим раствором электролита и обычным раствором электролита, хотя авторы настоящего изобретения попытались обнаружить определяющее правило, которое зависит от концентрации соли металла, но не зависит от типа соли металла и типа органического растворителя, эта попытка закончилась неудачей. Более конкретно, линейную зависимость относительно концентрации соли металла, независящую от типа соли металла и типа органического растворителя, найти не удалось. После дальнейшего исследования авторы настоящего изобретения неожиданно обнаружили, что одна группа растворов электролита, в которой существует конкретное соотношение между плотностью и концентрацией, действует подходящим образом в качестве раствора электролита батареи по сравнению с обычным раствором электролита, и пришли к одному варианту настоящего изобретения.
[0025] Раствор электролита, который представляет собой один вариант настоящего изобретения, является раствором электролита, содержащим соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом, причем d/c, получаемое путем деления плотности d (г/см3) раствора электролита на концентрацию c соли (моль/л) в растворе электролита, удовлетворяет условию 0,15≤d/c≤0,71.
[0026] Как описано выше, авторы настоящего изобретения обнаружили, что раствор электролита с конкретной солью лития, добавленной к нему в количестве большем, чем обычно используемое количество, сохраняет состояние раствора. В дополнение к этому, авторы настоящего изобретения нашли, что такой раствор электролита демонстрирует ионную проводимость и имеет высокую вязкость по сравнению с обычным раствором электролита. Кроме того, авторы настоящего изобретения после выполнения анализа этого раствора электролита обнаружили, что раствор электролита, в котором существует конкретное соотношение между вязкостью и ионной проводимостью, является выгодным, в частности в качестве раствора электролита батареи, и пришли к еще одному варианту настоящего изобретения.
[0027] Раствор электролита, который является одним вариантом настоящего изобретения, представляет собой раствор электролита, содержащий соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом, причем вязкость η (мПа·с) раствора электролита удовлетворяет условию 10<η<500, а ионная проводимость σ (мСм/см) раствора электролита удовлетворяет условию 1≤σ.
[0028] Как описано выше, авторы настоящего изобретения обнаружили, что вопреки общеизвестным техническим сведениям раствор электролита с добавленной к нему в качестве электролита солью лития в большем чем обычно используемое количестве сохраняет состояние раствора. В дополнение к этому, авторы настоящего изобретения нашли, что такой раствор электролита подходящим образом действует в качестве раствора электролита конденсатора. После выполнения анализа этого раствора электролита авторы настоящего изобретения обнаружили, что раствор электролита, в котором существует конкретное соотношение в пиках, наблюдаемых в ИК спектре или рамановском спектре, является особенно выгодным в качестве раствора электролита конденсатора, и пришли к одному варианту настоящего изобретения.
[0029] Конденсатор по настоящему изобретению является конденсатором, включающим в себя раствор электролита, содержащий соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом, причем в отношении интенсивности пика, получаемого от органического растворителя в спектре колебательной спектроскопии раствора электролита, удовлетворяется условие Is>Io, когда интенсивность исходного пика органического растворителя обозначается как Io, а интенсивность пика, получаемого в результате сдвига исходного пика, обозначается как Is.
ПОЛЕЗНЫЕ ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
[0030] Новый раствор электролита в соответствии с каждым из вариантов настоящего изобретения улучшает различные характеристики батареи. В дополнение к этому, новый конденсатор по настоящему изобретению демонстрирует подходящую электрическую емкость.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
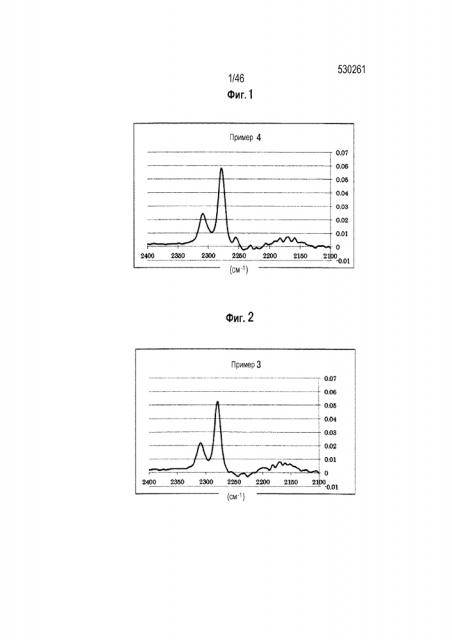
[0031] Фиг. 1 представляет собой ИК спектр раствора электролита Примера 4;
Фиг. 2 - ИК спектр раствора электролита Примера 3;
Фиг. 3 - ИК спектр раствора электролита Примера 14;
Фиг. 4 - ИК спектр раствора электролита Примера 13;
Фиг. 5 - ИК спектр раствора электролита Примера 11;
Фиг. 6 - ИК спектр раствора электролита Сравнительного примера 7;
Фиг. 7 - ИК спектр раствора электролита Сравнительного примера 14;
Фиг. 8 - ИК спектр ацетонитрила;
Фиг. 9 - ИК спектр (CF3SO2)2NLi;
Фиг. 10 - ИК спектр (FSO2)2NLi (от 2100 до 2400 см-1);
Фиг. 11 - ИК спектр раствора электролита Примера 15;
Фиг. 12 - ИК спектр раствора электролита Примера 16;
Фиг. 13 - ИК спектр раствора электролита Примера 17;
Фиг. 14 - ИК спектр раствора электролита Примера 18;
Фиг. 15 - ИК спектр раствора электролита Примера 19;
Фиг. 16 - ИК спектр раствора электролита Сравнительного примера 15;
Фиг. 17 - ИК спектр диметилкарбоната;
Фиг. 18 - ИК спектр раствора электролита Примера 20;
Фиг. 19 - ИК спектр раствора электролита Примера 21;
Фиг. 20 - ИК спектр раствора электролита Примера 22;
Фиг. 21 - ИК спектр раствора электролита Сравнительного примера 16;
Фиг. 22 - ИК спектр этилметилкарбоната;
Фиг. 23 - ИК спектр раствора электролита Примера 23;
Фиг. 24 - ИК спектр раствора электролита Примера 24;
Фиг. 25 - ИК спектр раствора электролита Примера 25;
Фиг. 26 - ИК спектр раствора электролита Сравнительного примера 17;
Фиг. 27 - ИК спектр диэтилкарбоната;
Фиг. 28 - ИК спектр (FSO2)2NLi (от 1900 до 1600 см-1);
Фиг. 29 - ИК спектр раствора электролита Примера 26;
Фиг. 30 - ИК спектр раствора электролита Примера 27;
Фиг. 31 - рамановский спектр раствора электролита Примера 12;
Фиг. 32 - рамановский спектр раствора электролита Примера 13;
Фиг. 33 - рамановский спектр раствора электролита Сравнительного примера 14;
Фиг. 34 - рамановский спектр раствора электролита Примера 15;
Фиг. 35 - рамановский спектр раствора электролита Примера 17;
Фиг. 36 - рамановский спектр раствора электролита Примера 19;
Фиг. 37 - рамановский спектр раствора электролита Сравнительного примера 15;
Фиг. 38 показывает результат восприимчивости к повторному быстрому заряду/разряду в Оценочном примере 10;
Фиг. 39 представляет собой график ДСК, полученный, когда раствор электролита и заряженный положительный электрод литий-ионной аккумуляторной батареи Примера B в Оценочном примере 11 были помещены вместе;
Фиг. 40 представляет собой график ДСК, полученный, когда раствор электролита и заряженный положительный электрод литий-ионной аккумуляторной батареи Сравнительного примера B в Оценочном примере 11 были помещены вместе;
Фиг. 41 показывает кривые заряда/разряда полуячейки Примера E;
Фиг. 42 показывает кривые заряда/разряда полуячейки Примера F;
Фиг. 43 показывает кривые заряда/разряда полуячейки Примера G;
Фиг. 44 показывает кривые заряда/разряда полуячейки Примера H;
Фиг. 45 показывает кривые заряда/разряда полуячейки Сравнительного примера E;
Фиг. 46 - график, показывающий соотношение между потенциалом (от 3,1 до 4,6 В) и током отклика в полуячейке Примера I;
Фиг. 47 - график, показывающий соотношение между потенциалом (от 3,1 до 5,1 В) и током отклика в полуячейке Примера I;
Фиг. 48 - график, показывающий соотношение между потенциалом (от 3,1 до 4,6 В) и током отклика в полуячейке Примера J;
Фиг. 49 - график, показывающий соотношение между потенциалом (от 3,1 до 5,1 В) и током отклика в полуячейке Примера J;
Фиг. 50 - график, показывающий соотношение между потенциалом (от 3,1 до 4,6 В) и током отклика в полуячейке Примера L;
Фиг. 51 - график, показывающий соотношение между потенциалом (от 3,1 до 5,1 В) и током отклика в полуячейке Примера L;
Фиг. 52 - график, показывающий соотношение между потенциалом (от 3,1 до 4,6 В) и током отклика в полуячейке Примера M;
Фиг. 53 - график, показывающий соотношение между потенциалом (от 3,1 до 5,1 В) и током отклика в полуячейке Примера M;
Фиг. 54 - график, показывающий соотношение между потенциалом (от 3,1 до 4,6 В) и током отклика в полуячейке Сравнительного примера F;
Фиг. 55 - график, показывающий соотношение между потенциалом (от 3,0 до 4,5 В) и током отклика в полуячейке Примера J;
Фиг. 56 - график, показывающий соотношение между потенциалом (от 3,0 до 5,0 В) и током отклика в полуячейке Примера J;
Фиг. 57 - график, показывающий соотношение между потенциалом (от 3,0 до 4,5 В) и током отклика в полуячейке Примера K;
Фиг. 58 - график, показывающий соотношение между потенциалом (от 3,0 до 5,0 В) и током отклика в полуячейке Примера K;
Фиг. 59 - график, показывающий соотношение между потенциалом (от 3,0 до 4,5 В) и током отклика в полуячейке Сравнительного примера G;
Фиг. 60 - график, показывающий соотношение между потенциалом (от 3,0 до 5,0 В) и током отклика в полуячейке Сравнительного примера G;
Фиг. 61 - график, показывающий кривые напряжения литий-ионной аккумуляторной батареи Примера N при соответствующих значениях номинального тока;
Фиг. 62 - график, показывающий кривые напряжения литий-ионной аккумуляторной батареи Сравнительного примера H при соответствующих значениях номинального тока;
Фиг. 63 - годограф комплексного импеданса батареи в Оценочном примере 18;
Фиг. 64 показывает кривые заряда/разряда конденсаторов Примера R и Сравнительного примера J;
Фиг. 65 показывает кривые заряда/разряда конденсаторов Примера S и Сравнительного примера K;
Фиг. 66 показывает кривые заряда/разряда конденсатора Примера S при напряжениях отсечки от 0 до 2 В;
Фиг. 67 показывает кривые заряда/разряда конденсатора Примера S при напряжениях отсечки от 0 до 2,5 В;
Фиг. 68 показывает кривые заряда/разряда конденсатора Примера S при напряжениях отсечки от 0 до 3 В;
Фиг. 69 показывает кривые разряда конденсатора Примера S при соответствующих напряжениях отсечки; и
Фиг. 70 показывает кривые заряда/разряда литий-ионного конденсатора Примера T.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0032] Далее описываются варианты осуществления настоящего изобретения. Если конкретно не указано иное, диапазон численных значений «от а до b», используемый в настоящей заявке, включает в себя нижний предел «a» и верхний предел «b». Диапазон численных значений может быть образован путем произвольного комбинирования таких значений верхних пределов, значений нижних пределов, а также численных значений, описанных в Примерах. В дополнение к этому, численные значения, произвольно выбранные в пределах диапазона численных значений, могут использоваться в качестве численных значений верхнего предела и нижнего предела.
[0033] Раствор электролита, который является одним вариантом настоящего изобретения, представляет собой раствор электролита, содержащий соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом. Что касается интенсивности пика, получаемого от органического растворителя в спектре колебательной спектроскопии раствора электролита, удовлетворяется условие Is>Io, когда интенсивность пика при волновом числе исходного пика органического растворителя обозначается как Io, а интенсивность пика, получающегося в результате сдвига волнового числа исходного пика органического растворителя, обозначается как Is.
[0034] Соотношение между Is и Io в обычном растворе электролита удовлетворяет условию Is<Io.
[0035] Раствор электролита, который является одним вариантом настоящего изобретения, представляет собой раствор электролита, содержащий соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом. Отношение «d/c», получаемое путем деления плотности d (г/см3) раствора электролита на концентрацию с соли (моль/л) в этом растворе электролита, удовлетворяет условию 0,15≤d/c≤0,71.
[0036] Обычный раствор электролита не удовлетворяет вышеописанным соотношениям.
[0037] Раствор электролита, который является одним вариантом настоящего изобретения, представляет собой раствор электролита, содержащий соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом. Вязкость η (мПа·с) раствора электролита удовлетворяет условию 10<η<500, а ионная проводимость σ (мСм/см) раствора электролита удовлетворяет условию 1≤σ.
[0038] Конденсатор по настоящему изобретению является конденсатором, включающим в себя раствор электролита, содержащий соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием, и органический растворитель с гетероэлементом. Что касается интенсивности пика, получаемого от органического растворителя в спектре колебательной спектроскопии раствора электролита, удовлетворяется условие Is>Io, когда интенсивность пика при волновом числе исходного пика органического растворителя обозначается как Io, а интенсивность пика, получающегося в результате сдвига волнового числа исходного пика, обозначается как Is.
[0039] В дальнейшем «соль, катион которой является щелочным металлом, щелочноземельным металлом или алюминием» иногда называется «солью металла» или просто «солью», а растворы электролита соответствующих вариантов настоящего изобретения иногда все вместе называются «раствором электролита по настоящему изобретению».
[0040] Соль металла может быть используемым в качестве электролита соединением, таким как LiClO4, LiAsF6, LiPF6, LiBF4 или LiAlCl4, обычно содержащимся в растворе электролита батареи или конденсатора. Примеры катиона соли металла включают в себя щелочные металлы, такие как литий, натрий и калий, щелочноземельные металлы, такие как бериллий, магний, кальций, стронций и барий, а также алюминий. Катион соли металла является предпочтительно ионом металла, идентичным носителю заряда той батареи, в которой используется этот раствор электролита. Например, когда раствор электролита по настоящему изобретению должен использоваться в качестве раствора электролита для литий-ионных аккумуляторных батарей, катион соли металла является предпочтительно литием.
[0041] Химическая структура аниона соли может включать в себя по меньшей мере один элемент, выбираемый из галогена, бора, азота, кислорода, серы или углерода. Конкретные примеры химической структуры аниона, включающей галоген или бор, включают в себя: ClO4, PF6, AsF6, SbF6, TaF6, BF4, SiF6, B(C6H5)4, B(оксалат)2, Cl, Br и I.
[0042] Химическая структура аниона, включающего азот, кислород, серу или углерод, конкретно описывается ниже.
[0043] Химическая структура аниона соли предпочтительно является химической структурой, представленной следующей общей формулой (1), общей формулой (2) или общей формулой (3).
[0044]
| (R1X1)(R2X2)N | Общая формула (1) |
(R1 выбран из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; CN; SCN или OCN.
R2 выбран из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; CN; SCN или OCN.
Кроме того, R1 и R2 необязательно связываются друг с другом с образованием кольца.
X1 выбран из SO2, C=O, C=S, RaP=O, RbP=S, S=O или Si=O.
X2 выбран из SO2, C=O, C=S, RcP=O, RdP=S, S=O или Si=O.
Ra, Rb, Rc и Rd, каждый, независимо выбраны из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; OH; SH; CN; SCN или OCN.
В дополнение к этому, Ra, Rb, Rc и Rd, каждый, необязательно связываются с R1 или R2 с образованием кольца).
[0045]
| R3X3Y | Общая формула (2) |
(R3 выбран из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; CN; SCN или OCN.
X3 выбран из SO2, C=O, C=S, ReP=O, RfP=S, S=O или Si=O.
Re и Rf, каждый, независимо выбраны из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; OH; SH; CN; SCN или OCN.
В дополнение к этому, Re и Rf, каждый, необязательно связывается с R3 с образованием кольца.
Y выбран из O или S).
[0046]
| (R4X4)(R5X5)(R6X6)C | Общая формула (3) |
(R4 выбран из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; CN; SCN или OCN.
R5 выбран из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; CN; SCN или OCN.
R6 выбран из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; CN; SCN или OCN.
В дополнение к этому, любые две или три из R4, R5 и R6 необязательно связываются друг с другом с образованием кольца.
X4 выбран из SO2, C=O, C=S, RgP=O, RhP=S, S=O или Si=O.
X5 выбран из SO2, C=O, C=S, RiP=O, RjP=S, S=O или Si=O.
X6 выбран из SO2, C=O, C=S, RkP=O, RlP=S, S=O или Si=O.
Rg, Rh, Ri, Rj, Rk и Rl, каждый, независимо выбраны из: водорода; галогена; алкильной группы, необязательно замещенной группой заместителя; циклоалкильной группы, необязательно замещенной группой заместителя; ненасыщенной алкильной группы, необязательно замещенной группой заместителя; ненасыщенной циклоалкильной группы, необязательно замещенной группой заместителя; ароматической группы, необязательно замещенной группой заместителя; гетероциклической группы, необязательно замещенной группой заместителя; алкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной алкоксигруппы, необязательно замещенной группой заместителя; тиоалкоксигруппы, необязательно замещенной группой заместителя; ненасыщенной тиоалкоксигруппы, необязательно замещенной группой заместителя; OH; SH; CN; SCN или OCN.
В дополн