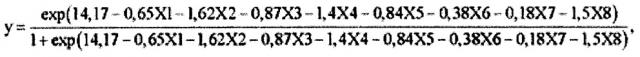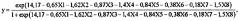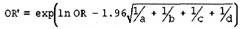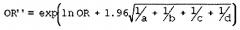Способ прогнозирования риска формирования атопической бронхиальной астмы у детей с аллергическим ринитом
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к педиатрии, пульмонологии и аллергологии. Определяют частоту острого респираторного заболевания (ЧОРЗ). Определяют клинические характеристики острого респираторного заболевания (КХОРЗ). Определяют наличие атопического дерматита в анамнезе (АД). Выявляют факт использования в лечении топических ингаляционных глюкокортикостероидов (ИГКС). Определяют общую физическую работоспособность по степ-тесту (ОФР) в абсолютных величинах. Оценивают признаки в баллах. Затем вычисляют значение z по заявленной формуле. Если значение z≥1,0 прогнозируют высокий риск формирования бронхиальной астмы у детей с аллергическим ринитом. Способ позволяет просто, точно и доступно провести прогноз риска формирования атопической бронхиальной астмы у детей с аллергическим ринитом за счет оценки комплекса наиболее значимых показателей. 2 пр.
Реферат
Изобретение относится к медицине, а именно к педиатрии, пульмонологии и аллергологии, и может быть использовано для прогнозирования развития атопической бронхиальной астмы у детей с аллергическим ринитом.
Многочисленные эпидемиологические исследования доказали тесную взаимосвязь аллергического ринита (АР) и бронхиальной астмы (БА). Доказано, что 30-40% больных АР имеют БА. Пациенты с АР в три раза чаще заболевают БА, чем пациенты, не имеющие АР, при этом БА носит более тяжелое и плохо поддающееся терапии течение. Поэтому актуальным становится проведение профилактических мероприятий у больных с АР.
Существует способ (аналог) прогнозирования формирования бронхиальной астмы (БА) как психосоматического расстройства у детей младшего школьного возраста (патент RU 2373865, 2009). Определяют факторы риска развития бронхиальной астмы, а именно: пол ребенка (x1); наличие: ОРВИ (х2), иммунодефицитных состояний (х3), искусственного вскармливания (х4), наследственной отягощенности по аллергическим заболеваниям (х5), неудовлетворительных бытовых условий (х6); посещения детского дошкольного учреждения (ДДУ) (х7); нарушения вербально-мнестической деятельности (х8). Присваивают им числовые значения, а именно: фактору риска XI в случае мужского пола присваивают 1, а в случае женского пола - 2, для х2-х8 в случае отсутствия фактора риска - 1, а в случае наличия фактора риска - 2, и расчете прогностического коэффициента у по формуле:
значение у>0,5 свидетельствует о благоприятном прогнозе, вероятность возникновения бронхиальной астмы у детей низка. Недостатком данного способа является использование лишь анамнестических данных в качестве риска реализации психосоматических нарушений без учета функциональных возможностей организма больного и атопического фона. Возможности метода ограничены возрастными рамками (младший школьный возраст) и фенотипическими особенностями заболевания (БА как психосоматическое расстройство).
Существует способ (аналог) прогнозирования развития аспириновой бронхиальной астмы у детей (патент 2001121741, 2003) путем сбора анамнеза. Предварительно определяют присутствие признаков аспириновой бронхиальной астмы хотя бы у одного родственника первой степени родства, затем ребенку выполняют пероральный провокационный тест с аспирином и антипириновый тест с определением периода полувыведения и клиренса антипирина, при этом если показатель периода полувыведения антипирина увеличен, а клиренс снижен на 30% и более относительно показателя практически здоровых лиц прогнозируют риск развития аспириновой астмы, а при сочетании этих условий с положительным аспириновым тестом прогнозируют высокую степень риска развития аспириновой астмы у ребенка.
Описанный выше способ прогнозирования формирования БА у детей лимитирован единственным фенотипом заболевания (аспириновая) и анализом анамнестических данных. Кроме того, используют инвазивные методики.
Существует способ (аналог) прогнозирования БА, при котором выделяют ДНК из периферической крови методом фенольно-хлороформной экстракции. Кровь набирают в пробирку с консервантом, содержащим 0,48% лимонной кислоты, 1,32% лимоннокислого натрия, 1,47% глюкозы, в соотношении 6:1, тщательно перемешивают и хранят при температуре 40°C не более одной недели. Для выделения ДНК к 8 мл крови добавляют 32 мл лизирующего буфера, содержащего 320 мМ сахарозы, 1% тритон Х-100, 5 мМ MgCl2, 10 мМ трис-HCl, pH 7,6. Полученную смесь перемешивают и центрифугируют при 4°C, 4000 об/мин в течение 20 минут. Надосадочную жидкость сливают, к осадку повторно приливают 20 мл лизирующего буфера и центрифугируют при тех же условиях в течение 10 мин. К полученному осадку добавляют 400 мкл буфера Soline ЭДТА (25 мМ ЭДТА, pH 8,0 и 75 мМ NaCl), 40 мкл 10% SDS, 30-40 мкл протеиназы К (10 мг/мл) и инкубируют при 37°C в течение 16 часов. После этого из лизата последовательно в три этапа проводят экстракцию ДНК равными объемами забуференного фенола (200 мкл меркаптоэтанола на 50 мл фенола - Трис-HCl, pH 7,8), смесью фенол-хлороформа (1:1) и хлороформа с центрифугированием при 10000 об/мин в течение 10 минут и отбором водной фазы после каждого этапа. ДНК осаждают двумя объемами 96% этанола. Осадок промывают 70% этанолом, подсушивают на воздухе, растворяют в дистиллированной воде и хранят при -20°C. Выделенная ДНК используется для проведения полимеразной цепной реакции синтеза ДНК (ПЦР).
Амплификацию изученных ДНК-локусов (-590С>Т полиморфизма гена IL4 и Ile50Val полиморфизма гена IL4Rα) проводят методом ПЦР синтеза ДНК в 25 мкл общего объема смеси, содержащей 2,5 мкл 10×Taq-буфера (67 мМ трис-HCl (pH 8,8), 16,6 мМ (NH4)2SO4, 1,5 мМ MgCl2, 0,01% Tween-20), 0,1 мкг геномной ДНК, смесь dNTP (dATP, dGTP, dCTP, dTTP по 200 мкМ каждого), 1 ед. ДНК-полимеразы Termus aquaticus (производства фирмы «Силекс», г. Москва) и 5-10 пМ локусспецифичных олигонуклеотидных праймеров. Для определения нуклеотидных замен проводят гидролиз амплифицированных фрагментов соответствующей рестриктазой. Рестрикцию полиморфного локуса -590С>Т гена IL4 проводят эндонуклеазой рестрикции Aν aII, Ile50 Val полиморфизма гена IL4Rα - эндонуклеазой MslI в соответствии с рекомендациями фирм-производителей. Разделение фрагментов ДНК после амплификации и рестрикции проводят при помощи электрофореза в 7% полиакриламидном геле (ПААГ), приготовленном из 30% раствора ПААГ (соотношение акриламид: N,N'-метиленбисакриламид - 29:1).
Частоты аллелей определяются по формуле [Животовский Л.А., Популяционная биометрия. - М.: Наука, 1991].
pi=Ni/N, где Ni - число i-ых аллелей, N - объем выборки.
Стандартная ошибка частоты аллелей рассчитывается по формуле:
При попарном сравнении частот генотипов и аллелей в группах больных и здоровых лиц используется критерий χ2 (Р) для таблиц сопряженности 2×2 с поправкой Иэйтса на непрерывность, вычисляемый по формуле:
где n1 и n2 - объемы сравниваемых распределений; p1 и p2 - частоты соответствующих классов. При числе наблюдаемых случаев <5 используется точный двусторонний критерий Фишера p(F2).
Для выявления факторов повышенного и пониженного риска развития бронхиальной астмы, проводится, для статистически значимо различающихся вариаций вышеуказанных полиморфных ДНК-локусов, оценка статистики связи - показателя отношения шансов (OR - odds ratio), а также границ его 95% доверительного интервала (CI 95%). OR является мерой ассоциации, количественно определяющей взаимосвязь между фактором риска и развитием определенного признака. Степень ассоциаций оценивается в значениях показателя соотношения шансов по формуле: OR=(a×d)/(b×c),
где а - число лиц с наличием, b - с отсутствием маркера среди больных; c и d - число лиц соответственно с наличием и отсутствием маркера среди здоровых. При OR=1 нет ассоциации, OR>1 рассматривается как положительная ассоциация с аллелем или генотипом («фактор повышенного риска») и OR<1 - как отрицательная ассоциация («фактор пониженного риска»). Доверительный интервал для показателя отношения шансов рассчитывается по следующей формуле:
Недостатки указанного способа - трудоемкость и высокая стоимость, что препятствует его использованию в практическом здравоохранении.
Известен способ прогнозирования риска возникновения бронхиальной астмы (аналог) на основании учета роли наследственного фактора, согласно которому считается, что, если один из родителей болен БА, то риск развития БА у ребенка достигает 20-30%, а если больны оба - 75% (Аллергология. Т. 1. Под редакцией чл-кор. РАМН Г.Б. Федосеевой, СПб.: Нормед-Издат, 2001. С. 138). Использование лишь одного показателя определяет низкую точность и информативность данного способа.
Существует способ (аналог) прогнозирования риска развития профессиональной бронхиальной астмы (RU 2583948, 2016). Выявляют наличие родственников с аллергической реакцией, наличие в анамнезе ринита, крапивницы либо другой аллергической реакции, бытовой, пищевой и лекарственной аллергической реакции, профессиональной вредности, при этом дополнительно определяют концентрацию общего IgE в сыворотке крови, в качестве профессиональной вредности определяют «симптомы элиминации», «экспозиционный тест», «эффект реэкспозиции» каждый признак оценивают в баллах. Далее баллы суммируют и при их сумме менее 15 прогнозируют низкую степень риска профессиональной бронхиальной астмы, 16-30 баллов - среднюю степень риска, 31 балл и более - высокую степень риска. Использование данного способа в педиатрической практике неоправданно.
Наиболее близким по технической сущности (прототипом) является способ прогнозирования риска возникновения БА (патент RU 2275863, 2006), при котором пациенту проводят пробы на пыльцевую, пылевую и пищевую аллергии, на непереносимость антибиотиков, анальгетиков, аспирина и при положительных пробах, а также при наличии родственников, страдающих БА, подверженности респираторным инфекциям более двух раз в году, атопического дерматита, экземы, крапивницы и других аллергических синдромов, заболеваний желудочно-кишечного тракта или печени, и профессиональной вредности прогнозируют риск развития заболевания по формуле: R=(S/(S+1))⋅100%, где S=0,0526⋅9X1⋅6X2⋅4X3⋅7X4⋅3X5⋅2X6⋅20X7⋅6X8⋅2X9⋅15X10⋅3X11. При этом X1 - наличие родственников, страдающих БА: при наличии - 1, при отсутствии - 0; Х2 - наличие более двух родственников, страдающих БА: при наличии - 1, при отсутствии - 0; Х3 - подверженность респираторным инфекциям более двух раз в году: при наличии - 1, при отсутствии - 0; Х4 - подверженность вазомоторному риниту: при наличии - 1, при отсутствии - 0; Х5 - наличие атонического дерматита, экземы, крапивницы или других аллергических синдромов: при наличии - 1, при отсутствии - 0; Х6 - наличие заболеваний желудочно-кишечного тракта или печени: при наличии - 1, при отсутствии - 0; Х7 - проба на пыльцевую и пылевую аллергии: при положительной пробе - 1, при отрицательной - 0; Х8 - проба на пищевую аллергию: при положительной пробе - 1, при отрицательной - 0; Х9 - непереносимость антибиотиков: при наличии - 1, при отсутствии - 0; X10 - непереносимость анальгетиков или аспирина: при наличии - 1, при отсутствии - 0; X11 - наличие профессиональной вредности: при наличии - 1, при отсутствии - 0. При значении R более 70% прогнозируют высокий риск возникновения бронхиальной астмы, при значении R 50-70% - средний риск, а при значении R менее 50% - низкий риск. Способ основан на расчете риска заболевания по целому ряду анамнестических и клинических признаков, но лишь у взрослых пациентов. Кроме этого не учитываются функциональные параметры здоровья больного.
Цель предлагаемого способа - упрощение, повышение точности и доступности прогноза риска развития атопической бронхиальной астмы у детей с аллергическим ринитом.
Поставленная цель достигается тем, что вычисляют значение уравнения множественного логистического регрессионного анализа по формуле:
z=-1,9+К1×ЧОРЗ+К2×КХОРЗ+К3×АД+К4×ИГКС+К5×ОФР,
где
-1,9 - константа;
ЧОРЗ - частота острых респираторных заболеваний;
КХОРЗ - клиническая характеристика острых респираторных заболеваний;
АД - наличие атопического дерматита в анамнезе;
ИГКС - использование в лечении топических ингаляционных глюкокортикостероидов;
ОФР - общая физическая работоспособность, определяемая по степ-тесту, в абсолютных величинах.
К1=3,9; К2=1,8; К3=-2,6; К4=2,7; К5=-0,4.
Значение z≥1,0 свидетельствует о неблагоприятном прогнозе, о высоком риске формирования БА у конкретного пациента с АР.
Новизна предлагаемого способа заключается в том, что при расчете риска развития атопической бронхиальной астмы у детей с аллергическим ринитом используют кроме клинических факторов (частота и клиническая картина острого респираторного заболевания) такие показатели, как объем терапии (использование топических ИГКС) и функциональные параметры сердечно-сосудистой системы (ссс) ребенка - реакция ссс на нагрузку (общая физическая работоспособность (ОФР), определяемая по степ-тесту; вычисляют риск развития атопической БA (z) по формуле:
z=-1,9+K1×ЧОРЗ+К2×КХОРЗ+К3×АД+К4×ИГКС+К5×ОФР,
где -1,9 - константа;
ЧОРЗ - частота острых респираторных заболеваний;
КХОРЗ - клиническая характеристика острых респираторных заболеваний;
АД - наличие атопического дерматита в анамнезе;
ИГКС - использование в лечении топических ингаляционных глюкокортикостероидов;
ОФР - общая физическая работоспособность, определяемая по степ-тесту, в абсолютных величинах.
К1=3,9; К2=1,8; К3=-2,6; К4=2,7; К5=-0,4.
И если значение z≥1,0, прогнозируют высокий риск формирования БА у конкретного пациента.
Технические решения, имеющие признаки, совпадающие с отличительными признаками предлагаемого нами способа, не выявлены, что позволяет сделать вывод о соответствии предлагаемого способа критерию «изобретательский уровень».
Предлагаемый способ прогнозирования риска развития атопической бронхиальной астмы у детей с аллергическим ринитом, осуществляется следующим образом:
У детей с аллергическим ринитом определяют показатели: частота острых респираторных заболеваний (ЧОРЗ): при частоте 0-4 раза в год присваивают числовое значение «0»; при 5-6 раза в год - «1», клиническая характеристика острых респираторных заболеваний (КХОРЗ): при отсутствии ОРЗ присваивают числовое значение «0», при наличии ринита - «1», трахеита - «2», бронхита - «3»; наличие атопического дерматита в анамнезе (АД): при отсутствии АД присваивают числовое значение «0», при наличии АД - «1»; использование в лечении топических ингаляционных глюкокортикостероидов (ИГКС): если ИГКС не использовались, то присваивают числовое значение «0», если использовались - «1»; общая физическая работоспособность (ОФР), определяемая по степ-тесту, в абсолютных величинах.
Затем вычисляют значение уравнения множественного логистического регрессионного анализа по формуле (z):
z=-1,9+К1×ЧОРЗ+К2×КХОРЗ+К3×АД+К4×ИГКС+К5×ОФР,
где -1,9 - константа; коэффициенты переменных (β): К1=3,9; К2=1,8; К3=-2,6; К4=2,7; К5=-0,4.
Значение z≥1,0 свидетельствует о неблагоприятном прогнозе, о высоком риске формирования БА у конкретного пациента с АР.
В процессе разработки способа было проведено обследование 126 человек детей с АР. Наблюдение в течение 5 лет (2009-2014) выявило, что за истекший период 43 ребенка сформировали БА. С целью проведения сравнительного анализа дети, не реализовавшие риск развития БА (83 ребенка), составили основную группу, дети с БА составили группу сравнения.
Изучение катамнестических данных среди больных АР позволило осуществить разработку математической модели прогноза риска развития атопической бронхиальной астмы у детей, больных аллергическим ринитом. При этом применен метод множественного логистического регрессионного анализа, который позволяет предсказывать значение одной (бинарной) категориальной величины по двум или более другим.
После включения абсолютных величин кардио-респираторных и силовых тестов, качественных данных катамнеза (заболеваемость, использование в терапии препаратов различных групп (антибиотики, топические ингаляционные глюкокортикостероиды, антилейкотриеновые и антигистаминовые), проверки переменных на коллинеарность и взаимодействие, используя метод включения по А. Вальду), были выбраны 5 предикторных показателей, вошедших в итоговое уравнение: частота ОРЗ (ЧОРЗ), клиническая характеристика ОРЗ (КХОРЗ), наличие атопического дерматита в анамнезе (АД), использование в лечении топических ингаляционных глюкокортикостероидов (ИГКС), общая физическая работоспособность, определяемая по степ-тесту (ОФР) в абсолютных величинах.
Вычисляют риск развития атопической бронхиальной астмы у детей с аллергическим ринитом по формуле:
z=-1,9+К1×ЧОРЗ+К2×КХОРЗ+К3×АД+К4×ИГКС+К5×ОФР,
где -1,9 - константа;
переменные: ЧОРЗ - частота ОРЗ; КХОРЗ - клиническая характеристика ОРЗ; АД - наличие атопического дерматита в анамнезе; ИГКС - использование в лечении топических ингаляционных глюкокортикостероидов; ОФР - общая физическая работоспособность, определяемая по степ-тесту, в абсолютных величинах;
коэффициенты переменных (β):
К1=3,9; К2=1,8; К3=-2,6; К4=2,7; К5=-0,4.
Значение z≥1,0 свидетельствует о неблагоприятном прогнозе, о высоком риске формирования БА у конкретного пациента с АР.
Предлагаемый способ иллюстрируется следующими примерами клинического использования:
Пример 1. Мальчик Леонид 9 лет с аллергическим ринитом, частые ОРЗ, до 10 раз в год (1), протекают с клиникой бронхита (3). При анализе раннего анамнеза выявлено наличие атопического дерматита (1), при лечении аллергического ринита отказывались использовать топические ИГКС (0). При проведении степ-теста ОФР=9,1.
Вычислили значение уравнения множественного логистического регрессионного анализа по формуле:
z=-1,9+3,9×1+1,8×3-2,6×1+2,7×0-0,4×9,1=1,2
Таким образом, z≥1,0, что указывает на риск формирования атопической БА. Это подтверждается клиническими и инструментальными данными: у мальчика имели место эпизоды обратимой бронхиальной обструкции, купированной применением бронхолитиков, Ig>150 ME, ОФВ1<60,0%, положительная проба с бронхолитиками (прирост ОФВ1>12%).
Пример 2. Мальчик Александр 11 лет с аллергическим ринитом, ОРЗ регистрируются редко, до 2 раз в год (0), протекают с клиникой ринита (1). При анализе раннего анамнеза выявлено наличие атопического дерматита (1), при лечении аллергического ринита использовались топические ИГКС (1). При проведении степ-теста ОФР=12,6.
Вычислили значение уравнения множественного логистического регрессионного анализа по формуле:
z=-1,9+3,9×0+1,8×1-2,6×1+2,7×1-0,4×12,6=-5,04.
Таким образом, z<1,0, что указывает на отсутствие риска формирования атопической БА у данного пациента. Это подтверждается клиническими и инструментальными данными: у мальчика отсутствовали эпизоды обратимой бронхиальной обструкции, по результатам функции внешнего дыхания (ОФВ1=100,0%), отрицательная проба с бронхолитиками (прирост ОФВ1<12%).
Предлагаемый способ прогнозирования риска развития атопической бронхиальной астмы у детей с аллергическим ринитом применен в ГУЗ ЯО «Детская поликлиника №3» и может быть использован как в амбулаторных, так и стационарных условиях.
Способ прогнозирования риска формирования атопической бронхиальной астмы у детей с аллергическим ринитом, включающий определение частоты острого респираторного заболевания (ЧОРЗ), клинической характеристики острого респираторного заболевания (КХОРЗ), наличия атопического дерматита в анамнезе (АД), отличающийся тем, что дополнительно определяют факт использования в лечении топических ингаляционных глюкокортикостероидов (ИГКС) и общую физическую работоспособность по степ-тесту (ОФР) в абсолютных величинах, оценивают признаки в баллах: ЧОРЗ присваивают «0 баллов» при частоте 0-4 раза в год, «1 балл» при частоте 5-6 раз в год; КХОРЗ присваивают «0 баллов» при отсутствии ОРЗ, «1 балл» при наличии ринита, «2 балла» - трахеита, «3 балла» - бронхита; АД присваивают «0 баллов» при отсутствии и «1 балл» при наличии; ИГКС присваивают «0 баллов», если не использовались и «1 балл», если использовались; затем вычисляют значение z по формуле:
z=-1,9 + К1 × ЧОРЗ + К2 × КХОРЗ + К3 × АД + К4 × ИГКС + К5 × ОФР,
где -1,9 - константа;
К1=3,9; К2=1,8; К3=-2,6; К4=2,7; К5=-0,4 - коэффициенты переменных,
и если значение z≥1,0, прогнозируют высокий риск формирования бронхиальной астмы у детей с аллергическим ринитом.