Рекомбинантный штамм мицелиального гриба penicillium canescens cl14, продуцирующий компонент целллюлосомы clostridium thermocellum, и способ его культивирования
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Предложен рекомбинантный штамм мицелиального гриба Penicillium canescens СL14 ВКМ F-4706D, продуцирующий бактериальную термофильную целлюлазу Cel5L из Clostridium thermocellum с молекулярной массой 48 кДа. Указанный штамм получают путем трансформации исходного штамма P.canescens RN3-11-7 niaD(-) плазмидой, несущей ген celL, кодирующей целлюлазу Cel5L из бактерии Clostridium thermocellum. Предложен также способ культивирования указанного штамма, включающий выращивание штамма на питательной среде следующего состава (г/л): соевая мука – 45, кукурузный экстракт – 40, KH2PO4 – 6, CaCl2 - 0,23, MgSO4×7H2O - 0,3, дрожжевой экстракт – 10, пшеничные отруби – 10. Группа изобретений обеспечивает эффективную продукцию целлюлазы Cel5L из Clostridium thermocellum в гетерологичном грибном штамме-хозяине. 2 н.п. ф-лы, 6 ил., 1 табл., 4 пр.
Реферат
Изобретение в области биотехнологии относится к микробиологической промышленности и представляет собой способ получения и культивирования рекомбинантного штамма мицелиального гриба Penicillium canescens CL14 ВКМ F-4706D, секретирующего термостабильную целлюлазу Cel5L из Clostridium thermocellum.
Реконструкция целлюлосомы in vitro является технологически востребованной задачей в связи с уникальными гидролитическими свойствами комплекса бактериальных целлюлаз по отношению к целлюлозосодержащим растительным материалам [Roy H.Doi and Akihiko Kosugi, Cellulosomes: Plant-Cell-Wall-Degrading Enzyme Complexes, Nature Reviews, 2004, V.2, 541-551]. Разработка нового рекомбинантного штамма на основе мицелиального гриба Penicillium canescens, продуцирующего термостабильную целлюлазу 5-го семейства гликозил-гидролаз, Cel5L, позволит получить новый компонент целлюлосомы грамположительной бактерии Clostridium thermocellum, что является необходимым шагом для реконструкции целлюлосомы in vitro. Техническая значимость создания синтетической целлюлосомы (реконструкции) состоит в способности бактериальных целлюлаз к синергетическому взаимодействию, что приводит к повышению эффективности каталитического расщепления растительных полимеров до технических сахаров [Stern J, Kahn A, Vazana Y, Shamshoum M, Moraïs S, Lamed R, et al. (2015) Significance of Relative Position of Cellulases in Designer Cellulosomes for Optimized Cellulolysis. PLoS ONE 10(5): e0127326. doi:10.1371/journal.pone.0127326].
Cel5L является одной из основных структурных единиц целлюлосомы Clostridium thermocellum, мультиферментного комплекса, состоящего из ряда целлюлаз с различной субстратной специфичностью. Недавно было показано, что фермент Cel5L обладает свойствами процессивной целлобиозидазы, включая высокую активность по отношению к аморфной и кристаллической целлюлозе, а также существенной активностью по β-глюкану [Pillip J.Brumm et al, Clostridium thermocellum Cel5L- Cloning and Characterization of a New, Thermostable GH5 Cellulase, IJBcRR, 2015, V.6(2), 62-74].
К числу наиболее перспективных микроорганизмов для получения ферментных препаратов карбогидраз на сегодняшний день относятся микроскопические грибы рода Trichoderma, Penicillium, а также Aspergillus, что обусловлено в основном их высоким уровнем секреции внеклеточных ферментов [Gusakov A.V. Alternatives to Trichoderma reseei in biofuel production / Trends in Biotechnology. – 2011. - T. 29. - № 9. - С. 419-425, Чекушина А.В., Доценко Г.С., Синицын А.П. / Сравнение эффективности процессов биоконверсии растительного сырья с использованием биокатализаторов на основе Penicillium и Trichoderma. // Катализ в промышленности. – 2012. - № 6. - С. 68-76].
Полученные ранее патенты показывают, что одним из возможных биотехнологически значимых микроорганизмов может являться штамм P.canescens RN3-11-7 niaD(-), неоднократно успешно используемый как реципиент для получения продуцентов гомологичных и гетерологичных белков с использованием сильных промоторов гена ксиланазы и β-галактозидазы, например гетерологичной эндо-1,4-β-глюканазы III P.verruculosum с использованием сильных промоторов гена ксиланазы и β-галактозидазы [Рожкова А.М. Волков П.В., Кондратьева Е.А., Сатрутдинов А.Д. и др. Создание продуцентов биотехнологически важных ферментов на основе рекомбинантного штамма гриба Penicillium canescens. Хранение и переработка сельхозсырья. – 2010. - № 7. - С. 37-39, патент РФ2238974 (С2) опубл. 27.10.2004, ДНК-фрагмент мицелиального гриба Penicillium verruculosum, кодирующего синтез секретируемой эндоглюканазы и группа штаммов Penicillium сanescens, продуцирующих эндоглюканазу III Penicillium verruculosum, cконструированных методами трансформации и генетической инженерии, основываясь на этих фрагментах], α-галактозидазы и пектинлиазы А из P.canescens, целлобиогидролазы I, целлобиогидролазы II и ЭГ II из P.verruculosum [Бушина Е.В., Рожкова А.М., Зоров И.Н., Сатрутдинов А.Д., Беккаревич А.О., Кошелев А.В., Окунев О.Н., Синицын А.П. Создание комплексных ферментных препаратов пектиназ и целлюлаз для переработки свекловичного жома. // Прикладная биохимия и микробиология. – 2012. – T. 48. - № 5. - С. 543-549], β-глюкозидазы и инулиназ из A.niger [Волков П.В., Синицына О.А., Федорова Е.А., Рожкова А.М., Сатрутдинов А.Д., Зоров И.Н., Окунев О.Н., Гусаков А.В., Синицын А.П. Выделение и свойства рекомбинантных инулиназ Aspergillus sp. // Биохимия. – 2012. - Т. 77, - № 5. - С. 611-621]. В качестве примера, демонстрирующего потенциал гриба Penicillium canescens как реципиента для экспрессии гетерологичных генов, следует привести монографию [Sinitsyn AP and Rozhkova AM, Penicillium canescens host as the platform for development of a new recombinant strains producers of carbohydrases, Microbiology Monographs, «Mocroorganisms in Biorefineries», Ed. B.Kamm, Springer, 2015, p.1-19, ISSN 1862-5576, ISBN 978-3-662-45208-0, DOI 10.1007/978-3-662-45209-7, Springer].
Прототипом разработанного технического решения может служить патент РФ № 2378372 «Генетическая конструкция для обеспечения экспрессии целевых гомологичных и гетерологичных генов в клетках мицелиального гриба Penicillium verruculosum, используемого в качестве хозяина, способ получения штамма гриба Penicillium verruculosum и способ получения ферментного препарата».
Техническая задача, решаемая в результате применения группы разработанных технических решений, состоит в создании штамма-продуцента путем трансформации исходного штамма P.canescens RN3-11-7 niaD(-) плазмидой, несущей ген celL, кодирующей термостабильную целлюлазу Cel5L из Clostridium thermocellum, и подбор среды для культивирования полученного штамма-продуцента с целью получения полноразмерного белка Cel5L.
Техническим результатом, получаемым при реализации разработанных технических решений, является возможность эффективной продукции целлюлазы из Clostridium thermocellum в гетерологичном хозяине Penicillium canescens RN3-11-7 niaD(-).
Для получения указанного технического результата используют полинуклеотидную последовательность гена целевого белка. Целевая плазмида содержит кодирующую последовательность гена celL и функционально связанные с ним регуляторные элементы, промотор и терминатор гена ксиланазы А (xylA) из P.canescens. При реализации указанного способа получают штамм гриба Penicillium canescens CL14 ВКМ F- F-4706D, мультикопийный по гену celL из C.thermocellum.
Кроме того, для получения указанного технического результата предложен способ культивирования полученного штамма-продуцента P.canescens, секретирующего целевой белок Cel5L, на среде, состав которой существенно отличается от стандартной среды для культивирования гриба P.canescens. Одним из ключевых изменений в составе среды является добавление дополнительного количества хлорида кальция и замена дрожжевого экстракта на соевую муку, обеспечивающего стабильность секретируемого целевого белка Cel5L.
Указанные варианты не исчерпывают возможности разработанного способа получения рекомбинантных штаммов P.canescens, экспрессирующих гетерологичные гены из C.thermocellum.
Схема разработки способа получения каждого из рекомбинантных штаммов, секретирующих целлюлосомальные ферменты из C.thermocellum, состоит из трех типовых этапов.
Этап 1. Амплифицируют целевой ген целлюлосомального фермента из C.thermocellum – celL, а также промоторную и терминаторную область гена xylA из P.canescens. Конструируют плазмиду pCelL, представляющую собой полинуклеотидную последовательность, состоящую из промоторной области гена xylA, сигнального пептида, целевого гена celL и терминаторной области гена xylA.
Этап 2. Проводят трансформацию реципиентного высокопродуктивного штамма P.canescens RN3-11-7 niaD(-) целевой плазмидой pCelL, полученной на Этапе 1, в условиях котрансформации вместе с плазмидой, несущей последовательность niaD гена, как маркера селекции, и осуществляют отбор трансформантов, секретирующих в культуральную жидкость целевой фермент. Проводят ферментацию отобранных трансформантов в качалочных колбах и среди них выбирают наиболее продуктивные варианты штаммов-продуцентов.
Этап 3. Подбирают оптимальные условия культивирования наиболее продуктивного варианта штаммов-продуцентов, обеспечивающих стабильность целевого белка во время культивирования и его максимальную продуктивность.
Изобретение иллюстрируется следующими примерами.
Пример 1
Получение целевой плазмиды pCelL заключалось в клонировании гена сelL [https://www.ncbi.nlm.nih.gov/genome/?term=Clostridium+thermocellum] в универсальный вектор, обеспечивающий экспрессию целевого гена под контролем промотора и терминатора гена xylA из P.canescens.
Амплификацию гена celL из C.thermocellum проводили с использованием праймеров соответствующего состава:
CLU 5' GCACAGGCAGCAGGAGCTTCGCCCACTGTTGCTGCTGATC 3'
CLL 5' AGAGCAAGCCGAGCAGGTTACTCCAGAATAGGAATCTTC 3'
Методом секвенирования по Сэнгеру были определены нуклеотидные последовательности полученных фрагментов. Схематическое изображение структуры экспрессионных кассет показано на Рис. 1. Косым штрихом на Рис.1 обозначена промоторная область гена ксиланазы А (xylA) из P.canescens, черным цветом – сигнальный пептид (bgaS SS), прямым штрихом - целевой ген из C.thermocellum (celL), квадратным штрихом – терминаторная область гена ксиланазы А (xylA) из P.canescens.
Аминокислотная последовательность целевого фермента CEL5L представлена на Рис.2, где подчеркнут сигнальный пептид β-галактозидазы.
Пример 2. Трансформация высокопродуктивного штамма-реципиента P.canescens RN3-11-7 niaD(-) плазмидами, указанными в Примере 1, для получения набора рекомбинантных штаммов, секретирующих целлюлосомальный фермент Cel5L из C.thermocellum.
К смеси двух плазмид (1 мкг котрансформационной плазмиды PSTA10, несущей ген niaD из A.niger, и 10 мкг плазмиды pCelL, несущей ген celL из C.thermocellum) объемом 20 мкл добавляют 200 мкл раствора протопластов штамма P.canescens RN3-11-7 niaD(-), полученных по методике, описанной в статье [A. Y. Aleksenko, N. A. Makarova, I. V. Nikolaev, A. J. Clutterbuck Integrative and replicative transformation of Penicillium canescens with a heterologous nitrate-reductase gene, Curr. Genet. - 1995. - V. 28. - P. 474-477] и 50 мкл буфера PCT1, содержащего: 50 %-ный ПЭГ 4000 (по объему)+ 0.01M трис-HCl pH 7.5 + 0.02M CaCl2. Смесь аккуратно перемешивают и оставляют на 20 мин во льду. Затем добавляют 500 мкл буфера PCT1 и оставляют на 5 мин при комнатной температуре. Параллельно проводят эксперимент с контрольными протопластами без добавления ДНК. Далее пробирки со смесью протопластов и ДНК центрифугируют при 5000 об/мин в течение 20 мин. Супернатант сливают, а осадок ресуспендируют в 200 мкл стерильного раствора сорбитола (182,2 г/л). Трансформационную смесь стерильно переносят над пламенем горелки в 5 мл верхнего агара (для приготовления 100 мл верхнего агара берут 21,86 г 1,2 М сорбитола, 0,7 г агара, 0,8 г глюкозы, 1 мл 1 М источника азота) перемешивают и распределяют агар по поверхности предварительно подготовленных чашек с нижним агаром (для приготовления 100 мл нижнего агара берут 21,86 г 1,2 М сорбитола, 2 г агара, 0,8 г глюкозы, 1 мл 1М источника азота). Так же переносят и контрольные смеси.
Готовят три чашки Петри с нижним агаром, две с селективной средой (источник азота: NaNO3 10 мM) и одна – с неселективной (источник азота: NH4Cl 10 мM). Чашки Петри помещают в инкубатор на 30°С и оставляют там на 6 дней. На шестой день роста трансформанты переносят на селективную минимальную среду (источник азота: NaNO3 10 мM). В результате трансформации реципиентного штамма P.canescens RN3-11-7 смесью плазмид получают около от 90 до 170 трансформантов на 10 мкг введенной целевой ДНК, что соответствует стандартной частоте трансформации грибных штаммов.
Чтобы среди полученных трансформантов отобрать штаммы, в хромосоме которых содержится встроенный ген целевого белка, проводят первичный скрининг трансформантов методом ПЦР-реакции. Скрининг трансформантов pCELL осуществляли с использованием пары праймеров CLU и CLL. Размер полученного ПЦР-продукта ~1500 п.н. соответствует размеру полинуклеотидной последовательности гена celL из C.thermocellum (Рис. 3, РС – штамм-реципиент, 1-23 – трансформанты, PR – плазмида pCELL, отобранные для культивирования клоны подчеркнуты).
Пример 3. Получение рекомбинантных штаммов P.canescens CL14, мультикопийного по гену celL из C.thermocellum (5-е семейство гликозид-гидролаз, теоретическая молекулярная масса 50 кДа).
Полученные в Примере 2 позитивные по целевому гену celL трансформанты пересевают на чашки с минимальной средой и источником азота NaNO3 и инкубируют при 28ºС в течение 140 часов до образования конидий. Затем трансформанты ферментируют в качалочных колбах, используя ферментационную среду следующего состава, в г/л: соевая шелуха – 45, кукурузный экстракт – 50, KH2PО4 – 25. Колбы инкубируют на качалке при 30оС и 220 об/мин в течение 144 ч. Далее отбирают рекомбинантные штаммы, ферментный комплекс которых содержит целевой белок.
Для культуральной жидкости отобранных штаммов проводят ДДС-электрофорез в денатурирующих условиях, чтобы идентифицировать полосу, соответствующую целевому белку Cel5L (см. Рис. 4, соответствующая полоса обведена овалом). Для доказательства принадлежности экспрессированного белка к целлюлазе CEL5L был проведен масс-спектрометрический анализ образцов полос, вырезанных из гелей, молекулярная масса которых соответствовала искомой - 45-50 кДа. Результаты MALDI-TOF спектрометрии подтвердили наличие ожидаемого CEL5L белка (см. Рис. 5, совпадающие пептиды обозначены подчеркиванием).
Таким образом, среди полученных трансформантов был выбран штамм Penicillium canescens CL14, который был депонирован в Всероссийскую коллекцию микроорганизмов под номером ВКМ F-4706 D.
Пример 4. Оптимизация условий культивирования рекомбинантного штамма P.canescens CL14, мультикопийного по гену celL из C.thermocellum.
Поскольку стандартная среда для культивирования гриба P.canescens содержит 25 г/л дигидрофосфата калия, то в процессе культивирования в среде должен наблюдаться дефицит ионов кальция, выпадающего в осадок в виде фосфата. В отсутствие ионов кальция в среде для культивирования целлюлосомальный белок Cel5L из C.thermocellum нестабилен, что приводит к деформации белковой глобулы фермента и доступности сайтов протеолиза. Поэтому при формировании состава сред, представленных в Таблице 1, был учтен предыдущий опыт работы с бактериальными целлюлазами, экспрессированными в грибном реципиенте (Среды 1-4, с постепенным снижением количества фосфат-ионов и введением ионов кальция). Основной особенностью сред 5-8 является полная замена соевой шелухи на соевую муку с постепенным снижением концентрации соевой муки в среде и введением стабилизирующих компонентов, взятых на основании предыдущих экспериментов с экспрессией другой целлюлазы Cel48S в грибном штамме Penicillium canescens.
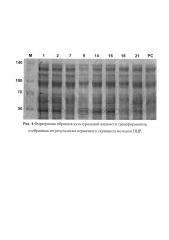
На фореграммах образцов культуральной жидкости рекомбинантных штаммов P.canescens CL14 в 12%-ном ПААГ на 6-е сутки культивирования (Рис. 6) видно, что при использовании сред 1-4 с соевой шелухой молекулярная масса целлюлазы Cel5L ниже теоретически посчитанной (трек 4, Рис. 6, примерно 43-44 кДа), что может быть связано с протеолитическим отщеплением С-конца белка. При замене соевой шелухи на соевую муку в случае использования среды 6 (трек 6, Рис.6, обведено овалом) наблюдалось изменение положения полосы, соответствующей целлюлазе Cel5L. Молекулярная масса Cel5L в случае использования среды 6 составляла 48 кДа, что соответствует теоретической. Следует отметить, что среда 5 (трек 5, Рис.6) без добавления стабилизирующих агентов приводила к увеличению экспрессии целевого, но неполноразмерного белка, а среды 7 и 8 со сниженным содержанием соевой муки приводили к низкой экспрессии Сel5L (данные не приведены).
Таким образом, целевой белок, Cel5L, был стабилизирован в результате снижения концентрации дигидрофосфата калия до 6 г/л, добавления 0,23 г/л хлорида кальция и замене соевой шелухи на соевую муку в концентрации 45 г/л.
Анализируя полученные данные, можно заключить, что состав среды № 6 является оптимальным для культивирования рекомбинантного штамма P.canescens CL14 ВКМ F-4706D.
Таблица 1
Состав сред для культивирования продуцента P.canescens CL14
| Компоненты, г/л | Номер среды | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |
| Соевая шелуха | 45 | 45 | 45 | 45 | ||||
| Соевая мука | 45 | 45 | 35 | 35 | ||||
| Кукурузный экстракт | 50 | 50 | 50 | 40 | 40 | 40 | 50 | 50 |
| KH2PO4 | 25 | 12,5 | 6 | 6 | 6 | 6 | 6 | 6 |
| CaCl2 | - | - | - | 0,23 | - | 0,23 | - | 0,23 |
| MgSO4×7H2O | - | - | - | 0,3 | - | 0,3 | - | |
| Дрожжевой экстракт | - | - | - | 10 | - | 10 | - | |
| Пшеничные отруби | - | - | - | 10 | - | 10 | - |
1. Рекомбинантный штамм гриба Penicillium canescens CL14 (ВКМ F-4706D), продуцирующий бактериальную термофильную целлюлазу Clostridium thermocellum c молекулярной массой 48 кДа.
2. Способ культивирования штамма по п. 1, отличающийся тем, что штамм по п. 1 выращивают на питательной среде следующего состава, г/л: соевая мука - 45, кукурузный экстракт - 40, КН2РО4 - 6, СaCl2 - 0,23, MgSO4×7H2O - 0,3, дрожжевой экстракт - 10, пшеничные отруби - 10.