Штамм бактерий pseudomonas fluorescens для защиты растений от фитопатогенных грибов и бактерий и стимуляции роста растений
Иллюстрации
Показать всеИзобретение относится к микробиологии. Предложен штамм бактерий Pseudomonas fluorescens BS1506 для защиты растений от фитопатогенных грибов и бактерий и стимуляции роста растений. Штамм выделен из ризосферы диких злаков, растущих на территории очистных сооружений г. Пущино. Штамм бактерий Pseudomonas fluorescens депонирован во Всероссийской коллекции микроорганизмов ИБФМ им. Г.К. Скрябина РАН под номером ВКМ B-2955D. Штамм способен подавлять развитие фитопатогенных грибов и бактерий за счет продукции гетероциклических антибиотиков феназин-1-карбоновой кислоты и феназин-1-карбоксамида и стимулировать рост растений за счет повышения биодоступности фосфатов. 4 ил., 5 табл., 7 пр.
Реферат
Изобретение относится к микробиологической промышленности и биотехнологии и касается нового бактериального штамма Pseudomonas fluorescens ВКМ В-2955Д, обладающего способностью подавлять развитие фитопатогенных грибов и бактерий за счет продукции феназиновых антибиотиков и стимулировать рост растений за счет растворения неорганических фосфатов. Предлагаемый штамм может быть использован для получения на его основе бактериального препарата.
В настоящее время одной из наиболее важных мировых проблем остается обеспечение продуктами сельскохозяйственного производства растущего населения планеты. Серьезной проблемой растениеводства являются фитопатогенные микроорганизмы и вредители, приводящие ежегодно к 30% потерям в мировом сельскохозяйственном производстве (Tilman D., Balzer C., Hill J., Beford B.L. Global food demand and the sustainable intensification of agriculture // Proc. Natl. Acad. Sci. - 2011. - №108. - P. 20260-20264). Поэтому повышение урожайности сельскохозяйственных культур и создание эффективных и экологичных способов борьбы с фитопатогенными микроорганизмами становится все более актуальной задачей.
Анализ мирового опыта показывает возрастающую роль биологических средств защиты растений в комплексе природоохранных мероприятий, которые в отличие от химических пестицидов, безвредны для окружающей среды и потребителя. Разработкой и производством коммерческих биопрепаратов для сельского хозяйства на основе PGPR Pseudomonas интенсивно занимаются практически во всех развитых странах (Lucy М., Reed Е., Glick B.R. Applications of free living plant growth-promoting rhizobacteria // Antonie van Leeuwenhoek. - 2004. - V. 86. - P. 1-25).
Известно, что PGPR Pseudomonas способны продуцировать широкий спектр антибиотических веществ, которые ингибируют рост и метаболизм других микроорганизмов при незначительных концентрациях (Haas D., and Biological control of soil-born pathogens by fluorescent pseudomonads // Nat. Rev. Microbiol. - 2005. - V. 3(4). - P. 307-319). Наиболее хорошо изученными антибиотиками, играющими важную роль в подавлении болезней растений, являются гетероциклические феназиновые антибиотики. Известно, что феназин-1-карбоновая кислота является относительно слабыми антибиотиком (Смирнов В.В., Киприанова Е.А. Бактерии рода Pseudomonas. - Киев; Наук. думка, 1990. - 264 с.). Ее антагонистическое действие зависит от кислотности среды и значительно снижается при повышении pH. Феназин-1-карбоксамид менее подвержен влиянию кислотности среды. (Chin-A-Woeng T.F.C., G.V. Bloemberg, A.J. van der Bij, K.M.G.M. van der Drift, J. Schripsema, B. Kroon, et al. Biocontrol by phenazine-1-carboxamide-producing Pseudomonas chlororaphis PCL1391 of tomato root rot caused by Fusarium oxysporum f. sp. radicis-lycopersici // Mol. Plant Microbe Interact. - 1998. - V. 11(11). - P. 1069-1077; Patent US 20140309232). Например, при pH 5.7 феназин-1-карбоксамид был в десять раз активнее в отношении фитопатогена Fusarium oxysporum f. sp. radices-lycopersici по сравнению с феназин-1-карбоновой кислотой. Активность феназин-1-карбоновой кислоты полностью уменьшалась при повышении pH до 5.9-7, в то время как антифунгальная активность феназин-1-карбоксамида сохранялась при всех исследованных значениях pH 3.1-7.
Известен штамм бактерий Pseudomonas sp. ЦМПМ В-348, используемый для получения препарата при защите злаковых от возбудителя обыкновенной корневой гнили Helminthosporium sativum (Авторское свидетельство СССР №1464468).
Однако этот штамм неэффективен для подавления корневой гнили злаков, вызываемой комплексом грибов Fusarium spp. и Helminthosporium sativum.
Известен штамм бактерий Pseudomonas putida BKM В-1743Д, подавляющий рост грибов рода Fusarium, и предназначенный для получения препарата, используемого для стимуляции роста растений и защиты растений от грибных патогенов (Патент RU 1805849).
Недостатком штамма является узкий спектр антагонистического действия.
Известен штамм бактерий Pseudomonas species В-696, проявляющий антагонистическую активность к фитопатогенным грибам Alternaria spp., Bipolaris sorokiniana, Fusarium oxysporum, Fusarium gibbosum, Fusarium sumbucinum, и препарат на его основе, используемый для стимуляции роста и защиты растений от фитопатогенных микроорганизмов (Патент RU 2130261).
Однако отсутствуют сведения о действии этого штамма на такие широко распространенные возбудители болезней растений, как Fusarium culmorum, Fusarium graminearum, Fusarium nivale, Fusarium semitectum, Fusarium solani.
Известен штамм бактерий Pseudomonas aureofaciens ИБ 51, проявляющий антагонистическую активность по отношению к фитопатогенным грибам Alternaria alternata, Bipolaris sorokiniana, Fusarium oxysporum, Fusarium gibbosum, Fusarium culmorum, Fusarium graminearum, Fusarium nivale, Fusarium oxysporum, Fusarium semitectum, Fusarium solani, Penicillium funiculosum (Патент RU 2203945).
Однако отсутствуют сведения о действии этого штамма на такой широко распространенный возбудитель заболевания корней пшеницы как Gaeumannomyces graminis var. tritici.
Известен штамм бактерий Pseudomonas aureofaciens Тх-1 (АТСС 55670) и метод его применения для контроля грибных и бактериальных инфекций растений. Метод основан на применении культуральной жидкости штамма Pseudomonas aureofaciens Тх-1, содержащей бактериальные клетки данного штамма и биологически активные метаболиты, главным образом феназин-1-карбоновую кислоту. Метод применим для обработки двудольных, однодольных и хвойных растений, рассады и семян (Patent US 6348193).
Однако отсутствуют сведения о содержании в культуральной жидкости бактериального штамма Pseudomonas aureofaciens Тх-1 других феназиновых производных, в частности феназин-1-карбоксамида.
Известен трансгенный флуоресцирующий штамм бактерий Pseudomonas sp. для биоконтроля грибных болезней растений. Данный штамм содержит локус для биосинтеза феназин-1-карбоновой кислоты, стабильно встроенный в геном и собственные гены для продукции антибиотика 2,4-диацетилфлороглюцина. Таким образом, штамм способен продуцировать два антибиотика - феназин-1-карбоновую кислоту и 2,4-диацетилфлороглюцин. Штамм подавляет фитопатогенные грибы родов Rhizoctonia, Gaeumannomyces graminis и Pythium (Patent US 6277625).
Недостатком штамма является то, что он получен в результате генетических манипуляций и представляет собой генетически модифицированный микроорганизм.
Известен биоинженерный штамм Pseudomonas sp., для продукции нового микробиологического фунгицида, главным компонентом которого является феназин-1-карбоксамид. Данный штамм получен в результате трансформации родительского штамма-продуцента феназин-1-карбоновой кислоты Pseudomonas spp. M18 или M18G рекомбинантной плазмидой, несущей ген phzH, в результате чего биоинженерный штамм становится способным продуцировать феназин-1-карбоксамид. Штамм подавляет фитопатогенные грибы родов Pythium, Phytophthora и Rhizoctonia (Patent US 20140309232).
Недостатком штамма является то, что он получен в результате генетических манипуляций и представляет собой генетически модифицированный микроорганизм.
Особенностью изобретения является использование в качестве фунгицида культуральной жидкости (fermentation broth), содержащей феназин-1-карбоксамид или выделенный из нее антибиотик.
Известен штамм Pseudomonas aeruginosa B5 и метод получения из его культуральной жидкости рамнолипида B и оксихлорорафина (феназин-1-карбоксамида). Штамм проявляет антифунгальную активность против фитопатогенных грибов М. grisea, Alternaria mali, Alternaria panax, Alternaria slani, Botryosphaeria dothidia, Cercospora capsici, Botryosphaeria dothidia, Cercospora capsici, Cercospora kikuchi, Cladosporium и т.д. (Patent KR 20010038285).
Недостатком штамма является то, что вид бактерий Pseudomonas aeruginosa относится к условно-патогенным микроорганизмам (4 группа патогенности).
В качестве прототипа выбран штамм Pseudomonas chlororaphis NCIMB 40616, обладающий способностью продуцировать биологически активные антифунгальные метаболиты, подавляющие рост фитопатогенных грибов родов Drechslera, Microdochium, Tilletia и Ustilago, которые вызывают наиболее распространенные инфекционные болезни зерновых культур. Штамм может быть применим для обработки семян растений, вегетирующих растений и среды для выращивания растений (Patent US 5,900,236).
Однако в патенте отсутствуют сведения о химической природе продуцируемых антифунгальных метаболитов. Из описания не ясно, имеются ли в культуральной жидкости бактериального штамма Pseudomonas chlororaphis NCIMB 40616 феназиновые производные, в частности феназин-1-карбоновая кислота и феназин-1-карбоксамид. Отсутствуют сведения о действии этого штамма на такой широко распространенный возбудитель пшеницы как Gaeumannomyces graminis var. tritici, а также на фитопатогенные грибы родов Pythium, Fusarium и Rhizoctonia.
Кроме того, во всех перечисленных аналогах и прототипе нет сведений о способности штаммов-антагонистов фитопатогенных грибов повышать доступность труднорастворимых фосфатов.
Известно, что фосфор является вторым элементом после азота по значению в питании растений. Он присутствует в почве в виде органических (отложения растительного, животного и микробного происхождения) и неорганических или минеральных соединений. Однако из этого общего пула фосфорных соединений только 1-5% доступны растениям (Molla М., and Chowdhury АА. Microbial mineralization of organic phosphate in soil // Plant Soil. - 1984. - V. 78. - P. 393-399). Некоторые микроорганизмы, в особенности микоризные грибы и некоторые ризобактерии, принадлежащие к родам Pseudomonas, Bacillus и Rhizobium, способны усиливать поступление фосфора в растения (Rodriguez Н., Fraga R. Phosphate solubilizing bacteria and their role in plant growth promotion // Biotechnol. Adv. - 1999. - V. 17(4-5). - P. 319-339). Способность ризосферных бактерий растворять неорганические фосфаты почвы считается одним из важнейших фитостимулирующих свойств и учитывается при использования таких микроорганизмов для создания биопрепаратов.
Задачей изобретения является выделение нового природного штамма бактерий, используемого для защиты растений от фитопатогенных грибов и бактерий за счет синтеза гетероциклических антибиотиков феназин-1-карбоновой кислоты и феназин-1-карбоксамида и стимуляции роста растений за счет растворения неорганических фосфатов.
Техническим эффектом, который может быть получен при использовании предлагаемого штамма, является улучшение урожайности сельскохозяйственных культур и качества сельскохозяйственной продукции за счет подавления грибных и бактериальных инфекций растений и повышения биодоступности фосфатов.
Поставленная задача достигается выявлением и использованием бактериального штамма Pseudomonas fluorescens О9-10, выделенного из ризосферы диких злаков, растущих на территории очистных сооружений г. Пущино (Московская область).
Штамм Pseudomonas fluorescens O9-10 имеет лабораторный номер BS1506 и депонирован во Всероссийской коллекции микроорганизмов ИБФМ им. Т.К. Скрябина РАН под номером ВКМ В-2955Д.
Штамм Pseudomonas fluorescens ВКМ В-2955Д характеризуется следующими признаками.
Среды культивирования
Штамм хорошо растет на следующих средах (г/л, мл/л): LB (бакто-триптон - 10, дрожжевой экстракт - 5, хлористый натрий - 10, pH 7.2); Кинга Б (пептон - 20, K2HPO4 - 1.5, MgSO4×7H2O - 1.5, глицерин - 10); триптозо-соевом агаре (триптозо-соевый экстракт - 30); минеральной синтетической среде М9 (Na2HPO4 - 6, KH2PO4 - 3, NH4Cl - 1, NaCl - 0.5, 1М MgSO4 - 2,1M CaCl2 - 1, глюкоза - 2).
Морфология колоний
Морфологию колоний на питательных средах определяли после 4-5 сут роста при 28°C.
Колонии на среде LB круглые с ровными краями, гладкие, слабовыпуклые, непрозрачные, бежевые, не слизистой консистенции, диаметр 5-6 мм, пигмент не выражен.
На среде Кинга Б колонии зеленые, пигмент интенсивно-зеленый флуоресцирующий, диффундирует в среду.
Культурально-морфологические признаки
Клетки подвижные, палочковидные, с полярными жгутиками, грамотрицательные, спор не образуют.
Физиолого-биохимические признаки
Облигатный аэроб, температурный оптимум роста 24-30°C, растет при 4°C, растет в пределах pH среды от 5.2 до 8.0; оптимальное для роста значение pH 6.8-7.4.
В дополнительных факторах роста не нуждается (прототроф).
В качестве источника углерода использует глюкозу, трегалозу, глицерин, янтарную кислоту, бензойную кислоту, антранилат, мезо-инозит.
Разжижает желатин
Проверенные неиспользуемые источники углерода: ксилоза, сахароза, гиппуровая кислота, фенилуксусная кислота, адипиновая кислота, салициловая кислота, нафталин, фенантрен, камфора, гексадекан, капролактам.
Устойчивость к антибиотикам
Штамм проявляет устойчивость к карбенициллину (1000 мкг/мл), цефтазидиму (20 мкг/мл), цефепиму (20 мкг/мл), меропенему (20 мкг/мл), гентамицину (20 мкг/мл), амикацину (30 мкг/мл), тобрамицину (50 мкг/мл), стрептомицину (50 мкг/мл), тетрациклину (30 мкг/мл), хлорамфениколу (100 мкг/мл). Чувствителен к канамицину (50 мкг/мл). В скобках указана максимальная концентрация антибиотика в мкг/мл в агаризованной среде LB, при которой наблюдается рост бактерий.
Хромосомная устойчивость к тяжелым металлам
Штамм обладает исходным уровнем хромосомной устойчивости к цинку и меди. Максимальная толерантная концентрация (МТК) цинка - 2.0 мМ, меди - 1.5 мМ.
Штамм способен к росту при повышенных концентрациях (5%) хлористого натрия в среде выращивания.
Принципиальные физиологические свойства
Штамм обладает фунгицидными и бактерицидными свойствами.
Принципиальные специфические продукты.
Штамм синтезирует гетероциклические феназиновые антибиотики феназин-1-карбоновую кислоту и феназин-1-карбоксамид, цианид водорода (HCN), сидерофоры, индолил-3-уксусную кислоту.
Сведения по биологической безопасности
Штамм не патогенен для теплокровных животных и человека. Не обладает фитопатогенной активностью, о чем свидетельствует отсутствие мацерации на ломтиках картофеля при нанесении на них уколом живых клеток штамма.
Штамм бактерий Pseudomonas fluorescens ВКМ В-2955Д хранят на чашках со средой LB при 4-7°C. Пересевы на свежие среды - один раз в месяц. Может храниться не менее 1 года в 15% глицерине при -20°C, не более 10 лет под вазелиновым маслом в полужидкой среде следующего состава (г/л): питательный бульон (Difco) - 4, NaCl - 5, агар - 6, рН 6.8.
Штамм бактерий Pseudomonas fluorescens ВКМ B-2955D угнетает рост следующих фитопатогенных грибов: Gaeumannomyces graminis var. tritici штамм Ggt 1818, Gaeumannomyces graminis var. tritici штамм 119(2), Gaeumannomyces graminis var. tritici штамм PIT, Fusarium graminearum, Fusarium moniliforme, Fusarium oxysporum, Fusarium geterosporum, Fusarium culmorum, Fusarium sporotrichum, Fusarium solani ВКМ F-2316, Rhizoctonia solani, Verticillium alba-artrum, Verticillium dahliae ВКМ F-933, Sclerotonia sclerotiorum, Alternaria brassicae ВКМ F-4284.
Штамм бактерий Pseudomonas fluorescens ВКМ B-2955D угнетает рост фитопатогенных бактерий Pectobacterium carotovorum В15 и Burkholderia caryophylli ВКМ В-1296.
Штамм бактерий Pseudomonas fluorescens ВКМ B-2955D может быть использован для защиты растений от широкого круга фитопатогенных инфекций.
Возможность осуществления предлагаемых объектов изобретений подтверждается следующими примерами, но не ограничивается ими.
Пример 1. Получение биомассы бактериального штамма Pseudomonas fluorescens ВКМ B-2955D.
Штамм выращивают в течение 24 ч при 24-30°С с аэрацией до титра 109 КОЕ/мл на среде LB следующего состава (г/л): пептон - 10, дрожжевой экстракт - 5, натрий хлористый - 10, вода водопроводная - 1 л. При необходимости суспензию клеток разводят водой до необходимого титра.
Пример 2. Антагонистическая активность штамма Pseudomonas fluorescens ВКМ B-2955D в отношении фитопатогенных грибов родов Gaeumannomyces, Fusarium, Rhizoctonia, Verticillium, Sclerotonia, Alternaria.
Штамм бактерий Pseudomonas fluorescens ВКМ B-2955D выращивают в жидкой среде LB 18 ч. На чашку Петри с агаризованной средой Каннера сеют 5 мкл бактериального штамма Pseudomonas fluorescens ВКМ B-2955D (пятном
диаметром 5 мм на расстоянии 3-3.5 см от центра чашки) и выращивают в течение 2 суток для достижения полного синтеза вторичных метаболитов. Затем в центр чашки Петри на поверхность агара помещают сегмент мицелия (диаметром 5-10 мм) грибного штамма. Мицелий гриба выращивают заранее на глюкозо-картофельном агаре при комнатной температуре в течение 7 суток.
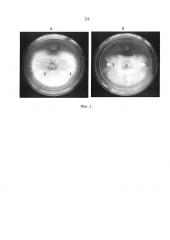
Чашки Петри заклеивают парафильмом для поддержания необходимой влажности и инкубируют при комнатной температуре в течение 5-10 суток, после чего визуально оценивают наличие зоны подавления роста фитопатогенов (таблица 1, фиг. 1).
Из таблицы 1 следует, что бактериальный штамм Pseudomonas fluorescens ВКМ B-2955D ингибирует, в той или иной степени, все используемые в данном эксперименте фитопатогенные грибы.
На фиг. 1 показано подавление роста мицелия фитопатогенных грибов Gaeumannomyces graminis var. tritici (штамм Ggt 1818) (а) и Fusarium graminearum (б) предлагаемым штаммом бактерий Pseudomonas fluorescens ВКМ B-2955D (1) и ризосферными штаммами бактерий (2, 3), не являющимися продуцентами феназиновых антибиотиков. Хорошо видна зона подавления роста тест-гриба около штамма Pseudomonas fluorescens ВКМ В-2955D (1). Ризосферные штаммы (2, 3) не оказывают ингибирующего влияния на формирование мицелия исследуемых грибов. Зон подавления вокруг них нет.
Пример 3. Антибактериальная активность штамма Pseudomonas fluorescens ВКМ B-2955D.
Штамм бактерий Pseudomonas fluorescens ВКМ B-2955D и тест-микроорганизмы, приведенные в таблице 2, выращивают в жидкой среде LB 18 ч. Используют неразбавленную культуру тест-микроорганизмов, а также ее разведения в 10, 100 и 1000 раз. 100 мкл культуры тест-микроорганизмов наносят на предварительно подсушенную агаризованную среду LB и равномерно распределяют микробиологическим шпателем. Затем на расстоянии 3-3.5 см от центра чашки наносят 3-5 мкл культуры штамма
бактерий Pseudomonas fluorescens ВКМ B-2955D. Чашки инкубируют в течение 7 суток при 24°С. Наличие зоны подавления роста тест-микроорганизмов определяют визуально на 1, 3 и 7 сутки (таблица 2, фиг. 2). Зоны измеряют в мм, измеряя от края колонии штамма бактерий Pseudomonas fluorescens ВКМ B-2955D.
Из таблицы 2 следует, что штамм бактерий Pseudomonas fluorescens ВКМ B-2955D ингибирует, в той или иной степени, все используемые в данном эксперименте тест-микроорганизмы. Штамм угнетает рост как грамотрицательных, так и грамположительных бактерий.
На фиг. 2 показано подавление роста бактериального штамма Burkholderia caryophylli ВКМ В-1296 (0 разведение) предлагаемым штаммом бактерий Pseudomonas fluorescens ВКМ B-2955D (1) и ризосферными штаммами бактерий (2, 3), не являющимися продуцентами феназиновых антибиотиков. Хорошо видна зона подавления роста тест-микроорганизма около штамма Pseudomonas fluorescens ВКМ B-2955D (1). Ризосферные штаммы (2, 3) не оказывают ингибирующего влияния на развитие тест-микроорганизма. Зон подавления вокруг них нет.
Пример 4. Способность бактериального штамма Pseudomonas fluorescens ВКМ B-2955D продуцировать феназиновые антибиотики.
Качественный анализ феназиновых антибиотиков (феназин-1-карбоновой кислоты и феназин-1-карбоксамида) проводят с использованием метода тонкослойной хроматографии (ТСХ). Для экстрагирования феназинов бактериальные культуры выращивают в течение 72 ч при 24°С в 10 мл триптозно-соевого бульона или среды Кинга Б. После осаждения клеток (5 мин, 10000 об/мин) супернатант подкисляют с помощью HCl до рН 2 и экстрагируют равным объемом хлороформа. После центрифугирования отбирают хлороформенную фракцию и выпаривают.
Для ТСХ пробы растворяют в 20 мкл ацетонитрила. 3-5 мкл раствора наносят на силикагелевые пластины с флуоресцентным анализатором (Fluka, Германия) и применяют систему растворителей хлороформ : этилацетат :
муравьиная кислота (5:4:1). В качестве стандартов используют феназин-1-карбоновую кислоту и феназин-1-карбоксамид (Sigma, США).
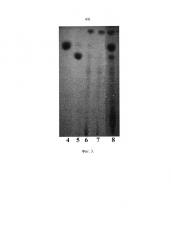
На фиг. 3 приведена тонкослойная хроматография феназин-1-карбоновой кислоты (величина Rf 0.8) (4), феназин-1-карбоксамида (величина Rf 0.7) (5), экстрактов культуральной жидкости (6, 7) ризосферных штаммов, не являющихся антагонистами фитопатогенных грибов и продуцентами феназиновых антибиотиков и экстракта культуральной жидкости (8) предлагаемого штамма бактерий Pseudomonas fluorescens ВКМ B-2955D.
На ТСХ видно, что в экстракте культуральной жидкости (8) предлагаемого штамма бактерий Pseudomonas fluorescens ВКМ B-2955D накапливается целый ряд соединений. Два соединения (величины Rf 0.8 и 0.7) по окраске в видимом свете, флуоресценции под действием УФ и по значениям Rf идентичны феназин-1-карбоновой кислоте (4) и феназин-1-карбоксамиду (5). При длительном выращивании предлагаемого штамма бактерий Pseudomonas fluorescens ВКМ B-2955D возможно выпадение феназиновых антибиотиков в виде сине-зеленых кристаллов в среде культивирования.
В экстрактах культуральной жидкости (6, 7) ризосферных штаммов, не являющихся антагонистами фитопатогенных грибов, не накапливается указанных феназиновых антибиотиков. Пятна со значениями Rf 0.8 и 0.7 отсутствуют на пластине ТСХ.
Пример 5. Способность бактериального штамма Pseudomonas fluorescens ВКМ B-2955D к растворению неорганических фосфатов.
Способность к растворению неорганических фосфатов оценивают по появлению прозрачных зон (гало) при культивировании бактерий на селективной минеральной среде с гидроксиапатитом кальция (Са10(PO4)6(ОН)2) или фосфатом кальция (Са3(PO4)2) в качестве единственного источника фосфора.
Селективная среда с гидроксиапатитом кальция содержит в г/л: MgSO4×7Н2О - 2; NaCl - 1; NH4Cl - 10; трис (трис(гидроксиметил)аминометан) - 1; глюкоза - 10, агар - 15, раствор гидроксиапатита кальция - 5%. Раствор гидроксиапатита кальция (Са10(PO4)6(ОН)2) (Calcium phosphate hydroxide, type 3, Sigma, США) готовят заранее. Для этого 10 г гидроксиапатита кальция 10-15 раз промывают деионизованной водой. Отмытый гидроксиапатит кальция заливают 100 мл деионизованной воды и стерилизуют. К расправленной агаризованной среде (20 мл) добавляют 1 мл приготовленной суспензии гидроксиапатита кальция, интенсивно перемешивают на шейкере и разливают по чашкам Петри.
Бактериальные штаммы выращивают заранее на полноценной среде LB. Биомассу ресуспендируют в физ. растворе (0.85% NaCl) и наносят по 3-5 мкл на чашки с агаризованной селективной средой с гидроксиапатитом кальция или фосфатом кальция. Через 5-7 суток культивирования определяют появление прозрачных зон (гало) вокруг бактериальной культуры.
На фиг. 4 видно, что наибольшая зона растворения гидроксиапатита кальция (более 3 мм) наблюдается около колонии предлагаемого штамма бактерий Pseudomonas fluorescens ВКМ B-2955D (1).
Ризосферные штаммы бактерий, не способные к растворению фосфатов и не являющиеся продуцентами феназиновых антибиотиков могут расти на данной селективной среде, но зоны просветления либо не образуются (2, 3), либо образуются в радиусе 0.5-1 мм от них (9).
Пример 6. Определение фитостимулирующей способности у предлагаемого штамма бактерий Pseudomonas fluorescens ВКМ B-2955D.
Определение способности стимулировать рост корней растений (пшеница, рожь, маш (фасоль золотистая)) проводят в чашках Петри, сравнивая обработанные предлагаемым штаммом семена с контрольными. Семена растений одного размера (20 штук) помещают в пробирку с разведенной в 100 раз культурой штамма бактерий Pseudomonas fluorescens ВКМ B-2955D и встряхивают их до полного смачивания. Семена инкубируют при комнатной температуре в течение 2 часов, затем равномерно раскладывают в чашки Петри на поверхность бумажного фильтра, смоченного 10 мМ раствором сульфата магния. В качестве контроля используют семена, помещенные в пробирку с 10 мл раствора 10 мМ сульфата магния без бактерий. Чашки инкубируют в термостате при 24°C в темноте в течение 3 суток. Измеряют среднюю и суммарную длину корней инокулированных проростков и сравнивают с контролем (необработанные проростки). Повторность эксперимента 3-х кратная.
Из таблицы 3 видно, что длина корней проростков, обработанных предлагаемым штаммом бактерий Pseudomonas fluorescens ВКМ B-2955D, больше по сравнению с контрольными растениями. Средняя длина корня у обработанных проростков маша увеличивается на 10%, у ржи на 45%, у пшеницы на 54%.
Пример 7. Влияние обработки штаммом Pseudomonas fluorescens ВКМ B-2955D на развитие грибных заболеваний и урожайность озимой пшеницы в полевых экспериментах.
Исследования проведены на опытном поле муниципального бюджетного учреждения «Благоустройство» городского округа г. Пущино Московской области. Тип почвы - серая лесная.
Посев семян озимой пшеницы сорта Губернатор Дона проведен в первой декаде сентября с нормой высева 2.5 ц/га на глубину 5-7 см по черному пару.
Подготовку опытного образца биопрепарата на основе предлагаемого штамма Pseudomonas fluorescens ВКМ B-2955D проводят следующим образом. Штамм выращивают в течение 24 ч при 24-30°С с аэрацией до титра 109-1010 КОЕ/мл на среде LB. Культуру разводят в 100 раз водопроводной водой до титра 107-108 КОЕ/мл. Опрыскивание растений озимой пшеницы проводят с помощью ранцевого опрыскивателя дважды за вегетационный период: в фазе кущения - начала выхода в трубку (5 мая) и по флаговому листу (31 мая) в норме расхода рабочего раствора 300 л/га. Для сравнения используют коммерческий биопрепарат Псевдобактерин-2 на основе штамма бактерий Pseudomonas aureofaciens BS1393. В качестве контроля используют растения без обработки. Опрыскивание растений проводят в утренние часы при безветрии. Площадь делянок 20 м2, повторность 4-кратная.
Наблюдения за пораженными растениями и их учет проводят в течение всей вегетации перед обработками и после обработок (на 10-20 день). Учет листовых болезней осуществляют путем отбора проб и последующим анализом в лабораторных условиях.
Интенсивность развития болезни определяют по площади пораженной поверхности листьев, покрытых пятнами, налетами, пустулами. Развитие болезни учитывают глазомерно, с помощью специальной палетки, повышающей точность оценки, и определяют процент поверхности пораженной ткани растения.
Распространенность болезни устанавливают по общепринятой формуле:
Р(%)=(n×100)/N, где
Р - распространенность болезни;
n - количество больных растений в пробах;
N - общее количество растений в пробах.
Учет технической (биологической) эффективности защитного мероприятия ведут по формуле:
Б=((Рк-Po)×100)/Рк, где
Б - биологическая эффективность в %;
Рк - показатель развития болезни в контроле;
Po - аналогичный показатель в опыте.
Хозяйственную эффективность определяют разницей фактического урожая на обработанном и контрольном участках в пересчете на 1 га по формуле:
Х=((А-В)×100)/А, где
X - хозяйственная эффективность в %;
А - урожай на обработанном участке поля;
В - урожай в контроле.
Уборку зерна озимой пшеницы осуществляют 7 июля в фазе полной спелости площадочным способом (4×0.25 м2 на делянках). Массу 1000 зерен определяют по ГОСТ 10842-89. Данные учета болезней и урожайности зерна
подвергают математической обработке методом дисперсионного анализа.
Результаты обработок озимой пшеницы предлагаемым штаммом бактерий Pseudomonas fluorescens ВКМ B-2955D на зараженность растений грибными патогенами представлены в таблице 4.
Из таблицы видно, что распространенность грибных заболеваний на флаговом листе у растений, обработанных предлагаемым штаммом, была ниже после первой и второй обработок (23 и 60% соответственно) по сравнению с контролем (47 и 72% соответственно).
Распространенность грибных заболеваний на первом листе у растений, обработанных предлагаемым штаммом, после первой обработки, также ниже (81%) по сравнению с контролем (91%).
Биологическая эффективность предлагаемого штамма бактерий Pseudomonas fluorescens ВКМ B-2955D сравнима с коммерческим препаратом Псевдобактерин-2 (таблица 4).
Влияние обработок предлагаемым штаммом Pseudomonas fluorescens ВКМ B-2955D на урожайность озимой пшеницы представлено в таблице 5. Прибавка урожая при обработке предлагаемым штаммом Pseudomonas fluorescens ВКМ B-2955D составляет 2.1 ц/га (6.9%) по сравнению с контролем и выше по сравнению с коммерческим биопрепаратом Псевдобактерин-2 (1.2 ц/га, 2.9%). Хозяйственная эффективность предлагаемого штамма в данных условиях составляет 6.4%.
Таким образом, предлагаемый штамм бактерий Pseudomonas fluorescens ВКМ B-2955D обладает способностью к подавлению роста широкого круга фитопатогенов и растворению фосфатов. Штамм не токсичен для растений в рекомендуемых для обработок концентрациях. Он может быть использован для создания на его основе биопрепарата, предназначенного для защиты растений от фитопатогенных грибов и бактерий и стимуляции роста растений за счет повышения биодоступности фосфатов.
Штамм бактерий Pseudomonas fluorescens BS1506, депонированный во Всероссийской коллекции микроорганизмов ИБФМ им. Г.К. Скрябина РАН под номером ВКМ B-2955D, для защиты растений от фитопатогенных грибов и бактерий и стимуляции роста растений.