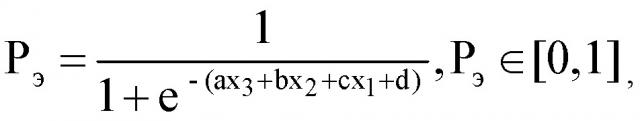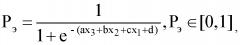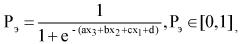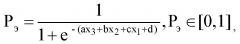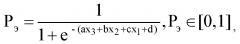Способ прогнозирования эндометриопатии у женщин с репродуктивными нарушениями
Иллюстрации
Показать всеИзобретение относится к области медицины и представляет собой способ прогнозирования эндометриопатии, отличающийся тем, что в образце менструальной крови определяют концентрации интерлейкина-6 (ИЛ-6), глутатионпероксидазы-1 (ГТП 1) и растворимой формы Е-селектина и определяют коэффициент вероятности эндометриопатии (Р) по формуле:
где
а=0,0002782; b=0,0381529; с=-0,1205126; d=-1,1189533; e - экспонента (константа) = 2,7; X3 - значение концентрации ИЛ-6, пг/мл; Х2 - значение концентрации растворимой формулы Е селектина, нг/мл; X1 - значение концентрации ГТП 1, нг/мл; и при значении Рэ > 0,29 прогнозируют наличие эндометриопатии. Изобретение обеспечивает повышение точности и объективности оценки состояния эндометрия у женщин с репродуктивными нарушениями. 3 пр.
Реферат
Изобретение относится к области медицины, а именно к исследованию биологического материала с помощью физических и химических методов исследования и может быть использовано в гинекологической практике для первичной неинвазивной диагностики и прогнозирования эндометриопатии (в том числе хронического эндометрита, регенераторно-пластической эндометриальной дисфункции) у пациенток с репродуктивными нарушениями в анамнезе, а также для динамической оценки эффективности лечения на этапе подготовки к беременности.
Расстройства фертильности часто ассоциированы с «маточным фактором», в связи с чем патология эндометрия играет определяющую роль в генезе бесплодия, невынашивания и осложнений беременности, неудач методов ВРТ. Среди наиболее вероятных причин несостоятельности эндометрия выделяют инфекционно-воспалительный процесс в полости матки, дистрофию и сосудистую недостаточность ткани, системную и локальную эндокринопатию. В подавляющем большинстве случаев имеют место сочетанные этиопатогенетические факторы неполноценности эндометрия, причем одни нередко являются следствием других. В соответствии с классическими путями патоморфоза морфологические изменения в ткани как результат прямой альтерации клеток (вследствие экстремального воздействия различных эндогенных и экзогенных факторов) либо нарушения процессов биосинтеза (ввиду повреждений генома или истощения регенераторных способностей) ткани в итоге являются причиной расстройств функционального состояния слизистой полости матки. Десинхронизация созревания эндометрия, замещение его функционально неактивными участками склероза, нарушение рецепторной чувствительности ведут к последующим дефектам процесса имплантации эмбриона и дальнейшим репродуктивным потерям или гестационным осложнениям. Сложный патологический процесс в полости матки при отсутствии значимых клинических проявлений нередко становится одним из механизмов как нарушений фертильности, так и расстройств менструального цикла с формированием дис/атрофических или гиперпластических процессов эндометрия.
Основным способом оценки состояния эндометрия и ее слизистой до настоящего времени является гистероскопия (диагностическая эффективность при изолированном использовании ГС для определения эндометриопатии не превышает 35-70%) в сочетании с биопсией и морфологическим (иммуногистохимическим) исследованием ткани эндометрия.
Однако адекватность диагностики нарушений, последующее лечение и прогноз восстановления функции эндометрия у данной группы больных зависят не только от информативности используемых способов, но и от возможности осуществить диагностические процедуры с минимальной инвазией и снижением риска ятрогенного повреждения ткани. Кроме того, традиционный подход к диагностике патологии полости матки с помощью базовых общепринятых методов не позволяет исключить значимость субпороговых факторов функциональной дезорганизации эндометрия, что отражается нарушением синтеза ключевых молекул в зависимости от состояния ткани. В связи с этим наиболее значимым в данном аспекте представляется возможность прогнозирования, т.е. оценка вероятности наличия патологии эндометрия, что позволило бы определить более четкие показания (целесообразность и необходимость) проведения на следующем этапе обследования гистероскопии и/или биопсии эндометрия. Поэтому продолжается разработка новых способов, позволяющих улучшить диагностику состояния эндометрия и сделать ее более объективной и безопасной. Одним из перспективных способов оценки выраженности патологического процесса в эндометрии в последние годы стало исследование менструальных выделений. Существует ряд лабораторных параметров, которые целесообразно определять именно в образце менструальной крови, так как она является субстратом, отделяемым из очага предполагаемого патологического процесса.
За прототип предлагаемого изобретения выбран известный способ оценки состояния эндометрия на этапе подготовки к беременности, включающий сбор анамнеза и проведение лабораторных исследований, в том числе образца менструальной крови (РФ Патент №2242009, МПК G01N 33/68, публ. от 10.12.2004 «Способ оценки эффективности предгравидарной подготовки женщин к беременности с невынашиванием гормонального генеза в анамнезе» / Краснопольский В.И., Серова О.Ф. /). В способе проводят количественное определение эндометриального белка - альфа-2 микроглобулина фертильности (АМГФ) в смыве из полости матки и в менструальных выделениях и прогестерона до и после лечения и по увеличению уровня всех показателей оценивают подготовку как эффективную.
Как видно из вышеописанного, известный способ громоздок, длителен по времени, требует создания специальных условий. Кроме того, к его недостаткам относится то, что он применим только к невынашиванию гормонального генеза и не обеспечивает возможность прогноза риска развития эндометриопатии в случае инфекционно-воспалительного и дистрофического процесса в полости матки, а также вследствие сосудистой недостаточности ткани. Не исключается и не обосновывается также инвазивность диагностических мероприятий в комплексном обследовании. Неясная точность и низкая прогностическая значимость известного способа являются его главными недостатками в связи с измерением лишь единственного параметра в менструальной крови, не отражающего других звеньев патогенеза.
Технический результат предлагаемого изобретения заключается в обеспечении возможности прогноза эндометриопатии, повышении точности и объективности оценки состояния эндометрия у женщин с репродуктивными нарушениями.
Технический результат достигается тем, что в известном способе оценки состояния эндометрия на этапе подготовки к беременности, включающем сбор анамнеза и проведение лабораторных исследований, в том числе образца менструальной крови, в образце менструальной крови определяют концентрации интерлейкина-6, глутатионпероксидазы-1 (ГТП 1) и растворимой формы Е-селектина, а также определяют коэффициент вероятности эндометриопатии по формуле:
где
Рэ - коэффициент вероятности эндометриопатии
а=0,0002782
b=0,0381529
с=-0,1205126
d=-1,1189533
e - экспонента (константа) = 2,7
X3 - значение концентрации интерлейкина-6 (ИЛ-6), пг/мл, Х2 - значение концентрации растворимой формулы Е селектина, нг/мл, X1 - значение концентрации глутатионпероксидазы-I (ГТП 1), нг/мл, при значении коэффициента вероятности эндометриопатии Рэ > 0,29 (29%) прогнозируют наличие эндометриопатии.
Предлагаемое изобретение отвечает критерию «новизна», так как в результате проведенных патентно-информационных исследований не выявлены источники информации, порочащие новизну предлагаемого способа.
Из литературных источников известно, что интерлейкин-6 (ИЛ-6) - один из гормоноподобных белков межклеточного взаимодействия (цитокинов), секретируемых при воспалении. Он продуцируется активированными моноцитами, макрофагами, эндотелием, фибробластами, Т-лимфоцитами. Активный синтез ИЛ-6 начинается после воздействия на клетки бактерий, вирусов, митогенов, различных медиаторов воспаления. По многообразию клеточных источников продукции и мишеней биологического действия ИЛ-6 является одним из наиболее активных цитокинов, участвующих в реализации воспалительной реакции и иммунного ответа, что позволяет отнести его к провоспалительным факторам. Поскольку цитокины являются локальными медиаторами и действуют преимущественно в зоне их образования, наиболее целесообразно измерять их содержание непосредственно в тканях после экстракции протеинов или в естественных биологических жидкостях. Определение уровня ИЛ-6 помогает оценить также выраженность и динамику воспалительного процесса.
Также известно, что глутатионпероксидаза I (ГПТ I) обнаруживается в цитоплазме практически всех тканей и играет основную роль в предотвращении окислительного стресса в организме, характерного для различных повреждений. Глутатионпероксидаза катализирует восстановление перекисей липидов в соответствующие спирты и восстановление перекиси водорода до воды. Дефицит данного фермента может приводить к нарушениям структуры и функции сосудистой сети. Измерение ее активности целесообразно для выявления больных, которым показана антиоксидантная терапия.
Известно, что патологические изменения в тканях зачастую сопровождаются в той или иной степени выраженными сосудистыми и реологическими нарушениями - спазмом, склерозом, облитерацией, сладжем, тромбозом. В связи с этим одним из чувствительных лабораторных маркеров состояния сосудистого эндотелия при различных патологических процессах, сопровождающихся микроангиопатиями, является растворимая формула Е-селектина. Данный показатель представляет собой молекулу адгезии, гликопротеин, находящийся на поверхности клеток эндотелия (включая сосудистый). В физиологических условиях эндотелиальные клетки практически не экспрессируют молекулы адгезии. Экспрессия Е-селектина индуцируется в случае повреждения ткани; он играет роль в иммуноадгезии, опосредуя взаимодействие лейкоцитов и тромбоцитов с клетками эндотелия. Интерес к определению уровня Е-селектина в патологическом очаге продиктован возможностью оценки активационной и/или адгезионной способности клеток (эндотелия сосудов, лейкоцитов, тромбоцитов и т.д.), когда имеют место гемодинамические, реологические и метаболические расстройства.
Таким образом, предлагаемый способ, включающий определение и интегративную оценку трех основных параметров в менструальной крови - антиоксидативного фермента (ГТП-I), провоспалительного цитокина ИЛ-6 и растворимой молекулы адгезии (sE-селектина) с использованием предлагаемого прогностического коэффициента вероятности эндометриопатии, из современного уровня техники не известен, что позволяет сделать вывод о соответствии предлагаемого технического решения критерию «изобретательский уровень». Авторы предлагаемого изобретения определили также нормы для указанных показателей - интерлейкина 6 от 500 до 3000 пг/мл, для растворимой формулы Е-селектина от 4 до 27 нг/мл, для глутатионперксидазы-1 от 4 до 310 нг/мл.
Технический результат предлагаемого способа заключается в обеспечении возможности прогнозирования риска возникновения и развития эндометриопатии у женщин с репродуктивными нарушениями за счет оценки ведущих звеньев патогенеза патологического процесса в ткани эндометрия и выявлении взаимосвязи между эндометриопатией и предложенными параметрами, определяемыми в менструальных выделениях.
Для подтверждения технического результата было обследовано 60 пациентов репродуктивного возраста с наличием репродуктивных нарушений (30 пациентов) и без него (30 пациентов).
Значения нормы составили:
ИЛ-6: 500-3000 пг/мл,
sE-селектина: 4-27 нг/мл,
ГТП-1: 4-310 нг/мл.
Для анализа полученных результатов был выбран метод логистической регрессии с коэффициентами корреляции. Коэффициент корреляции [-1;1]. Чем ближе абсолютное значение к 1, тем более сильную зависимость имеют данные. Была разработана программа, которая обучалась на основе указанных параметров менструальной крови и выдавала коэффициенты формулы логистической регрессии (математической модели). В ходе математической обработки оценка полученной регрессионной модели была проверена путем построения ROC - кривой. Полученные результаты говорят о ее отличном качестве, о чем свидетельствует показатель AUC=0,9714, а значит предложенное уравнение может быть использовано для оценки вероятности развития болезни.
Вычисленная средняя вероятность заболевания Рср по обследованным больным составила 0,78 (78%), по здоровым - 0,22 (22%).
Диагностическая чувствительность данного теста составляет 93,3%, диагностическая специфичность - 92,86%.
Технический результат заключается также в том, что предложенная оценка трех чувствительных параметров менструальных выделений и разработанного интегративного показателя (коэффициент вероятности эндометриопатии) практически исключает возможность ложно-отрицательного результата, позволяет с высокой степенью достоверности диагностировать дисфункцию эндометрия (скрининг эндометриопатии) в случае нарушений репродукции и при необходимости определять показания к проведению инвазивных методов. Способ позволяет обосновать и повысить эффективность назначаемой этиопатогенетической терапии у женщин, заинтересованных в беременности с репродуктивными неудачами в анамнезе и оценить в динамике адекватность проведенного лечения без необходимости контрольной диагностической инвазии в полость матки. Способ удобен и прост в исполнении, легко воспроизводим, не требует инвазивных вмешательств для забора исследуемого материала, существенных экономических затрат.
Предлагаемый способ осуществляют следующим образом.
Больной проводят сбор анамнеза и комплексное обследование, которое включает исследование образца менструальной крови на начальном этапе оценки роли маточного фактора. Менструальную кровь для исследования забирают в самый обильный (как правило, второй) день менструации. После предварительного опорожнения мочевого пузыря пациентка размещается на гинекологическом кресле. Вводят вагинальное зеркало (створчатое или ложкообразное) по общепринятой методике, исключая контакт внутренней его поверхности с вагинальным отделяемым. В случае обильных или умеренных выделений кровь изливается из полости матки самопроизвольно в достаточном количестве и скапливается в ложке зеркала. При наличии скудных менструальных выделений целесообразно бережно надавить свободной рукой на низ живота пациентки и немного подождать, когда объем образца будет достаточным. Менструальную кровь аккуратно сливают из зеркала и помещают в пластиковую пробирку Эппендорфа. На 1 анализ требуется 1 мл отделяемого. Наличие большого количества ферментов и других биологически активных веществ, способных видоизменять менструальную кровь с течением времени, обусловливает необходимость быстрой доставки субстрата для соответствующей лабораторной обработки. При невозможности быстрой доставки допускается непродолжительное хранение образца в холодильнике без замораживания. После этого определяют концентрации соответствующих биомаркеров в менструальной крови следующим образом. После стойкой ретракции сгустка пробирку помещают в центрифугу (MINISKRIN PLUS EPPENDORF) и центрифугируют при 10000-6000 об/мин в течение 15 мин. Если образца недостаточно для постановки, его предварительно разводят 0,9% раствором NaCl. В таком случае при расчете результата учитывают дополнительное разведение. Далее пробу анализируют на аппарате IMMULITE 1000. Для определения ИЛ-6 используют твердофазный хемилюминесцентный иммуноферментный метод «сэндвич» с моноклональными мышиными антителами к интерлейкину-6.
Определение Е-селектина и ГТП-1 основано на иммуноферментном анализе «сэндвич» с использованием специфических моноклональных антител к sE-селектину или человеческой глутатион-пероксидазе-1.
Далее определяют коэффициент вероятности эндометриопатии по формуле:
где
Рэ - коэффициент вероятности эндометриопатии
а=0,0002782
b=0,0381529
с=-0,1205126
d=-1,1189533
е - экспонента (константа) - 2,7
Х3 - значеие концентрации интерлейкина-6 (ИЛ-6), Х2 - значение концетрации растворимой формулы Е-селектина, X1 - значение концентрации глутатионпероксидазы-I (ГТП 1). При значении коэффициента вероятности эндометриопатии Рэ>0,29 (29%) оценивают состоятельность эндометрия как неудовлетворительную, при норме для ИЛ-6: 500-3000 пг/мл, для sE-селектина: 4-27 нг/мл, для ГТП-1: 4-310 нг/мл.
Примеры конкретного выполнения даны в виде выписок из историй болезни и амбулаторных карт.
Пример 1. Больная М., 29 лет. Жалобы на эпизодические тянущие боли в низу живота, неприятные выделения из половых путей. Заинтересована в беременности. Год назад произведено лечебно-диагностическое выскабливание полости матки в связи с неразвивающейся беременностью малого срока и повторным выскабливанием по поводу остатков плодного яйца. В последующем проводилась противовоспалительная терапия и соответствующее комплексное обследование супружеской пары. Пролечены по поводу микоплазменной инфекции. В анализах на репродуктивные гормоны, АФЛ-синдром патологии не выявлено. Общесоматический статус без особенностей. Тесты функциональной диагностики выявили овуляторные циклы с полноценной второй фазой.
Проведено также обследование по предложенному методу: в менструальной крови пациентки отмечен уровень ГТП-I 5,4 нг/мл, повышение ИЛ-6 до 55900,0 пг/мл и sE-селектина до 60,0 нг/мл. Прогностический коэффициент вероятности эндометриопатии на основе предложенной математической модели составил - Рэ=0,999 (99,9%).
По данным гистероскопии и морфологического заключения - хронический эндометрит вне обострения.
Проведено противовоспалительное лечение, по окончании которого больная жалоб не предъявляет. Повторно через 2,5 месяца проведено исследование образца менструальной крови: содержание ГТП-I повысилось до 17,4 нг/мл, значение ИЛ-6 снизилось до 9630,0 пг/мл, концентрация sE-селектина до 23,0 нг/мл, при этом коэффициент эндометриопатии составил Рэ=0,31 (31%). Эхографические симптомы хронического эндометрита отсутствуют. Через 4,5 месяца наступила беременность без клинических и ультразвуковых признаков угрожающего выкидыша.
Пример 2. Больная С., 33 лет. Жалобы на нарушение менструального цикла в течение последних 3-х лет в виде нерегулярных, эпизодически скудных менструаций, бесплодие. В анамнезе отсутствия наступления беременности в течение 1,5 лет в браке, затем 1 самопроизвольный выкидыш. Инструментальная ревизия полости матки 4 года назад, после чего беременность не наступает. Муж обследован - здоров. ИППП - abs. По данным ГСГ маточные трубы проходимы, по УЗИ ОМТ во 2-й фазе м.ц. (19-й день) отмечается гипоплазия эндометрия (М-эхо 7 мм), размеры, эхоструктура яичников и фолликулярный запас адекватные. Ректальная температура двухфазная, циклы овуляторные, однако отмечается укорочение второй фазы м.ц. до 9-10 дней. В соответствии с результатами гормонального обследования отмечено умеренное снижение уровней эстрадиола на 5-й д.м.ц. и прогестерона на 21 д.м.ц. По морфологическому заключению биоптата эндометрия, полученного за 2-3 дня до предполагаемой менструации, - недостаточная секреторная трансформация эндометрия, склеротические изменения сосудов, убедительных данных за воспалительный процесс не получено. Это явилось свидетельством яичниковой недостаточности и гиподистрофических изменений в ткани эндометрия. Проведено исследование по предлагаемому способу. В менструальной крови снижение ГТП-I 2 нг/мл, умеренное повышение ИЛ-6 до 3450,0 пг/мл, концентрация sE-селектина 22,2 нг/мл. Значение коэффициента вероятности эндометриопатии - Рэ=0,55 (55%).
Назначен курс реабилитирующей терапии с включением иммуномодуляторов, гормональных препаратов, физиолечения. Через 3,5 месяца менструальный цикл нормализовался, М-эхо на 20-й д.м.ц. 9,5 мм, эхоструктура эндометрия соответствует дню цикла. После проведенного лечения показатели менструальной крови составили: ГТП-1 4,6 нг/мл, ИЛ-6 1870,0 пг/мл, концентрация sE-селектина 10,2 нг/мл. Коэффициент вероятности эндометриопатии составил - Рэ=0,18 (18%).
Еще через 2 месяца на фоне гормональной поддержки прогестагенами наступила самостоятельная беременность, которая закончилась срочными родами без осложнений.
Пример 3. Больная С., 42 лет. Жалобы на отсутствие детей во втором браке, скудные менструации. В анамнезе - 1 роды и 2 аборта в первом браке, 2 самопроизвольных выкидыша, затем бесплодие в течение 1,5 лет и неудачная попытка ЭКО и ПЭ 4 месяца назад. В криобанке имеется 2 замороженных эмбриона. По данным спермограммы - супруга без патологии. ИППП - abs. АФЛ-синдром и тромбофилии исключены. Уровень АМГ на нижней границе нормы. М-эхо на 18 д.м.ц. - 6,5 мм, спиральные и базальные артерии не визуализируются.
Проведено исследование образца менструальной крови по предлагаемому способу: отмечено снижение ГТП-I до 0,6 нг/мл, повышение ИЛ-6 до 8300,0 пг/мл, sE-селектина до 46,2 нг/мл. Коэффициент эндометриопатии: Рэ=0,949 (94,9%).
По данным гистероскопии и морфологического исследования - хронический эндометрит, гипопластический вариант, вне обострения. Проведено комплексное этиопатогенетическое лечение, по окончании которого больная жалоб не предъявляет. Повторное исследование образца менструальной крови: содержание ГТП-I повысилось до 4,14 нг/мл, значение ИЛ-6 в снизилось до 7712,0 пг/мл, sE-селектина до 11,5 нг/мл. Коэффициент вероятности эндометриопатии составил - Рэ=0,28 (28%). М-эхо на 19 д.м.ц. - 9 мм, по данным допплерометрии - нормальный субэндометриальный кровоток. Через 2,5 месяца после очередной попытки ВРТ диагностирована маточная беременность, которая прогрессирует.
Способ прогнозирования эндометриопатии у женщин с репродуктивными нарушениями на этапе подготовки к беременности, включающий сбор анамнеза и проведение лабораторных исследований, в том числе образца менструальной крови, отличающийся тем, что в образце менструальной крови определяют концентрации интерлейкина-6 (ИЛ-6), глутатионпероксидазы-1 (ГТП 1) и растворимой формы Е-селектина, а также определяют коэффициент вероятности эндометриопатии по формуле:
где
Рэ - коэффициент вероятности эндометриопатии
а=0,0002782
b=0,0381529
с=-0,1205126
d=-1,1189533
e - экспонента (константа) = 2,7
X3 - значение концентрации интерлейкина-6 (ИЛ-6), пг/мл, Х2 - значение концентрации растворимой формулы Е селектина, нг/мл, X1 - значение концентрации глутатионпероксидазы-I (ГТП 1), нг/мл, и при значении коэффициента вероятности эндометриопатии Рэ > 0,29 (29%) прогнозируют наличие эндометриопатии.