Средство и способ для профилактики метаболических нарушений костной ткани при длительном употреблении глюкокортикоидов
Иллюстрации
Показать всеИзобретение относится к химико-фармацевтической промышленности и представляет собой способ профилактики нарушения метаболизма кальция в костной ткани, вызванного длительным приемом глюкокортикоидов, путем перорального употребления средства, обладающего антирадикальной активностью, отличающийся тем, что в качестве средства антирадикальной защиты используют масляный раствор серосодержащего антиоксиданта тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид на фоне глюкокортикоидной терапии. Изобретение обеспечивает снижение уровня резорбции костного матрикса и предотвращение повреждений структурных компонентов костной ткани при длительном приеме глюкокортикоидов. 1 з.п. ф-лы, 1 ил., 1 табл., 1 пр.
Реферат
Изобретение относится к медицине, в частности к средствам для предотвращения развития нарушения метаболизма кальция, индуцированного длительным применением глюкокортикоидов и сопровождающихся резорбцией матрикса костной ткани.
Способ профилактики нарушения метаболизма кальция в костной ткани и, как следствие, переломов костей, включающий прием препарата тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфида, являющегося серосодержащим фенольным антиоксидантом.
Актуальность профилактики нарушений метаболизма кальция в костной ткани, развивающихся при терапии глюкокортикоидами, обусловлена высоким уровнем развития данной разновидности патологий у пациентов преимущественно трудоспособного возраста, с их последующей инвалидизацией. В то же время, на рынке лекарственных препаратов эффективные остеопротективные средства представлены крайне ограничено.
Целью настоящего изобретения является представление средства профилактики структурно-функциональных нарушений компонентов костной ткани, индуцированных приемом глюкокортикоидных препаратов.
Наиболее близким к предлагаемому средству лечения метаболических заболеваний костной ткани, в частности остеопороза, относится фармацевтическая композиция, включающая в качестве активных компонентов фосфонаты и эстроген (Способ лечения остеопороза, композиция для лечения остеопороза, применение активно действующего на кости фосфоната и эстрогенного гормона для лечения остеопороза (RU 2113848)). Как было четко показано, эстрогены действительно прекращают потери костной ткани, наблюдаемые после менопаузы и ограничивают прогрессирование остеопороза: но состояние пациентов ухудшается из-за связанных с действием эстрогенов побочных эффектов. Эти побочные эффекты включают развитие мастодинии, повышение риска возникновения рака матки и, возможно, повышение риска возникновения рака молочной железы.
Известны способы предотвращения потерь костной массы, предполагающие как медицинское терапевтическое, так и/или профилактическое их использование в зависимости от необходимости. В качестве активных компонентов в них предлагается использование фосфонокарбоксилатных соединений и 2-фенил-3-ароилбензотиефенов, их солей или сольватов (Фосфонокарбоксилатные соединения для лечения анормального кальциевого и фосфатного метаболизма, фармацевтическая композиция (RU 2118530), Применение 2-фенил-3-ароилбензотиефенов, их солей или сольватов для ингибирования потерь костной ткани, фармацевтическая композиция, содержащая 2-фенил-3-ароилбензотиефены, и их соли или сольваты (RU 2100024).
Однако данные соединения многим недоступны, а также, вероятно, оказывают кратковременное воздействие.
Одним из ведущих механизмов развития осложнений глюкокортикоидной терапии является активизация процессов свободнорадикального перекисного окисления липидов и/или угнетение активности собственных систем антиоксидантной защиты организма, получившее название «окислительный стресс» (Меньшикова Е.Б., Зенков Н.К., Ланкин В.З. Окислительный стресс: Патологические состояния и заболевания. Новосибирск: АР-ТА. 2008. 284 с.). Однако в применяющихся схемах профилактики и лечения остеопороза этот аспект патогенеза не учитывается.
Обнаружено, что помимо непосредственного повреждения компонентов костной ткани, при длительном приеме глюкокортикоидов под действием образующихся свободнорадикальных соединений происходит нарушение структурно-функциональной организации слизистой оболочки кишечника, сопровождающееся нарушением процессов всасывания в кровь различных веществ (в том числе ионов) и, как следствие, минерализации кости (Луканина C.H. Влияние антиоксиданта тиофана на структурно-функциональную организацию кишечника крыс в условиях глюкокортикоидной нагрузки // Сибирский вестник сельскохозяйственной науки. - 2010. - №3. - С. 61-68; Луканина C.H., Сахаров А.В., Просенко А.Е., Аношина Н.А., Букреева Л.Н. Особенности обмена кальция в кишечнике и костной ткани крыс при глюкокортикоид-индуцированном окислительном стрессе // Вестник КрасГАУ. - 2012. - №7. - С104-108.).
Наиболее близким по технической сущности к заявляемому изобретению является средство, при котором для предотвращения нарушений компонентов костной ткани, индуцированных длительным приемом глюкокортикоидов, можно использовать природный антиоксилант «α-токоферол» (Луканина C.H., Сахаров А.В., Просенко А.Е., Ефремов А.В. Оценка специфической активности антиоксидантов «Тиофан» и «α-токоферол» при моделировании окислительного стресса // Медицина и образование в Сибири. - №6. - 2013). Недостатком данного способа является низкая эффективность антиоксиданта «α-токоферол», выражающаяся в недостаточном уровне антирадикальной защиты клеток и компонентов костного матрикса.
Задачей, на решение которой направлено предлагаемое изобретение, является увеличение степени сохранности и предотвращение развития повреждений костной ткани при длительном приеме глюкокортикоидов, которая достигается выбором средства антирадикальной защиты компонентов костной ткани.
Задача решается использованием препарата тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфида в качестве средства антирадикальной защиты костной ткани при длительном использовании глюкокортикоидов, способного повысить степень сохранности компонентов костной ткани.
Тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид многофункциональный пространственно-затрудненный фенольный серосодержащий антиоксидант нового поколения, относится к нетоксичным соединениям, обладает выраженными цитопротекторными и мембраностабилизирующими свойствами и может использоваться для антирадикальной защиты костной ткани в условиях длительно применения глюкокортикоидных препаратов.
Предложено средство, обладающее антирадикальной активностью, для защиты компонентов костной ткани при длительном употреблении глюкокортикоидов, используемое путем перорального приема. В качестве средства антирадикальной защиты используют эмульсию серосодержащего антиоксиданта тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфида. Используют концентрацию масляного раствора тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфида из расчета 100 мг на 1 кг веса 2 раза в сутки за 30 мин до приема пищи в течение всего периода использования глюкокортикоидов.
Принципиально новым в предлагаемом изобретении является то, что в качестве антирадикального и противопероксидного средства используется серосодержащий антиоксидант нового поколения тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфида для профилактики нарушений компонентов костной ткани, индуцированных длительным приемом глюкокортикоидов.
Таким образом, данное техническое решение соответствует критериям изобретения: «новизна», «изобретательский уровень», «промышленная применимость».
Новые свойства антиоксиданта тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид были обнаружены благодаря экспериментальным исследованиям.
Сущность изобретения иллюстрируется примером, таблицей и рисунком.
Пример
Исследование проводили на самцах крыс линии Вистар массой 250-300 г. Манипуляции с животными осуществлялись в соответствии с международными принципами Хельсинской декларации о гуманном отношении к животным. Все крысы были распределены в 4 группы по 10 особей в каждой. Животных интактной группы содержали в стандартных условиях вивария без ограничения доступа к воде и корму. Крысам контрольной и двух групп сравнения ежедневно в течение 14 суток вводили водную суспензию синтетического глюкокортикоида "Преднизолон Никомед" ("Никомед Австрия ГмбХ", Линц, Австрия) в дозе 50 мг/кг с помощью внутрижелудочного зонда, инициируя у них развитие окислительного стресса (Валеева И.Х., Зиганшина Л.Е., Бурнашова З.А., Зиганшин А.У. Влияние димефосфона и ксидифона на показатели перекисного окисления липидов и антиоксидантной системы крыс, длительно получавших преднизолон // Экспериментальная и клиническая фармакология. 2002. №2.). Через три часа после проведенных манипуляций животные первой группы сравнения аналогичным способом получали антиоксидант тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид (в дозе 100 мг/кг веса), растворенный в 0,2 мл растительного масла производства ОАО «ЭФКО» торговой марки «Altero Golden». Для чистоты эксперимента и стандартизации манипуляций, связанных с введением в организм веществ, крысам второй группы сравнения через три часа после преднизолона вводили 0,2 мл водопроводной воды. В связи с тем, что тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид является жирорастворимым антиоксидантом, крысам контрольной группы после приема преднизолона внутрижелудочно вводили растворитель антиоксиданта - растительное масло производства ОАО «ЭФКО» торговой марки «Altero Golden» (0,2 мл).
На 15 сутки наблюдения крыс выводили из эксперимента под эфирным наркозом. У животных всех групп забирали тела позвонков грудного отдела позвоночного столба. Для проведения морфологического исследования образцы позвонков животных фиксировали в 10%-м растворе нейтрального формалина, декальцинировали в трилоне Б, обезвоживали в растворах изопропанола возрастающей концентрации и заливали в гистомикс. С помощью полуавтоматического ротационного микротома (SLEE CUT 5062, Германия) изготавливали серийные срезы толщиной 3-5 микрон. Для получения обзорных препаратов, срезы окрашивали гематоксилином Бемера и эозином.
Особенности структурной организации костной ткани тел позвонков изучали методами морфогистохимического анализа. Морфометрические параметры моделирования и ремоделирования костной ткани оценивали с помощью комплекса оптико-структурного анализа на базе AxioImager.M2 с программным обеспечением для анализа изображений AxioVision Z2 М2 (CARL ZEISS, Германия). Съемку изображений осуществляли CCD-камерой AxioCam HR с программным обеспечением ZenLite (CARL ZEISS, Германия).
Элементный состав костной ткани определяли методом атомно-эмиссионного анализа с индуктивно связанной плазмой (спектрометр "Optima 2100 DV", зарегистрированный в Государственном реестре средств измерений, "Perkin Elmer", США, шифр методики КХА: МУК 4.1.1482-03).
Результаты измерений представлены в таблице и рисунке.
Согласно данным таблицы, введение преднизолона приводит к уменьшению площади компактного и губчатого слоев костной ткани на 58,77 и 53,31% соответственно, по сравнению с животными интактной группы (таблица). При гистологическом анализе образцов тел позвонков крыс, получавших только глюкокортикоиды, отмечено неравномерное снижение толщины кортикальных пластинок со стороны дорсальной и вентральной поверхностей тела позвонка. На дорсальной поверхности идентифицированы очаги интенсивной резорбции матрикса костной ткани.
Изменения губчатого слоя пластинчатой костной ткани проявляются истончением костных перекладин, снижением занимаемой ими площади по сравнению с аналогичными образцами позвонков животных интактной группы. В структуре костных балок отчетливо заметно расширение лакун остеоцитов и снижение тинкториальных свойств матрикса на их периферии. Типичным признаком остается наличие многочисленных бесклеточных лакун.
Подобные изменения характерны также для образцов тел позвонков животных контрольной группы (таблица).
Использование антиоксиданта тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфида при длительном использовании глюкокортикоидов препятствует развитию структурных нарушений костной ткани тела позвонка. Результаты исследования препаратов животных второй группы сравнения в проходящем свете позволяют отметить статистически значимое увеличение площади компактного и губчатого слоев пластинчатой костной ткани на 34,53 и 46,97% соответственно, по сравнению с животными, получавшими только глюкокортикоиды (таблица). Как и в исследуемых образцах животных интактной группы, костные балки располагаются параллельно продольной оси тела позвонка и формируют характерную для строения губчатого слоя кости ячеистую структуру.
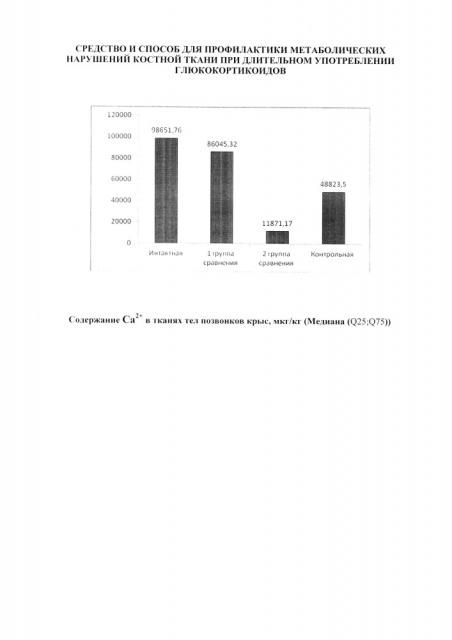
Согласно рисунку, длительное применение глюкокортикоидов приводит к достоверному снижению содержания в матриксе костной ткани такого остеотропного макроэлемента, как Са2+. У животных, получавших преднизолон, значение содержания данного показателя были ниже, чем у крыс интактной группы в 8,3 раза. Полученные результаты являются отражением нарушения обмена важнейшего элемента костной ткани при глюкокортикоидной нагрузке (рисунок).
Содержание Са2+ в костной ткани крыс, получавших антиоксидант тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид на фоне приема глюкокортикоидов не имело достоверных отличий от показателей животных интактной группы. По сравнению с крысами 2 группы сравнения и контрольной групп, у животных получавших антиоксидант тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид, зарегистировано статистически достоверное превышение содержания Са2+ в костной ткани в 7,3 и 1,8 раз (соответственно) (рисунок).
Таким образом, применение полифункционального серосодержащего антиоксиданта тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид оказывает остеопротективный эффект, снижает уровень резорбции костной ткани и является перспективном средством свободнорадикальной защиты клеток и матрикса костной ткани при длительном приеме глюкокортикоидов.
1. Способ профилактики нарушения метаболизма кальция в костной ткани, вызванного длительным приемом глюкокортикоидов, путем перорального употребления средства, обладающего антирадикальной активностью, отличающийся тем, что в качестве средства антирадикальной защиты используют масляный раствор серосодержащего антиоксиданта тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил]сульфид на фоне глюкокортикоидной терапии.
2. Способ по п. 1, отличающийся тем, что используют масляный раствор тио-фан-бис-[(3,5-ди-трет-бутил-4-гидроксифенил)пропил] сульфид с концентрацией из расчета 100 мг/кг веса 2 раза в сутки за 30 мин до приема пищи в течение всего периода использования глюкокортикоидов.