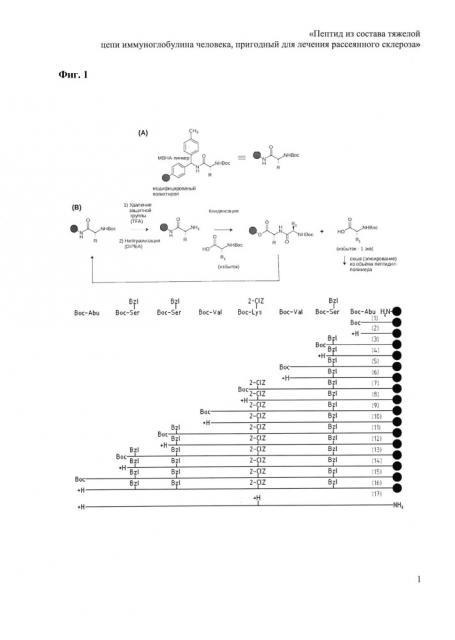
Пептид из состава тяжелой цепи иммуноглобулина человека, пригодный для лечения рассеянного склероза
Иллюстрации
Показать всеИзобретение относится к медицине и касается пептида с последовательностью Abu-Ser-Ser-Val-Lys-Val-Ser-Abu (Abu – α-аминомасляная кислота), соответствующего консервативному участку домена VH тяжелой цепи иммуноглобулинов человека, предназначенного для лечения рассеянного склероза у человека. Изобретение обеспечивает подавление пролиферативной активности лимфоцитов. 1 пр., 3 ил., 1 табл.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к области фармацевтики, в частности к разработке метода медикаментозного лечения различных форм рассеянного склероза у человека.
Несмотря на активные исследования, до настоящего времени не предложено надежного этиотропного метода лечения рассеянного склероза. Механизм возникновения рассеянного склероза экспериментально не доказан. Основными патентообладателями средств терапии этого заболевания традиционно используется следующее описание этого процесса:
1. Причиной нарушения двигательных функций организма больного является разрушение миелиновых оболочек центральной нервной системы. На основании анализа клинической картины РС можно подразделить на четыре категории: RRMS – ремиттирующая форма (85% случаев в мире), PPMS (10% случаев) – первичная прогрессирующая форма, SPMS – вторичная прогрессирующая форма (как правило, развивается при прогрессии заболевания у пациентов с RRMS), PRMS - возвратно-прогрессирующая (5% случаев).
2. Разрушение миелиновых оболочек, состоящих из белков: ОБМ (MBP), основной белок миелина; ПЛП (PLP), протеолипидный протеин; МАГ (MAG) миелин-ассоциированный гликопротеин; МОГ (MOG), миелин-олигодендроцитарный гликопротеин; носит аутоиммунный характер, причем основной вклад в патологию вносят не Т, а В-лимфоциты.
3. В популяции В-лимфоцитов имеется субпопуляция клеток, продуцирующих ростовой лимфокин GM-CSF (гранулоцитарно-макрофагальный колониестимулирующий фактор). Активность этой популяции приводит к снижению уровня продукции тормозного медиатора иммунной системы IL-10. Подавление продукции GM-CSF или инактивация продуцирующих его клеток приводит к облегчению симптомов рассеянного склероза.
4. Т-лимфоциты, специфично распознающие антигены белков миелиновой оболочки: ОБМ, ПЛП, МАГ и МОГ, способны подавлять активность B-лимфоцитов, направленную на разрушение миелиновых оболочек. Поэтому стимуляция Т-клеточного ответа при рассеянном склерозе положительно сказывается на состоянии больных.
5. Под влиянием интерферонов, особенно интерферона β, происходит подавление активности B-лимфоцитов при одновременной стимуляции Т-лимфоцитов, благодаря чему происходит улучшение состояния пациентов с РС.
6. Снижение активности иммунной системы в целом или отдельных ее частей приводит к симптоматическому облегчению течения рассеянного склероза. Поэтому для лечения этого заболевания используются все основные классы иммунодепрессантов различной степени специфичности: неспецифические цитостатики и иммунодепрессанты, блокаторы проникновения лимфоцитов в ткани (антагонисты рецептора адгезии на эндотелии сосудов интегрина 4α), антитела, распознающие поверхностные рецепторы В-лимфоцитов (CD20, рецептор IL2), блокаторы S1P-рецепторов лимфоцитов, в частности финголимод. Эти соединения блокируют сфингозин-1-фосфатные рецепторы (S1P-рецепторы).
Анализ патентной литературы, а также публикаций и материалов маркетингового характера, позволяет предложить следующую классификацию типов лекарственных средств для терапии рассеянного склероза:
1. Неспецифические цитостатики, аналогичные применяемым для лечения онкологических заболеваний, и иммунодепрессанты кортикостероидной природы и на основе адренокортикотропного гормона;
2. Препараты интерферонов, в том числе интерферонов β-1a, β-1b и γ, включая их химически модифицированные формы;
3. Модуляторы S1P-рецепторов – 2-амино-2-[2-(4-октилфенил)этил]пропан-1,3-диол (финголимод) и другие;
4. Т-клеточные вакцины, направленные на активацию или подавления антиген-зависимого распознавания белков миелина;
5. Блокаторы рецепторов на поверхности В-лимфоцитов: CD20 и субъединицы рецептора IL-2, рецептор Fcγ;
6. Антитела против лимфокина GM-CSF;
7. Пептиды, имитирующие ОБМ или другие антигены миелиновой оболочки;
8. Композиции известных субстанций, включая перечисленные выше;
9. Физиотерапевтические способы воздействия лечения и их комбинации с перечисленными медикаментозными средствами.
Уровень техники
Анализ научно-технической литературы в области разработки средств лечения рассеянного склероза позволил выявить следующие характеристики технического уровня и тенденций развития методов медикаментозного лечения рассеянного склероза.
Рассеянный склероз (РС) - англ. Multiple sclerosis (MS) представляет собой воспалительное заболевание, проявляющееся в нарушении миелиновой оболочки центральной нервной системы. РС широко распространен во всем мире. Например, в США в настоящее время зарегистрировано свыше 300 000 пациентов с РС. Заболевание как правило начинается в достаточно молодом возрасте: у 70-80% пациентов первые симптомы РС проявились в возрасте от 20 до 40 лет (Anderson et al. Ann Neurology 31(3):333-6 (1992); Noonan et al. Neurology 58:136-8 (2002)). Диагностика РС основана на клиническом осмотре невропатологом, магнитно-резонансном исследовании ЦНС (МРТ), гистологическом анализе материалов биопсии и аутопсии (Lucchinetti et al. Ann Neurol 47:707-17 (2000)). Болезнь имеет множество различающихся клинических проявлений, затрагивающих функции спинного мозга, головного мозга, черепных нервов, мозжечка, когнитивные функции. Большинство пациентов с РС полностью утрачивают подвижность через 25 лет после появления первых симптомов заболевания. Более половины пациентов с РС через 15 лет после начала болезни могут передвигаться только на костылях. РС является самой распространенной в мире неврологической патологией у пациентов молодого возраста. До настоящего времени для лечения этой болезни не предложено эффективного этиотропного средства. Диагностика РС затруднена чрезвычайным многообразием клинических проявлений. При этом не выработано универсального метода клинической диагностики, позволяющего однозначно оценивать тяжесть заболевания. Использование МРТ, электроэнцефалографии и биохимический анализ пунктатов спинно-мозговой жидкости, хотя и дают ценные сведения о состоянии больного, не всегда могут быть интерпретированы однозначно. Многие частные проявления РС могут быть вызваны не связанными с ним причинами: инфекционными заболеваниями, сосудистыми патологиями, аутоиммунными заболеваниями различной природы (McDonald et al. Ann Neurol 50:121-7 (2001)). РС может быть подразделен на четыре формы: возвратно-ремиттирующую (приступообразную) RRMS - 80%-85% всех регистрируемых случаев, первичную прогрессирующую - PPMS (10-15% случаев), возвратно-прогрессирующую - PRMS (5% случаев) и вторично-прогрессирующую - SPMS (Kremenchutzky et al. Brain 122 (Pt 10):1941-50 (1999); Confavreux et al. N Engl J Med 343(20):1430-8 (2000)). Около 50% пациентов с RRMS приобретают симптомы SPMS через 10 лет после начала заболевания. Свыше 90% пациентов с RRMS в конечном итоге приобретают симптоматику SPMS (Weinshenker et al. Brain 112 (Pt 1):133-46 (1989)).
Иллюстрируя различия в особенностях течения различных форм РС, необходимо отметить, что в 2010 г. в США было допущено к применению шесть препаратов для лечения RRMS, но ни один из них не был разрешен для лечения PPMS. Для лечения RRMS допущены препараты:
1) Класс интерферонов: ИФН-β-1a (REBIF® и AVONEX®); ИФН-β-1b (BETASERON®);
2) Ацетат глатирамера (COPAXONE®), полипептид со случайной последовательностью;
3) Натализумаб (TYSABRI®) - гуманизированное моноклональное антитело против α4-интегрина;
4) Митоксантрон (NOVANTRONE®), блокатор топоизомеразы II, цитостатик.
В ходе испытаний с различной степенью успеха использовались другие препараты: иммунодепрессанты-кортикостероиды, цитостатики метатрексат, циклофосфамид, азатиоприн, внутривенные инъекции нормального иммуноглобулина. По данным метаанализа публикаций, существующие методы лечения позволяют добиться улучшения у ~30% пациентов с RRMS, проявляющиеся в сокращении частоты и силы приступов (Filippini et al. Lancet 361:545-52 (2003)).
Использование для лечения РС других иммуномодулирующих препаратов, в частности антител к TNF((Infliximab) не только не облегчало, но и усугубляло течение РС (Lenercept Multiple Sclerosis Study Group and the University of British Columbia MS/MRI Neurology 53:457-65 (1999); Bielekova et al. Nat Med 6:1167-75 (2000), erratum appears in Nat Med 6:1412 (2000)).
В литературе господствует мнение, что патофизиология РС обусловлена воспалительной реакцией, регулируемой Т-лимфоцитами CD4+Th1-типа. Терапия препаратами ИФН-(и ацетата глатирамера, хотя и не приводят к стойкому излечению, позволяют купировать приступы болезни и замедлить инвалидизацию.
В последние десятилетия при исследовании спинно-мозговой жидкости пациентов с РС удалось убедительно доказать существование специфических для этого заболевания олигоклональных антител класса IgG, которые используются в диагностике РС (Siden A. J Neurol 221:39-51 (1979); McDonald et al. Ann Neurol 50:121-7 (2001); Andersson et al. Eur J Neurol 9:243-51 (2002); O'Connor, P. Neurology 59:S1-33 (2002)). Наличие таких олигоклональных антител, свободных легких цепей иммуноглобулинов, повышение уровня IgM в спинно-мозговой жидкости является признаком, усугубляющим прогноз течения РС у конкретного пациента (Rudick et al. Mult Scler 1:150-5 (1995); Zeman et al. Acta Cytol 45:51-9 (2001); Izquierdo et al. Acta Neurol Scand 105:158-63 (2002); Wolinsky J. J Neurol Sci 206:145-52 (2003); Villar et al. Ann Neurol 53:222-6 (2003)).
Антитела к белкам миелина: ОБМ и МОГ могут служить маркером тяжести РС (Reindl et al. Brain 122:2047-56 (1999); Egg et al. Mult Scler 7(5):285-9 (2001)). Особенно заметно накопление таких антител в спинно-мозговом ликворе пациентов с РС (Reindl et al. Brain 122:2047-56 (1999); Egg et al. Mult Scler 7(5):285-9 (2001); Andersson et al. Eur J Neurol 9:243-51 (2002)). Кроме этого, у пациентов с РС отмечается появление антител к ганглиозидам и нейрофиламентам (Mata et al. Mult Scler 5:379-88 (1999); Sadatipour et al. Ann Neurol 44:980-3 (1998)). По последним данным уровень антител к ОБМ и МОГ позволяет оценивать степень демиелинизации ЦНС у пациентов с RRMS (Berger et al. N Engl J Med 349:139-45 (2003)). Наличие антител к обоим указанным белкам миелина позволило предсказать скорое начало приступа у 76,5% наблюдавшихся пациентов, тогда как наличие антител только к MOG позволило выявить только 31,6% таких пациентов.
Многие специалисты в области РС считают, что наличие в ликворе плазматических клеток, продуцирующих антитела, является значимым фактором образования очагов демиелинизации при РС (Prineas and Wright, Lab Invest 38:409-21 (1978); Esiri M. Neuropathol Appl Neurobiol 6:9-21 (1980); Genain et al. Nat Med 5:170-5 (1999); Lucchinetti et al. Ann Neurol 47:707-17 (2000); Wingerchuk et al. Lab Invest 81:263-81 (2001)). Высокая концентрация B-лимфоцитов в ликворе является значимым отрицательным прогностическим признаком при РС (Cepok et al. Brain 124 (Pt 11):2169-76 (2001)).
У пациентов с RRMS, как и у больных с опсо-миоклональным синдромом, удается добиться стойкого улучшения состояния за счет внутривенного введения Ритуксимаба – гуманизированных моноклональных антител к CD20, основному поверхностному маркеру B-лимфоцитов (Pranzatelli et al. Neurology 60(Suppl1) PO5.128:A395 (2003); Cross et al. “Preliminary Results from a Phase II Trial of Rituximab in MS” (abstract) Eighth Annual Meeting of the Americas Committees for Research and Treatment in Multiple Sclerosis ACTRIMS 20-1 (2003)). See also Cree et al. “Tolerability and Effects of Rituximab “Anti-CD20 Antibody” in Neuromyelitis Optica and Rapidly Worsening Multiple Sclerosis” Meeting of the Am. Acad. Neurol. (2004).
Поверхностный антиген В-лимфоцитов CD20, известный также, как антиген дифференцировки B-лимфоцитов Bp35, представляет собой гидрофобный трансмембранный белок массой ~35 кДа, имеющийся как у зрелых B-лимфоцитов, так и у их предшественников (Valentine et al. J. Biol. Chem. 264(19):11282-11287 (1989); and Einfeld et al. EMBO J. 7(3):711-717 (1988)). Этот антиген часто (более чем в 90% случаев) обнаруживается на поверхности клеток неходжкинских лимфом (Anderson et al. Blood 63(6):1424-1433 (1984)). Однако CD20 отсутствует на поверхности стволовых кроветворных клеток, плазматических клеток и других нормальных тканей человека (Tedder et al. J. Immunol. 135(2):973-979 (1985)). CD20 regulates an early step(s) in the activation process for cell cycle initiation and differentiation (Tedder et al., J. Immunol. 135(2): 973-979 (1985)). Высказывались предположения, что CD20 представляет собой кальциевый канал (Tedder et al. J. Cell. Biochem. 14D:195 (1990)).
С учетом высокой избирательности экспрессии CD20 на поверхности В-лимфоцитов и В-клеточных лимфом его традиционно используют в качестве мишени для адресации терапевтических агентов в этот тип опухолей. Именно с этой целью компанией Genetech из США был разработан препарат гуманизированных моноклональных антител Ритуксимаб (Rituximab) (RITUXAN®) (U.S. Pat. No. 5,736,137). В настоящее время он нашел широкое применение и для лечения РС, особенно RRMS.
Известен и ряд других препаратов гуманизированных моноклональных антител против CD20 человека и их конъюгатов с цитотоксическими агентами, предназначенных для внутривенного введения людям. В это число входят:
1. Ibritumomab Tiuxetan (ZEVALIN®) – конъюгированное с Иттрием-90 производное гуманизированных мышиных моноклональных антител 2B8 (Y2B8)” производства IDEC Pharmaceuticals, Inc. (U.S. Pat. No. 5,736,137). Клон 2B8 депонирован в ATCC под номером доступа HB11388 в июне 1993);
2. Tositumomab (BEXXAR™) – мышиные моноклональные антитела класса IgG2a меченные 131I производства Corixa (U.S. Pat. No. 5,595,721);
3. 1F5 - Мышиные моноклональные антитела и их гуманизированное производное (Press et al. Blood 69(2):584-591 (1987); WO03/002607, Leung, S.) Клон депонирован в ATCC под номером HB-96450;
4. huMax-CD20 - Мышиные моноклональные антитела 2H7 и их гуманизированное производное 2H7 (U.S. Pat. No. 5,677,180; WO2004/035607) производства Genmab, Дания;
5. AME-133 - гуманизированное производное мышиного моноклонального антитела производства Applied Molecular Evolution;
6. IMMU-106 - гуманизированное производное мышиного моноклонального антитела А20 (US 2003/0219433, Immunomedics) и его искусственные производные с удаленным остатком Leu16 в антиген-связывающем центре, с двойной специфичностью связывания CD22/CD20, а также его конъюгат с IL-2 (US 2005/0069545A1; WO 2005/16969; Carr et al.);
7. hLL2xhA20 – моноклональные антитела с двойной специфичностью (WO2005/14618, Chang et al.);
8. Моноклональные антитела L27, G28-2, 93-1B3, B-C1 и NU-B2, распространяемые группой International Leukocyte Typing Workshop (Valentine et al., In: Leukocyte Typing III (McMichael, Ed., p.440, Oxford University Press (1987));
9. Конъюгат моноклональных антител 1H4 с ауристатином Е производства Seattle Genetics;
10. Конъюгаты моноклональных антител против CD20 с IL2 производства EMD/Biovation/City of Hope;
11. Моноклональные антитела против CD20 производства EpiCyte;
12. Моноклональные антитела TRU 015 против CD20 производства Trubion.
Еще одним коммерчески доступным препаратом, активно применяемым для лечения РС путем воздействия на популяцию лимфоцитов, является Даклизумаб, рекомбинантное гуманизированное антитело класса IgG1, направленное против α-субъединицы (Тас) рецептора IL-2. Этот препарат обладает мощными иммуносупрессорными свойствами. Связываясь с субъединицей Тас высокоаффинного рецептора IL−2, экспрессирующегося на активированных Т-клетках, Даклизумаб специфично подавляет передачу сигнала через этот рецептор, угнетает опосредованную IL−2 активацию лимфоцитов, тормозит иммунную реакцию отторжения трансплантата.
Основное назначение даклизумаба - предотвращение острого отторжения почечного аллотрансплантата после пересадки. После 6-месячного применения и последующей отмены даклизумаба частота отторжения остается приемлемой. Увеличивает 6- и 12-месячную выживаемость больных после трансплантации. Антитела к даклизумабу обнаруживаются у 9% больных, но они не изменяют его сывороточные концентрации, эффективность и безопасность.
Мутагенной и канцерогенной активности не обнаружено. Многократное введение яванским макакам доз 1,5; 5,0 и 15 мг/кг/сут в течение 28 дней и однократное введение мышам доз 125 мг/кг не сопровождалось проявлениями токсичности.
Cmax у больных, перенесших аллогенную пересадку почки, после однократного введения дозы 1 мг/кг составляет 21±14 мкг/мл, после 5 инфузий (доза 1 мг/кг) каждые 14 дней - 32±22 мкг/мл. Полное насыщение рецепторов к IL−2 происходит при сывороточных концентрациях 0,5-0,9 мкг/мл, подавление опосредованной IL−2 биологической активности - при уровне в плазме 5-10 мкг/мл. Соблюдение режима дозирования позволяет поддерживать достаточные сывороточные концентрации на протяжении более 90 дней после трансплантации.
Еще одним препаратом, активно используемым для лечения РС, является иммунодепрессант финголимод. Механизм его действия заключается в том, что, проникая в лимфоциты, он метаболизируется сфингозинкиназой до активного метаболита финголимода фосфата. В низких наномолярных концентрациях финголимода фосфат связывается с S1P-рецепторами лимфоцитов 1, 3, и 4 типов и быстро проникает в центральную нервную систему (ЦНС) через гематоэнцефалический барьер, связываясь с S1P-рецепторами нервных клеток 1, 3, и 5 типов. Связывая S1P-рецепторы лимфоцитов, финголимода фосфат блокирует способность лимфоцитов покидать лимфатические узлы, что приводит к перераспределению лимфоцитов в организме. При этом не происходит уменьшения общего количества лимфоцитов в организме. Перераспределение лимфоцитов приводит к снижению лимфоцитарной инфильтрации ЦНС, уменьшению выраженности воспаления и степени повреждения нервной ткани. В течение 4-6 часов после однократного приема препарата в дозе 0,5 мг число лимфоцитов крови снижается приблизительно до 75% от исходного значения. При длительном ежедневном применении препарата число лимфоцитов продолжает снижаться в течение 2-х недель, достигая минимального показателя 500 клеток/мкл или приблизительно 30% от исходного уровня. У 18% больных отмечалось (по крайней мере, однократное) снижение числа лимфоцитов ниже 200 клеток/мкл. При регулярном приеме препарата снижение числа лимфоцитов сохранялось. Поскольку большинство Т- и В-лимфоцитов постоянно проходят через лимфоидные органы, влияние финголимода на эти клетки выражено в наибольшей степени. Однако около 15-20% Т-лимфоцитов, являющихся эффекторными клетками памяти и играющими важную роль в периферическом иммунном контроле, не проходят через лимфоидные органы и не подвержены воздействию финголимода. В течение нескольких дней после прекращения приема препарата в крови отмечается повышение числа лимфоцитов. Нормализация количества лимфоцитов происходит через 1-2 месяца после прекращения лечения. Постоянный прием финголимода приводит к небольшому снижению числа нейтрофилов приблизительно до 80% от исходного показателя. Моноциты не подвержены воздействию финголимода. При применении у пациентов с ремиттирующим РС (средний балл по шкале инвалидности, EDSS, 2,0) финголимод в дозе 0,5 мг снижает частоту клинических обострений болезни на 54%. При приеме препарата у 70 % отмечалась стабильная ремиссия в течение 2-х лет (по сравнению с 45,6% в группе плацебо). Финголимод достоверно снижал риск прогрессирования нетрудоспособности. При применении препарата достоверно увеличивалось время до наступления 3-месячного и 6-месячного периода подтвержденного прогрессирования нетрудоспособности (оцениваемого как повышение оценки по шкале EDSS от исходных показателей) по сравнению с плацебо. Результаты магнитно-резонансной томографии (МРТ) головного мозга больных ремиттирующим РС, на фоне лечения финголимодом подтверждают значительное снижение активности течения заболевания (интенсивности воспалительного процесса в ЦНС, размеров и количества очагов демиелинизации).
Результаты выполненного патентного поиска показывают, что в области патентования исследуемой темы явных лидеров не существует, тем не менее, основными патентодержателями являются американские компании Genetech и Novartis, университет Южной Калифорнии, университет Альберты (Канада), а также израильская компания Teva Pharmaceutical Industries Ltd. В целом, количество патентов по данной тематике достаточно велико, что свидетельствует о перспективности данного направления и патентоемкости рынка.
Для анализа и обобщения сведений, полученных из описаний изобретений, их можно сгруппировать по следующим направлениям.
1. Неспецифические цитостатики и иммунодепрессанты;
2. Препараты интерферонов, включая их химически модифицированные формы;
3. Блокаторы рецептора SlP;
4. Т-клеточные вакцины;
5. Блокаторы рецепторов на поверхности В-лимфоцитов;
6. Пептиды, имитирующие антигены миелиновой оболочки;
7. Блокаторы GM-CSF;
8. Композиции известных субстанций, включая перечисленные выше;
9. Физиотерапевтические способы воздействия лечения и их комбинации с перечисленными медикаментозными средствами.
Анализ отобранной информации свидетельствует, что организации и фирмы многих развитых стран мира проявляют интерес к проблеме лечения РС. Особенно интенсивно исследования проводятся в США.
Патенты по использованию пептидов предлагаемой нами последовательности для лечения РС нами не обнаружены, хотя имеется ряд патентов по использованию в этом качестве фрагментов ОБМ и других антигенов миелина.
В патенте РФ 2471482 «Композиция для лечения рассеянного склероза (варианты)», автора Фазылова М.Ф., патентообладателя «Общество с ограниченной ответственностью "ВАЛЕНТА ИНТЕЛЛЕКТ" (RU)», дата подачи заявки (приоритет) 27.10.2011, опубликованном 10.01.2013, раскрывается изобретение, относящееся к области фармацевтики. Изобретение представляет собой фармацевтическую композицию для лечения РС, включающую терифлуномид в качестве активного начала и вспомогательные вещества при следующем соотношении компонентов, мас.%: терифлуномид - 3,0-13,5; лактоза и/или лудипресс LCE -48,5-65,0; крахмал - 7,0-16,0; микрокристаллическая целлюлоза и/или гипромеллоза - 20,0-30,0; коллидон VA-64 - 3,5-4,5; стеарат магния - 0,8-1,2; аэросил - 0,8-1,2; бенецел МР-824 - 13,5-15,5.
В патенте РФ 2492234 «Композиции для лечения рассеянного склероза (варианты)», автора Фусса А. (FR), патентообладателя «ТИксСЕЛЛ (FR)», дата подачи заявки (приоритет) 17.10.2008, опубликованного 10.09.2013, раскрывается изобретение, относящееся к получению популяции регуляторных Т-клеток (Tr1-клеток), направленных против антигена, ассоциированного с РС, и может быть использовано для восстановления нарушенной толерантности к белкам миелина. Выделяют популяцию Tr1-клеток, направленных против антигена, ассоциированного с РС, и имеющих в покое фенотип CD4+CD25-FoxP3-. Полученную популяцию Tr1-клеток в комбинации с одним или несколькими фармацевтически приемлемыми носителями либо в комбинации с одним или более фармацевтическим средством, применяемым для лечения РС, выбираемым из группы, включающей интерферон-β, глатимера ацетат, митоксантрон, циклофосфамид, метотрексат, азиатропин или натализумаб, используют в составе фармацевтических композиций для лечения РС.
В патенте РФ 2199339 «Способ лечения рассеянного склероза», авторов Барбас И.М., Тотолян Н.А., Скоромец А.А., Смирнов М.Н., Животовская М.Л., Яковлева В.С., патентообладателя «Общество с ограниченной ответственностью "БИОТЕХ"», дата подачи заявки (приоритет) 23.02.2001, опубликованном 27.02.2003, раскрывается метод лечения больных РС. Больным в стадии обострения вводят внутривенно капельно препарат интерлейкина-2 человека (IL-2), например Ронколейкин, в дозе не менее 1 млн. ME 1 раз в 7 дней. Способ позволяет значительно сократить сроки лечения больных РС с выраженным иммунодефицитом, добиться упреждения рецидивов RRMS, продлить период трудоспособности пациентов.
В патенте РФ 2130308 «Применение замещенных производных аденина для лечения рассеянного склероза», автора Беутлер Э.(US), патентообладатель «The Scripps Research Institute (US)», дата подачи заявки (приоритет) 18.02.1993, опубликовано 20.05.1999, МПК А61К 31/70 (1995.01) описывается новый способ лечения пациентов, страдающих РС, с помощью терапевтических средств, содержащих производные аденина, такие как 2-хлор-2-дезоксиаденозин. Препарат значительно улучшает состояние больного, не дает технических побочных эффектов в виде тошноты, рвоты, кожной сыпи, почечные или печеночные нарушения.
В патенте РФ 2137131 «Гибридная клеточная линия (варианты), препарат антител (варианты), способ диагностики рассеянного склероза у человека (варианты), способ лечения человека, полипептид», авторов Клайн Э.Л. (US), Зиммерман Д.Х. (US), патентообладатель «Molecular RX Inc. (US), CellMed Inc. (US)», дата подачи заявки (приоритет) 17.12.1993, опубликовано 10.09.1999, МПК G01N 33/53 (1995.01), C12N 5/08 (1995.01), C12N 15/06 (1995.01), A61K 38/17 (1995.01), A61K 39/00 (1995.01), C07K 14/435 (1995.01) описан метод выявления антигенов, ассоциированных с РС. Также предметом изобретения является метод получения гибридов, которые продуцируют моноклональные антитела, специфичные в отношении антигенов, ассоциированных с РС. Возможности применения изобретения заключается в диагностике РС и в текущем диспансерном наблюдении за больными РС с точки зрения развития болезни либо реакции на терапию. Техническим результатом изобретения является возможность диагностики и лечения РС и других демиелинизирующих заболеваний.
В патенте РФ 2563521 «Способы и композиции для диагностики и лечения аутоиммунной болезни, возникающей вследствие рассеянного склероза», Коуолз А.Дж. (GB), Джоунз Д.Л. (GB), Компстон А. (GB), патентообладатель «КЕМБРИДЖ ЭНТЕРПРАЙЗ ЛИМИТЕД (GB)», дата подачи заявки (приоритет) 08.10.2009, опубликовано 20.09.2015, Бюл. №26, МПК C12Q 1/68 (2006.01) описаны способы диагностики пациентов с PC. Способы предусматривают идентификацию пациентов с РС, имеющих повышенный риск развития рецидива аутоиммунного заболевания после курса истощения популяции лимфоцитов с применением гуманизированного моноклонального антитела против маркера В-лимфоцитов CD52. Также предусматриваются способы выбора схемы лечения для пациентов с PC и реагентов, пригодных для использования в вышеописанных способах.
В патенте РФ 2140247 «Способ лечения рассеянного склероза и дегенераций нервной системы», авторов Казанцева Н.В., Гусев Е.И., Макарова Л.Д., Тимофеев В.Т., патентообладатель Казанцева Наталья Вениаминовна, дата подачи заявки (приоритет) 30.12.1998, опубликовано 27.10.1999, МПК A61G 10/02 (1995.01), A61K 31/47 (1995.01), A61K 31/525 (1995.01), A61K 31/19 (1995.01) описан метод лечения РС с применением оксидантов. Больному назначают ежедневный прием препаратов, усиливающих митохондриальное окисление в терапевтических дозах. Помещают больного в лечебную барокамеру. Проводят компрессию до достижения избыточного давления 0,03 - 0,1 атм. Через 10 - 20 мин завершают сеанс, проводя декомпрессию. Ежедневно повторяют воздействие до 4 - 10 сеансов. Выбор параметров лечебного режима и количества сеансов проводится индивидуально в зависимости от тяжести и характера заболевания под контролем динамики неврологического статуса, капнограммы и/или КЩС, проводят повторные курсы лечения 2 раза в год, а при ухудшении состояния и чаще, под контролем ПОЛ, иммунного статуса, вызванных потенциалов мозга и ЭЭГ. В остром периоде аутоиммунного воспаления метод сочетают с гормонами, цитостатиками и иммуномодуляторами в меньшей, чем принято, дозе, под контролем иммунного статуса. Способ позволяет снижать содержание продуктов перекисного окисления липидов в плазме крови и повышать уровень естественной защиты организма.
В патенте РФ 2509573 «Лекарственное средство для лечения рассеянного склероза и способ лечения рассеянного склероза», автора Эпштейн О.И., патентообладатель Эпштейн О.И., дата подачи заявки (приоритет) 27.07.2010, опубликовано 20.03.2014, Бюл. №8, МПК A61K 39/395 (2006.01), A61P 25/28 (2006.01) описан способ лечения рассеянного склероза с применением гомеопатических доз («активированная-потенцированная форма») антител к гамма-интерферону человека (ИФН-() и антител к мозгоспецифическому белку S-100.
В патенте РФ 2539034 «Лечение рассеянного склероза», авторов Штайдль С. (DE), Дюрр, М. (DE), Томассен-Вольф Э. (DE), Даунхэм М. (IT), Фрайзен Р. (NL), патентообладатель «МорфоСис АГ (DE)», дата подачи заявки (приоритет) 04.05.2010, опубликовано 10.01.2015, Бюл. №1, МПК C07K 16/22 (2006.01), C07K 16/24 (2006.01), C12N 15/13 (2006.01), A61K 39/395 (2006.01), A61P 25/28 (2006.01) описан метод получения гуманизированных моноклональных антител, нейтрализующих активность гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) и применения этих антител для лечения или профилактики пациентов с РС.
В патенте РФ 2384345 «Способ лечения рассеянного склероза» автора Фрона П.А. (US), патентообладатель, Genentech Inc. (US)», дата подачи заявки (приоритет) 02.06.2005, опубликованном 20.03.2010, Бюл. №8, МПК A61K 39/395 (2006.01) описана группа изобретений, включающая способ и изделие, предназначенные для лечения РС. Способ заключается во введении пациентам с ремиттирующей формой РС моноклональных гуманизированных антител против поверхностного рецептора В-лимфоцитов CD20 в количестве 0,5-4,0 г. Через 16-60 недель повторяют введение. Проводится до 4 и более воздействий антитела. Каждое из воздействий - в виде одной или двух доз антитела. Антитело может вводиться внутривенно, подкожно или эпидурально. При этом может использоваться второе лекарственное средство.
В патенте РФ 2390334 «Способ лечения рассеянного склероза», авторов Евдошенко Е.П., Маслянский А.Л., Заславский Л.Г., патентообладатель Государственное образовательное учреждение высшего профессионального образования "Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова Федерального агентства по здравоохранению и социальному развитию", дата подачи заявки (приоритет) 17.12.2008, опубликовано 27.05.2010, Бюл. №15, МПК A61K 31/137 (2006.01), A61K 39/39 (2006.01), A61P 25/28 (2006.01) описан метод лечения больных РС, заключающийся в инфузии ритуксимаба в дозе 1 г с последующим введением митоксантрона в дозе 20 мг и повторной инфузии ритуксимаба в дозе 1 г через 13-15 дней. Перед инфузией ретуксимаба проводят премедикацию по описанному ранее методу. Способ позволяет достичь быстрого терапевтического эффекта и длительной ремиссии при всех формах РС без сопутствующей терапии, в т.ч. химиотерапии.
В патенте РФ 2208443 «Способ лечения рассеянного склероза» авторов Луцевич Э.В., Праздников Э.Н., Стулин И.Д., Самохин Г.Г., Савин А.А., Ушаков С.О., Вельшер Л.З., Золотовская И.К., патентообладатель Самохин Г.Г., дата подачи заявки (приоритет) 20.02.2001, опубликованном 10.03.2003, Бюл. №7, МПК A61K 35/39 (2000.01), A61K 31/197 (2000.01), A61K 31/44 (2000.01), A61K 31/375 (2000.01), A61K 31/395 (2000.01) описан способ лечения больных демиелинизирующими заболеваниями, в частности РС. Способ включает введение ингибитора протеолиза и водорастворимого антиоксиданта в разные поверхностные паховые лимфатические узлы в разовых дозах на порядок меньше среднетерапевтических со скоростью 0,4 мл/мин ежедневно в течение 20 суток.
В патенте РФ 2523058 «Способ терапии ремиттирующего рассеянного склероза», авторов Завалишин И.А., Елисеева Д.Д., Быковская С.Н., патентообладатель Общество с ограниченной ответственностью "Регенекс" (RU), дата подачи заявки (приоритет) 29.06.2012, опубликованном 20.07.2014, Бюл №20, МПК A61K 35/14 (2006.01), A61P 25/28 (2006.01) описан способ лечения ремиттирующего РС. Для этого больному в стадии ремиссии ремиттирующего РС вводят выращенные ex vivo аутологичные регуляторные Т-клетки CD4+CD25+Foxp3+(супрессоры аутоиммунного ответа) из расчета 4,5-5,5 млн клеток на 1 кг веса пациента. Использование данного способа приводит к повышению уровня CD4+CD25+Foxp3+регуляторных Т-клеток в 2 и более раза и поддержанию на уровне нормы, что позволяет пролонгировать состояние ремиссии заболевания до 12 месяцев.
В патенте РФ 2393861 «Композиция для лечения рассеянного склероза», авторов Страдомский Б.В., Вилков Г.А., патентообладатель Аверин К.М., Солодунов Ю.Ю., Страдомский Б.В., Вилков Г.А., дата подачи заявки (приоритет) 15.01.2009, опубликованном 10.07.2010, Бюл. №19, МПК A61K 31/4184 (2006.01), A61K 31/14 (2006.01), A61K 47/32 (2006.01), A61K 9/08 (2006.01), A61K 9/20 (2006.01), A61K 9/48 (2006.01), A61P 25/28 (2006.01) описана композиция (твердая или жидкая форма) для лечения РС, содержащая цитостатик трийодид 1,3-диэтилбензимидазолия в качестве активного начала, поливинилпирролидон низкомолекулярный медицинский, являющийся солюбилизатором и стабилизатором активного начала, и дополнительно в жидкой форме - спирт этиловый в качестве растворителя.
В патенте РФ 2414899 «Средства для лечения рассеянного склероза» авторов Страдомский Б.В., Вилков Г.А., патентообладатель Аверин К.М., Вилков Г.А., Страдомский Б.В., Солодунов Ю.Ю., дата подачи заявки (приоритет) 29.12.2009, опубликованном 27.03.2011, Бюл. №9, МПК A61K 31/4184 (2006.01), A61K 31/14 (2006.01), A61P 25/28 (2006.01) описана композиция (твердая или жидкая форма) для лечения РС на основе трийодида 1,3-диэтилбензимидазолия в качестве активного начала, поливинилпирролидона низкомолекулярного медицинского, являющегося солюбилизатором и стабилизатором активного начала, и дополнительно, в жидкой форме - спирт этиловый в качестве растворителя.
В патенте РФ 2278687 «Способ лечения ремиттирующего рассеянного склероза», авторов Гуфранова Р.Г., Новикова Л.Б., Сперанский В.В., патентообладатель Государственное образовательное учреждение высшего профессионального образования "Башкирский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию" (ГОУ ВПО БГМУ РОСЗДРАВА РОССИИ) (RU), дата подачи заявки (приоритет) 16.06.2005, опубликованном 27.06.2006, Бюл. №18, МПК A61K 38/08 (2006.01), A61K 38/43 (2006.01), A61K 38/01 (2006.01), A61P 25/28 (2006.01), A61P 37/00 (2006.01) описан способ лечения РС. Комплексная терапия включает плазмаферез, интерферонотерапию, введение копаксона, цитостатиков, симптоматических и общеукрепляющих средств, циклоспорина А. При этом исключают введение стероидов и дополнительно в течение 10 дней вводят препараты: церулоплазмин внутривенно капельно по 100 мг и церебролизат внутримышечно по 10 мл. Способ обеспечивает достижение устойчивой ремиссии - до 12 месяцев - у 89,2% больных, снижение степени инвалидизации за счет восстановления регуляторных взаимоотношений нервной и иммунной систем.
В патенте РФ 2493845 «Композиция для лечения рассеянного склероза», автора Фазылов М.Ф., патентообладатель Общество с ограниченной ответственностью "ВАЛЕНТА ИНТЕЛЛЕКТ" (RU), дата подачи заявки (приоритет) 07.06.2012, опубликованном 27.09.2013, Бюл. №27, МПК A61K 31/277 (2006.01), A61K 9/20 (2006.01), A61K 47/26 (2006.01), A61K 47/38 (2006.01), A61P 25/28 (2006.01) описано средство для лечения РС: композиция (твердая оральная дозированная форма) пригодна для сублингвальной, буккальной доставки или доставки через слизистую десны (Z)-2-циано-3-гидрокси-бут-2-эноик кислоты-(4′-трифторметилфенил)-амид (Терифлуномида) в качестве активного начала.
В патенте РФ 2471482 «Композиция для лечения рассеянного склероза», автора Фазылов М.Ф., патентообладатель Общество с ограниченной ответственностью "ВАЛЕНТА ИНТЕЛЛЕКТ" (RU), дата подачи заявки (приоритет) 27.10.2011, опубликованном 10.01.2013, Бюл. №1, МПК A61K 31/277 (2006.01), A61P 25/02 (2006.01), A61P 25/28 (2006.01) описана фармацевтическая композиция для лечения РС, включающая терифлуномид в качестве активного начала и вспомогательные вещества при следующем соотношении компонентов, мас.%: терифлуномид - 3,0-13,5; лактоза и/или лудипресс LCE -48,5-65,0; крахмал - 7,0-16,0; микрокристаллическая целлюлоза и/или гипромеллоза - 20,0-30,0; коллидон VA-64 - 3,5-4,5; стеарат магния - 0,8-1,2; аэросил - 0,8-1,2; бенецел МР-824 - 13,5-15,5.
В патенте РФ 2257915 «Способ лечения обострений рассеянного склероза», авторов Лиждвой В.Ю., Котов С. В., Сидорова О.П., патентообладатель Государственное учреждение Московский областной научно-исследовательский институт им. М.Ф. Владимирского (МОНИКИ им. М.Ф. Владимирского) (RU), дата подачи заявки (приоритет) 17.10.2003, опубликованном 10.08.2005, Бюл. №22, МПК A61K 39/395 (2000.01), A61K 31/185 (2000.01), A61B 5/107 (2000.01), A61P 25/28 (2000.01) описан способ включает определения интерферонового статуса у пациентов с РС с последующей лекарственной терапией. При этом дополнительно определяют площадь тела больного и при зарегистрированной I степени угнетения системы интерферонов в качестве лекарственной терапии назначают препарат «Антилимфолин Кз» в/в капельно в курсовой дозе (0,5-0,6)г×S, где S - площадь тела больного, через день, и тиоктацид в дозе 300-600 мг в/в капельно ежедневно курсом 6-8 дней. При II и III степени угнетения системы интерферонов назначают «Антилимфолин Кз» в курсовой дозе 0,4-0,5 г/м2 и 0,3-0,4 г/м2, а тиоктацид в дозе 600-900 мг и 900-1200 мг соответственно. Способ позволяет эффективно избирательно воздействовать на иммунную систему за счет совместного назначения иммуномодулятора и средства, ускоряющего его введение при подавлении активности провоспалительных цитокинов, что удлиняет ремиссию заболевания, предупреждая прогрессирование иммунологических нарушений.
В патенте РФ 2562571 «Педиатрические композиции для лечения рассеянного склероза» Коварик Д. (CH), Шмоудер Р. (US), Бастьен М.-К. (US), Давид О. (CH), Карлссон Г. (CH), Буйон Т. (CH), патентообладатель «НОВАРТИС АГ (CH)», дата подачи заявки (приоритет) 19.06.2009, конвенционный приоритет 20.06.2008 US 61/132,621, опубликованном 10.09.2015, Бюл. №25, МПК A61K 31/137 (2006.01), A61P 37/00 (2006.01), A61K 38/00 (2006.01), A61K 38/21 (2006.01), A61K 39/00 (2006.01), A61K 45/00 (2006.01) предложены: фармацевтическая композиция указанного назначения для детей, содержащая 0,25 мг и менее 2-амино-2-[2-(4-С2-С20-алкилфенил)этил]пропан-1,3-диола или его фармацевтически приемлемой соли для введения 1 раз в день, применение указанного соединения (FTY720) по 0,25 мг и менее для изготовления лекарственного средства для лечения, предупреждения или замедления развития РС у пациента педиатрического возраста для введения 1 раз в день и соответствующий способ лечения, предупреждения или замедления развития РС у пациента педиатрического возраста.
В патенте РФ 2522251 «Вещества и способы лечения рассеянн