Системы и способы для улучшенной стабильности электрохимических сенсеров
Иллюстрации
Показать всеГруппа изобретений относится к области медицинского тестирования, в частности к определению концентрации аналита в образце. Способ определения концентрации аналита в образце включает: введение образца с аналитом в электрохимическую ячейку; определение первой концентрации аналита; определение результата измерения параметра, коррелирующего с физическим свойством электрохимической ячейки; вычисление поправочного коэффициента и определение концентрации аналита с учетом поправочного коэффициента. Электрохимическая ячейка имеет первый и второй электроды, при этом на втором электроде отсутствует покрытие из слоя реагента. При этом определение емкости электрохимической ячейки содержит: приложение первого тестового потенциала Е1 между первым и вторым электродами, приложение второго тестового потенциала Е2 между первым и вторым электродами и обработку части тестовых токов посредством суммирования токов. Также раскрывается вариант способа определения концентрации аналита в образце и варианты электрохимической системы. Группа изобретений обеспечивает сохранение точности определения концентрации аналита во время хранения электрохимической системы. 4 н. и 15 з.п. ф-лы, 9 ил., 4 табл., 5 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Представленные здесь система и способ относятся к области медицинского тестирования, в частности, определения наличия и/или концентрации аналита (аналитов) в образце (например, физиологических жидкостей, включая кровь).
УРОВЕНЬ ТЕХНИКИ
Значение определения концентрации аналита в физиологических жидкостях (например, в крови или препаратах крови, таких как плазма) в современном обществе непрерывно возрастает. Такой анализ находит применение во множестве сфер и условий, таких как клиническое лабораторное тестирование, тестирование на дому и т.д., где результаты тестирования играют значительную роль в диагностике и контроле многих заболеваний. Представляющие интерес аналиты включают глюкозу при контроле диабета, холестерин при контроле сердечно-сосудистых заболеваний и др.
Общий способ определения концентрации аналита основан на электрохимии. В таких способах жидкий водный образец помещают в реакционную камеру для образца в сенсоре, например, в электрохимическую ячейку, содержащую не менее двух электродов, т.е. рабочий электрод и противоэлектрод, причем электроды имеют импеданс, который делает их пригодными для амперометрического или кулонометрического измерения. Анализируемому компоненту дают прореагировать с реагентом, образуя окисляемое (или восстанавливаемое) вещество в количестве, пропорциональном концентрации аналита. Затем это количество имеющегося окисляемого (или восстанавливаемого) вещества оценивают электрохимически и соотносят с концентрацией аналита в образце.
Желательное качество всех элементов сенсора заключается в том, чтобы они обладали длительным сроком годности, т.е. чтобы характеристика чувствительности элемента сенсора не изменялась значительным образом между производством и применением (т.е. во время хранения). Однако при хранении в течение продолжительных периодов времени и/или в неоптимальных условиях хранения, например, при высоких температурах, высокой влажности и т.д., эксплуатационные качества сенсоров могут ухудшиться. Например, точность определений концентрации аналита, выполненных при помощи таких сенсоров, может снизиться. Задачей настоящего изобретения является преодоление или частичное устранение этих и других недостатков в уровне техники.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Здесь представлены разные аспекты системы и способа определения концентрации аналита в образце (пробе). В одном таком аспекте системы и способы включают применение электрохимической ячейки, в которой прикладывают потенциал и измеряют ток. Можно также измерить параметр, коррелирующий с физическим свойством электрохимической ячейки. На основании измерений тока и параметра, коррелирующего с физическим свойством, способы и системы позволяют быстро найти концентрацию аналита при минимизации влияния физического свойства электрохимической ячейки.
В различных обсуждаемых далее вариантах реализации электрохимическую ячейку можно использовать в различных устройствах для анализа образцов, таких как сенсоры (датчики) глюкозы или иммуносенсоры. Анализируемый образец может содержать кровь. В одном варианте реализации кровь может содержать цельную кровь. Аналит, концентрацию которого анализируют, может включать глюкозу. Анализ концентрации глюкозы может включать окисление глюкозы до глюконовой кислоты. В одном варианте реализации можно использовать фермент глюкозодегидрогеназу (GDH) в присутствии кофактора флавинадениндинуклеотида (FAD) для катализа превращения глюкозы в глюконовую кислоту. В тех вариантах реализации, в которых устройство для анализа образцов является иммуносенсором, аналит, концентрацию которого анализируют, может включать С-реактивный белок.
В одном из аспектов раскрыт способ определения концентрации аналита в образце. Способ включает введение образца в электрохимическую ячейку устройства для анализа образцов, чтобы вызвать превращение аналита. Можно использовать различные электрохимические ячейки, включая, например, ячейку с первым и вторым электродами в разнесенном взаимном расположении и реагентом. После введения образца способ включает в себя определение параметра, коррелирующего с физическим свойством электрохимической ячейки, и вычисление поправочного коэффициента, причем поправочный коэффициент учитывает по меньшей мере параметр, коррелирующий с физическим свойством электрохимической ячейки. Затем способ включает в себя определение концентрации аналита с учетом поправочного коэффициента.В другом аспекте раскрыта электрохимическая система. Электрохимическая система может включать электрохимическую ячейку с первым электродом и вторым электродом и измерительный прибор, соединенный с электрохимической ячейкой. Измерительный прибор может включать в себя блок управления, соединенный с электрохимической ячейкой так, чтобы блок управления прикладывал потенциал между первым электродом и вторым электродом электрохимической ячейки и чтобы блок управления определял результат измерения параметра, коррелирующего с физическим свойством электрохимической ячейки, и использовал упомянутый результат измерения для расчета скорректированной (т.е. с поправкой) концентрации аналита в образце.
В некоторых вариантах реализации физическое свойство, с которым коррелирует поправочный коэффициент, может быть связано с по меньшей мере одним из старения электрохимической ячейки и/или условия хранения электрохимической ячейки. Например, условие хранения может включать температуру хранения и время хранения. В одном аспекте параметр, коррелирующий с физическим свойством электрохимической ячейки, может включать измеренную емкость электрохимической ячейки.
В другом аспекте представлен способ измерения концентрации аналита с поправкой. Способ включает нанесение образца на тестовую полоску. После нанесения образца способ включает приложение в течение первого интервала времени между первым электродом и вторым электродом первого тестового напряжения, достаточного для окисления первого медиатора на втором электроде. После приложения первого тестового напряжения способ включает приложение в течение второго интервала времени между первым электродом и вторым электродом второго тестового напряжения, достаточного для окисления восстановленного медиатора на первом электроде. Затем можно рассчитать первую концентрацию глюкозы на основании значений тестового тока в течение первого интервала времени и второго интервала времени.
Этот способ может включать определение емкости тестовой полоски и вычисление концентрации глюкозы с поправкой на емкость на основании первой концентрации глюкозы и емкости. Например, этап вычисления концентрации глюкозы с поправкой на емкость может включать вычисление поправочного коэффициента на основании емкости и первой концентрации глюкозы, причем концентрацию глюкозы с поправкой на емкость вычисляют на основании первой концентрации глюкозы и поправочного коэффициента. Например, поправочный коэффициент может быть около нуля, когда емкость примерно равна предварительно определенной идеальной емкости тестовой полоски. В этих вариантах реализации этап вычисления концентрации глюкозы с поправкой на емкость дополнительно может включать деление поправочного коэффициента на сто и добавление единицы для получения промежуточного члена, и умножение промежуточного члена на первую концентрацию глюкозы для получения концентрации глюкозы с поправкой на емкость.
В некоторых вариантах реализации концентрацию глюкозы с поправкой на емкость можно рассчитывать, когда емкость ниже первого порога емкости, а первая концентрация глюкозы выше первого порога концентрации глюкозы. В некоторых вариантах реализации способ также может включать определение того, больше ли поправочный коэффициент, чем пороговое значение поправочного коэффициента, в этом случае поправочный коэффициент принимают равным пороговому значению поправочного коэффициента.
В другом аспекте представлена электрохимическая система. Электрохимическая система может включать тестовую полоску и тестер (измерительный прибор для проведения тестов). Тестовая полоска может включать электрохимическую ячейку и электрические контакты для сопряжения с тестером. Электрохимическая ячейка может включать первый электрод и второй электрод в разнесенном взаимном расположении и реагент. Тестер может включать в себя процессор, приспособленный для получения данных о токе от тестовой полоски, а также приспособленный для определения концентрации глюкозы с поправкой на емкость на основании вычисленной концентрации глюкозы и измеренной емкости. Например, измеренная емкость может коррелировать с физическим свойством тестовой полоски, соотносящимся с по меньшей мере одним из старения тестовой полоски и условия хранения тестовой полоски. Условие хранения может включать, например, температуру хранения и время хранения.
В одном примерном варианте реализации тестовое устройство может включать хранилище данных, содержащее порог концентрации глюкозы и порог емкости. В некоторых вариантах реализации, например, процессор может определять значение концентрации глюкозы с поправкой на емкость, когда измеренная емкость меньше, чем порог емкости, а вычисленная концентрация глюкозы выше, чем порог концентрации глюкозы.
В различных обсужденных выше системах и способах примерный способ определения емкости электрохимической ячейки может включать приложение первого тестового напряжения между первым электродом и вторым электродом. Первое тестовое напряжение может иметь переменнотоковую компоненту напряжения и постояннотоковую компоненту напряжения, и переменнотоковая компонента напряжения может быть приложена на заданное количество времени после приложения первого тестового напряжения. Тестовое напряжение также может иметь постояннотоковую компоненту напряжения с достаточной величиной, чтобы вызвать предельный тестовый ток на втором электроде, причем на втором электроде отсутствует покрытие слоем реагента. Способ также может включать обработку части тестовых токов, возникающей в результате приложения переменнотоковой компоненты напряжения, в значение емкости электрохимической ячейки.
Эти и другие варианты реализации, признаки и преимущества станут очевидными специалистам при учете приведенного ниже более подробного описания различных примерных вариантов реализации изобретения в сочетании с соответствующими чертежами, которые сначала кратко описаны.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Различные признаки настоящего изобретения изложены со скрупулезностью в прилагаемой формуле изобретения. Эти признаки можно лучше понять, обратившись к следующему подробному описанию, где приведены пояснительные, неограничивающие варианты реализации, и к соответствующим чертежам, на которых:
ФИГ. 1А иллюстрирует изображение в перспективе примерной тестовой полоски;
ФИГ. 1В иллюстрирует изображение в перспективе с пространственным разделением деталей тестовой полоски с ФИГ. 1А;
ФИГ. 1С иллюстрирует изображение в перспективе дистальной части тестовой полоски с ФИГ. 1А;
ФИГ. 2 иллюстрирует вид снизу тестовой полоски с ФИГ. 1А;
ФИГ. 3 иллюстрирует вид сбоку тестовой полоски с ФИГ. 1А;
ФИГ. 4А иллюстрирует вид сверху тестовой полоски с ФИГ. 1А;
ФИГ. 4В иллюстрирует частичный вид сбоку дистальной части тестовой полоски, согласующийся со стрелками 4В-4В на ФИГ. 4А;
ФИГ. 5 иллюстрирует упрощенную схему, показывающую тестер, электрически сопрягающийся с контактными площадками тестовой полоски;
ФИГ. 6 иллюстрирует вид с пространственным разделением деталей примерного варианта реализации иммуносенсора в соответствии с настоящим изобретением;
ФИГ. 7А иллюстрирует форму сигнала тестового напряжения, с которой тестер прикладывает множество тестовых напряжений в течение предписанных интервалов времени;
ФИГ. 7В иллюстрирует транзиент тестового тока, сгенерированного с формой сигнала тестового напряжения по ФИГ. 6;
ФИГ. 8А иллюстрирует форму сигнала тестового напряжения, с которой тестер прикладывает множество тестовых напряжений при противоположной полярности в течение предписанных интервалов времени по сравнению с ФИГ. 7А;
ФИГ. 8В иллюстрирует транзиент тестового тока, сгенерированного с тестовыми напряжениями по ФИГ. 8А;
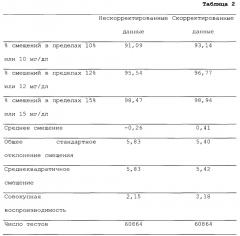
ФИГ. 9 - это график, на котором показана взаимосвязь между емкостью и процентной долей смещения для множества тестов.
ПОДРОБНОЕ ОПИСАНИЕ
Следующее подробное описание следует читать с обращением к чертежам, на которых аналогичные элементы на различных чертежах пронумерованы одинаково. Чертежи, не требующие масштабирования, изображают избранные варианты реализации и не предназначены ограничивать объем изобретения. Подробное описание иллюстрирует в качестве примера, а не ограничения, принципы изобретения.
Использованные здесь термины "примерно" или "приблизительно" для любых численных значений или диапазонов указывают на подходящее допустимое отклонение величины, позволяющее детали или набору компонентов функционировать по своему назначению, как описано ниже. Кроме того, использованные здесь термины "пациент", "реципиент", "пользователь" и "объект" относятся к любому объекту - человеку или животному и не предназначены ограничиваться системами или способами для применения в отношении человека, хотя применение данного изобретения в отношении пациента-человека представляет собой предпочтительный вариант реализации.
Далее будут описаны некоторые примерные варианты реализации, дающие общее представление о принципах конструкции, функционировании, изготовлении и применении обсуждаемых далее систем и способов. Один и более из примеров этих вариантов реализации показаны на сопроводительных чертежах. Специалисты поймут, что системы и способы, особо описанные далее и показанные на прилагаемых чертежах, представляют собой неограничивающие примерные варианты реализации и что объем настоящего изобретения определяется исключительно формулой изобретения. Признаки, проиллюстрированные или описанные в связи с одним примерным вариантом реализации, могут быть скомбинированы с признаками других вариантов реализации. Предполагается, что такие изменения и вариации входят в объем настоящего изобретения.
Описанные здесь системы и способы пригодны для применения при определении широкого спектра аналитов в широком спектре образцов и особенно пригодны для определения аналитов в цельной крови, плазме, сыворотке, межклеточной жидкости или их производных. В примерном варианте реализации система теста на глюкозу на основе тонкослойной ячейки с противоположными электродами и трехимпульсным быстрым электрохимическим детектированием (например, время анализа примерно 5 секунд) требует небольшого образца (например, примерно 0,4 мкл) и может обеспечить повышенную надежность и точность измерений уровня глюкозы в крови. В реакционной ячейке для анализа аналита глюкозу в образце может быть окислена до глюконолактона при помощи глюкозодегидрогеназы, и при этом может быть использован электрохимически активный медиатор для переноса электронов от этого фермента к палладиевому рабочему электроду. Конкретнее, покрытие из слоя реагента по меньшей мере одного из электродов в реакционной ячейке может включать глюкозодегидрогеназу (GDH) в присутствии кофактора пирролохинолинхинона (PQQ) и феррицианида. В другом варианте реализации фермент GDH в присутствии кофактора PQQ можно заменить на фермент GDH в присутствии кофактора флавинадениндинуклеотида (FAD). При добавлении в реакционную камеру крови или контрольного раствора глюкоза окисляется под действием 60Н(окисл.), и в этом процессе происходит превращение CDH(окисл.) в GDH(bocct.), как показано в химической реакции Т.1 ниже. Отметим, что CDH(окисл.) относится к окисленному состоянию GDH, a GDH(восст.) относится к восстановленному состоянию GDH.
Т.1 D-глюкоза+GDH(окисл.)→глюконовая кислота+GDH (восст.)
Можно использовать потенциостат для приложения трехимпульсного сигнала напряжения между рабочим электродом и противоэлектродом, что приводит к появлению транзиентов тестового тока, используемых для расчета концентрации глюкозы. Затем дополнительную информацию, полученную из транзиентов тестового тока, можно использовать для распознавания матриц образцов и поправки на изменчивость в образцах крови из-за гематокрита, колебания температуры, электрохимически активных компонентов, а также выявления возможных системных ошибок.
Данные способы можно, в принципе, применять в случае любого типа электрохимической ячейки с разнесенными первым и вторым электродами и слоем реагента. Например, электрохимическая ячейка может быть в виде тестовой полоски. В одном аспекте тестовая полоска может включать два противоположных электрода, разделенных тонкой прокладкой для ограничения принимающей образец камеры или зоны, в которой расположен слой реагента. Заявители отмечают, что с описанными здесь способами можно также использовать другие типы тестовых полосок, включая, например, тестовые полоски с копланарными электродами.
Электрохимические ячейки
На ФИГ. 1А-4В показаны различные виды примерной тестовой полоски 62, пригодной для применения с описанными здесь способами. Как показано, тестовая полоска 62 может включать продолговатое тело, простирающееся от проксимального конца 80 до дистального конца 82, с боковыми краями 56, 58. Проксимальная часть тела 59 может включать реакционную камеру 61 для образца с несколькими электродами 164, 166 и реагентом 72, тогда как дистальная часть тела 59 тестовой полоски может включать элементы для обеспечения электрической связи с тестером. При эксплуатации в реакционную камеру 61 для образца вводят физиологическую жидкость или контрольный раствор для электрохимического анализа.
В показанном варианте реализации тестовая полоска 62 может включать первый электродный слой 66 и второй электродный слой 64 с расположенным между ними слоем 60 прокладки. Первый электродный слой 66 может обеспечивать первый электрод 166 и первую соединительную дорожку 76 для электрического соединения первого электрода 166 с первым электрическим контактом 67. Аналогично, второй электродный слой 64 может обеспечивать второй электрод 164 и вторую соединительную дорожку 78 для электрического соединения второго электрода 164 со вторым электрическим контактом 63.
В одном варианте реализации реакционная камера 61 для образца ограничена первым электродом 166, вторым электродом 164 и прокладкой 60, как показано на ФИГ. 1А-4В. Точнее, первый электрод 166 и второй электрод 164 образуют, соответственно, дно и верх реакционной камеры 61 для образца. Вырез 68 прокладки 60 может образовывать боковые стенки реакционной камеры 61 для образца. В одном аспекте реакционная камера 61 для образца может дополнительно включать ряд отверстий 70, которые обеспечивают вход образца и/или вентиляционное отверстие. Например, одно из отверстий может обеспечивать поступление жидкого образца, а другое отверстие может действовать как вентиляционное отверстие.
Реакционная камера 61 для образца может иметь малый объем. Например, объем может составлять от примерно 0,1 микролитра до примерно 5 микролитров, предпочтительно от примерно 0,2 микролитра до примерно 3 микролитров, а еще более предпочтительно от примерно 0,3 микролитра до примерно 1 микролитра. Как будет понятно специалистам, реакционная камера 61 для образца может иметь различные другие такие объемы. Для обеспечения, малого объема образца вырез 68 может иметь площадь в диапазоне от примерно 0,01 см2 до примерно 0,2 см2, предпочтительно от примерно 0,02 см2 до примерно 0,15 см2, а еще более предпочтительно от примерно 0,03 см2 до примерно 0,08 см2. Аналогично, специалистам будет понятно, что объемный вырез 68 может иметь разные другие такие площади. Кроме того, первый и второй электроды 166, 164 могут отстоять друг от друга на расстояние от примерно 1 микрона до примерно 500 микрон, предпочтительно в диапазоне от примерно 10 микрон до примерно 400 микрон, а еще более предпочтительно в диапазоне от примерно 40 микрон до примерно 200 микрон. В других вариантах реализации такой диапазон может колебаться между различными другими значениями. Близкое расположение электродов может также обеспечивать возможность окислительно-восстановительного циклирования, при котором окисленный медиатор, образовавшийся на первом электроде 166, может диффундировать ко второму электроду 164, чтобы восстанавливаться, а затем диффундировать обратно к первому электроду 166, чтобы вновь окисляться.
На дистальном конце тела 59 тестовой полоски первый электрический контакт 67 можно использовать для установления электрического соединения с тестером. Доступ тестера ко второму электрическому контакту 63 можно обеспечить через U-образную прорезь 65, как показано на ФИГ. 2. Заявители отмечают, что тестовая полоска 62 может содержать ряд альтернативных электрических контактов, предназначенных для обеспечения электрического соединения с тестером. Например, патент США №6379513, все содержание которого настоящим включено сюда по ссылке, описывает средства подсоединения электрохимической ячейки.
В одном варианте реализации первый электродный слой 66 и/или второй электродный слой 64 могут представлять собой проводящий материал, образованный из таких материалов, как золото, палладий, углерод, серебро, платина, оксид олова, иридий, индий и их сочетания (например, легированный индием оксид олова). Кроме того, электроды можно сформировать путем нанесения проводящего материала на изолирующий лист (не показан) при помощи различных технологий, таких как, например, напыление, нанесение покрытия методом химического восстановления или трафаретная печать. В одном примерном варианте реализации второй электродный слой 64 может представлять собой напыленный золотой электрод, а первый электродный слой 66 может представлять собой напыленный палладиевый электрод. Подходящие материалы, которые можно использовать в качестве слоя 60 прокладки, включают различные изоляторы, такие как, например, пластики (например, ПЭТ, ПЭТГ, полиимид, поликарбонат, полистирол), кремний, керамика, стекло, клеи и их сочетания.
Слой реагента 72 можно нанести внутри реакционной камеры 61 для образца при помощи таких технологий, как щелевое нанесение, нанесение с подачей из конца трубки, нанесение чернилами и трафаретная печать. Такие технологии описаны, например, в следующих патентах США №№: 6749887, 6869411, 6676995, и 6830934, каждый из которых целиком включен сюда по ссылке. В одном из вариантов реализации слой реагента 72 может включать, по меньшей мере, медиатор и фермент и может быть осажден на первый электрод 166. В пределы сути и объема данного изобретения попадают различные медиаторы и/или ферменты. Например, подходящие медиаторы включают феррицианид, ферроцен, производные ферроцена, комплексы бипиридилосмия и производные хинона. Примеры подходящих ферментов включают глюкозооксидазу, глюкозодегидрогеназу (GDH) в присутствии кофактора пирролохинолинхинона (PQQ), GDH в присутствии кофактора никотинамидадениндинуклеотида и GDH в присутствии кофактора флавинадениндинуклеотида [Е.С.1.1.99.10]. Один из примерных составов реагентов, пригодный для формирования слоя реагента 72, описан в совместно поданной заявке на патент США №10/242951, озаглавленной: "Способ производства стерилизованного и калиброванного биосенсорного медицинского устройства", опубликованной под номером публикации заявки на патент США № 2004/0120848, которая настоящим целиком включена сюда по ссылке.
Либо первый электрод 166, либо второй электрод 164 могут функционировать как рабочий электрод, окисляющий или восстанавливающий лимитирующее количество медиатора в зависимости от полярности приложенного тестового потенциала тестера. Например, если лимитирующее ток вещество представляет собой восстановленный медиатор, то оно может окисляться на первом электроде 166, пока к нему приложен достаточно положительный потенциал по отношению ко второму электроду 164. В такой ситуации первый электрод 166 выполняет функцию рабочего электрода, а второй электрод 164 выполняет функцию противоэлектрода/электрода сравнения. Следует отметить, что если не указано иное для тестовой полоски 62, все потенциалы, приложенные тестером 100, будут далее указаны в отношении второго электрода 164.
Аналогично, если приложен достаточно отрицательный потенциал по отношению ко второму электроду 164, то восстановленный медиатор может окисляться на втором электроде 164. В такой ситуации второй электрод 164 выполняет функцию рабочего электрода, а первый электрод 166 выполняет функцию противоэлектрода/электрода сравнения.
Изначально предлагаемый способ может включать введение некоторого количества представляющего интерес жидкого образца в тестовую полоску 62, которая имеет первый электрод 166, второй электрод 164 и слой реагента 72. Жидкий образец может представлять собой цельную кровь или ее производную или фракцию, или же контрольный раствор. Жидкий образец, например, кровь, можно ввести в реакционную камеру 61 для образца через отверстие 70. В одном аспекте отверстие 70 и/или реакционная камера 61 для образца могут быть сконструированы так, что действие капиллярных сил заставляет жидкий образец заполнять реакционную камеру 61 для образца.
На ФИГ. 5 показана упрощенная схема тестера 100, сопрягающегося с первым электрическим контактом 67 и вторым электрическим контактом 63, которые электрически связаны соответственно с первым электродом 166 и вторым электродом 164 тестовой полоски 62. Тестер 100 может быть выполнен с возможностью электрического соединения с первым электродом 166 и вторым электродом 164 через первый электрический контакт 67 и второй электрический контакт 63 соответственно (как показано на ФИГ. 2 и 5). Как будет понятно специалистам, в описанном здесь способе можно использовать множество различных тестеров. Однако в одном варианте реализации тестер включает в себя по меньшей мере процессор, который может включать в себя один или более блоков управления, предназначенных для выполнения расчетов, позволяющих вычислять поправочный коэффициент с учетом по меньшей мере одного измеряемого параметра, коррелирующего с физическим свойством электрохимической ячейки, а также предназначенных для сортировки и/или хранения данных. Микропроцессор может быть в виде процессора смешанного типа (MSP), т.е. аналого-цифрового, такого как, например, Texas Instrument MSP 430. TI-MSP 430 может быть также предназначен выполнять часть функции потенциостата и функции измерения тока. Кроме того, MSP 430 также может включать в себя энергозависимую и долговременную память. В другом варианте реализации многие из электронных компонентов могут быть интегрированы с микроконтроллером в виде специализированной интегральной схемы.
Как показано на ФИГ. 5, электрический контакт 67 может включать в себя два штыря 67а, 67b. В одном примерном варианте реализации тестер 100 отдельно соединяется со штырями 67а, 67b так, чтобы при сопряжении тестера 100 с тестовой полоской 62 цепь замыкалась. Тестер 100 может измерять сопротивление или неразрывность электрической цепи между штырями 67а, 67b, чтобы определить, наличествует ли электрическое подключение между тестовой полоской 62 и тестером 100. Заявители отмечают, что тестер 100 может использовать множество различных сенсоров и цепей для определения того, правильно ли расположена тестовая полоска 62 по отношению к тестеру 100.
В одном варианте реализации цепь, расположенная в тестере 100, может прикладывать тестовый потенциал и/или ток между первым электрическим контактом 67 и вторым электрическим контактом 63. Как только тестер 100 выявляет, что была вставлена полоска 62, тестер 100 включается и запускает режим обнаружения жидкости. В одном варианте реализации режим обнаружения жидкости вынуждает тестер 100 подавать постоянный ток в 1 микроампер между первым электродом 166 и вторым электродом 164. Поскольку тестовая полоска 62 изначально сухая, тестер 100 измеряет максимальное напряжение, которое ограничено аппаратными средствами в тестере 100. Однако как только пользователь вводит жидкий образец во входное отверстие 70, это приводит к заполнению реакционной камеры 61 для образца. Когда жидкий образец заполняет промежуток между первым электродом 166 и вторым электродом 164, тестер 100 измеряет уменьшение измеренного напряжения (например, как описано в патенте США №6193873, который целиком включен сюда по ссылке), которое ниже заданного порога, что заставляет тестер 100 автоматически начинать тест на глюкозу.
Следует отметить, что измеренное напряжение может уменьшаться ниже заданного порога, когда заполнена только некая доля реакционной камеры 61 для образца. Способ автоматического выявления того, что жидкость нанесена, не обязательно позволяет установить, что реакционная камера 61 для образца целиком заполнена, и может только подтвердить наличие некоторого количества жидкости в реакционной камере 61 для образца. Как только тестер 100 определяет, что на тестовую полоску 62 нанесена жидкость, может потребоваться еще небольшое, но ненулевое количество времени для того, чтобы позволить жидкости целиком заполнить реакционную камеру 61 для образца.
Другой примерный вариант реализации устройства для анализа образца для применения в сочетании с по меньшей мере некоторыми из описанных здесь способов, иммуносенсор 110, показан на ФИГ. 6 и описан в заявке на патент США с порядковым №12/570268 авторов Chatelier и др., озаглавленной "Адгезивные составы для применения в иммуносенсоре" и поданной 30 сентября 2009 г., содержимое которой целиком включено сюда по ссылке. В иммуносенсоре может быть образовано множество камер, включая камеру заполнения, через которую образец может быть введен в иммуносенсор, реакционную камеру, в которой образец может прореагировать с одним и более желательными материалами, и камеру детектирования, при помощи которой можно определить концентрацию конкретного компонента образца. Эти камеры могут быть сформированы в по меньшей мере части первого электрода, второго электрода и сепаратора имммуносенсора. Иммуносенсор может также иметь вентиляционное отверстие, позволяющее воздуху входить в иммуносенсор и выходить из него по мере необходимости, и первую и вторую герметизирующие детали для селективной герметизации первой и второй сторон вентиляционного отверстия. Первая герметизирующая деталь также может образовывать стенку камеры заполнения.
Как показано, иммуносенсор 110 включает в себя первый электрод 112 с двумя нанесенными на него полосками жидких реагентов 130, 132. Первый электрод 112 может быть сформирован с применением любого числа методик, используемых для формирования электродов, но в одном варианте реализации на лист полиэтилентерефталата (ПЭТ), наполненный сульфатом бария, напыляют золото методом ионного распыления. Лист ПЭТ также может быть наполнен диоксидом титана. Другой неограничивающий пример формирования электрода раскрыт в патенте США №6521110 авторов Ходжеса и др., озаглавленном "Электрохимическая ячейка", с датой подачи 10 ноября 2000 г., содержимое которого целиком включено сюда по ссылке.
Аналогично, жидкие реагенты 130, 132 могут иметь ряд различных составов. В одном варианте реализации первый жидкий реагент 130 включает антитело, сопряженное с ферментом, такое как GDH-PQQ, в буферном растворе, содержащем сахарозу, а также полоксамер, такой как блок-сополимеры Pluronics®, антикоагулянт, такой как цитраконат, и ионы кальция. В одном варианте реализации второй жидкий реагент 132 включает смесь феррицианида, глюкозы и второго медиатора, такого как феназинэтосульфат, в кислом буферном растворе, таком как разбавленный раствор цитраконовой кислоты. Первый и второй жидкие реагенты 130, 132 могут быть высушены на первом электроде 112. Ряд методик можно использовать для сушки реагентов 130, 132, но в одном варианте реализации после нанесения полосок реагентов 130, 132 на первый электрод 112 в отношении реагентов 130, 132 могут быть использованы одна и более инфракрасных (ИК) сушилок. Можно также использовать одну и более воздушных сушилок, например, после ИК-сушилок. Ссылки на первый реагент и первый жидкий реагент и второй реагент и второй жидкий реагент в настоящем документе взаимозаменяемы и необязательно являются указанием на то, что реагенты находятся в их жидкой или сухой форме в данное время в данном конкретном варианте реализации. Далее, некоторые из компонентов, ассоциированных с первым и вторым жидкими реагентами, можно использовать взаимозаменяемо и/или в обоих, первом и втором, жидких реагентах, по желанию. В качестве неограничивающего примера, антикоагулянт можно ассоциировать с любым из первого жидкого реагента 130 и второго жидкого реагента 132 или ими обоими.
На напыленном золоте между реагентами 130, 132 можно сформировать линию так, что край реагента 132 находится очень близко к линии или соприкасается с ней. Линию можно нанести путем лазерного выжигания или при помощи металлического острия. В одном примерном варианте реализации линию можно сформировать до того, как полоски реагентов 130, 132 нанесены на электрод. Линия может быть предназначена для электрической изоляции области первого электрода 112 под камерой детектирования от области, которая будет под реакционной камерой. Это может обеспечить лучшее определение площади рабочего электрода во время электрохимического анализа.
Иммуносенсор 110 также может включать в себя второй электрод 114 с одним или более магнитными бусинками 134, содержащими поверхностно-связанные на них антигены. Антигены можно подобрать так, чтобы они реагировали с антителом, расположенным на первом электроде 112, и образцом внутри реакционной камеры 118, как подробно описано далее. Специалист согласится, что компоненты, расположенные на первом электроде 112 и на втором электроде 114, могут быть взаимозаменяемыми. Таким образом, первый электрод 112 может включать один и более магнитных бусинок 134, а второй электрод 114 может включать две нанесенные на него полоски жидких реагентов 130, 132. Далее, хотя в описанном варианте реализации длина электрода 112 соответствует всей длине всего тела иммуносенсора 110, в других вариантах реализации электрод может представлять собой только часть слоя иммуносенсора, которая служит первым или вторым электродами, или же множественные электроды могут быть расположены на одном слое иммуносенсора. Кроме того, поскольку приложенное к иммуносенсору напряжение можно поменять на обратное или сделать переменным, каждый из первого и второго электродов может на разных стадиях служить и рабочим электродом, и противоэлектродом или противоэлектродом сравнения. Для простоты описания в настоящей заявке первый электрод рассматривается как рабочий электрод, а второй электрод - как противоэлектрод или противоэлектрод сравнения.
Сепаратор 116, расположенный между первым и вторым электродами 112, 114, может иметь множество различных форм и размеров, но обычно он сконфигурирован так, чтобы желательным образом соприкасаться с первым и вторым электродами 112, 114, образуя иммуносенсор 110. В одном примерном варианте реализации сепаратор 116 содержит клей на обеих сторонах. Сепаратор 116 может дополнительно включать антиадгезионный материал с каждой из двух сторон сепаратора 116. Сепаратор 116 может быть вырезан таким образом, что образует по меньшей мере две полости. Первая полость может быть образована так, чтобы служить реакционной камерой 118, а вторая полость - камерой 120 детектирования. В одном варианте реализации сепаратор 116 может быть надсечен так, чтобы реакционная камера 118 была совмещена с электродами 112, 114, позволяя проходить в ней реакции антиген-антитело, а камера 120 детектирования была совмещена с электродами 112, 114, обеспечивая возможность электрохимического определения в ней ферроцианида.
В одном варианте реализации сепаратор 116 можно поместить на первый электрод 112 таким образом, который позволяет магнитным бусинкам 134 второго электрода 114 и первому реагенту 130 первого электрода 112 быть по меньшей мере частично расположенными в реакционной камере 118, а сочетанию феррицианид-глюкоза второг