Профилактическое или терапевтическое лекарственное средство для лечения запора
Иллюстрации
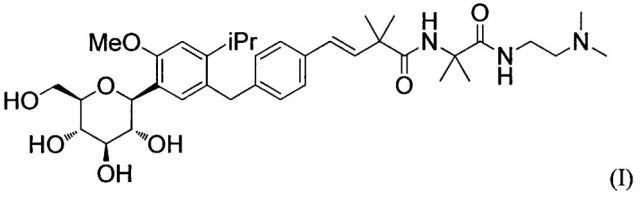
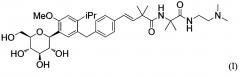
Показать всеИзобретение относится к медицине. Предложено терапевтическое или профилактическое лекарственное средство для профилактики и/или лечения запоров, включающее ингибитор SGLT1 4-изопропилфенилглюцитол формулы (I) или его фармацевтически приемлемые соли в качестве активного ингредиента. Технический результат: средство является химически стабильным и не подвергается метаболизму в среде пищеварительного тракта, включая желудок, до тонкой кишки, быстро оказывает свой эффект в достаточно небольших количествах; оказывает свое действие, подвергаясь небольшой абсорбции in vivo из тонкой кишки, проявляет меньше побочных эффектов даже при использовании в больших, чем эффективные, количествах. 1 з.п. ф-лы, 4 ил., 1 табл., 4 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к профилактическому или терапевтическому лекарственному средству для лечения запора и, точнее, к профилактическому или терапевтическому лекарственному средству для лечения запора, включающему в качестве активного ингредиента соединение, которое ингибирует натрий-зависимый глюкозный котранспортер 1 (далее называемый как SGLT1).
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Запор относится к состояниям, когда количество дефекаций и количество стула снижается настолько, что процесс дефекации вызывает боль или затруднения. За счет изменения пищевых привычек, недостаточной физической нагрузки, ограниченной по времени и стрессовой социальной жизни и увеличения популяции пожилых частота запоров предсказуемо увеличивается.
В обычных условиях пища, поступающая в полость рта, переваривается и абсорбируется, оставляя непереваренными отходы в виде содержимого кишечника, которые затем продвигаются из тонкой в толстую кишку. В толстой кишке отходы отвердевают, так как вода абсорбируется, и в процессе перистальтического движения в направлении ануса они достигают сигмовидной кишки, где хранятся в виде стула. Когда стул проталкивается в прямую кишку посредством сократительного движения, называемого форсируемой перистальтикой, стенки прямой кишки растягиваются, вызывая стимуляцию, которая передается в центр дефекации в спинном мозге и развивается дефекационный рефлекс, вызывая расслабление мышцы анального сфинктера и сокращение прямой кишки. Одновременно мозжечок распознает необходимость пропускать фекалии и произвольно повышается внутрибрюшное давление, стимулируя начало дефекации. Составляющие запора, по сообщениям, включают сниженную автономную иннервацию, функции двигательного или дефекационного рефлекса в нижнем отделе пищеварительного тракта, избыточную абсорбцию воды в кишечнике, сниженную секрецию пищеварительных соков и др.
Основные известные случаи запоров включают, например, функциональные запоры, органические запоры, симптоматические запоры и запоры, индуцированные лекарственными средствами. Известно, что функциональные запоры включают, например, транзиторные простые запоры, атонические запоры из-за снижения перистальтики толстой кишки, спазматические запоры из-за повышенного тонуса ободочной кишки, опосредованного автономными нервами, и ректальный запор из-за слабого рефлекса дефекации при появлении стула в прямой кишке. Органические запоры вызваны обструкцией или сокращением кишечного тракта из-за предсуществующих заболеваний в пределах или в окружении кишечного тракта. Симптоматические запоры являются частью симптомов предсуществующих заболеваний, таких как метаболические, эндокринные, неврологические и миопатические заболевания. Лекарственные препараты, известные как вызывающие запоры, индуцированные лекарственными средствами, включают психотропные или антидепрессантные средства, обладающие антихолинергической активностью, наркотики, такие как морфин, и алкалоиды винка, в качестве противораковых средств.
Запор также развивается в результате патологической перистальтики кишечника при синдроме раздраженной кишки, который включает дискомфорт в брюшной полости или боль, которые облегчаются или исчезают при дефекации. Пожилые люди часто жалуются на запор, ассоциированный с физиологическими изменениями из-за старения кишечного тракта. Запор наиболее часто встречается у женщин, чем у мужчин, так как, с одной стороны, они имеют свои собственные физические характеристики, такие как слабые мышцы брюшной стенки, и, с другой стороны, они подвержены гормональным изменениям в течение менструального цикла. Беременные женщины также жалуются на запоры из-за гормональных изменений и различных других эффектов, включая компрессию кишечника, сниженную подвижность диафрагмы и ослабление мышц брюшной стенки. Запор также развивается как соматический симптом психических заболеваний, таких как депрессия и тревожный невроз (Непатентные документы 1 и 2).
Лекарственные препараты для лечения запоров включают: осмотические слабительные, классифицируемые как солевые слабительные, такие как оксид магния, или сахаридные слабительные, такие как D-сорбит; слабительные, увеличивающие объем кишечного содержимого, такие как поликарбофил кальция; стимулирующие слабительные, такие как производные сенны; и инфильтрирующие слабительные, такие как сульфосукцинат диоктилнатрия. Также используют агонисты рецепторов 4 5-гидрокситриптамина (5-НТ4), такие как прукалоприд и агонисты хлоридных каналов 2 типа (ClC-2), такие как лубипростон. Глицерин является одним из лекарственных препаратов, используемых в качестве клизм.
Медицинская терапия запоров начинается с применения солевых слабительных или слабительных, увеличивающих объем кишечного содержимого. Солевое слабительное оксид магния требует предосторожностей относительно гипермагниемии, особенно когда его используют в пожилом возрасте или у пациентов с заболеваниями почек. Слабительное, увеличивающее объем кишечного содержимого, поликарбофил кальция обладает мягким действием, развивающимся постепенно. Если такие лекарственные препараты оказываются неэффективными, используют стимулирующие слабительные. Стимулирующие слабительные действуют на нервные сплетения в толстом кишечнике, усиливая перистальтику, но при длительном применении они вызывают привыкание, вызывая атрофию нервного сплетения, усиливая расслабление толстой кишки. Применение стимулирующих слабительных ограничено наименьшим возможным количеством и самым коротким возможным периодом. Следовательно, для многих пациентов окажутся полезными лекарственные препараты для лечения запоров, которые является более безопасными и более эффективными с менее выраженными побочными эффектами, которые будучи мягкими по действию, достаточно быстро оказывают эффект. В качестве дополнительной проблемы стимулирующие слабительные обладают эффектом раздражения слизистой оболочки, так что при растворении в желудке или разрушении желудочной кислотой слизистая оболочка желудка раздражается, вызывая различные побочные эффекты, такие как выраженная боль в желудке, тошнота и рвота; следовательно, рекомендуется использовать стимулирующие слабительные в виде суппозиториев. Следовательно, желательно, чтобы даже при пероральном приеме, который является удобным и наиболее желательным, лекарственные препараты предпочтительно не имели побочных эффектов и чтобы активный ингредиент оставался химически стабильным и не подвергался метаболизму при прохождении через сильно кислое окружение желудка и затем через нейтральный кишечник до того, как он окажет свое действие в целевом участке кишечника.
В настоящее время натрий-зависимый котранспортер глюкозы 1 (SGLT1) представляет собой котранспортер натрия, который преимущественно обнаруживается в эпителиальных клетках тонкой кишки и который отвечает за абсорбцию глюкозы и галактозы, которые образуются в результате переваривания углеводов, содержащихся в пище. Так как соединения, которые ингибируют SGLT1, существующий в тонкой кишке, подавляют абсорбцию сахаридов, они расцениваются как применимые в качестве сахароснижающих лекарственных средств, лекарственных средств для лечения сахарного диабета или лекарственных средств для лечения ожирения, и предпринимались попытки разработки указанных фармацевтических препаратов. Представленные таким образом соединения, способные подавлять SGLT1, включают DSP-3235 (KGA-2727 или GSK1614235) (патентный документ 1), SAR474832 (непатентный документ 3) и LX4211 (патентный документ 2), а также несколько других соединений (патентные документы 3 и 4). Однако ни одно из этих соединений, ингибирующих SGLT1, не известно как эффективное в профилактике или лечении запоров.
СПИСОК ССЫЛОК
ПАТЕНТНАЯ ЛИТЕРАТУРА
Патентный документ 1: Международная публикация WO2004/018491
Патентный документ 2: Международная публикация WO2008/042688
Патентный документ 3: Международная публикация WO2010/095768
Патентный документ 4: Международная публикация WO2012/023598
НЕПАТЕНТНАЯ ЛИТЕРАТУРА
Непатентный документ 1: medicina, 2012, 49(2), 199-202
Непатентный документ 2: Supplementary volume of Nippon Rinsho, New Syndrome by Area Series, No. 12, “Shoukakan Shoukougun (Digestive tract syndrome) (vol. 2 in two volumes)”, 2009, 422-427.
Непатентный документ 3: 49th Annu. Meet. Soc. Toxicol. (March 7-11, Salt Lake City) 2010, Abst 2100
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКИЕ ПРОБЛЕМЫ
Задачей настоящего изобретения является предоставление нового лекарственного средства, применимого в профилактике или лечении запоров.
Другой задачей настоящего изобретения является предоставление лекарственного средства для лечения запоров, которое является более безопасным и более эффективным с меньшим количеством побочных эффектов, обладая мягким действием, может быстро оказывать эффект.
Еще одной задачей настоящего изобретения является предоставление лекарственного средства для лечения запоров, которое даже при пероральном введении не имеет проблем побочных эффектов и в котором активный ингредиент остается химически стабильным и не подвергается метаболизму при прохождении через сильно кислую среду желудка и затем через нейтральную среду кишечника до того, как он оказывает свой эффект в целевом участке кишечника.
РЕШЕНИЕ ПРОБЛЕМЫ
Авторы настоящего изобретения провели обширные исследования в свете решения вышеупомянутых задач и в результате обнаружили, что соединения, ингибирующие SGLT1, в частности соединение 4-изопропилфенилглюцитола, представленное следующей формулой (I), обладает превосходным действием в отношении облегчения запоров. Авторы настоящего изобретения также обнаружили, что соединение 4-изопропилфенилглюцитола, представленное следующей формулой (I), является химически стабильным и не подвергается метаболизму в среде пищеварительного тракта, включая желудок, до тонкой кишки, быстро оказывая свой эффект в достаточно небольших количествах; авторы изобретения дополнительно обнаружили, что, так как соединение по формуле (I) оказывает свое действие, подвергаясь небольшой абсорбции in vivo из тонкой кишки, оно проявляет меньше побочных эффектов даже при использовании в больших, чем эффективные, количествах.
Следовательно, настоящее изобретение предоставляет:
(1) Профилактическое или терапевтическое лекарственное средство для лечения запора, включающее соединение, ингибирующее SGLT1, или его фармацевтически приемлемую соль в качестве активного ингредиента.
(2) Профилактическое или терапевтическое лекарственное средство для лечения запора по (1), где соединение, ингибирующее SGLT1, представляет собой соединение 4-изопропилфенилглюцитола, представленное следующей формулой (I):
[Формула I]
ПРЕИМУЩЕСТВЕННЫЕ ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
Настоящее изобретение позволяет предоставить лучшее профилактическое или терапевтическое лекарственное средство для лечения запоров, которое включает в качестве активного ингредиента соединение, ингибирующее SGLT1. Соединение 4-изопропилфенилглюцитола, представленное формулой (I), может предоставить лекарственное средство для лечения запора, которое является безопасным и более эффективным с меньшим количеством побочных эффектов, так как оно обладает мягким действием и все еще быстрым началом действия. Кроме того, соединение 4-изопропилфенилглюцитола, представленное формулой (I), даже при пероральном введении не имеет побочных эффектов и активный ингредиент остается химически стабильным и не подвергается метаболизму при прохождении через сильно кислое содержимое желудка и затем через нейтральную среду кишечника, до того пока он не проявит свое действие в целевом участке кишечника.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 представляет собой диаграмму, иллюстрирующую, насколько хорошо облегчается запор у крыс в качестве модели запора (увеличивается влажная масса стула) в результате введения соединения, представленного формулой (I).
Фиг. 2 представляет собой диаграмму, иллюстрирующую, насколько хорошо облегчается запор у крыс в качестве модели запора (увеличивается содержание влаги стула) в результате введения соединения, представленного формулой (I).
Фиг. 3 представляет собой диаграмму, иллюстрирующую, насколько хорошо облегчается запор у крыс в качестве модели запора (увеличивается влажная масса стула) в результате введения соединения, представленного формулой (I).
Фиг. 4 представляет собой диаграмму, иллюстрирующую, насколько хорошо облегчается запор у крыс в качестве модели запора (увеличивается содержание влаги стула) в результате введения соединения, представленного формулой (I).
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
На следующих страницах настоящее изобретение описано подробно с объяснением значений символов, терминов и подобного, которые используют в спецификации настоящей заявки, но необходимо понимать, что настоящее изобретение никак не ограничивается моделями, проиллюстрированными ниже.
Термин «профилактическое или терапевтическое лекарственное средство для лечения запоров», как используется в настоящем описании, относится к фармацевтическому препарату для облегчения запоров, который используют для обеспечения дефекации или перистальтики кишечника.
Термин «запор», как используется в настоящем описании, относится к симптомам, когда количество дефекаций и количество стула снижается настолько, что процесс дефекации вызывает боль или затруднения; запор включает множество случаев, которые манифестируют или остро, или хронически, такие как функциональные, симптоматические и индуцированные лекарственными средствами запоры. Также включают, например, запоры при синдроме раздраженной толстой кишки, запоры, ассоциированные с физиологическими изменениями в пожилом возрасте из-за старения кишечного тракта, запоры у женщин из-за, например, гормональных изменений во время менструального цикла, запоры у беременных женщин и запоры как соматический симптом психических заболеваний, таких как депрессия или тревожный невроз. В определенных случаях дефекация имеет место, но наблюдается ощущение неполной дефекации (стул не полностью проходит) или дискомфорт (например, вздутие); даже такие состояния включают в термин «запор». Кроме того, применение «профилактического или терапевтического лекарственного средства для лечения запоров» в соответствии с настоящим изобретением не ограничено профилактикой или лечением различных случаев запоров, упомянутых выше, и они также могут быть использованы в качестве фармацевтических препаратов, обеспечивающих дефекацию, для различных целей, например, опустошения кишечного тракта во время обследований пищеварительного тракта или и до и после операций на брюшной полости, помощи в дефекации после операции или обеспечения дефекации после введения контрастного вещества. Применение также может быть возможно в качестве лекарственного препарата для опустошения пищеварительного тракта от вредных материалов, таких как неперевариваемые вещества или токсические вещества. Дополнительно применение также возможно в качестве лекарственных препаратов для обеспечения дефекации в таких случаях, которые имеется риск гипертензии, инсульта головного мозга, инфаркта головного мозга, инфаркта миокарда и др.
«Соединения, ингибирующие SGLT1», указанные в настоящем описании, могут быть проиллюстрированы следующими соединениями:
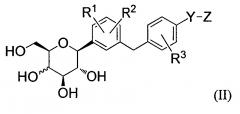
(i) Соединения С-фенилглюцитола, представленные следующей общей формулой (II), которые описаны в международной публикации WO2007/136116
[Формула 2]
где определения заместителей R1, R2, R3, Y и Z в формуле (II) соответствуют содержанию Международной публикации WO2007/136116;
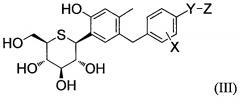
(ii) Соединения С-фенил 1-тиоглюцитола, представленные следующей общей формулой (III), которые описаны в Международной публикации WO2008/001864
[Формула 3]
где определения заместителей Х, Y и Z в формуле (III) соответствуют содержанию Международной публикации WO2008/001864;
(iii) соединения 1-фенил 1-тио-D-глюцитола, перечисленные ниже, которые описаны в Международной публикации WO2008/072726:
(1S)-1,5-ангидро-1-[4-метил-5-(4-метилбензил)-2-гидроксифенил]-1-тио-D-глюцитол;
(1S)-1,5-ангидро-1-[5-(4-метоксибензил)-4-метил-2-гидроксифенил]-1-тио-D-глюцитол;
(1S)-1,5-ангидро-1-[5-(4-этилбензил)-2-гидрокси-4-метилфенил]-1-тио-D-глюцитол;
(1S)-1,5-ангидро-1-[2-гидрокси-4-метил-5-[4-(метилсульфанил)бензил]фенил]-1-тио-D-глюцитол;
(1S)-1,5-ангидро-1-[4-хлор-2-гидрокси-5-(4-метилбензил)фенил]-1-тио-D-глюцитол;
(1S)-1,5-ангидро-1-[4-хлор-2-гидрокси-5-(4-этилбензил)фенил]-1-тио-D-глюцитол; и
(1S)-1,5-ангидро-1-[4-хлор-2-гидрокси-5-(4-метоксибензил)фенил]-1-тио-D-глюцитол.
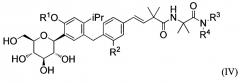
(iv) соединения 4-изопропилфенилглюцитола, представленные следующей общей формулой (IV), которые описаны в Международной публикации WO2010/095768
[Формула 4]
где определения заместителей R1, R2, R3, и R4 в формуле (IV) соответствуют содержанию Международной публикации WO2010/095768, и специфически,
R1 представляет собой атом водорода или С1-4 алкильную группу,
R2 представляет собой атом водорода или метильную группу,
R3 представляет собой С1-4 алкильную группу, замещенную аминогруппой, или С1-4 алкиламиногруппу, или пиперидиловую группу,
R4 представляет собой атом водорода или R3 и R4 вместе с соседним атомом азота образуют пиперидиногруппу или пиперазиниловую группу, которая может быть замещена С1-4 алкильной группой или диметиламиногруппой.
Соединения, представленные следующей общей формулой (IV), более точно проиллюстрированы следующим:
[Формула 5]
Обратите внимание, что соединение, представленное следующей формулой (I), представляет собой одно из соединений, представленных вышеуказанной общей формулой (IV):
[Формула 6]
(v) (Е)-N-(1-амино-2-метил-1-оксопропан-2-ил)-4-(4-(2-изопропил-4-метокси-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2Н-пиран-2-ил)бензил)-3-метилфенил)-2,2-диметилбут-3-енамид, который описан в Международной публикации WO2012/023600
[Формула 7]
(iv) соединения 4-изопропилфенилглюцитола, представленные следующей общей формулой (V), которая описана в Международной публикации WO2012/023582
[Формула 8]
где определения заместителей R1, R2, R3, R4, R5, R6, R7, W, Y и n в формуле (V) соответствуют содержанию Международной публикации WO2012/023582;
(vii) соединения пиразола, представленные следующей общей формулой (VI), которые описаны в Международной публикации WO2004/014932
[Формула 9]
где определения заместителей R1, R2, R3, R4, R5, R6, R7, Q, T, X, Y и Z в формуле (VI) соответствуют содержанию Международной публикации WO2004/014932;
(viii) соединения пиразола, представленные следующей общей формулой (VII), которые описаны в Международной публикации WO2004/018491
[Формула 10]
где определения заместителей R1, R2, R3, R4, R5, R6, Q, T, X, Y и Z в формуле (VII) соответствуют содержанию Международной публикации WO2004/018491;
(ix) соединения пиразола, представленные следующей формулой (VIII), которые описаны в Международной публикации WO2004/019958.
[Формула 11]
где определения заместителей R1, R2, R3, R4, R5, R6, Q и T в формуле (VIII) соответствуют содержанию Международной публикации WO2004/019958;
(х) 3-(3-{4-[3-(β-D-глюкопиранозилокси)-5-изопропил-1Н-пиразол-4-илметил]-3-метилфенокси}пропиламино)-2,2-диметилпропионамид, как описано в Международной публикации WO2009/084531 и Международной публикации WO2009/128421;
(ix) 5-гидрокси-3-метил-2-{4-[3-(3-пиридилметил)уреидо]бензил}фенил β-D-глюкопиранозид и 3-(β-D-глюкопиранозилокси)-4-{[4-(2-гуанидиноэтокси)-2-метилфенил]метил}-5-изопропил-1Н-пиразол, который описан в Международной публикации WO2004/050122;
(xii) соединения бензилфенилглюкопиранозида, представленные следующей общей формулой (IX), которые описаны в Международной публикации WO2008/016132.
[Формула 12]
где определения заместителей R1, R2, R3, R4, R5, R6, R8, R9, X и n в формуле (IX) соответствуют содержанию Международной публикации WO2008/016132;
(xiii) соединения фторглюкозида, представленные следующей общей формулой (X), которые описаны в Международной публикации WO2005/121161.
[Формула 13]
где определения заместителей R1, R2, R3, R4, R5, R6, R8, R9, A, B, X, L, Y, Cyc1 и Cyc2 в формуле (Х) соответствуют содержанию Международной публикации WO2005/121161;
(xiv) соединения, представленные следующей общей формулой (XI), которые описаны в Международной публикации WO2008/042688.
[Формула 14]
где определения заместителей R1, R2, R2В, R2С, A и X в формуле (ХI) соответствуют содержанию Международной публикации WO2008/042688.
«Соединения, ингибирующие SGLT1», могут образовывать фармацевтически приемлемые соли, а также множество сольватов, включая гидраты. Соединение по формуле (I) может принимать кристаллическую форму, которая описана в WO2012/023598.
«Соли», как указано в настоящем описании, никак не ограничиваются, пока они способны образовывать фармацевтически приемлемые соли с соединениями, ингибирующими SGLT1, и примеры включают: аддитивные соли кислот, включая соли минеральных кислот, такие как гидрохлорид, гидробромид, гидройодид, фосфат, сульфат и нитрат, соли сульфоновой кислоты, такие как метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат и трифторметансульфонат, и соли органических кислот, такие как оксалат, тартрат, цитрат, малеат, сукцинат, ацетат, бензоат, манделат, аскорбат, лактат, глюконат, малат, фумарат и моносебакат; соли аминокислот, такие как соль глицина, соль лизина, соль аргинина, соль орнитина, глютамат и аспартат; неорганические соли, такие как соль лития, соль натрия, соль калия, соль кальция и соль магния; и соли с органическими основаниями, такие как соль аммония, соль триэтиламина, соль диизопропиламина и соль циклогексиламина. Необходимо отметить, что соли включают водные соли.
«Соединения, ингибирующие SGLT1», как указано в настоящем описании, могут иметь центр асимметрии, и в таком случае появляется множество оптических изомеров. Следовательно, соединения по настоящему изобретению способны существовать в виде отдельных оптически активных (R) и (S) форм; альтернативно, они могут существовать в виде рацемата или (RS) смеси. В случае соединений, имеющих два или более центров асимметрии, также доступны дополнительные формы - диастереомеры из-за оптического изомеризма из каждого центра асимметрии. Соединения по настоящему изобретению даже охватывают таковые, которые содержат все указанные формы в желаемых пропорциях. Диастереомеры могут быть разделены методами, хорошо известными специалисту в области техники, например фракционирующей кристаллизацией, и оптически активные формы могут быть получены методиками в органической химии, которые хорошо известны для этих целей. Кроме того, соединения по настоящему изобретению могут иногда существовать в виде геометрических изомеров, включая цис- и транс-формы. Соединения по настоящему изобретению охватывают такие изомеры в виде форм, содержащих такие изомеры в желаемых пропорциях.
Ингибирующая активность в отношении SGLT1 соединений, ингибирующих SGLT1, может быть измерена известными методами.
Следовательно, любой специалист, обладающий обычными навыками в области техники, к которой принадлежит настоящее изобретение, может использовать такие известные методы для оценки любого соединения в отношении его ингибирующей активности на SGLT1 и идентифицировать соединения, которые способны ингибировать SGLT1.
Далее описан тестовый пример, показывающий, что соединения, ингибирующие SGLT1, по настоящему изобретению являются применимыми в качестве фармацевтических композиций для облегчения запоров (тест 1). Соединением, используемым в тестовом примере, является таковое, представленное вышеупомянутой формулой (I) ((1S)-1,5-ангидро-1-[5-(4-{(1Е)-4-[(1-{[2-(диметиламино)этил]амино}-2-метил-1-оксопропан-2-ил)амино]-3,3-диметил-4-оксобут-1-ен-1-ил}бензил)-2-метокси-4-(проан-2-ил)фенил]-D-глюцитол).
Соединение (I) уже описано в примере 15-2 Международной публикации WO2010/095768 и может быть получено методом, описанным в указанном документе. Кроме того, кристалл указанного соединения может быть получен методом, описанным в Международной публикации WO2012/023598.
Соединение (I) также может быть получено методом, позднее описанным в Справочных примерах.
До настоящего времени соединения, описанные под номерами (i)-(xiv) выше, или их фармацевтически приемлемые соли известны как соединения, ингибирующие SGLT1. Как уже упомянуто выше, эффект ингибирования SGLT1 таких известных соединений может быть подтвержден известными методиками.
И соединения с подтвержденным эффектом ингибирования SGLT1 или их фармацевтически приемлемые соли являются применимыми в качестве активного ингредиента фармацевтических композиций для облегчения запоров по настоящему изобретению.
«Соединение, ингибирующие SGLT1», предпочтительно проиллюстрировано соединениями 4-изопропилфенилглюцитола, описанными под номерами (iv)-(v) выше, или их фармацевтически приемлемыми солями.
Особенно предпочтительным является следующее соединение, представленное формулой (I): (1S)-1,5-ангидро-1-[5-(4-{(1Е)-4-[(1-{[2-(диметиламино)этил]амино}-2-метил-1-оксопропан-2-ил)амино]-3,3-диметил-4-оксобут-1-ен-1-ил}бензил)-2-метокси-4-(пропан-2-ил)фенил]-D-глюцитол.
Профилактическое или лечебное лекарственное средство для лечения запоров по настоящему изобретению может быть получено различными методами, например методами, описанными в вышеуказанных документах.
Профилактическое или лечебное лекарственное средство для лечения запоров по настоящему изобретению можно вводить или перорально, или парентерально. Предпочтительным методом введения является пероральный путь.
Профилактическое или терапевтическое лекарственное средство для лечения запоров по настоящему изобретению может быть получено из вышеупомянутых соединений, ингибирующих SGLT1, или их фармацевтически приемлемых солей и известных носителей, разбавителей или других соответствующих добавок, которые рецептируют вместе в подходящие формы фармацевтической композиции. Специфически при использовании в качестве пероральных агентов они могут быть таблетками, присыпкой, порошками, гранулами, жидкостями/растворами, капсулами, сухими сиропами, желе и др.
Профилактическое или лечебное лекарственное средство для лечения запоров по настоящему изобретению может быть рецептировано обычно используемыми методами. Предпочтительные лекарственные формы включают таблетки, порошки, измельченные гранулы, гранулы, покрытые оболочкой таблетки, капсулы, сиропы, пастилки, ингаляторы и др.
Профилактические или лечебные лекарственные средства для лечения запоров по настоящему изобретению, когда их необходимо получать в форме перорального агента, могут быть смешаны с другими известными добавками, в качественном или количественном диапазоне, который не влияет на предусматриваемые эффекты настоящего изобретения, что проиллюстрировано витаминами, аминокислотами, сырыми лекарственными средствами, натуральными веществами, вспомогательными веществами, регуляторами рН, охлаждающими веществами, суспендирующими веществами, вязкими веществами, усилителями растворения, дезинтегрирующими веществами, вяжущими веществами, смазывающими веществами, антиоксидантами, средствами для покрытия оболочкой, красителями, ароматизаторами, поверхностно-активными веществами, пластификаторами, отдушками, стабилизаторами и др.
Примерные вспомогательные вещества включают лактозу, крахмал, микрокристаллическую целлюлозу, маннит, мальтозу, гидрофосфат кальция, легкий ангидрид кремния, карбонат кальция и др.; примерные дезинтегрирующие вещества включают крахмал, карбоксиметилцеллюлозу кальция и др.; примерные вяжущие вещества включают крахмал, поливинилпирролидон, гидроксипропилцеллюлозу, этилцеллюлозу, карбоксиметилцеллюлозу, гуммиарабик и др.; примерные смазывающие вещества включают стеарат магния, тальк, отвержденный жир и др.; и примерные стабилизаторы включают лактозу, маннит, мальтозу, полисорбаты, макроголы, полиоксиэтиленовое отвержденное касторовое масло и др.
Дозировка профилактического или терапевтического лекарственного средства для лечения запоров по настоящему изобретению варьируется в зависимости от пациента, получающего лечение, пути введения, заболевания, которое лечат, симптомов заболевания и др., но в случае перорального введения взрослым пациентам, страдающим от запоров, обычная разовая дозировка варьируется от 0,1 мг до 1000 мг, предпочтительно от 1 мг до 200 мг в отношении активного ингредиента; такое количество желательно вводят от одного до трех раз в сутки, предпочтительно до или после еды.
В соответствии с настоящим изобретением могут быть предоставлены новые лекарственные средства для лечения запоров, которые являются эффективными в облегчении запоров. Профилактические или терапевтические лекарственные средства для лечения запоров по настоящему изобретению являются применимыми в качестве фармацевтических препаратов для профилактики или лечения запора или в качестве фармацевтических препаратов, которые обеспечивают дефекацию. Кроме того, соединения, ингибирующие SGLT1, по настоящему изобретению или их фармацевтически приемлемые соли проявляют более выраженное ингибирующее действие на SGLT1, и они являются применимыми в качестве фармацевтических препаратов для профилактики или лечения запора или в виде фармацевтических препаратов, которые обеспечивают дефекацию. Следовательно, фармацевтические композиции по настоящему изобретению и соединения, ингибирующие SGLT1, в соответствии с настоящим изобретением являются применимыми в качестве профилактических или терапевтических лекарственных средств для различных видов запоров и эффективными в качестве профилактических или терапевтических лекарственных средств для различных видов запоров, которые проявляются или остро или хронически, например функциональных запоров, органических запоров, симптоматических запоров, запоров, индуцированных лекарственными средствами, и др., а также запоров при синдроме раздраженной кишки, запоров, сопровождающих физиологические изменения в пожилом возрасте, вызванные старением кишечного тракта, запоров у женщин вследствие, например, гормональных изменений во время менструального цикла, запоров у беременных женщин и запоров как соматического симптома психических заболеваний, таких как депрессия или тревожный невроз. Кроме того, применение фармацевтических композиций по настоящему изобретению и соединений, ингибирующих SGLT1, по настоящему изобретению не ограничивается профилактикой или лечением различных типов запоров, упомянутых выше, и они также могут быть использованы в качестве фармацевтических препаратов, обеспечивающих дефекацию для различных целей, например опустошения кишечного тракта во время исследований пищеварительного тракта или и до и после операций на брюшной полости, помощи в дефекации после хирургического вмешательства или обеспечении дефекации после введения контрастного вещества. Также существует возможность использования медикаментов для освобождения пищеварительного тракта от вредных веществ, таких как неперевариваемые материалы или токсические вещества. Для лекарственных препаратов также существует дополнительная возможность обеспечения дефекации в случаях повышенного риска гипертонии, церебрального инсульта, церебрального инфаркта, инфаркта миокарда и др.
Далее даны справочные примеры, тестовые примеры и примеры композиций для более точного описания настоящего изобретения, но необходимо понимать, что настоящее изобретение не ограничивается настоящими примерами.
Следующими справочными примерами показан способ синтеза соединения (I).
Соединение (I) может быть получено в соответствии со схемой I, показанной ниже.
Схема 1: Получение соединения (I)
[Формула 15]
(В схеме МОМ обозначает метоксиметил и TMS триметилсилил.)
Справочный пример 1
Получение соединения (I)
Стадия 1: Получение соединения 3
К раствору соединения 1 (95,0 г, 281 ммоль) в тетрагидрофуране (1395 мл), раствор гексана н-бутиллития (2,66 М, 111 мл) добавляли по каплям в атмосфере азота при -75 до -72°С в течение 45 минут с последующим перемешиванием при -75 до -72°С в течение 33 минут. Впоследствии раствор соединения 2 (138 г, 295 ммоль) в тетрагидрофуране (400 мл) добавляли по каплям при -78 до -73°С в течение одного часа и 37 минут с последующим перемешиванием при -76 до -73°С в течение 20 минут. Впоследствии триметилсилилхлорид (32,1 г, 295 ммоль) добавляли по каплям при -76 до -73°С в течение 5 минут с последующим перемешиванием при -76 до -73°С в течение одного часа и 15 минут. Впоследствии раствор гексана н-бутиллития (2,66 М, 153 мл) добавляли при -76 до -72°С в течение одного часа и 5 минут с последующим перемешиванием при -76 до -72°С в течение 20 минут. Впоследствии раствор 4-бромбензальдегида (57,2 г, 309 ммоль) в тетрагидрофуране (400 мл) добавляли при -75 до -72°С в течение одного часа и 5 минут с последующим перемешиванием при -75 до -72°С в течение 20 минут. К реакционной смеси добавляли воду (1430 мл) и толуол (1430 мл) для отделения органического слоя и водного слоя. После возгонки органического слоя при пониженном давлении остаток растворяли в метаноле (1378 мл) и к полученному раствору добавляли метансульфоновую кислоту (2,70 мг, 28,1 ммоль) и смесь нагревали в колбе с обратным холодильником в течение одного часа. После охлаждения до 25°С добавляли триэтиламин (5,69 г, 56,2 ммоль). После последующей возгонки при пониженном давлении остаток растворяли в толуоле (634 мл) и полученный раствор промывали водой три раза для разделения на органический и водный слой. К органическому слою добавляли 1 М водный раствор гидроксида натрия (350 мл) и толуола (550 мл) и смесь перемешивали с последующим разделением на органический и водный слой. К водному слою добавляли толуол (250 мл) и смесь перемешивали с последующим разделением на органический и водный слой. К водному слою добавляли 1 М соляную кислоту (400 мл) и толуол (550 мл) и смесь перемешивали с последующим разделением на органический и водный слой. Органический слой промывали 10% водным раствором хлорида натрия (550 мл) с последующим разделением на органический и водный слой. Органический слой возгоняли при пониженном давлении и полученный сырой продукт (111 г) подвергали колоночной хроматографии на силикагеле [последовательно элюируя хлороформом:метанолом = 20:1, 10:1 и 5:1 (об/об)] и фракции большей чистоты концентрировали для получения соединения 3 (1,10 г) в виде светло-желтого аморфного вещества.
1H ЯМР (500 МГц, ДМСО-d6) с контролем TMS (0,00 ч./млн) δ: 0,93 (1,65H, д, J=6,6 Гц), 0,94 (1,35H, д, J=6,6 Гц), 0,97 (3H, д, J=6,6 Гц), 2,99 (1,65H, с), 3,04 (1,35H, с), 3,05 (1H, с, J=6,6 Гц), 3,15 (1H, дд, J=8,9 и 4,0 Гц), 3,25 (1,35H, с), 3,26 (1,65H, с), 3,29-3,38 (1H, м), 3,41-3,47 (1H, м), 3,57-3,60 (1H, м), 3,65-3,72 (2H, м), 4,70-4,78 (1H, м, взаимозаменяемый с D2O), 4,87 (0,55H, д, J=5,5 Гц, взаимозаменяемый с D2O), 4,88 (0,45H, д, J=5,8 Гц, взаимозаменяемый с D2O), 5,03 (0,55H, д, J=5,5 Гц, взаимозаменяемый с D2O), 5,04 (0,45H, д, J=5,5 Гц, взаимозаменяемый с D2O), 5,44 (1H, с), 5,63 (1H, уш.с, взаимозаменяемый с D2