Способ производства твердой дозированной формы
Иллюстрации
Показать всеГруппа изобретений относится к области производства твердых дозированных форм. Способ производства твердой дозированной формы, включает: подачу порошковой смеси, содержащей фармацевтически активный агент, в дозирующую насадку с использованием отрицательного давления, и измерение ее количества; подачу порошковой смеси из дозирующей насадки в формирующую полость внутри блока пресс-формы, причем формирующая полость имеет внутреннюю стенку, первое отверстие на поверхности первой стороны блока пресс-формы, и второе отверстие на поверхности с противоположной стороны блока пресс-формы; перемещение первого формирующего инструмента в формирующую полость через первое отверстие так, что порошковая смесь приобретает форму дозированной формы внутри формирующей полости; приложение РЧ-энергии между первым РЧ-электродом и вторым РЧ-электродом так, что энергия нагревает порошковую смесь внутри формирующей полости с образованием дозированной формы; и извлечение дозированной формы из формирующей полости. Также раскрываются варианты способов производства твердой дозированной формы. Группа изобретений обеспечивает создание многокомпонентной твердой дозированной формы для эффективного лечения таких патологических состояний, как боль, лихорадка, воспаление и т.д. 3 н. и 16 з.п. ф-лы, 22 ил., 8 табл., 5 прим.
Реферат
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА СМЕЖНЫЕ ИЗОБРЕТЕНИЯ
Настоящая заявка истребует приоритет преимуществ по предварительной заявке на патент США с серийным № 61/640910, поданной 1 мая 2012 г., и предварительной заявке на патент США с серийным № 61/704773, поданной 24 сентября 2012 г. Полное описание упомянутой выше смежной заявки на патент США включено в настоящий документ путем ссылки для всех целей.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Фармацевтические таблетки и другие прессованные таблетированные формы в виде кондитерских изделий очень распространены и широко используются в качестве несущих сред для фармацевтических активных веществ или порошков. Они обеспечивают удобное средство прессования относительно большого объема порошков низкой плотности в небольшой компактный формат, который легко обрабатывать, глотать или жевать. На рынке широко представлены различные формы, размеры и конфигурации. Подавляющее большинство данных таблетированных форм производят из сухих смесей прессуемых порошков или гранул, которые затем подают в ротационные машины для прессования таблеток (например, такие как доступные в продаже от компаний Fette America Inc., г. Рокэвей, штат Нью-Джерси, США, или Manesty Machines LTD, г. Ливерпуль, Великобритания). Данные машины для прессования таблеток точно дозируют определенное количество порошка в полость пресс-формы. Затем порошок прессуют с использованием пуансонов, которые, ударяя по порошку, уплотняют его внутри полости пресс-формы. Конечной стадией операции, завершающей производственную последовательность, является выталкивание готовой таблетированной формы из полости пресс-формы. Большинство конструкций таблеток, полученных в результате данного процесса, представляют собой простые однокомпонентные формы, однако иногда данные машины можно модифицировать для изготовления более сложных многослойных таблеток путем добавления множества станций подачи и прессования. Изготовление многослойных таблеток с помощью данного средства представляет собой последовательную и поэтапную процедуру, в которой слои или секции формируют послойно. Для каждого слоя требуется дополнительный дозирующий узел пуансонов и дополнительный узел прессования. Так как данные машины имеют относительно массивную конструкцию вследствие очень высокой интенсивности уплотнения, необходимой для получения составов для надлежащего прессования (довольно распространены машины, которые могут обеспечивать до 89 килоньютон (20000 фунтов силы)), машины для производства многослойных таблеток могут быть очень дорогостоящими и сложными в обслуживании. Дополнительным недостатком изготовления таблеток данным способом являются ограничения геометрии слоев. Области таблетки с ориентацией, перпендикулярной направлению выталкивания таблетки, исключительно сложно изготовить, и это потребовало бы более тщательных и сложных модификаций.
Дополнительный недостаток производства таблеток с помощью последовательности наслоения специфичен для изготовления таблеток для рассасывания в полости рта. Данные таблетки должны иметь низкую плотность и высокую пористость конструкции таблетки, чтобы слюна в полости рта быстро проникала в таблетку, разрушая связи между частицами для создания эффекта быстрого растворения. Подход с наслоением требует, чтобы полость пресс-формы сначала заполнили первым слоем порошкообразного материала, причем поверхность полости пресс-формы должна быть очищена для достижения необходимого объема заполнения. Затем данный первый слой заполнения прессуют с помощью пуансона до управляемой глубины проникновения в полость пресс-формы. Необходимо точное управление данной глубиной проникновения и равномерное уплотнение порошка, чтобы создать управляемый объем для второго заполнения порошкообразного материала. Следующая стадия операции - заполнение данного вновь созданного объема вторым порошком. Затем данный порошок соскабливают на уровне с верхней поверхностью полости пресс-формы, а на конечной стадии происходит уплотнение второго слоя на первом слое во второй раз с помощью пуансона, который давит на оба слоя таблетки. Данное двойное уплотнение раздавливает мелкие воздушные пузырьки между частицами, вызывая негативное воздействие на пористую структуру, желательную для таблетки для рассасывания в полости рта. В фармацевтическом производстве невозможно пропустить данную стадию двойного прессования, поскольку плотный однородный первый слой является необходимым условием для достижения точного дозирования второго слоя порошкообразного лекарственного средства. Точное дозирование лекарственных средств производителями фармацевтической продукции крайне важно для сохранения здоровья и безопасности пациентов.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В одном аспекте настоящее изобретение включает способ производства твердой дозированной формы, включающий следующие стадии: (a) измерение количества первой порошковой смеси внутри дозирующей насадки, причем первая порошковая смесь включает фармацевтически активный агент; (b) подачу измеренного количества первой порошковой смеси из дозирующей насадки в формирующую полость внутри блока пресс-формы, причем формирующая полость имеет внутреннюю стенку, первое отверстие на поверхности одной стороны блока пресс-формы и второе отверстие на поверхности с противоположной стороны блока пресс-формы; (c) перемещение первого формирующего инструмента в формирующую полость через первое отверстие формирующей полости так, что первая порошковая смесь приобретает форму дозированной формы внутри формирующей полости между внутренней стенкой, первым формирующим инструментом и вторым формирующим инструментом, который находится внутри полости или смежен с ней; (d) приложение РЧ-энергии между первым электродом и вторым электродом так, что энергия нагревает первую порошковую смесь внутри формирующей полости с образованием дозированной формы; и (e) извлечение дозированной формы из формирующей полости.
В другом аспекте настоящее изобретение включает способ производства твердой дозированной формы, причем способ включает следующие стадии: (a) измерение количества первой порошковой смеси внутри первой дозирующей насадки, причем первая порошковая смесь включает фармацевтически активный агент; (b) подачу измеренного количества первой порошковой смеси из первой дозирующей насадки в формирующую полость внутри блока пресс-формы, причем формирующая полость имеет внутреннюю стенку, первое отверстие на поверхности одной стороны блока пресс-формы и второе отверстие на поверхности с противоположной стороны блока пресс-формы; (c) измерение количества второй порошковой смеси внутри второй дозирующей насадки; (d) подачу измеренного количества второй порошковой смеси из дозирующей насадки в формирующую полость; (e) перемещение первого формирующего инструмента в формирующую полость через первое отверстие формирующей полости так, что первая порошковая смесь и вторая порошковая смесь приобретают форму дозированной формы внутри формирующей полости между внутренней стенкой, первым формирующим инструментом и вторым формирующим инструментом, который находится внутри полости или смежен с ней; (f) приложение РЧ-энергии между первым электродом и вторым электродом так, что энергия нагревает первую порошковую смесь внутри формирующей полости с образованием дозированной формы; и (g) извлечение дозированной формы из формирующей полости.
В другом аспекте настоящее изобретение включает способ производства твердой дозированной формы, причем способ включает следующие стадии: (a) измерение количества первой порошковой смеси внутри первой дозирующей насадки, причем первая порошковая смесь включает фармацевтически активный агент; (b) подачу измеренного количества первой порошковой смеси из первой дозирующей насадки в формирующую полость внутри блока пресс-формы, причем формирующая полость имеет внутреннюю стенку, первое отверстие на поверхности одной стороны блока пресс-формы и второе отверстие на поверхности с противоположной стороны блока пресс-формы, причем формирующая камера дополнительно включает выполненный с возможностью перемещения разделитель, выполненный с возможностью формирования первой камеры и второй камеры внутри формирующей полости, а первую порошковую смесь подают в первую камеру; (c) измерение количества второй порошковой смеси внутри второй дозирующей насадки; (d) подачу измеренного количества второй порошковой смеси из дозирующей насадки во вторую камеру; (e) извлечение выполненного с возможностью перемещения разделителя из формирующей полости так, что первая порошковая смесь находится в контакте со второй порошковой смесью внутри формирующей полости; (f) перемещение первого формирующего инструмента в формирующую полость через первое отверстие формирующей полости так, что первая порошковая смесь и вторая порошковая смесь приобретают форму дозированной формы внутри формирующей полости между внутренней стенкой, первым формирующим инструментом и вторым формирующим инструментом, который находится внутри полости или смежен с ней; (g) приложение РЧ-энергии между первым электродом и вторым электродом так, что энергия нагревает первую порошковую смесь внутри формирующей полости с образованием дозированной формы; и (h) извлечение дозированной формы из формирующей полости.
Другие особенности и преимущества настоящего изобретения станут очевидны из подробного описания настоящего изобретения и пунктов формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ФИГУР
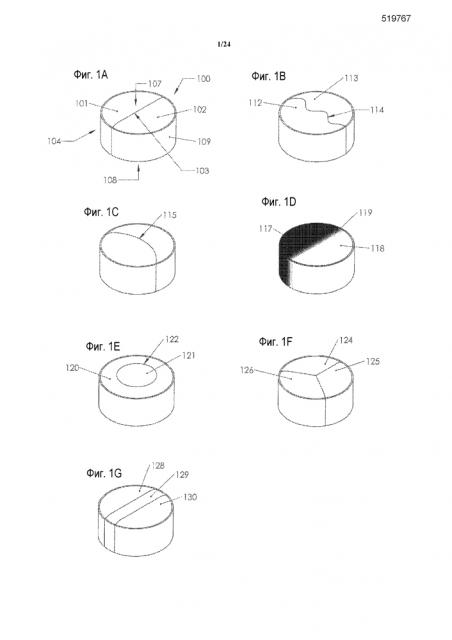
Фиг. 1A-G представляют собой виды в перспективе таблеток со множеством областей.
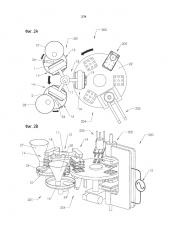
Фиг. 2A представляет собой вид сверху многокомпонентной таблеточной машины 200.
Фиг. 2B представляет собой вид в перспективе многокомпонентной таблеточной машины 200.
Фиг. 3A-3B представляют собой виды в сечении дозирующего модуля 14 над первым лотком для порошка 15.
Фиг. 4A представляет собой вид в сечении дозирующего модуля 14 над первым лотком для порошка 15.
Фиг. 4B-4C представляет собой вид в перспективе дозирующего модуля 14, который перемещается от первого лотка для порошка 15 ко второму лотку для порошка 16.
Фиг. 5A-5B представляют собой виды в сечении дозирующего модуля 14 над вторым лотком для порошка 16.
Фиг. 6A представляет собой вид в сечении дозирующего модуля 14 над вторым лотком для порошка 16.
Фиг. 6B представляет собой вид в перспективе дозирующего модуля 14, который перемещается от второго лотка для порошка 16 в положение над блоком пресс-формы 19.
Фиг. 7A и 7C представляют собой виды в сечении дозирующего модуля 14 над блоком пресс-формы 19.
Фиг. 7B представляет собой вид в перспективе части блока пресс-формы 19, формирующего инструмента 20 и части насадок 3 и 4.
Фиг. 8A-8B представляют собой виды в сечении дозирующего модуля 14 над блоком пресс-формы 19.
Фиг. 9 представляет собой вид в перспективе формирующей станции 202.
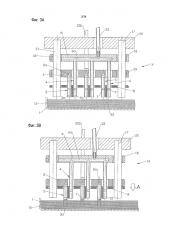
Фиг. 10 представляет собой вид в сечении, на котором показана выполненная с возможностью перемещения электродная пластина 340 и выполненная с возможностью перемещения электродная пластина 341 в открытом положении.
Фиг. 11 представляет собой вид в сечении, на котором показаны выполненная с возможностью перемещения электродная пластина 340 и выполненная с возможностью перемещения электродная пластина 341 в закрытом положении.
Фиг. 12A представляет собой вид в сечении, на котором показаны формирующие инструменты 420 и 421 с накладками 440 и 430, изготовленными из изоляционного от РЧ-энергии материала.
Фиг. 12B и 12C представляют собой виды в сечении станции выталкивания таблеток 203.
Фиг. 13A-C представляют собой виды в перспективе различных вариантов осуществления пластин разделителя.
Фиг. 14A представляет собой вид в перспективе наружной дозирующей насадки 630 и внутренней дозирующей насадки 631.
Фиг. 14B-J представляют собой виды в сечении наружной дозирующей насадки 630 и внутренней дозирующей насадки 631.
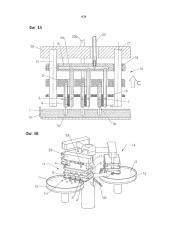
Фиг. 15A представляет собой вид сверху многокомпонентной таблеточной машины 1500.
Фиг. 15B представляет собой вид в перспективе многокомпонентной таблеточной машины 1500.
Фиг. 16A-16B представляют собой виды в сечении дозирующего модуля 714 над первым лотком для порошка 15.
Фиг. 17A представляет собой вид в сечении дозирующего модуля 714 над первым лотком для порошка 15.
Фиг. 17B представляет собой вид в перспективе дозирующего модуля 714, который перемещается от первого лотка для порошка 15 в положение над блоком пресс-формы 19.
Фиг. 18A и 18B представляют собой виды в сечении дозирующего модуля 714 над блоком пресс-формы 19.
Фиг. 19 представляет собой вид в перспективе формирующей станции 202.
Фиг. 20 представляет собой вид в сечении, на котором показаны выполненная с возможностью перемещения электродная пластина 340 и выполненная с возможностью перемещения электродная пластина 341 в открытом положении.
Фиг. 21 представляет собой вид в сечении, на котором показаны выполненная с возможностью перемещения электродная пластина 340 и выполненная с возможностью перемещения электродная пластина 341 в закрытом положении.
Фиг. 22A и 22B представляют собой виды в сечении станции выталкивания таблеток 203.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Предполагается, что специалист в данной области может в полной мере использовать настоящее изобретение на основе представленного в настоящем документе описания. Представленные ниже конкретные варианты осуществления изобретения можно рассматривать лишь в качестве иллюстрирующих, которые никаким образом не ограничивают остальную часть настоящего описания.
Если не указано иное, все используемые в настоящем документе технические и научные термины имеют такие же значения, которые хорошо известны среднему специалисту в области, к которой относится настоящее изобретение. Кроме того, все публикации, заявки на патенты, патенты и другие представленные в настоящем документе ссылки включены в настоящий документ путем ссылки. В настоящем документе все процентные значения, если не указано иное, представлены по весу.
Как описано выше, в одном аспекте настоящее изобретение включает способ производства твердой дозированной формы, причем способ включает следующие стадии: (a) измерение количества первой порошковой смеси внутри дозирующей насадки, причем первая порошковая смесь включает фармацевтически активный агент; (b) подачу измеренного количества первой порошковой смеси из дозирующей насадки в формирующую полость внутри блока пресс-формы, причем формирующая полость имеет внутреннюю стенку, первое отверстие на поверхности одной стороны блока пресс-формы и второе отверстие на поверхности с противоположной стороны блока пресс-формы; (c) перемещение первого формирующего инструмента в формирующую полость через первое отверстие формирующей полости так, что первая порошковая смесь приобретает форму дозированной формы внутри формирующей полости между внутренней стенкой, первым формирующим инструментом и вторым формирующим инструментом, который находится внутри полости или смежен с ней; (d) приложение РЧ-энергии между первым электродом и вторым электродом так, что энергия нагревает первую порошковую смесь внутри формирующей полости с образованием дозированной формы; и (e) извлечение дозированной формы из формирующей полости.
Хотя в конкретных вариантах осуществления, описанных в настоящем документе, основное внимание уделено таблеткам, такую машину и процесс также можно использовать для получения других дозированных форм, таких как пастилки и жевательные резинки.
Порошковая смесь
В одном варианте осуществления таблетку производят путем приложения энергии к порошковой смеси, содержащей по меньшей мере один фармацевтически активный агент (как описано в настоящем документе) и необязательно по меньшей мере один первый материал (как описано в настоящем документе), по меньшей мере один второй материал (как описано в настоящем документе), по меньшей мере одно плавкое связующее вещество (как описано в настоящем документе) и/или другие подходящие эксципиенты.
В одном варианте осуществления порошковая смесь имеет плотность менее приблизительно 0,5 г/см3, такую как менее приблизительно 0,4 г/см3, такую как менее приблизительно 0,3 г/см3. В одном варианте осуществления порошковая смесь по существу свободна от жидкого материала (например, менее 1%, например, менее 0,5%, например, менее 0,01%, например 0%).
В одном варианте осуществления порошковая смесь содержит по меньшей мере один первый материал и по меньшей мере один второй материал. В одном варианте осуществления по меньшей мере один фармацевтически активный агент содержится внутри частиц, таких как частицы с полимерным покрытием. В одном варианте осуществления общее количество таких частиц по меньшей мере одного первого материала и по меньшей мере одного второго материала включает по меньшей мере 90% по весу порошковой смеси/таблетки, например по меньшей мере 95%, например по меньшей мере 98% по весу порошковой смеси/таблетки.
В одном варианте осуществления порошковая смесь/таблетка содержит по меньшей мере 60% по весу по меньшей мере одного первого материала и по меньшей мере одного второго материала, например по меньшей мере 75%, например по меньшей мере 90%. В одном варианте осуществления отношение по меньшей мере одного первого материала к по меньшей мере одному второму материалу составляет от приблизительно 20:80 до приблизительно 70:30, например от приблизительно 25:75 до приблизительно 60:40, например от приблизительно 35:65 до приблизительно 45:55.
Примеры подходящих эксципиентов включают, без ограничений, смазывающие вещества, скользящие вещества, подсластители, вкусоароматические агенты, антиоксиданты, консерванты, улучшители текстуры, красители, а также их смеси. В одной частице порошковой смеси могут присутствовать один или более из вышеописанных ингредиентов.
Примеры подходящих смазывающих веществ включают, без ограничений, длинноцепочечные жирные кислоты и их соли, такие как стеарат магния и стеариновая кислота, тальк, глицеридные воски и их смеси.
Примеры подходящих скользящих веществ включают, без ограничений, коллоидный диоксид кремния.
Примеры подсластителей для настоящего изобретения включают, без ограничений, высокоинтенсивные подсластители, такие как синтетические или природные сахара; искусственные подсластители, такие как сахарин, сахарин натрия, аспартам, ацесульфам, тауматин, глицирризин, сукралоза, дигидрохалькон, алитам, миракулин, монеллин и стевиозид.
Примеры вкусоароматических веществ включают, без ограничений, эфирные масла, включая дистилляты, экстрагированные растворителями или холодным прессованием измельченные цветы, листья, очищенные или перетертые целые плоды, содержащие смеси спиртов, эфиров, альдегидов и лактонов; эссенции, включающие либо разбавленные растворы эфирных масел, либо смеси синтетических химических веществ, смешанных для соответствия природному вкусу плода (например, клубники, малины и черной смородины); искусственные и природные вкусы пива и других алкогольных напитков, например коньяка, виски, рома, джина, хереса, портвейна и вина; табака, кофе, чая, какао и мяты; фруктовых соков, включая выжатый сок из вымытых и очищенных фруктов, таких как лимон, апельсин, лайм; мяты кудрявой, мяты перечной, грушанки, корицы, какао, ванили, лакрицы, ментола, эвкалипта, аниса, орехов (например, арахиса, кокоса, фундука, каштана, грецкого ореха, ореха кола), миндаля, изюма; а также пудра, мука или части растительного материала, включая части растения табака, например рода Nicotiana, в количествах, незначительно повышающих уровень никотина, а также имбирь.
Примеры антиоксидантов включают, без ограничений, токоферолы, аскорбиновую кислоту, пиросульфит натрия, бутилгидрокситолуол, бутилированный гидроксианизол, этилендиаминтетрауксусную кислоту и соли этилендиаминтетрауксусной кислоты, а также их смеси.
Примеры консервантов включают, без ограничений, лимонную кислоту, винную кислоту, молочную кислоту, яблочную кислоту, уксусную кислоту, бензойную кислоту и сорбиновую кислоту, а также их смеси.
Примеры улучшителей текстуры включают, без ограничений, пектин, полиэтиленоксид и каррагинан, а также их смеси. В одном варианте осуществления улучшители текстуры используются в концентрациях от приблизительно 0,1% до приблизительно 10% по весу.
В одном варианте осуществления настоящего изобретения порошковая смесь имеет средний размер частиц менее 500 микрон, например от приблизительно 50 микрон до приблизительно 500 микрон, например от приблизительно 50 микрон до 300 микрон. Частицы в таком диапазоне размеров в особенности пригодны к использованию в процессах прямого уплотнения.
В одном варианте осуществления порошковая смесь по существу свободна от полиэтиленгликолей, гидратированных целлюлозных полимеров, камедей (таких как ксантановая камедь и каррагинаны) и желатинов. В настоящем документе термин «по существу свободен» означает содержание менее 5%, например менее 1%, например менее 0,1%, например полностью свободен (например, 0%). Такая композиция имеет преимущества для поддержания профиля растворения с немедленным высвобождением, что позволяет свести к минимуму затраты на обработку и материал и обеспечить оптимальную физическую и химическую стабильность таблетки.
В одном варианте осуществления порошковая смесь/таблетка по существу свободна от нерастворимых в воде наполнителей для прямого прессования. Нерастворимые в воде наполнители включают, без ограничений, микрокристаллическую целлюлозу, микрокристаллическую целлюлозу для прямого прессования, целлюлозы, нерастворимые в воде целлюлозы, крахмал, кукурузный крахмал и модифицированные крахмалы. Как описано в настоящем варианте осуществления, термин «по существу свободен» означает менее 2 процентов, например, менее 1 процента или полное отсутствие.
В одном варианте осуществления порошковая смесь по существу свободна от суперразрыхлителей. Суперразрыхлители включают кроскармеллозу натрия, крахмалгликолят натрия и поперечносшитый повидон. Композиция, по существу свободная от суперразрыхлителей, имеет преимущество в отношении усиления вкусовых ощущений и стабильности таблетки вследствие снижения гигроскопичности.
В одном варианте осуществления по меньшей мере 90% по весу таблетки составляет материал, имеющий точку плавления более 60°C, например по меньшей мере 70°C, например по меньшей мере 80°C.
Первый материал
Порошковая смесь/таблетка настоящего изобретения включает по меньшей мере один первый материал, который является диэлектрическим водосодержащим материалом, (i) включающим от приблизительно 1 до приблизительно 5 процентов по весу связанной воды, например от приблизительно 1,5 до приблизительно 3,2 процентов по весу связанной воды, например от приблизительно 1,7 до приблизительно 3 процентов по весу связанной воды, и (ii) имеет диэлектрические потери, измеренные при плотности в диапазоне от 0,15 до 0,5 г/см3, от приблизительно 0,05 до приблизительно 0,7, например от приблизительно 0,1 до приблизительно 0,5, например от 0,25 до приблизительно 0,5.
В одном варианте осуществления первый материал представляет собой крахмал. Примеры таких крахмалов включают, без ограничений, гидролизованные крахмалы, такие как мальтодекстрин и сухая кукурузная патока. Такие крахмалы могут быть получены из различных растительных источников, таких как зерно, бобы и клубни, и примеры включают, без ограничений, крахмалы, полученные из кукурузы, пшеницы, риса, гороха, бобов, тапиоки и картофеля.
В одном варианте осуществления насыпная плотность первого материала при добавлении в порошковую смесь составляет менее приблизительно 0,4 г/см3, например менее приблизительно 0,3 г/см3, например менее 0,2 г/см3.
В одном варианте осуществления средний размер частиц первого материала составляет менее 500 микрон, например менее 150 микрон.
Первый (-е) материал (-ы) может (-гут) присутствовать в концентрации по меньшей мере приблизительно 15 процентов по весу таблетки, например по меньшей мере приблизительно 20 процентов, например от приблизительно 20 процентов до приблизительно 45 процентов порошковой смеси/таблетки, например от приблизительно 20 процентов до приблизительно 42 процентов порошковой смеси/таблетки, например от приблизительно 20 процентов до приблизительно 40 процентов порошковой смеси/таблетки
Второй материал
В одном варианте осуществления порошковая смесь/таблетка настоящего изобретения включает по меньшей мере один второй материал, (i) имеющий растворимость в воде от приблизительно 20 до приблизительно 400 г на 100 г воды при 25°C, (ii) имеющий диэлектрические потери, измеренные при плотности в диапазоне от 0,5 до 1,1 г/см3, менее приблизительно 0,05, например менее приблизительно 0,01, например менее 0,005, например приблизительно 0. В одном варианте осуществления второй материал имеет кристаллическую форму при 25°C.
В одном варианте осуществления второй материал представляет собой сахар или его спирт или гидрат. Примеры сахаров включают, без ограничений, моносахариды и дисахариды, такие как сахароза, фруктоза, мальтоза, декстроза, лактоза, а также спирты и их гидраты.
Примеры сахарных спиртов включают, без ограничений, эритрит, изомальт, маннит, мальтит, лактит, сорбит и ксилит.
Второй(-ые) материал(-ы) может(-гут) присутствовать в концентрации от приблизительно 18 процентов до приблизительно 72 процентов порошковой смеси/таблетки, например от приблизительно 20 процентов до приблизительно 64 процентов порошковой смеси/таблетки, например от приблизительно 39 процентов до приблизительно 56 процентов порошковой смеси/таблетки.
Плавкое связующее вещество
В одном варианте осуществления порошковая смесь/таблетка настоящего изобретения включает по меньшей мере одно плавкое связующее вещество. В одном варианте осуществления температура плавления плавкого связующего вещества составляет от приблизительно 40°C до приблизительно 140°C, например от приблизительно 55°C до приблизительно 100°C. Размягчение или плавление плавкого(-их) связующего(-их) веществ(-а) приводит к спеканию таблетированной формы благодаря связыванию размягченного или расплавленного связующего вещества с фармацевтически активным агентом и/или другими ингредиентами внутри уплотненной порошковой смеси.
В одном варианте осуществления плавкое связующее вещество представляет собой связующее вещество, расплавляемое РЧ-излучением. Под связующим веществом, расплавляемым РЧ-излучением, понимается твердое связующее вещество, которое размягчается или плавится под воздействием РЧ-энергии. Связующее вещество, расплавляемое РЧ-излучением, как правило, является полярным и может повторно застывать или затвердевать при охлаждении.
В одном варианте осуществления плавкое связующее вещество представляет собой связующее вещество, не расплавляемое РЧ-излучением. В таком варианте осуществления порошковая смесь содержит эксципиент, который нагревается под воздействием РЧ-энергии (например, полярный эксципиент), так что полученное тепло может размягчить или расплавить плавкое связующее вещество. Примеры таких эксципиентов включают, без ограничений, полярные жидкости, такие как вода и глицерин; порошкообразные металлы и соли металлов, такие как порошкообразное железо, хлорид натрия, гидроксид алюминия и гидроксид магния; стеариновая кислота; и стеарат натрия.
Примеры подходящих плавких связующих веществ включают: жиры, такие как масло какао, гидрогенизированное растительное масло, такое как пальмоядровое масло, хлопковое масло, подсолнечное масло и соевое масло; моно-, ди- и триглицериды; фосфолипиды; цетиловый спирт; воски, такие как карнаубский воск, спермацетовый воск, пчелиный воск, канделильский воск, шеллачный воск, микрокристаллический воск и парафиновый воск; водорастворимые полимеры, такие как полиэтиленгликоль, поликапролактон, GlycoWax-932, глицериды лауроилмакрогола-32 и глицериды стеароилмакрогола-32; полиэтиленоксиды и эфиры сахарозы.
В одном варианте осуществления плавкое связующее вещество представляет собой связующее вещество, расплавляемое РЧ-излучением, причем связующее вещество, расплавляемое РЧ-излучением, представляет собой полиэтиленгликоль (ПЭГ), такой как ПЭГ-4000. Особенно предпочтительное связующее вещество, расплавляемое РЧ-излучением, представляет собой ПЭГ, имеющий по меньшей мере 95% по весу частиц ПЭГ менее 100 микрон (измеряют традиционными средствами, такими как рассеивание света или лазерного излучения, или с помощью гранулометрического анализа) и молекулярную массу в диапазоне от 3000 до 8000 дальтон.
Плавкое(-ие) связующее(-ие) вещество(-а) может(-гут) присутствовать в концентрации от приблизительно 0,01 процента до приблизительно 70 процентов порошковой смеси/таблетки, например от приблизительно 1 процента до приблизительно 50 процентов, например от приблизительно 10 процентов до приблизительно 30 процентов порошковой смеси/таблетки.
Углевод
В одном варианте осуществления порошковая смесь/таблетка содержит по меньшей мере один углевод в дополнение к любому первому материалу, второму материалу или плавкому связующему веществу, которое также является углеводом. В одном варианте осуществления порошковая смесь/таблетка содержит как плавкое связующее вещество, так и углевод. Углевод может влиять на растворимость и ощущение таблетки при нахождении в ротовой полости, способствовать распределению других ингредиентов по большей площади поверхности, а также разбавлению и смягчению фармацевтически активного агента. Примеры углеводов включают, без ограничений, водорастворимые прессуемые углеводы, такие как сахара (например, декстроза, сахароза, мальтоза, изомальт и лактоза), крахмалы (например, кукурузный крахмал), сахарные спирты (например, маннит, сорбит, мальтит, эритрит, лактит и ксилит) и гидролизаты крахмала (например, декстрины и мальтодекстрины).
Углевод(-ы) может(-гут) присутствовать в концентрации от приблизительно 5 процентов до приблизительно 95 процентов порошковой смеси/таблетки, например от приблизительно 20 процентов до приблизительно 90 процентов или от приблизительно 40 процентов до приблизительно 80 процентов порошковой смеси/таблетки. Если в порошковой смеси содержится плавкое связующее вещество, размер частиц углевода может влиять на концентрацию используемого плавкого связующего вещества, причем при большем размере частицы углевода обеспечивается меньшая площадь поверхности и, следовательно, требуется меньшая концентрация плавкого связующего вещества. В одном варианте осуществления, в котором содержание углевода(-ов) составляет более 50% по весу порошковой смеси, а средний размер частицы углевода(-ов) составляет более 100 микрон, плавкое связующее вещество находится в диапазоне от приблизительно 10 до приблизительно 30 процентов по весу порошковой смеси/таблетки.
Фармацевтически активный агент
Порошковая смесь/таблетка настоящего изобретения включает по меньшей мере один фармацевтически активный агент, содержащий частицы. Термин «фармацевтически активный агент» означает агент (например, соединение), который разрешен или одобрен Управлением по контролю за качеством пищевых продуктов и лекарственных средств США, Европейским агентством по лекарственным средствам или любым из их правопреемников в качестве препарата для перорального применения при лечении состояния или заболевания. Подходящие фармацевтически активные агенты включают, без ограничений, анальгетики, противовоспалительные агенты, жаропонижающие, антигистаминные, антибиотики (например, антибактериальные, противовирусные и противогрибковые агенты), антидепрессанты, противодиабетические агенты, спазмолитики, средства, подавляющие аппетит, бронходилататоры, агенты для лечения сердечно-сосудистых заболеваний (например, статины), агенты для лечения центральной нервной системы, противокашлевые средства, антиконгестанты, диуретики, отхаркивающие средства, средства для лечения заболеваний желудочно-кишечного тракта, анестетики, муколитики, мышечные релаксанты, агенты для лечения остеопороза, стимуляторы, никотин и седативные средства.
Примеры подходящих агентов для лечения заболеваний желудочно-кишечного тракта включают, без ограничений, следующие: антациды, такие как алюминийсодержащие фармацевтически активные агенты (например, карбонат алюминия, гидроксид алюминия, карбонат дигидроксиалюминия натрия и фосфат алюминия), бикарбонатсодержащие фармацевтически активные агенты, висмутсодержащие фармацевтически активные агенты (например, алюминат висмута, карбонат висмута, субкарбонат висмута, субгаллат висмута и субнитрат висмута), кальцийсодержащие фармацевтически активные агенты (например, карбонат кальция), глицин, магнийсодержащие фармацевтически активные агенты (например, магалдрат, алюмосиликаты магния, карбонат магния, глицинат магния, гидроксид магния, оксид магния и трисиликат магния), фосфатсодержащие фармацевтически активные агенты (например, фосфат алюминия и фосфат кальция), калийсодержащие фармацевтически активные агенты (например, бикарбонат калия), натрийсодержащие фармацевтически активные агенты (например, бикарбонат натрия) и силикаты; слабительные средства, такие как размягчающие стул средства (например, докузат) и слабительные стимулирующего действия (например, бисакодил); антагонисты H2-рецепторов, такие как фамотидин, ранитидин, циметидин и низатидин; ингибиторы протонного насоса, такие как омепразол, декслансопразол, эзомепразол, пантопразол, рабепразол и лансопразол; желудочно-кишечные цитопротекторы, такие как сукральфат и мизопростол; желудочно-кишечные прокинетики, такие как прукалоприд; антибиотики, активные в отношении H. pylori, такие как кларитромицин, амоксициллин, тетрациклин и метронидазол; противодиарейные средства, такие как субсалицилат висмута, каолин, дифеноксилат и лоперамид; гликопирролат; анальгетики, такие как мезаламин; противорвотные средства, такие как ондансетрон, циклизин, дифенгидрамин, дименгидринат, меклизин, прометазин и гидроксизин; пробиотические бактерии, включая, без ограничений, молочнокислые бактерии; лактазу; рацекадотрил; а также ветрогонные средства, такие как полидиметилсилоксаны (например, диметикон и симетикон, включая описанные в патентах США №№ 4906478, 5275822 и 6103260); их изомеры; а также их фармацевтически приемлемые соли и пролекарства (например, эфиры).
Примеры подходящих анальгетиков, противовоспалительных и жаропонижающих средств включают, без ограничений, нестероидные противовоспалительные лекарственные средства (НПВС), такие как производные пропионовой кислоты (например, ибупрофен, напроксен, кетопрофен, флурбипрофен, фенбуфен, фенопрофен, индопрофен, кетопрофен, флупрофен, пирпрофен, карпрофен, оксапрозин, пранопрофен и супрофен) и ингибиторы циклооксигеназы, такие как целекоксиб; ацетаминофен; ацетилсалициловую кислоту; производные уксусной кислоты, такие как индометацин, диклофенак, сулиндак и толметин; производные фенаминовой кислоты, такие как мефенаминовая кислота, меклофенаминовая кислота и флуфенаминовая кислота; производные бифенилкарбоновой кислоты, такие как дифлунизал и флуфенизал; и оксикамы, такие как пироксикам, судоксикам, изоксикам и мелоксикам; их изомеры; а также их фармацевтически приемлемые соли и пролекарства.
Примеры антигистаминов и антиконгестантов включают, без ограничений, бромфенирамин, хлорциклизин, дексбромфенирамин, бромгексан, фениндамин, фенирамин, пириламин, тонзиламин, приполидин, эфедрин, фенилэфрин, псевдоэфедрин, фенилпропаноламин, хлорфенирамин, декстрометорфан, дифенгидрамин, доксиламин, астемизол, терфенадин, фексофенадин, нафазолин, оксиметазолин, монтелукаст, пропилгексадрин, трипролидин, клемастин, акривастин, прометазин, оксомемазин, меквитазин, буклизин, бромгексин, кетотифен, терфенадин, эбастин, оксатамид, ксилометазолин, лоратадин, дезлоратадин и цетиризин; их изомеры; а также их фармацевтически приемлемые соли и эфиры.
Примеры противокашлевых и отхаркивающих средств включают, без ограничений, дифенгидрамин, декстрометорфан, носкапин,