Способ оценки психического состояния пациентов с эндогенными психическими расстройствами при их клиническом обследовании и способ комплексной оценки состояния иммунной системы таких пациентов
Иллюстрации
Показать всеГруппа изобретений относится к медицине, а именно к психиатрии, и может быть использована для мониторинга состояния пациентов с эндогенными психозами, а также для оценки остроты психического состояния. Способ оценки психического состояния пациентов с эндогенными психическими расстройствами включает клиническое наблюдение и психометрическое обследование. Дополнительно осуществляют комплексную оценку состояния иммунной системы, при этом в качестве иммунологических показателей используют энзиматическую активность лейкоцитарной эластазы (ЛЭ), функциональную активность α1-протеиназного ингибитора (α1-ПИ) и уровень аутоантител к нейроантигенам - основному белку миелина (ОБМ) и белку S100B. Оценку психического состояния пациентов осуществляют путем сравнения степени отклонения определяемых иммунологических показателей сыворотки крови от аналогичных показателей образцов сыворотки крови здоровых лиц. Группа изобретений относится также к оценки состояния иммунной системы пациентов с эндогенными психическими расстройствами. Диапазон активности лейкоцитарной эластазы (ЛЭ) -(201-250) нмоль/мин × мл характеризуют как слабое повышение, диапазон - (251-300) нмоль/мин × мл - умеренное повышение, а повышение активности (ЛЭ) более 300 нмоль/мин × мл - выраженное повышение при нормальной активности ЛЭ в сыворотке крови человека - (150-200) нмоль/мин × мл. Сниженная или нормальная активность α1-протеиназного ингибитора (α1-ПИ) при повышенной активности ЛЭ свидетельствует о недостаточности антипротеолитической активности сыворотки крови при нормальной активности α1-ПИ -(28 - 32) ИЕ/мл; а повышение уровня аутоантител (аАТ) к основному белку миелина (ОБМ) и белку S100B, при норме (0,6-0,9) ед. опт. пл. характеризует наличие аутоиммунного компонента патологического процесса в мозге. Использование данной группы изобретений позволяет проводить комплексную оценку психического состояния пациентов с эндогенными психическими расстройствами с учетом патологического процесса в головном мозге на определенном временном отрезке развития заболевания, отражая степень активности (остроты) психотического состояния. 2 н. и 1 з.п. ф-лы, 2 пр., 1 табл., 2 ил.
Реферат
Изобретение относится к медицине, а именно к психиатрии, и может быть использовано в области диагностики и прогноза эндогенных психических заболеваний, в частности, для:
- объективизации оценки психического состояния больных, страдающих эндогенными приступообразными психозами, с целью определения степени активности патологического процесса на разных его этапах и степени выраженности регуляторных механизмов воспалительных реакций;
- мониторинга психического состояния пациентов в ходе патогенетически обусловленной редукции его проявлений;
- предикции степени редукции подспудных признаков остроты психотических проявлений и их динамики, внешне завуалированных в условиях психотропной терапии;
- оценки качества и степени полноты клинически диагностированной ремиссии;
- предикции экзацербации заболевания при длительном динамическом наблюдении пациентов в состоянии ремиссии разной степени качества и длительности.
Использованные термины и сокращения:
аАТ - аутоантитела
ЛЭ - лейкоцитарная эластаза
ОБМ - основной белок миелина
ОФД - ортофенилендиамин
α1-ПИ - a1-протеиназный ингибитор
PBS - фосфатный буферный раствор.
Несмотря на значительные успехи, достигнутые в последние годы клинической психиатрией в области диагностики и прогноза эндогенных психических заболеваний, практически нерешенными остаются вопросы о возможном использовании в психиатрической практике лабораторных методов, позволяющих объективно оценивать остроту и тяжесть патологического процесса в мозге, осуществлять мониторинг характеристик заболевания и предсказывать персонифицированные закономерности дальнейшего его течения.
Эндогенные приступообразные заболевания (шизофрения, аффективные и шизоаффективные психозы) объединяются эндогенными механизмами формирования и являются патогенетически запрограммированными патологическими процессами головного мозга со свойственными только им специфичностью проявлений, патокинезом расстройств, стереотипом развития и формой течения заболевания. Внешние (клинические) проявления эндогенного процесса находятся под влиянием как средовых факторов, так и используемой психофармакотерапии и при этом могут не совпадать по времени с этапами развития патологического процесса, закономерности которого жестко контролируются патогенетически. Это может затруднять истинное представление об объективном ходе его развития [Снежневский А.В. Синдромологическая и нозологическая классификация психической патологии // Руководство по психиатрии / Под ред. А.В. Снежневского. – М.: Медицина, 1983. - С. 80-96; Тиганов А.С. Шизофрения. Классификация. Типичные клинические проявления и течение // Психиатрия: Руководство для врачей: в 2 т. - М.: Медицина, 2012. - Т. 1. - С. 449-458].
Известны способы оценки психического состояния пациентов с эндогенными психическими расстройствами при их клиническом обследовании, включающие клиническое наблюдение и психометрическое обследование с использованием международных диагностических и оценочных шкал.
Клиническое наблюдение представляет собой качественную клиническую оценку психопатологических проявлений психических расстройств у пациента, как в виде отдельных признаков-симптомов, так и в виде синдромальной оценки состояния по характерному для каждого синдрома комплексу/набору симптомов. Кроме этого, оценивается выраженность психических расстройств, как позитивных, так и негативных. Синдромальная характеристика позволяет определить уже нозологическую принадлежность данного состояния пациента.
Психометрическое обследование с использованием международных психометрических шкал (как диагностических, так и оценочных, рейтинговых) позволяет разграничить шизофрению, аффективные психозы, эндогенные и неэндогенные депрессии, дать количественную оценку психопатологического состояния пациента в целом и оценить степень тяжести отдельных симптомов динамике в виде суммы балов (по предложенной в шкале градации), а также оценить побочные явления в процессе психофармакологической терапии. [Stanley R. Kay, Abraham Fiszbein. Lewis A. Opler. The Positive and Negative Syndrome Scale (PANSS) for Schizophrenia //Schizophr Bull. - 1987. - 13(2). - 261-276; Тиганов A.C. Психиатрия: Руководство для врачей в двух томах. - М.: Медицина. 2012, 808 с; Мосолов С.Н. Шкалы психометрической оценки шизофрении и концепция позитивных и негативных расстройств. М.: Новый цвет. - 2001. - 237 с]
Сочетание клинического обследования и психометрической оценки позволяет более объективно оценивать как изменения психического состояния в течение времени у отдельного пациента, так и сравнивать отдельные психические состояния у различные больных [Ann М. Mortimer. Symptom rating scales and outcome in schizophrenia // Br J Psychiatry. - 2 0 0 7. - 1 91 (supp 1. 5 0). – s. 7-14; Д.А. Смирнова. Негативные симптомы шизофрении в фокусе исследователя, клинициста и пациента (по материалам 26-го Конгресса Европейской коллегии нейропсихофармакологии) // Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. - 2014. - 02. – С. 7-18]. Данные количественной оценки психического статуса на основании психодиагностических шкал и опросников являются дополнением к традиционному клиническому психиатрическому обследованию.
Недостатком известных способов, включающих клиническую и психометрическую оценку является то, что они оба являются в значительной степени субъективными, т.к. зависят от мнения исследующего врача, его опыта, квалификации и т.д.
Известен лабораторный способ дифференциальной диагностики эндогенных психических расстройств, при котором проводят одномерный электрофорез сыворотки крови больных, и оценивают электрофоретический спектр распределения сывороточных белков. При выявлении белков с молекулярной массой 128, 114, 21 кДа диагностируют параноидную форму шизофрении, при выявлении белков с молекулярной массой 88 и 32 кДа диагностируют простую форму шизофрении, а при выявлении белков с молекулярной массой 65 и 38 кДа диагностируют острое полиморфное расстройство, [патент РФ №2522236, 2013 г.].
Однако, данный способ не предусматривает диагностику других форм психических заболеваний, таких как аффективные психозы, шизоаффективные, аутистические расстройства и др.; не предусматривает определения остроты и тяжести патологического процесса, а также не обладает предикционной способностью в плане дальнейшего развития заболевания, а кроме того, не предусматривает комплексное определении клинических параметров и показателей врожденного и приобретенного иммунитета в сыворотке крови пациентов для диагностики эндогенных психических расстройств.
На основании результатов многочисленных исследований, проведенных в последние годы в ФГНБУ НЦПЗ была выявлена вовлеченность врожденного (воспалительные реакции) и приобретенного (аутоантитела к нейроантигенам) иммунитета в патогенез эндогенных психических заболеваний. При исследовании клинико-биологических корреляций из широкого спектра воспалительных медиаторов был выделен ряд показателей, тесно взаимосвязанных с клиническими особенностями психического состояния пациента и степенью активности патологического процесса [Каледа В.Г., Клюшник Т.П., Сармаиова З.В., Отман И.П., Дупин A.M. Корреляция клинических и иммунологических показателей при первом приступе юношеского эндогенного психоза // Журнал неврологии и психиатрии им. С.С. Корсакова. - 2009. - Т. 109(1). - С. 16-19; Клюшник Т.П., Сиряченко Т.М., Сармаиова З.В., Отман И.Н., Дупин A.M. Иммунологические реакции при различных формах психической патологии // Журнал неврологии и психиатрии им. С.С. Корсакова. - 2009. - Т. 109(4). - С. 55-58; Щербакова И.В. Особенности врожденного и приобретенного иммунитета при высоком риске возникновения шизофрении и в процессе ее развития: Дис.… доктора мед. наук. - М., 2006].
В частности, была показана высокая энзиматическая активность лейкоцитарной эластазы - протеолитического фермента, принимающего участие в развертывании воспалительных реакций, что имеет место при обострении эндогенных психических заболеваний, но в ремиссии активность этого фермента снижается. Повышение энзиматической активности ЛЭ в острой стадии заболевания в большинстве случаев сопровождается также повышением функциональной активности α1-ПИ, синтезирующегося печенью белка острой фазы воспаления, который связывается с ЛЭ и снижает ее деструктивный потенциал, что в свою очередь способствует ограничению и разрешению воспалительного процесса. Низкая активность этого ингибитора может приводить к неконтролируемому протеолизу тканевых белков и развитию вторичных метаболических повреждений, что является неблагоприятным фактором в ходе дальнейшего развития заболевания [Клюшник Т.П., Сиряченко Т.М., Брусов О.С, Сарманова З.В., Отман К.Н., Дупин A.M. Поиск предикторов эффективности антипсихотической терапии шизофрении по иммунологическим показателям сыворотки крови // Журнал неврологии и психиатрии им. С.С. Корсакова. - 2008. - Т. 108(1). - С. 31-35].
Были также получены данные, свидетельствующие о том, что активация приобретенного иммунитета (появление в крови аутоантител к белкам нервной ткани) сопровождает наиболее тяжелые патологические процессы в головном мозге, преимущественно характерные для прогредиентных форм психических заболеваний [Каледа В.Г., Клюшник Т.П., Сармаиова З.В., Отман И.П., Дупин A.M. Корреляция клинических и иммунологических показателей при первом приступе юношеского эндогенного психоза // Журнал неврологии и психиатрии им. С.С. Корсакова. - 2009. - Т. 109(1). - С. 16-19; Клюшник Т.П., Сиряченко Т.М., Брусов О.С, Сарманова З.В., Отман К.Н., Дупин A.M. Поиск предикторов эффективности антипсихотической терапии шизофрении по иммунологическим показателям сыворотки крови // Журнал неврологии и психиатрии им. С.С. Корсакова. - 2008. - Т. 108(1). - С. 31-35; Щербакова К.В., Каледа B.Г., Бархатова А.Н., Клюшник Т.П. Маркеры эндотелиальной дисфункции при приступообразно-прогредиентной шизофрении // Журнал неврологии и психиатрии им. С.С. Корсакова. - 2005. - Т. 105(3). - С. 43-46].
Также показано, что изменения значений вышеперечисленных показателей врожденного иммунитета могут не только возникать синхронно с изменениями клинических проявлений психического состояния больных, но и порой опережать их по времени возникновения. В последнем случае изменения показателей врожденного иммунитета будут предшествовать по времени клиническим изменениям психического состояния [Клюшник Т.П., Зозуля С.А., Андросова Л.В., Сарманова З.В., Отман И.И., Дупин A.M., Пантелеева Т.П., Олейчик И.В. и др. Иммунологический мониторинг эндогенных приступообразных психозов // Журнал неврологии и психиатрии им. С.С.Корсакова. - 2014. - Т. 2. - С. 31-35], то есть определение иммунологических показателей в динамике может быть использовано для объективного прогноза дальнейшего развития заболевания и степени выздоровления больного при его клиническом обследовании.
Выявленные закономерности послужили основой для создания новой медицинской технологии «Нейро-иммуно-тест», объективно дополняющей клиническое обследование пациента в динамике. Технология заключается в комплексном определении клинических параметров и показателей врожденного и приобретенного иммунитета в сыворотке крови пациента в течение эндогенного психического заболевания.
Характер изменения этих показателей по сравнению с контрольными значениями позволяет определить активность течения патологического процесса в мозге пациента, оценивать степень его остроты и тяжести, на каждом этапе определять период активного течения процесса, а также полноту и качество наступившей ремиссии.
Анализ изменения показателей врожденного и приобретенного иммунитета в динамике позволяет вероятностно предсказывать закономерный ход дальнейшего развития заболевания. Сравнительная оценка этих параметров при экзацербации процесса (до начала терапии) и на последующих его этапах может свидетельствовать о степени выраженности психотических расстройств и их изменений в разные периоды заболевания, свойственные закономерностям его течения.
Оценку психического состояния пациентов проводят в точках взятия образцов крови для измерения иммунологических показателей. Она проводится как методом клинического наблюдения, так и психометрическим с использованием международных оценочных шкал PANSS (для оценки позитивных и негативных синдромов) и SANS (для оценки негативных симптомов в ремиссии). Больные в период обследования находятся на психофармакотерапии.
Затем определяют ряд показателей, характеризующих состояние врожденного и приобретенного иммунитета и взаимосвязанных с функционированием мозга, а именно: протеолитической активности ЛЭ, функциональной активности a1-протеиназного ингибитора и уровней аутоантител к нейроантигенам - основному белку миелина и белку S100B, - а также проводят последующую оценку полученных результатов.
Лейкоцитарная эластаза ЛЭ - высокоактивная сериновая протеаза с широкой субстратной специфичностью, содержащаяся в азурофильных гранулах нейтрофилов. ЛЭ секретируется во внеклеточное пространство при активации этих клеток в процессе развития неспецифического иммунного ответа на различные стимулы, включая инфекционные агенты, иммунные комплексы, эндотоксины и т.д. Попадающая во внеклеточное пространство ЛЭ расщепляет основное вещество, эластиновые и коллагеновые волокна сосудистых базальных мембран и соединительной ткани, белки плазмы крови, иммуноглобулины и т.д. [Яровая Г.А., Доценко В.Л., Мешкова Е.А. Патогенетическая роль лейкоцитарной эластазы. Новый спектрофотометрический метод ее определения в плазме крови человека // Информационный бюллетень. - М., 1995. - №1. - С. 16-18; Raptis S.Z., Pham С.Т. Neutrophil-derived serine proteases in immune complex-mediated diseases // Immunol. Res. - 2005. - V. 32. - №1-3. - P. 211-216].
Являясь звеном воспалительных реакций, носящих санационный характер, в ряде случаев этот фермент может проявлять значительный деструктивный потенциал в отношении сосудистого эндотелия (в случае повреждений мозга - эндотелия сосудов гематоэнцефалического барьера), способствуя вторичным метаболическим повреждениям мозга [Shimakura A., Kamanaka Y., Ikeda Y., Kondo K., Suzuki Y., Umemura K. Neutrophil elastase inhibition reduces cerebral ischemic damage in the middle cerebral artery occlusion // Brain Res. - 2000. - V. 858. - №1. - P. 55-60].
Основной регулятор активности фермента - α1-протеиназный ингибитор, отвечающий за 90% антипротеолитической активности плазмы крови (ингибирует активность трипсина, плазмина, некоторых факторов свертывания крови и т.д.) и подавляющий активность ЛЭ с высокой константой ассоциации (≥107 М×c-1). Контролируя протеолитическую активность ЛЭ, этот ингибитор создает условия для ограничения очага воспаления и/или деструкции. Показано, что функциональная активность α1-ПИ определяет течение многих воспалительных и/или деструктивных процессов [Travis J., Salvesen G.S. Human plasma proteinase inhibitors // Annual Review Biochemistry. - 1983. - V. 52. - P. 655-70].
Нормальными компонентами иммунной системы любого здорового человека являются естественные аутоантитела (аАТ) практически ко всем антигенам организма, в том числе к белкам нервной ткани. Естественное содержание и соотношение аАТ в сыворотке крови колеблется в определенных пределах, характерных для каждого возраста, и может резко изменяться при различных заболеваниях [Jankovic B.C., Djordjijevic D. Differential appearance of autoantibodies to human brain S100 protein, neuron specific enolase and myelin basic protein in psychiatric patients // Int. J. Neurosci. - 1991. - V. 60. - №1-2. - P. 119-127]. При реализации изобретения определяют уровни аАТ к двум белкам нервной ткани: белку S100B и основному белку миелина (OEM). ОБМ участвует в организации сборки и поддержания целостности миелина нервных волокон; S100B - Са2+ - связывающий белок нервной ткани - является трофическим фактором для серотонинергических нейронов, влияет на миграторную активность нейробластов, на координацию функционирования различных отделов нервной системы.
Известен способ прогнозирования психомоторного развития детей с перинатальным поражением центральной нервной системы, (патент РФ №2475747, 2011 г); способ лабораторного выявления последствий перинатальных поражений центральной нервной системы и определения степени их тяжести у детей, (патент РФ №2425371, 2010 г); способ определения характера патофизиологических нарушений психомоторного развития детей первого года жизни, патент РФ №2231074, 2003 г); способ выявления групп риска развития нервно-психических заболеваний, патент РФ №2218569, 2002 г), в которых частично описано определение ряда иммунологических показателей, однако ни один из них не описывает, не подразумевает и не предвосхищает предложенный способ оценки психического состояния пациентов, поскольку все они связаны с неврологическими расстройствами.
Здесь необходимо подчеркнуть, что общепринятой в медицинской науке считается точка зрения, согласно которой неврологические расстройства базируется на морфологическом уровне патологии нервной системы, а психические - в значительной степени связаны с функциональным уровнем поражения головного мозга. Поскольку цели воздействия в этих двух дисциплинах при лечении различны, то методы, применяемые в неврологии и в психиатрии, требуют отдельной независимой разработки и не могут быть механически перенесены из одной дисциплины в другую.
Авторами впервые было показано, что определение иммунологических показателей сыворотки крови пациентов, взаимосвязанных с функционированием мозга и характеризующих состояние врожденного и приобретенного иммунитета пациента, а также регистрация изменения таких показателей в динамике заболевания при сравнении с аналогичными показателями образцов сыворотки здоровых лиц позволяет осуществить комплексную оценку состояния иммунной системы пациентов и объективно оценить психическое состояние пациентов с эндогенными психозами.
Технической задачей настоящего изобретения является создание способа для мониторинга состояния пациентов с эндогенными психозами, для оценки остроты психического состояния, качества и степени полноты ремиссии, наступающей после снижения активности болезненного процесса, а также способа комплексной оценки состояния иммунной системы таких пациентов.
Целью изобретения является обеспечение возможности использования в психиатрической практике лабораторных методов, позволяющих объективно оценивать психическое состояние пациента с эндогенными психозами, остроту и тяжесть патологического процесса в мозге, осуществлять мониторинг характеристик заболевания и предсказывать персонифицированные закономерности дальнейшего его течения.
С этой целью в способе оценки психического состояния пациентов с эндогенными психическими расстройствами при их клиническом обследовании, включающем клиническое наблюдение и психометрическое обследование с использованием международных оценочных шкал и анализ полученных результатов, дополнительно осуществляют комплексную оценку состояния иммунной системы таких пациентов путем определения иммунологических показателей сыворотки крови, взаимосвязанных с функционированием мозга, и характеризующих состояние врожденного и приобретенного иммунитета, а также изменение таких показателей в динамике заболевания, при этом в качестве иммунологических показателей используют энзиматическую активность лейкоцитарной эластазы (ЛЭ), функциональную активность α1-протеиназного ингибитора (α1-ПИ) и уровень аутоантител к нейроантигенам - основному белку миелина (ОБМ) и белку S100B.
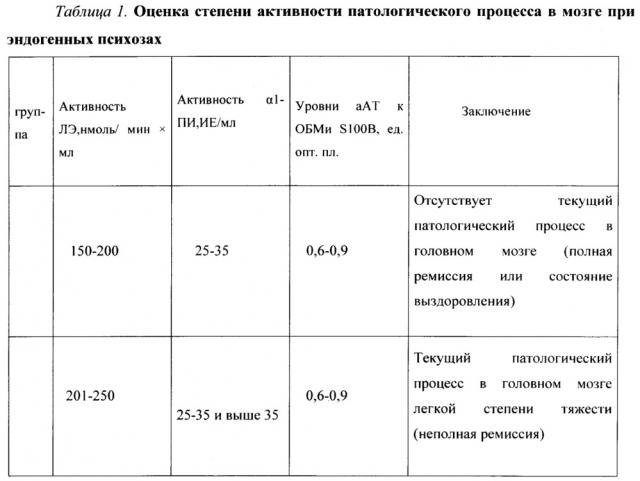
При этом анализ полученных результатов состояния иммунной системы пациентов проводят путем сравнения степени отклонения определяемых показателей врожденного и/или приобретенного иммунитета от аналогичных показателей образцов сыворотки здоровых лиц, при этом диапазон активности лейкоцитарной эластазы (ЛЭ) - (201-250) нмоль/мин × мл характеризуется как слабое повышение, диапазон - (251-300) нмоль/мин × мл - умеренное повышение, а повышение активности (ЛЭ) более 300 нмоль/мин × мл -выраженное повышение, при нормальной активности ЛЭ в сыворотке крови человека - (150-200) нмоль/мин × мл; сниженная или нормальная активность α1-протеиназного ингибитора (α1-ПИ) при повышенной активности ЛЭ свидетельствует о недостаточности антипротеолитической емкости сыворотки крови при нормальной активности α1-ПИ - (28-32) ИЕ/мл, а повышение уровня аутоантител (аАТ) к основному белку миелина (ОБМ) и белку S100B, при норме 0,6-0,9 ед. опт. пл. характеризует тяжесть патологического процесса в мозге.
Для решения поставленной задачи предложен также способ комплексной оценки состояния иммунной системы пациентов с эндогенными психическими расстройствами при их клиническом обследовании, при котором определяют иммунологические показатели сыворотки крови пациента, взаимосвязанные с функционированием мозга и характеризующие состояние врожденного и приобретенного иммунитета пациента, а также изменение таких показателей в динамике заболевания, и проводят анализ полученных результатов, при этом в качестве иммунологических показателей используют энзиматическую активность лейкоцитарной эластазы (ЛЭ), функциональную активность α1-протеиназного ингибитора (α1-ПИ) и уровень аутоантител к нейроантигенам - основному белку миелина (ОБМ) и белку S100B.
При этом анализ полученных результатов состояния иммунной системы пациентов проводят путем сравнения степени отклонения определяемых показателей врожденного и/или приобретенного иммунитета от аналогичных показателей образцов сыворотки здоровых лиц, при этом диапазон активности лейкоцитарной эластазы (ЛЭ) - (201-250) нмоль/мин × мл характеризуется как слабое повышение, диапазон - (251-300) нмоль/мин × мл - умеренное повышение, а повышение активности (ЛЭ) более 300 нмоль/мин × мл -выраженное повышение, при нормальной активности ЛЭ в сыворотке крови человека -(150-200) нмоль/мин × мл; сниженная или нормальная активность α1-протеиназного ингибитора (α1-ПИ) при повышенной активности ЛЭ свидетельствует о недостаточности антипротеолитической емкости сыворотки крови при нормальной активности α1-ПИ - (28-32)ИЕ/мл, а повышение уровня аутоантител (аАТ) к основному белку миелина (ОБМ) и белку S100B, при норме 0,6-0,9 ед. опт. пл. характеризует тяжесть патологического процесса в мозге.
Как уже отмечалось, характер изменения этих показателей по сравнению с контрольными значениями позволяет определить активность течения патологического процесса в мозге пациента, оценить степень его остроты и тяжести на каждом этапе, а также полноту и качество наступившей ремиссии.
Анализ изменения показателей врожденного и приобретенного иммунитета в динамике позволяет вероятностно предсказывать закономерный ход дальнейшего развития заболевания. Сравнительная оценка этих параметров при экзацербации процесса (до начала терапии) и на последующих его этапах может свидетельствовать о степени выраженности психотических расстройств и их изменений в разные периоды заболевания, свойственные закономерностям его течения.
Способ реализуют следующим образом.
Психиатры осуществляют оценку психического состояния пациентов, которая проводится как методом клинического наблюдения, так и с использованием психометрических международных оценочных шкал PANSS (для оценки позитивных и негативных синдромов) и SANS (для оценки негативных симптомов в ремиссии).
Клиническое наблюдение проводится в виде беседы врача-исследователя с пациентом, в процессе которой выявляются психопатологические расстройства, проявляющиеся в виде жалоб, высказываний, суждений, поведения, жестикуляции и мимики больного, и затем дается клиническая оценка состояния (качественная, синдромальная и по степени выраженности расстройств).
Кроме этого, проводится оценка состояния по отдельным симптомам (позитивным и негативным) путем прицельного опроса и последующего заполнения бланков, PANSS и SAN, с оценкой симптомов, по предложенным в шкалах градациям, в баллах. Это позволяет в результате получить количественную суммарную оценку, и отдельно - по позитивным и негативным субшкалам.
Больные в период обследования находятся на психофармакотерапии, включающей в себя соответствующую синдромальной характеристике их состояния комбинацию психотропных препаратов (нейролептиков, антидепрессантов, нормотимиков).
Сочетание качественной клинической и количественной психометрической оценок психопатологического состояния больного позволяет оценить остроту и стадию в развитии эндогенного заболевания, от выраженного острого, острого, подострого психотического состояния до неполной и полной ремиссии.
Для осуществления количественной психометрической оценки в точках взятия образцов крови для измерения иммунологических показателей у пациентов берут кровь, отделяют сыворотку, и определяют показатели, характеризующих состояние врожденного и приобретенного иммунитета, а именно: протеолитической активности ЛЭ, функциональной активности a1-протеиназного ингибитора и уровней аутоантител к нейроантигенам - основному белку миелина и белку S100B.
1. Для определения протеолитической активности ЛЭ применяют спектрофотометрический метод [Доценко В.Л., Пешкова Е.А., Яровая Т.А. Выявление лейкоцитарной эластазы человека из комплекса с плазменным α1-протеиназным ингибитором по ее энзиматической активности с синтетическим субстратом // Вопросы медицинской химии. - 1994. - Т. 40. - №3. - С. 20-25; Visser J., Blout E. The use of p-nitrophenyl N-tert-butyl-oxycarbonyl-L-alaninate as substrate for elastase // Biochem. Biophys. Acta. - 1972. - V. 268. - P. 257-260], который основан на частичном выделении эластазы из ее комплекса с ингибитором (α1-ПИ) и расщеплении ею специфического хромогенного субстрата N-терт-бутоксикарбонил-L-аланин-паранитрофенилового эфира (BOC-Ala-ONp) (ICN Biomedical Inc.), что приводит к возрастанию оптической плотности пробы. Контрольная проба состоит из 0,480 мл фосфатного буфера (рН 6,5) и 0,02 мл 0,40% раствора ВОС (3,1 мг BOC-Ala-ONp разводят в 1 мл ацетонитрила). Измерение проводят при t=25°С. Регистрируют оптическую плотность с помощью компьютерной программы SWIFT 1000 Reaction Kinetics (Version 2.03, Biochrom Ltd) на спектрофотометре Ultrospec 1100 (Amercham) в течение 3 мин при длине волны 347 нм, соответствующей максимуму поглощения продукта реакции (ΔЕ/минВОС). Опытная проба состоит из 0,480 мл фосфатного буфера (рН 6,5); 0,02 мл разведенного ацетонитрилом субстрата и 0,005 мл исследуемой сыворотки. Регистрацию оптической плотности проводят аналогичным образом (ΔЕ/минпроба).
Результат рассчитывают по следующим формулам:
1) определение среднего арифметического значения изменения оптической плотности, анализируемой пробы за 1 мин (ΔЕ) (ед. опт. пл./мин):
ΔЕ=ΔЕ/минпроба - ΔЕ /минВОС;
2) определение фактора пересчета (F):
F - K/Vcывор,
где К - пересчетный коэффициент, учитывающий объем пробы (0,5 мл) и коэффициент молярной экстинкции субстрата (4,6 мл × моль-1 × см-1); Vсыввop - объем сыворотки (мл);
3) определение активности лейкоцитарной эластазы (А) (нмоль/мин × мл):
А=ΔЕ × F.
Измерение активности ЛЭ каждого образца сыворотки рекомендуется проводить 3 раза, после чего вычислить среднее арифметическое значение активности ЛЭ.
2. Измерение функциональной активности а1-ПИ в сыворотке крови проводят с помощью унифицированного энзиматического метода [Нартикова В.Ф., Пасхина Т.С. Унифицированный метод определения активности α1-антитрипсина и α2-макроглобулина в сыворотке крови человека // Вопросы медицинской химии. - 1977. - Т. 25. - №4. - С. 492-497]. Метод основан на взаимодействии этого ингибитора с трипсином при использовании в качестве субстрата N-α-бензоил-L-аргининэтилового эфира гидрохлорида (BAEE) (ICN Biomedical Inc): α1-ПИ образует с трипсином комплекс, не гидролизующий ВАЕЕ. Активность α1-ПИ в сыворотке определяют по степени торможения ВАЕЕ-эстеразной активности трипсина определенным количеством исследуемой сыворотки. В кварцевых кюветах готовят две пробы: сначала контрольную, потом опытную. Контрольная проба состоит из 2,0 мл 0,05 М трис-HCl буфера (рН 8,0) и 0,01 мл 0,01% раствора трипсина в 1 мМ растворе HCl с 10 мМ CaCl2. Кювету инкубируют при +25°С в течение 3 мин. Затем добавляют 1 мл 1,5 мМ раствора ВАЕЕ и измеряют прирост оптической плотности (ΔЕ/мин) при длине волны 253 нм на спектрофотометре Ultrospec 1100 (Amercham). Регистрируют оптическую плотность с помощью компьютерной программы SWIFT 1000 Reaction Kinetics (Version 2.03, Copyright 1997-2002 Biochrom Ltd). Опытная проба состоит из 1,9 мл трис-HCl-буфера с рН 8,0; 0,01 мл 0,01% раствора трипсина и 0,1 мл разведенной физиологическим раствором (1:50) сыворотки крови. Кювету инкубируют при +25°С в течение 3 мин. Затем добавляют 1,0 мл субстрата и аналогичным образом измеряют прирост оптической плотности (АЕ/мин к).
Результат рассчитывают по следующей формуле:
где ΔЕ/минконтроль и ΔЕ/минпроба - скорости гидролиза
ВАЕЕ трипсином в контрольной и опытной пробах, соответственно равные приросту оптической плотности за 1 мин; 2,73 - расчетный коэффициент; 50 - фактор разведения сыворотки; 0,1 - количество сыворотки, взятой для анализа (мл).
Активность α1-ПИ выражают в ИЕ/мл.
3. Определение содержания аАТ к ОБМ и S100B в образцах сыворотки крови проводится методом стандартного твердофазного иммуноферментного анализа (Enzyme-Linked Immunosorbent Assay - ELISA).
Этапы определения:
1. В лунки планшета вносят по 100 мкл раствора белка в концентрации 1 мг/мл в 50 мМ фосфатном буферном растворе рН 8,1/8,5 (PBS) и инкубируют его 20 мин при +37°С, а затем в течение суток при +4°С. Для удаления несвязавшегося белка планшет 2-3 раза промывают дистиллированной водой.
2. Для предотвращения неспецифической сорбции в каждую лунку вносят по 200 мкл 0,5% раствора желатина в PBS и инкубируют 1 ч при +37°С. Для удаления избытка желатина планшет 5-7 раз промывают дистиллированной водой и 2 раза PBS, содержащем 0,05% твин-20.
3. В лунки планшета вносят по 100 мкл опытной или контрольной сыворотки в разведении 1:40 в PBS, содержащем 0,05% твин-20 и 0,5% желатин и инкубируют 1 ч при +37°С. Для удаления несвязавшихся аАТ планшет 5-7 раз промывают дистиллированной водой и 2 раза PBS, содержащем 0,05% твин-20.
4. В лунки планшета вносят по 100 мкл конъюгата антител с пероксидазой хрена к суммарным иммуноглобулинам человека в разведении согласно инструкции в PBS, содержащем 0,05% твин-20 и 0,5% желатин. Планшет инкубируют 1 ч при +37°С. Для удаления избытка конъюгата планшет 5-7 раз промывают дистиллированной водой, 2-3 раза PBS, содержащем 0,05% твин-20, и еще 2-3 раза дистиллированной водой.
5. В лунки планшета вносят по 100 мкл реакционной смеси, содержащей 0,05% ОФД и 0,01% перекись водорода в 5,0 мМ цитратном буфере (рН 5.0).
6. После развития окраски через 7 мин реакцию останавливают внесением в каждую лунку 50 мкл 1 М раствора серной кислоты и измеряют оптическую плотность при длине волны 492 нм с использованием многоканального спектрофотометра Multiskan RC (Labsystems, Финляндия).
Для стандартизации определений, получаемых на разных планшетах, в каждой постановке реакции в качестве контроля используют «стандартную» сыворотку, оптическая плотность которой в соответствующем разведении равна 1. Коэффициент соответствия между различными планшетами определяют как соотношение оптической плотности показателей контрольной сыворотки на этих планшетах: К=1/OD
Измерения образцов испытуемой и контрольных сывороток проводят в двух параллелях. Конечный результат, отражающий уровень аАТ, выражается в единицах оптической плотности и представляет собой среднее арифметическое из двух измерений, умноженное на коэффициент соответствия: OD=К × (OD1+OD2)/2.
Обработка полученных данных
В норме активность ЛЭ в сыворотке крови человека составляет 150-200 нмоль/мин х мл. Диапазон ее активности в 201-250 нмоль/мин × мл характеризует слабое повышение, а диапазон в 251-300 нмоль/мин × мл - умеренное. Повышение активности ЛЭ более 300 нмоль/мин × мл характеризует выраженное повышение.
Активность ЛЭ в норме может служить подтверждением отсутствия в организме человека тех или иных патологических процессов, связанных с воспалительными реакциями. Повышенная активность ЛЭ в крови пациентов с эндогенными психическими заболеваниями свидетельствует о наличии текущего патологического процесса в мозге с разной степенью его активности.
При повторных определениях в ходе течения заболевания повышение активности ЛЭ от нормального до слабого, умеренного или выраженного свидетельствует о нарастающей активации (обострении) патологического процесса в мозге и может предшествовать диагностике обострения психотической симптоматики клиническим методом.
Активность α1-ПИ в норме составляет 28-32 ИЕ/мл. Наблюдаемое при повышении активности ЛЭ параллельное повышение активности α1-ПИ направлено на ограничение воспалительных реакций и свидетельствует о сохранности антипротеолитического компенсаторного потенциала. Сниженная или нормальная активность α1-ПИ (при повышенной активности ЛЭ) свидетельствует о недостаточности антипротеолитической емкости сыворотки крови и является неблагоприятным прогностическим фактором плане дальнейшего развертывания патологического процесса в головном мозге.
Иммунологические показатели в оценке степени активности эндогенного психоза в условиях психофармакотерапии.
Анализ полученных результатов с использованием требований доказательной медицины позволил определить прогностическую значимость предложенных решений.
Если до начала лечения у пациента в сыворотке крови выявлена высокая активность ЛЭ и α1-ПИ (200 нмоль/мин × мл < ЛЭ <300 нмоль/мин × мл, α1-ПИ >35 ИЕ/мл), а уровень аутоантител к нейроантигенам в пределах нормы (0,6-0,9 ед. опт. пл.), то с вероятностью около 85% эти показатели являются прогностическим фактором благоприятного течения заболевания с выходом в ремиссию хорошего качества.
Если до начала лечения выявлена высокая активность ЛЭ и высокий уровень аутоантител к нейроантигенам (ЛЭ >300 нмоль/мин × мл, аАТ к ОБМ >0,9 ед. опт. пл., аАТ к S100B >0,9 ед. опт. пл.), то это означает, что с вероятностью около 80% у пациента течение эндогенного психического заболевания будет неблагоприятным с длительным сохранением резистентного к терапии психотического состояния и терапевтической ремиссией низкого качества с остаточной продуктивной симптоматикой.
Пример 1. Больная Ш., 1988 г.р. Диагноз: шизофрения приступообразная с повторными маниакально-парафренными состояниями в приступах (F20.01 + F 31.2 по МКБ-10).
Больная росла активной, общительной, мечтательной, любила фантазировать. В школе училась хорошо. Окончив филологический факультет МГУ, работала менеджером по связям с общественностью. С подросткового возраста страдала перепадами настроения: в депрессиях имели место явления дисморфофобии, идеи отношения, порчи, рудиментарные явления идеаторных автоматизмов, в гипоманиях - дромоманические тенденции, сексуальная расторможенность. В возрасте 24 лет (январь 2012 г.) родила дочь. Вскоре после родов возникло маниакально-бредовое состояние, в клинической картине которого преобладали психомоторное возбуждение, изменчивый фон настроения. Бредовые идеи преследования и порчи сменились идеями мессианства. По бредовым мотивам, пытаясь «спасти» ребенка, повезла его в храм Христа Спасителя и попала в ДТП, в результате которого младенец попал в реанимацию (скончался через 11 дней). Больная в психомоторном возбуждении была госпитализирована в ПБ, затем переведена в клинику НЦПЗ РАМН, и была включена в программу мониторинга пациентов с использованием лабораторной диагностики «Нейро-иммуно-тест».
Психическое состояние больной при поступлении оценивалось как подострое, маниакально-парафренное с частичной критикой к бредовым переживаниям. На реальную смерть ребенка адекватно не реагировала. Психометрическая оценка тяжести состояния по PANSS в день поступления равнялась 66 баллам, что свидетельствовало о подостром психотическом состоянии. Комплексная оценка иммунологических показателей от 14.03.2013 г. соответствовала уровню активности текущего патологического процесса в головном мозге легкой степени, свойственной состоянию неполной ремиссии (активность ЛЭ - 218,2 нмоль/мин х мл, α1-ПИ - 38,2 ИЕ/мл, уровень аАТ - 0,7 и 0,64 ед. опт. пл. соответственно) (см. табл. 1). Через месяц психофармакотерапии психопатологические проявления заболевания у больной редуцировались, фон настроения выровнялс