Способ магнетитового литья
Иллюстрации
Показать всеИзобретение относится к производству магнетитового литья и магнетитовых анодов, применяемых для электролиза водных сред (рН 2÷14) и катодной защиты от коррозии. Производят нагрев и плавление шихты из мелкой обогащенной магнетитовой руды, разлив в форму и кристаллизацию расплава в среде углекислого газа при атмосферном давлении. Перед плавлением шихту нагревают и выдерживают 30 минут при температуре 1560°С. Плавят в плавильной печи при температуре 1575°С. Расплав перед разливкой в формы выдерживают 25-35 минут при температуре 1630-1640°С. Формы с кристаллизованным литьем при температуре 1500-1200°С помещают в печь с защитной атмосферой на основе инертного газа азота или аргона при давлении 1 атм и парциальном давлении кислорода в защитной атмосфере 10-4-10-5 атм. Охлаждают до комнатной температуры 20-25°С со скоростью 40-60 град/ч. Получают литой магнетит стехиометрического состава однородного по структуре с достаточной воспроизводимостью по нестехиометрии и удельной электрической проводимости. 2 ил., 4 табл., 3 пр.
Реферат
Изобретение относится к области изготовления магнетитовых анодов, применяемых для процессов электролиза водных сред с рН 2-14 и в системах катодной защиты от коррозии.
Известен способ изготовления магнетитовых анодов (Пат. RU №2178010 от 01.10.2002 [1]) путем прессования и спекания в вакуумных печах (t=1300-1350°С; разряженная атмосфера воздуха Р≥1,31⋅10-7 атм) шихты, состоящей из связующего вещества и природного магнетита, измельченного в шаровых мельницах.
Известен способ изготовления литых магнетитовых анодов (Коррозия и защита в нефтегазовой промышленности, 1973, №4, с. 26-29 [2]) из обогащенной железной руды (мас.%: FeO - 28,0-30,0; Fe2O3 - 51,0-60,0; SiO2 - 6,8-8,0; CaO - 0,2-0,3; MgO - 0,1-0,2; Al2O3 и др. - 1,0-1,5), расплавленной в высокочастотной индукционной печи. Плавление, разливка, охлаждение и термообработка осуществляются в атмосфере воздуха.
Известен способ изготовления рабочего магнетитового слоя составного анода (Пат. RU №2169210 от 25.04.2000 [3]) послойной кристаллизацией из расплава железорудного концентрата (Fe - 65,4%) в атмосфере воздуха.
По совокупности существенных признаков и назначению ближайшим аналогом-прототипом является способ получения литого магнетита (Пат.RU №2280712 от 27.07. 2006 [4]). Способ включает плавку шихты из природного магнетита, заливку расплава при 1610°С в форму требуемой детали, помещенную в замкнутую емкость, в которую подается смесь СО+СO2 при давлении 1,5÷16 атм до завершения кристаллизации с последующим быстрым охлаждением магнетитового литья.
Во всех аналогах [1-3] схожи технические задачи - достижение высоких эксплуатационных параметров (коррозионная стойкость, электропроводность, механическая прочность, компактность и т.д.), но принципиально разные способы подготовки сырья (шихты) и получения компактного магнетита. Технологии [1-3] не обеспечивают оптимальных электропроводности и коррозионной стойкости, отсутствия высоких внутренних напряжений в материале, воспроизведения перечисленных свойств. При этом способу [1] присуща высокая трудоемкость и энергоемкость. Основной недостаток рассматриваемых способов [1-3] состоит в том, что они не ориентированы на получение компактного магнетита заданного состава.
Технология прототипа [4] позволяет получить достаточно компактный магнетит, по составу близкий к стехиометрическому. Однако, как показали собственные исследования, она не гарантирует воспроизводимость параметров оксида [5]. Так, колебания величины удельного электрического сопротивления магнетитового литья (ρ), полученного в различных плавках, может достигать 120%, а отклонения оксида (Fe3O4+γ) от стехиометрии (γ) - более чем 270%.
Задачей изобретения являлось получение компактного магнетита по составу, близкому к стехиометрическому с заданными параметрами: кислородной нестехиометрией (γ) и удельным электрическим сопротивлением (ρ).
Решение поставленной задачи достигается тем, что шихта из мелкой обогащенной магнетитовой руды нагревается, выдерживается 30 мин при 1560°С и плавится (~1575°С) в индукционной печи. Расплав выдерживается 25-35 минут при 1630-1640°С и разливается в металлические формы (кокили), где кристаллизуется. Все перечисленные операции производятся в среде углекислого газа при атмосферном давлении. Формы с кристаллизованным оксидом (литьем) при температурах 1500-1200°С помещаются в печь с защитной атмосферой, где парциальное давление кислорода В печи литье охлаждается до комнатных температур 20-25°С со скоростью 40-60 град/ч.
Важнейшим параметром электродного материала является удельное электрическое сопротивление (ρ, Ом⋅м). Оно должно быть минимальным. Согласно экспериментальным данным [5-7] для оксидов железа минимальные величины ρ имеют составы, близкие к стехиометрическому магнетиту. При этом, как следует из фиг. 1, особо велико влияние атомного соотношения Fe3+/Fe2+ в оксидной композиции на значения ρ со стороны двухфазной области (Fe3O4+Fe2O3). В таком случае необходимо учитывать точечную дефектность кристаллической решетки, в значительной мере определяющую физико-химические свойства оксида железа [8]. Как известно [8, 9], магнетит является соединением переменного состава с избытком кислорода (Fe3O4+γ). Его кислородная нестехиометрия (γ) увеличивается с ростом температуры и равновесного давления кислорода в газовой фазе, т.е. . Кроме того, концентрация железа II в оксиде функционально связана с кислородной нестехиометрией [Fe2+]=f(γ). Это позволяет по данным о содержании железа II в оксиде оценивать величину у композиции Fe3O4+γ из уравнения [10]
где х - число молей Fe2+ в 1 г оксида; М - молекулярная масса стехиометрического магнетита (Fe3O4).
Система из оксида фиксированного состава (γ=const) и кислородосодержащей газовой среды в соответствии с правилом фаз имеет одну степень свободы [11]. Таким образом, из двух переменных Т и только одна является независимой (Т), а вторая - ее функция . Чтобы получить конгруэнтно плавящийся магнетит с малой областью гомогенности необходимо готовить шихту (нагрев, выдержка вблизи температуры плавления, плавление) и кристаллизовать расплав в атмосфере углекислого газа. В этом случае в интервале температур 1575-1200°С парциальное давление кислорода в газовой фазе будет близким к равновесному давлению над стехиометрическим (0,001≤γ≤0,0038) оксидом (фиг. 2 [8]).
Величина при диссоциации углекислого газа в соответствии с реакцией СО2=СО+0,5О2 определяется уравнением [9]
,
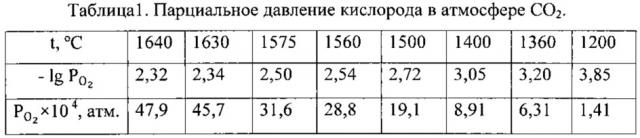
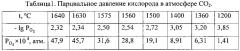
где Т - температура, K; - парциальное давление кислорода в атмосфере чистого СО2, атм.
Рассчитанные по уравнению (2) величины в атмосфере СO2 для предлагаемого интервала технологических температур представлены в таблице 1.
Как следует из фиг. 2, охлаждение оксидного литья в атмосфере чистого углекислого газа ниже 1200°С способствует возрастанию дефектности магнетита и образованию новой фазы - гематита (Fe2O3). Чтобы получить оксид Fе3O4+γ заданного состава (0,0004≤γ≤0,004), необходимо понизить парциальное давление кислорода в газовой фазе до ≤10-4 атм после достижения температуры литья 1500-1200°С (фиг. 2). Такой технологический прием позволяет уменьшить кислородную нестехиометрию (γ) оксидной композиции до нужного уровня [12]. Для сохранения заданной нестехиометрии и снижения внутренних механических напряжений литье охлаждается в разряженной по кислороду атмосфере со скоростью 40-60 град/ч до комнатных температур. В таких условиях количество кислорода в конденсированной фазе меняется незначительно [9] и характер изменения равновесного давления кислорода над магнетитом близок к зависимости , как показано на фиг 2.
С целью проверки воспроизводимости свойств магнетитового литья были проведены плавки обогащенной железной руды по предлагаемой технологии. Использовались железорудные концентраты трех российских месторождений. Плавки были рандомизированы во времени и осуществлялись в индукционной тигельной печи ИПП 100/50. Кислородная нестехиометрия магнетитового литья оценивалась из уравнения (1) по данным анализа на железо II [14] и гравиметрией при восстановлении оксида водородом до металла [15]. Удельное электрическое сопротивление материала рассчитывалось на основании измерений четырех зондовым методом [16, 17].
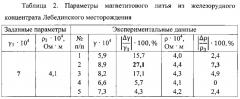
Пример 1. Шихта из железорудного концентрата Лебединского месторождения (мас.%: FeO - 28,27; Fe2O3 - 68,26; SiO2 - 4,4; Аl2О3 - 0,17; CaO - 0,2; MgO - 0,24; др. - 0,43) [17] нагревалась, выдерживалась 30 мин при 1560°С и плавилась (~1575°С). Расплав выдерживался 25 минут при 1640°С, разливался в кокили, кристаллизовался и охлаждался. Все операции производились в среде углекислого газа (Р≈1 атм). При температуре 1500°С формы с кристаллизованным оксидом помещались в печь с контролируемой атмосферой аргона (). Далее, литье охлаждалось до комнатных температур со скоростью 40 град/ч. Заданные и полученные параметры магнетитового литья представлены в табл. 2.
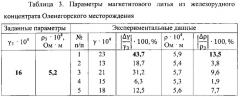
Пример 2. Шихта из железорудного концентрата Оленегорского месторождения (мас.%: FeO - 25,4; Fe2O3 - 65,24; SiO2 - 7,9; Аl2O3 - 0,28; CaO - 0,3; MgO - 0,39; др. - 0,49) [17] нагревалась, выдерживалась 30 мин при 1560°С и плавилась (~1575°С). Расплав выдерживался 35 минут при 1630°С, разливался в кокили, кристаллизовался и охлаждался. Все операции производились в среде углекислого газа (Р≈1 атм). При температуре 1300°С формы с кристаллизованным оксидом помещались в печь с контролируемой атмосферой аргона (). Далее, литье охлаждалось до комнатных температур со скоростью 60 град/ч Заданные и полученные параметры магнетитового литья представлены в табл. 3.
Пример 3. Шихта из железорудного концентрата Курской магнитной аномалии (мас.%: FeO - 28,01; Fe2O3 - 63,29; SiO2 - 7,35; Аl2О3 - 0,20; CaO - 0,20; MgO - 0,28; др. - 0,64) [17] нагревалась, выдерживалась 30 мин при 1560°С и плавилась (~1575°С). Расплав выдерживался 30 минут при 1635°С, разливался в кокили, кристаллизовался и охлаждался. Все операции производились в среде углекислого газа (Р=1 атм). При температуре 1200°С формы с кристаллизованным оксидом помещались в печь с контролируемой атмосферой аргона (). Далее, литье охлаждалось до комнатных температур со скоростью 50 град/ч. Заданные и полученные параметры магнетитового литья представлены в табл.4.
Во всех трех примерах (табл. 2-4) разброс индекса кислородной нестехиометрии магнетитового литья относительно заданных величин не превышает 44%, тогда как колебания величины удельного электрического сопротивления составляет менее 14%. Таким образом, возможно констатировать, что примененные в разработке технологические приемы позволяют решить задачу получения магнетитового литья с заданными параметрами.
Литература
1. Кузьмин Ю.Л., Лащевский В.О., Трощенко В.Н., Медяник Т.Е. Способ изготовления магнетитовых анодов для системы катодной защиты от коррозии изделий различного назначения - Пат. RU №2178010, опубл. 01.10.2002.
2. Зорин А.И., Коровников С.А., Никитенко Е.А. Производство литых магнетитовых анодов для катодной защиты подземных и подводных сооружений - Коррозия и защита в нефтегазовой промышленности, 1973, №4, с. 26-29.
3. Зорин А.И., Зорин А.А., Католикова Н.М. и др. Анод для катодной защиты от коррозии и способ формирования покрытия анода. Пат. RU №2169210, опубл. 25.04.2000.
4. Хоришко Б.А. Марценко К.Н., Давыдов А.Д., и др. Способ получения литого магнетита. Пат. RU №2280712 опубл. 27.07. 2006.
5. Хоришко Б.А., Давыдов А.Д., Иванова О.В. и др. Свойства и технология железо-оксидного электродного материала / Материалы VI Международной научной конференции «Современные методы в теоретической и экспериментальной электрохимии» - г. Плес, 2014. С. 8.
6. R. Itai, М. Shibuya, Т. Matsumura, and G. Ishi, Electrical Resistivity of Magnetite Anodes, J. Electrochem. Soc: Electrochemical Technology, vol. 118, №10, p. 1709-1711, 1971.
7. Разина Н.Ф. Окисные электроды в водных растворах - Алма-Ата: Наука, 1982. - 160 с.
8. Третьяков Ю.Д. Термодинамика ферритов. - Л.: Химия, 1967. - 304 с.
9. Третьяков Ю.Д. Химия нестехиометрических окислов. - Издательство МГУ, 1974. - 364 с.
10. Третьяков Ю.Д., Олейников Н.Н. Оценка дефектности шпинельных структур на основании данных химического анализа - ЖНХ, 1965. - Т 10, №8. - С. 1940-1942.
11. Горощенко Я.Г. Физико-химический анализ гомогенных и гетерогенных систем. - Киев: Наукова Думка, 1978. - 490 с.
12. Граник В.А., Олейников Н.Н., Пивоваров Л.З., Третьяков Ю.Д. Исследование физико-химической природы магнитных свойств некоторых ферритов как основа для выбора оптимальных условий их термической обработки / Сб.: «Магнитные и кристаллохимические исследования ферритов» - Изд-во МГУ, 1971, с. 220-238.
13. ГОСТ Р 53657-2009 Руды железные, концентраты, агломераты и окатыши. Метод определения железа (II) в пересчете на оксид. - М.: Стандартинформ, 2010. - 10 с.
14. Reed Т.В. Chemistry of Extended Defects in Non-Metallic Solids -Amsterdam, North-Holland Publ. Co., 1970, p. 21-35.
15. Павлов Л.П. Методы измерения параметров полупроводниковых материалов - М.: Высшая школа, 1987. - 239 с.
16. ГОСТ 24392-80 Кремний и германий монокристаллические. Измерение удельного электрического сопротивления четырехзондовым методом. - М.: Издательство Стандартов, 2001. - 5 с.
17. Крупнейшие месторождения железной руды в России. URL: http://emchezgia.ru/syrye/6_mestoroshdeniya_sheleznaya_ruda.php.
Способ литья для изготовления магнетитовых анодов, включающий нагрев и плавление шихты из мелкой обогащенной магнетитовой руды, разлив в форму и кристаллизацию расплава, охлаждение кристаллизованного литья, отличающийся тем, что нагрев и плавление шихты, разлив в форму и кристаллизацию расплава осуществляют в среде углекислого газа при атмосферном давлении, при этом перед плавлением шихту нагревают и выдерживают 30 минут при температуре 1560°С, после чего плавят в плавильной печи при температуре 1575°С, расплав перед разливкой в формы выдерживают 25-35 минут при температуре 1630-1640°С, формы с кристаллизованным литьем при температуре 1500-1200°С помещают в печь с защитной атмосферой на основе инертного газа азота или аргона при давлении 1 атм и парциальном давлении кислорода в защитной атмосфере 10-4-10-5 атм и охлаждают до комнатной температуры 20-25°С со скоростью 40-60 град/ч.