Улучшенные способы ацилирования майтанзинола
Иллюстрации
Показать всеИзобретение относится к способу получения сложного эфира аминокислоты и майтанзинола, представленного следующей формулой (I)
Технический результат: разработан новый способ получения майтанзинола, заключающийся во взаимодействии майтанзинола с N-карбоксиангидридом аминокислоты (NCA) в присутствии осушителя. Описан также улучшенный способ получения сложного эфира аминокислоты и майтанзинола, в котором нуклеофил добавляют к реакционной смеси после завершения реакции между майтанзинолом и N-карбоксиангидридом аминокислоты, позволяющий уменьшить образование нежелательных побочных продуктов и увеличить конечный выход. 2 н. и 32 з.п. ф-лы, 1 табл., 4 ил., 10 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
[1] В настоящей заявке в соответствии с §119(e) раздела 35 Кодекса законов США заявляется приоритет по дате подачи предварительной заявки на патент США №61/705731, поданной 26 сентября 2012 года, полное содержание которой включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[2] Настоящее изобретение представляет собой улучшенный способ получения промежуточных соединений для синтеза майтанзиноидов и их конъюгатов с антителами.
УРОВЕНЬ ТЕХНИКИ
[3] Майтанзиноиды представляют собой высоко цитотоксические соединения, в том числе майтанзинол и С-3 сложные эфиры майтанзинола (патент США №4151042), изображенные ниже:
[4] Природные и синтетические С-3 сложные эфиры майтанзинола можно разделить на две группы: (а) майтанзин (2) и его аналоги (например, DM1 и DM4), которые представляют собой С-3 сложные эфиры с N-метил-L-аланином или с производными N-метил-L-аланина (патенты США №4137230; 4260608; 5208020; и Chem. Pharm. Bull. 12:3441 (1984)); (b) ансамитоцины, которые представляют собой С-3 сложные эфиры с простыми карбоновыми кислотами (патенты США №4248870; 4265814; 4308268; 4308269; 4309428; 4317821; 4322348; и 4331598).
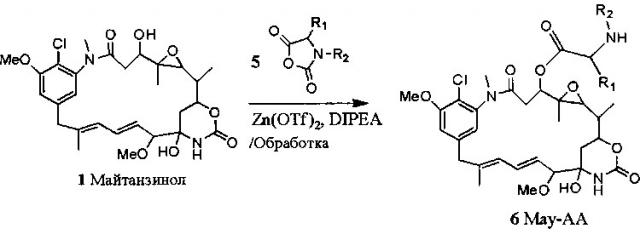
[5] Майтанзин (2), его аналоги и каждое из ансамитоциновых соединений представляют собой С3 сложные эфиры майтанзинола, которые могут быть получены эстерификацией майтанзинола (1). В патентах США №7301019 и 7598375 описаны способы ацилирования майтанзинола (1) N-карбоксиангидридом аминокислоты (NCA, 5) в присутствии основания с образованием сложного эфира аминокислоты и майтанзинола (Мау-АА, 6), как показано ниже:
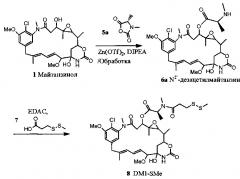
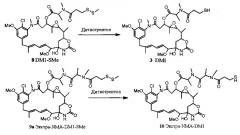
[6] Сложные эфиры аминокислот и майтанзинола представляют собой ценные промежуточные соединения, которые могут быть конденсированы с карбоновыми кислотами с получением майтанзиноидов. Например, реакция майтанзинола с (4S)-3,4-диметил-2,5-оксазолидиндионом (5а) приводит к образованию N2'-дезацетилмайтанзина (6а), который в свою очередь может быть конденсирован с 3-(метилдитио)пропионовой кислотой (7) с применением N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорида (EDAC) с образованием DM1-SMe (8), как показано ниже:
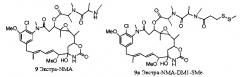
[7] Существенный недостаток указанной реакции ацилирования, в которой происходит образование сложных эфиров аминокислот и майтанзинола, заключается в том, что образуется также побочный продукт, содержащий лишний N-метилаланиловый фрагмент в С3 боковой цепи, который обозначен как «экстра-NMA» (9). При ацилировании N2'-дезацетилмайтанзина ацилируется также экстра-NMA (9) с образованием экстра-NMA-DM1-SMe (9а). Структуры экстра-NMA (9) и экстра NMA-DM1-SMe (9а) показаны ниже:
[8] DM1 (3) может быть получен из DM1-SMe (8) путем восстановления, в котором происходит также превращение экстра-NMA-DM1-SMe (9а) в экстра-NMA-DM1 (10), как показано ниже:
[9] Экстра-NMA-DM1 (10) трудно удалить из DM1 (3), поскольку оба соединения обладают схожей полярностью и дают перекрывающиеся пики при записи ВЭЖХ очищенного DM1 (3). DM1 (3) и DM4 (4) применяют для получения конъюгатов с антителами, несколько из которых в настоящее время проходят клинические испытания.
[10] Таким образом, существует необходимость в улучшении выхода и надежности способов получения таких майтанзиноидов и в минимизации количества побочных продуктов, образующихся во время реакций, используемых для их получения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[11] Было обнаружено, что добавление осушителя к реакции между майтанзинолом и N-карбоксиангидридом аминокислоты значительно увеличивает выход сложного эфира аминокислоты и майтанзинола, как показано в Примерах 1-4. Было также обнаружено, что добавление стадии предварительного гашения с применением нуклеофила, с последующим взаимодействием майтанзинола и N-карбоксиангидрида аминокислоты значительно снижает образование нежелательных побочных продуктов, таких как экстра-NMA, как показано в Примерах 6-8. На основании этих открытий в настоящем документе предложены улучшенные способы получения сложного эфира аминокислоты и майтанзинола.
[12] Первый вариант реализации настоящего изобретения представляет собой способ получения сложного эфира аминокислоты и майтанзинола, представленного Формулой (I):
,
где R1 представляет собой водород, необязательно замещенную C1-С10 алкильную группу или аминокислотную боковую цепь, при условии, что если указанная аминокислотная боковая цепь имеет функциональную группу, то эта функциональная группа является необязательно защищенной; и R2 представляет собой водород или необязательно замещенную C1-С10 алкильную группу.
[13] Указанный способ включает взаимодействие майтанзинола с N-карбоксиангидридом в реакционной смеси, дополнительно содержащей основание и осушитель. N-Карбоксиангидрид представлен следующей формулой:
.
Все переменные в Формуле (II) являются такими, как описано в Формуле (I).
[14] Второй вариант реализации настоящего изобретения представляет собой способ получения сложного эфира аминокислоты и майтанзинола, представленного Формулой (I), включающий: а) взаимодействие майтанзинола с N-карбоксиангидридом, представленным Формулой (II), в реакционной смеси, дополнительно содержащей основание; и b) взаимодействие непрореагировавшего N-карбоксиангидрида со стадии a) с нуклеофильным реагентом. Все переменные в Формулах (I) и (II) являются такими, как описано в первом варианте реализации настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигуры 1-2 представляют собой схематические изображения, иллюстрирующие ацилирование N2'-дезацетилмайтанзина карбоновой кислотой и конденсирующим агентом.
Фигуры 3-4 представляют собой схематические изображения, иллюстрирующие ацилирование N2'-дезацетилмайтанзина активированной карбоновой кислотой.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[15] Настоящее изобретение относится к способам получения сложного эфира аминокислоты, представленного Формулой (I), из майтанзинола и N-карбоксиангидрида, представленного Формулой (II). Сложный эфир аминокислоты может быть дополнительно эстерифицирован с получением майтанзиноидов, таких как DM1 и DM4, а затем может быть дополнительно преобразован в конъюгаты антител и майтанзиноида. Предпочтительно, сложный эфир аминокислоты представлен Формулой (Ia), а N-карбоксиангидрид представлен Формулой (IIa):
; и
.
Переменные в Формулах (Ia) и (IIa) являются такими, как описано для Формул (I) и (II).
[16] Предпочтительно, для Формул (I), (II), (Ia) и (IIa), R1 представляет собой боковую цепь природной аминокислоты, при условии, что если указанная боковая цепь имеет реакционноспособную функциональную группу, то эта функциональная группа является необязательно защищенной; и R2 представляет собой метил. Альтернативно, R1 представляет собой алкил, a R2 представляет собой метил. Более предпочтительно, оба R1 и R2 представляют собой метил.
[17] В первом варианте реализации настоящего изобретения указанный способ включает взаимодействие майтанзинола с N-карбоксиангидридом, представленным Формулой (II) или (IIa), в реакционной смеси, дополнительно содержащей основание и осушитель.
[18] В предпочтительном варианте реализации указанная реакционная смесь дополнительно содержит кислоту Льюиса. Предпочтительные кислоты Льюиса содержат катион металла.
[19] В другом предпочтительном варианте реализации сначала взаимодействуют майтанзинол и N-карбоксиангидрид, а затем реакционную смесь приводят в контакт с водным раствором, содержащим бикарбонат или карбонат, или реакционную смесь приводят в контакт с поглотителем металла. Можно использовать поглотители металла, известные в данной области техники (см., например, главу 9 в книге "The Power of Functional Resin in Organic Synthesis", автор Aubrey Mendoca, Wiley-VCH Verlag GmbH & Co. KGaA, 2008). Примеры поглотителей металлоа включают, но не ограничиваются ими, полимерные и кремнийсодержащие поглотители металла (например, QuadraPure™ и QuadraSil™ производства Sigma-Aldrich, SiliaMetS® производства SiliCycle, Smopex® производства Johnson Matthey и поглотители металла Biotage), углеродсодержащие поглотители (например, QuadraPure™ С производства Sigma-Aldrich).
[20] В другом предпочтительном варианте реализации сначала взаимодействуют майтанзинол и N-карбоксиангидрид, а затем из реакционной смеси удаляют катион металла из кислоты Льюиса. Например, катион металла из кислоты Льюиса удаляют из реакционной смеси приведением в контакт указанной реакционной смеси с водным раствором, содержащим бикарбонат или карбонат, или приведением в контакт реакционной смеси с поглотителем металла.
[21] Во втором варианте реализации указанный способ включает: а) взаимодействие майтанзинола с N-карбоксиангидридом, представленным формулой (II) или (IIa), в реакционной смеси, дополнительно содержащей основание; b) взаимодействие непрореагировавшего N-карбоксиангидрида со стадии а) с нуклеофильным реагентом.
[22] В одном предпочтительном варианте реализации реакционная смесь на стадии a) дополнительно содержит кислоту Льюиса. Предпочтительные кислоты Льюиса содержат катион металла.
[23] В другом предпочтительном варианте реализации реакционную смесь после стадии b) приводят в контакт с водным раствором, содержащим бикарбонат или карбонат, или с поглотителем металла.
[24] В другом предпочтительном варианте реализации катион металла из кислоты Льюиса удаляют из реакционной смеси после осуществления стадии b), т.е. после реакции нуклеофила с непрореагировавшим N-карбоксиангидридом. Например, катион металла из кислоты Льюиса удаляют из реакционной смеси приведением в контакт реакционной смеси с водным раствором, содержащим бикарбонат или карбонат, или приведением в контакт реакционной смеси с поглотителем металла.
[25] В другом предпочтительном варианте реализации реакционная смесь на стадии а) дополнительно содержит осушитель.
[26] Термин «основание» относится к веществу, которое принимает ионы водорода (протоны) или отдает пару валентных электронов. Иллюстративные основания не являются нуклеофильными и реакционноспособными в отношении N-карбоксиангидрида, представленного Формулой (II). Примеры подходящих оснований включают триалкиламин (например, диизопропилэтиламин, триэтиламин и 1,8-диазабициклоундец-7-ен), алкоксид металла (например, трет-бутоксид натрия и трет-бутоксид калия), алкилметалл (например, трет-бутиллитий, метиллитий, н-бутиллитий, трет-бутиллитий, лития диизопропиламид, пентилнатрий и 2-фенил-изопропилкалий), арилметалл (например, фениллитий), гидрид металла (например, гидрид натрия), амид металла (например, амид натрия, амид калия, диизопропиламид лития и тетраметилпиперидид лития) и кремнийсодержащий амид (например, натрия бис(триметилсилил)амид и калия бис(триметилсилил)амид). Предпочтительно, основание представляет собой триалкиламин. Более предпочтительно, основание представляет собой диизопропилэтиламин.
[27] Термин «осушитель» относится к агенту, который способен удалять воду из раствора. Примеры подходящего осушителя включают, но не ограничиваются ими, молекулярные сита, сульфат натрия, сульфат кальция, хлорид кальция и сульфат магния. Физические формы осушителей включают, но не ограничиваются ими, гранулированные шарики или порошки. Предпочтительно, осушитель представляет собой молекулярные сита. Альтернативно, осушитель представляет собой сульфат натрия.
[28] Термин «кислота Льюиса» относится к кислотному веществу, которое может использовать неподеленную электронную пару другой молекулы для завершения создания устойчивой группы одного из своих атомов. Иллюстративные кислоты Льюиса для применения в описанных способах включают трифлат цинка, хлорид цинка, бромид магния, трифлат магния, трифлат меди, бромид меди (II), хлорид меди (II) и хлорид магния. Предпочтительно, кислота Льюиса представляет собой трифлат цинка.
[29] Термин «нуклеофильный реагент» относится к реагенту, который взаимодействует с электроположительными центрами в N-карбоксиангидриде, представленном Формулой (II), с разрушением указанного N-карбоксиангидрида. Примеры подходящего нуклеофильного реагента включают воду, спирт (метанод, этанол, н-пропанол, изопропанол или трет-бутанол) и первичный или вторичный амин (например, метиламин, этиламин, диметиламин, диэтиламин и т.д.). Предпочтительно, нуклеофильный реагент представляет собой спирт. Альтернативно, нуклеофильный реагент представляет собой воду.
[30] Иллюстративные условия реакции для получения сложных эфиров аминокислот и майтанзинола, представленных Формулой (I), представлены ниже. Конкретные условия приведены в Примерах.
[31] Несмотря на то, что можно использовать эквимолярные количества майтанзинола относительно N-карбоксиангидрида, наиболее часто используют избыток N-карбоксиангидрида. Иллюстративные молярные отношения майтанзинола к N-карбоксиангидриду находятся в диапазоне от 1:1 до 1:10, более часто от 1:2 до 1:7 или от 1:1 до 1:4. В предпочтительном варианте реализации молярное отношение майтанзинола к N-карбоксиангидриду составляет около 1:5.
[32] В описанных способах необязательно используют кислоту Льюиса. При ее наличии она обычно используется в избытке относительно майтанзинола, например, в избытке, составляющем до 20 раз. Более часто молярное отношение майтанзинола к кислоте Льюиса находится в диапазоне от 1:5 до 1:8, более предпочтительно около 1:7. Также можно использовать меньшие количества кислоты Льюиса.
[33] Для удаления растворенной воды из растворителя реакционной смеси используют достаточные количества осушителей. Количество осушителя не критично, при условии, что реакционный раствор становится по существу безводным. Осушитель может быть использован непосредственно в реакционном сосуде или может находиться в сосуде с полупроницаемым барьером, таком как контейнер из пористого стекла.
[34] Время, необходимое для реакции, легко может контролировать специалист в данной области техники при помощи различных приемов, включая, но не ограничиваясь ими, высокоэффективную жидкостную хроматографию и тонкослойную хроматографию. Типичная реакция завершается после перемешивания в течение 24 часов, но может быть проведена с меньшей или большей скоростью в зависимости от различных факторов, таких как температура реакции и концентрации реагентов.
[35] Реакция может быть проведена при температуре от -20°С до 80°С, предпочтительно от -10°С до 60°С, более предпочтительно от -10°С до 40°С и наиболее предпочтительно от 0°С до 35°С.
[36] Подходящие растворители могут быть легко определены специалистами в данной области техники, и они включают, но не ограничиваются ими, полярные апротонные растворители, такие как безводный диметилформамид; диметилсульфоксид (ДМСО) или диметилацетамид (ДМА), гексаны, простые эфиры (такие как тетрагидрофуран, диэтиловый эфир, диметоксиэтан, диоксан), дихлорметан или их смеси.
[37] При наличии в реакционной смеси кислоты Льюиса, реакционную смесь после взаимодействия майтанзинола и N-карбоксиангидрида предпочтительно приводят в контакт с водным раствором, содержащим бикарбонат или карбонат, или с поглотителем металла. Предпочтительно, реакционная смесь взаимодействует с нуклеофильным реагентом для разложения избытка N-карбоксиангидрида до приведения в контакт реакционной смеси с водным раствором, содержащим бикарбонат или карбонат, или с поглотителем металла.
[38] При наличии в реакционной смеси кислоты Льюиса, содержащей катион металла, указанный катион металла предпочтительно удаляют из реакционной смеси в составе процедуры выделения продукта. Удаление катиона металла может быть осуществлено приведением в контакт реакционной смеси с водным раствором, содержащим бикарбонат или карбонат, или с поглотителем металла. Предпочтительно, N-карбоксиангидрид взаимодействует с нуклеофильным реагентом до удаления катиона металла.
[39] Количество нуклеофила на стадии b) может быть легко определено специалистом в данной области техники. Предпочтительно, используют достаточное количество нуклеофила для разложения непрореагировавшего N-карбоксиангидрида. Как правило, оно представляет собой эквимолярное количество нуклеофила, однако также можно использовать избыточные количества нуклеофила. Типичная реакция завершается после перемешивания в течение 1 часа, но она может быть проведена с меньшей или большей скоростью в зависимости от различных факторов, таких как температура.
[40] В рамки настоящего изобретения входит также способ ацилирования сложного эфира аминокислоты и майтанзинола. Указанный способ включает взаимодействие сложного эфира аминокислоты и майтанзинола, представленного Формулой (I) или Формулой (Ia), полученного так, как описано выше, с карбоновой кислотой, имеющей формулу «R3COOH», в присутствии конденсирующего агента или с активированной карбоновой кислотой, имеющей формулу «R3COX», с образованием соединения, представленного одной из следующих формул, соответственно:
и .
[41] В Формуле (III) или (IIIa) R1 и R2 являются такими, как описано в Формулах (I), (II), (Ia) и (IIa); R3 представляет собой алкильную группу или замещенную алкильную группу; и X в R3COX представляет собой уходящую группу. Предпочтительно, X представляет собой галогенид, алкокси-группу, арилокси-группу, имидазол, -S-фенил, где фенил необязательно замещено нитро или хлоридом, или -OCOR, где R представляет собой линейную C1-С10 алкильную группу, разветвленную C1-С10 алкильную группу, циклическую С3-С10 алкильную группу или C1-С10 алкенильную группу. В одном из вариантов реализации в формуле «R3COX», описанной выше, -СОХ представляет собой реакционноспособный сложный эфир; например, необязательно замещенный N-сукцинимидный эфир. Примеры реакционноспособного сложного эфира включают, но не ограничиваются ими, N-сукцинимидиловые, N-сульфосукцинимидиловые, N-фталимидиловые, N-сульфофталимидиловые, 2-нитрофениловые, 4-нитрофениловые, 2,4-динитрофениловые, 3-сульфонил-4-нитрофениловые и 3-карбокси-4-нитрофениловые эфиры.
[42] Предпочтительно, R3 представляет собой -Y-S-SR4, Y представляет собой С1-С10 алкилен, и R4 представляет собой C1-С10 алкил, арил или гетероарил. В другом альтернативном варианте Y представляет собой -СН2СН2- или -СН2СН2С(СН3)2-, и R4 представляет собой метил.
[43] В другом варианте реализации R3 представляет собой -L-E; L представляет собой или -(CH2CH2O)mCH2CH2NHC(=O)CH2CH2-, или ; Е представляет собой или , или или ; X' представляет собой галогенид; n равен 1, 2, 3, 4, 5 или 6; m равен 0 или целое число от 1 до 20; и q равен 0 или 1. Альтернативно, L представляет собой -(СН2)n-; и n является таким, как описано выше, или n равен 5. В другом альтернативном варианте L представляет собой а n и m являются такими, как описано выше; или, альтернативно, n равен 4, a m равен 3.
[44] В другом альтернативном варианте, R3 выбран из следующих формул:
; и
.
[45] Термин «конденсирующий агент» представляет собой реагент, который взаимодействует с гидроксильной группой карбоновой кислоты и превращает ее в уходящую группу, которая может быть вытеснена амино- или гидроксильной группой. Примеры подходящих конденсирующих агентов включают карбодиимид (N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорид), уроний, активный сложный эфир, фосфоний, 2-алкил-1-алкилкарбонил-1,2-дигидрохинолин (2-изобутокси-1-изобутоксикарбонил-1,2-дигидрохинолин), 2-алкокси-1~алкоксикарбонил-1,2-дигидрохинолин (2-этокси-1~этоксикарбонил-1,2-дигидрохинолин) или алкилхлорформиат (изобутилхлорформиат). Предпочтительно, конденсирующий агент представляет собой карбодиимид. Более предпочтительно, N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорид.
[46] Термин «уходящая группа» относится к группе заряженного или незаряженного фрагмента, которая может быть легко вытеснена нуклеофилом, таким как амин. Такие уходящие группы общеизвестны в данной области техники и включают, но не ограничиваются ими, галогениды, сложные эфиры, алкокси, гидроксил, алкокси, тозилаты, трифлаты, мезилаты, нитрилы, азиды, имидазол, карбамат, дисульфиды, сложные тиоэфиры, простые тиоэфиры (т.е. необязательно замещенный -S-фенил) и диазониевые соединения. Предпочтительно, уходящая группа представляет собой галогенид, алкокси-группу, арилокси-группу, имидазол, -S-фенил, необязательно замещенный группой -NO2 или хлором, или -OCOR, где R представляет собой линейную C1-С10 алкильную группу, разветвленную C1-С10 алкильную группу, циклическую С3-С10 алкильную группу или C1-С10 алкенильную группу. В другом предпочтительном варианте реализации уходящая группа представляет собой реакционноспособный сложный эфир (например, -СОХ), который может быть вытеснен. Реакционноспособные сложные эфиры включают, но не ограничиваются ими, N-сукцинимидиловый, N-сульфосукцинимидиловый, N-фталимидиловый, N-сульфофталимидиловый, 2-нитрофениловый, 4-нитрофениловый, 2,4-динитрофениловый, 3-сульфонил-4-нитрофениловый и 3-карбокси-4-нитрофениловый эфир.
[47] Настоящее изобретение включает также способ применения С3 сложного эфира майтанзинола для получения его производного. Указанный способ включает взаимодействие С3 сложного эфира майтанзинола, представленного Формулой (III) или (IIIa), полученного выше, с восстанавливающим агентом с образованием соединения, представленного одной из следующих формул:
и
[48] В Формуле (IV) и (IVa) R1 и R2 являются такими, как описано в Формулах (I), (II), (Ia) и (IIa); и Y является таким, как описано в Формуле (III) или (IIIa).
[49] Термин «восстанавливающий агент» представляет собой элемент или соединение в окислительно-восстановительной реакции, который превращает дисульфидную связь в гидросульфидную связь. Примеры подходящих восстанавливающих агентов включают дитиотреитол (DTT), (трис(2-карбоксиэтил)фосфин) (ТСЕР) и NaBH4.
[50] Соединение формулы (III) или (IIIa), если R3 представляет собой -L-E, или соединение формулы (IV) или (IVa) может взаимодействовать с антителом или модифицированным антителом с образованием конъюгата антитела и майтанзиноида. См., например, патенты США №7521541, 5208020 и 7811872. Альтернативно, соединение формулы (IV) или (IVa) может взаимодействовать с бифункциональным поперечно-сшивающим агентом с образованием линкерного соединения, содержащего реакционноспособную группу, которая может взаимодействовать с антителом с образованием конъюгата антитела и майтанзиноида. См., например, US 6441163, US 2011/0003969 А1 и US 2008/0145374.
[51] «Алкил», при использовании в настоящем документе, относится к линейному, разветвленному или циклическому алкилу.
[52] «Линейный или разветвленный алкил», при использовании в настоящем документе, относится к насыщенному линейному или разветвленному одновалентному углеводородному радикалу, содержащему от одного до двадцати атомов углерода. Примеры алкила включают, но не ограничиваются ими, метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-метил-1-пропил, -СН2СН(СН3)2, 2-бутил, 2-метил-2-пропил, 1-пентил, 2-пентил, 3-пентил, 2-метил-2-бутил, 3-метил-2-бутил, 3-метил-1-бутил, 2-метил-1-бутил, -CH2CH2CH(СН3)2, 1-гексил, 2-гексил, 3-гексил, 2-метил-2-пентил, 3-метил-2-пентил, 4-метил-2-пентил, 3-метил-3-пентил, 2-метил-3-пентил, 2,3-диметил-2-бутил, 3,3-диметил-2-бутил, 1-гептил, 1-октил и т.п. Предпочтительно, алкил имеет от одного до десяти атомов углерода. Более предпочтительно, алкил имеет от одного до четырех атомов углерода.
[53] «Алкилен», при использовании в настоящем документе, относится к линейному, разветвленному или циклическому алкилену.
[54] «Линейный или разветвленный алкилен», при использовании в настоящем документе, относится к насыщенному линейному или разветвленному двухвалентному углеводородному радикалу, содержащему от одного до двадцати атомов углерода. Примеры алкила включают, но не ограничиваются ими, метилен, этилен, 1-пропилен, 2-пропилен, 1-бутилен, 2-метил-1-пропилен, -CH2CH(СН3)2-, 2-бутилен, 2-метил-2-пропилен, 1-пентилен, 2-пентилен, 3-пентилен, 2-метил-2-бутилен, 3-метил-2-бутилен, 3-метил-1-бутилен, 2-метил-1-бутилен, -CH2CH2CH(СН3)2-, 1-гексил, 2-гексилен, 3-гексилен, 2-метил-2-пентилен, 3-метил-2-пентилен, 4-метил-2-пентилен, 3-метил-3-пентилен, 2-метил-3-пентилен, 2,3-диметил-2-бутилен, 3,3-диметил-2-бутилен, 1-гептилен, 1-октилен и т.п. Предпочтительно, алкилен имеет от одного до десяти атомов углерода. Более предпочтительно, алкилен имеет от одного до четырех атомов углерода.
[55] «Линейный или разветвленный алкенил» относится к линейному или разветвленному одновалентному углеводородному радикалу, содержащему от двух до двадцати атомов углерода по меньшей мере с одним центром ненасыщенности, т.е. двойной углерод-углеродной связью, при этом указанный алкенильный радикал включает радикалы, имеющие «цис» и «транс» ориентации или, альтернативно, «Е» и «Z» ориентации. Примеры включают, но не ограничиваются ими, этиленил или винил (-СН=CH2), аллил (-СН2СН=CH2) и т.п. Предпочтительно, алкенил имеет от двух до десяти атомов углерода. Более предпочтительно, алкенил имеет от двух до четырех атомов углерода.
[56] «Циклический алкил» относится к одновалентному насыщенному карбоциклическому кольцевому радикалу. Предпочтительно, циклический алкил представляет собой трех-десятичленный моноциклический кольцевой радикал. Более предпочтительно, циклический алкил представляет собой циклогексил.
[57] «Арил» означает одновалентный ароматический углеводородный радикал из 6-18 атомов углерода, полученный удалением одного атома водорода от одного атома углерода исходной ароматической кольцевой системы. Арил включает бициклические радикалы, содержащие ароматическое кольцо, конденсированное с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим или гетероциклическим кольцом. Типичные арильные группы включают, но не ограничиваются ими, радикалы, полученные из бензола (фенил), замещенных бензолов (например, пара-нитрофенил, орто-нитрофенил и динитрофенил), нафталина, антрацена, инденила, инданила, 1,2-дигидронафталина, 1,2,3,4-тетрагидронафтила и т.п. Предпочтительно, арил представляет собой необязательно замещенный фенил (например, фенил, фенол или защищенный фенол).
[58] «Гетероарил» относится к одновалентному ароматическому радикалу из 5- или 6-членных колец и включает конденсированные кольцевые системы (по меньшей мере одно из которых является ароматическим) из 5-18 атомов, содержащие один или более гетероатомов, независимо выбранных из азота, кислорода и серы. Примеры гетероарильных групп представляют собой пиридинил (например, 2-гидроксипиридинил), имидазолил, имидазопиридинил, пиримидинил (например, 4-гидроксипиримидинил), пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, триазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил.
[59] Подходящие заместители для алкильной группы представляют собой те, которые не оказывают существенного влияния на описанные реакции. Заместители, которые существенно не мешают описанным реакциям, могут быть защищенными в соответствии со способами, общеизвестными специалистам в данной области техники, например, в T.W. Greene и P.G.М. Wuts "Protective Groups in Organic Synthesis" John Wiley & Sons, Inc., Нью-Йорк, 1999. Иллюстративные заместители включают арил (например, фенил, фенол и защищенный фенол), гетероарил (например, индолил и имидазолил), галоген, гуанидиний [-NH(C=NH)NH2], -OR100, NR101R102, -ΝO2, -NR101COR102, -SR100, сульфоксид, представленный как -SOR101, сульфон, представленный как -SO2R101, сульфат -SO3R100, сульфонат -OSO3R100, сульфонамид, представленный как -SO2NR101R102, циано, азидо, -COR101, -OCOR101, -OCONR101R102; каждый R101 и R102 независимо выбран из Н, линейного, разветвленного или циклического алкила, алкенила или алкинила, имеющего от 1 до 10 атомов углерода.
[60] Термин «галогенид» относится к -F, -Cl, -Br или -I.
[61] Термин «аминокислота» относится к природным аминокислотам или неприродной аминокислоте, представленной как NH2-C(Raa'Raa)-C(=O)OH, где каждый Raa и Raa' независимо представляет собой Н, необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, имеющий от 1 до 10 атомов углерода, арил, гетероарил или гетероциклоалкил. Термин «аминокислота» относится также к соответствующему остатку, если один атом водорода удален из аминного и/или карбокси-конца аминокислоты, такому как -NH-C(Raa'Raa)-C(=O)O-. Конкретные примеры, представленные ниже, следует понимать только лишь как иллюстративные, но никоим образом не ограничивающие остальную часть настоящего описания. Без выполнения дополнительной разработки, предполагается, что на основании представленного описания специалисты в данной области техники могут применять настоящее изобретение в его самой полной мере. Все публикации, цитируемые в настоящем документе, в полном объеме включены в настоящий документ посредством ссылки. Кроме того, предложенный ниже механизм никоим образом не ограничивает рамки заявленного изобретения.
ПРИМЕРЫ
Материалы и способы
[62] Технологические параметры, представленные ниже, могут быть приняты и адаптированы специалистами в данной области техники для соответствия конкретным требованиям.
[63] Все реакции были проведены под атмосферой аргона при перемешивании на магнитной мешалке. Тетрагидрофуран и диметилформамид были приобретены в виде безводных растворителей у компании Aldrich. Майганзинол получили так, как описано ранее (Widdison et al., J. Med. Chem., 49: 4392-4408 (2006)). N-Карбоксиангидрид N-метилаланина, (4S)-3,4-диметил-2,5-оксазолидиндион получили так, как описано ранее (Akssira, M. et al., J. Marocain de Chimie Heterocyclique, 1:44-47 (2002)). Спектры ядерного магнитного резонанса (ЯМР) (1Н 400 МГЦ, 13C 100 МГц) записывали на приборе ЯМР Bruker серии ADVANCE™. Данные ВЭЖХ/МС получили при помощи масс-спектрометрической ионной ловушки Bruker ESQUIRE™ 3000 вместе с ВЭЖХ прибором Agilent серии 1100. Для анализа DM1 использовали способ 1 ВЭЖХ. Для всех остальных анализов использовали способ 2 ВЭЖХ.
[64] Аналитический способ 1 ВЭЖХ:
Водная ВЭЖХ система с УФ-детектором или эквивалентом
Колонка: YMC-Pack ODS-AQ 250×4,6 мм; 5 мкм (№ детали = AQ12S05-2546WT)
Поток: 1 мл/мин (градиент)
Подвижная фаза: А=1 мл 85% Н3РО4 в 1 литре воды; В = ацетонитрил / тетрагидрофуран, 30:70 (об./об.) (примечание: в анализе ЖХ/МС в подвижной фазе А использовали 0,1% ТФК вместо H3PO4
Таблица градиента:
Время записи хроматограммы: 60 минут + время восстановления колонки: 10 минут
УФ-обнаружение: 252 нм
Объем введенной пробы = 5 мкл приблизительно 1 мг/мл раствора DM1 в ацетонитриле
Температура колонки = 15°C (если не указано иное)
Температура образца = 2-8°C
[65] Аналитический способ 2 ВЭЖХ/МС:
Колонка: 150×4,6 мм С8, размер частиц 5 микрон, Zorbax Ρ/Ν 993967-906
Растворители: А деионизированная вода + 0,1% ТФК
Растворитель В: ацетонитрил
Скорость потока 1,0 мл/мин. Температура: окружающей среды
Объем введенной пробы: 15 мкл
Градиент
| Время | %В |
| 0 | 25 |
| 25 | 50 |
| 26 | 95 |
| 30 | 95 |
| 31 | 25 |
| 37 | 25 |
Данные отображали для 0-25 мин записи ВЭЖХ.
[66] Получение образца для аналитического способа 2 ВЭЖХ:
Аликвоты (20 мкл) данной смеси добавляли к ацетонитрилу (1,5 мл) в пробирке автоматического пробоотборника. Пробирку закрывали и встряхивали, затем помещали в автоматический пробоотборник при 15°C. Для каждого анализа ВЭЖХ анализировали объем вводимой пробы (15 мкл).
Пример 1. Получение DM1-SMe с добавлением молекулярных сит 4А в качестве осушителя
[67] Майтанзинол (50,1 мг, 0,0888 ммоль), (4S)-3,4-диметил-2,5-оксазолидиндион (30,2 мг, 0,233 ммоль, 2,6 экв.), трифлат цинка (133 мг, 0,366 моль) и молекулярные сита 4А (0,50 г), предварительно высушенные при 250°C под вакуумом, затем охлажденные до комнатной температуры, добавляли в 10 мл колбу. Содержимое растворяли в безводном диметилформамиде (0,75 мл), к которому добавляли диизопропилэтиламин (62 мкл, 0,357 ммоль). Смесь перемешивали при температуре окружающей среды в течение 24 часов. Образец неочищенной смеси анализировали при помощи ВЭЖХ, содержание продукта, N2'-дезацетилмайтанзина, составляло 80% от общей площади ВЭЖХ. Реакционную смесь разбавляли 1:1 смесью насыщенного раствора NaHCO3 : насыщенного раствора NaCl (1,2 мл) и этилацетатом (3 мл), перемешивали, затем отфильтровывали через целит, затем промывали фосфатно-калиевым буферным раствором (1 мл, 400 мМ, рН 7,5). Органический слой высушивали при помощи безводного сульфата магния, отфильтровывали, затем выпаривали с получением желтого твердого вещества. К этому твердому веществу добавляли 3-метилдитиопропановую кислоту (25 мг, 0,16 ммоль), N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорид (30 мг, 0,16 ммоль) и дихлорметан (3 мл). После перемешивания в течение 2 часов смесь разбавляли этилацетатом (8 мл), промывали 1,0 фосфатно-калиевым буферным раствором с рН 6,5 (2 мл), а водный раствор экстрагировали этилацетатом (2×8 мл). Органические слои объединяли, высушивали над безводным сульфатом магния, концентрировали и очищали хроматографией на силикагеле используя 95:5 смесь дихлорметана: метанола с получением 51 мг (70%) DM1-SMe.
Пример 2. 10-кратное масштабирование примера 1
[68] Реакцию Примера 1 выполняли в 10 раз более крупном масштабе, получая 490 мг (68%) DM1-SMe.
Пример 3. Получение DM1-SMe без добавления осушителя
[69] Майтанзинол (1,0 г, 1,77 ммоль) растворяли в безводном диметилформамиде (15 мл) в 25 мл колбе, которую охлаждали на бане со льдом и водой. Через 2 минуты добавляли диизопропилэтиламин (DIPEA, 0,92 г, 7,07 ммоль) и трифлат цинка (3,8 г, 10,6 ммоль) при перемешивании с помощью магнитной мешалки, затем быстро добавляли (4S)-3,4-диметил-2,5-оксазолидиндион (0,913 г, 7,07 ммоль) и перемешивали смесь в течение 24 часов. Образец неочищенной смеси анализировали при помощи ВЭЖХ, содержание продукта, N2'-дезацетилмайтанзина составляло 65% от общей площади ВЭЖХ. Реакционную смесь разбавляли 1:1 смесью насыщенного раствора NaHCO3 : насыщенного раствора NaCl (25 мл) и этилацетатом (40 мл), перемешивали, затем отфильтровывали через целит и промыли насыщенным раство