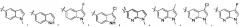Производные 2,4-дизамещенного фенилен-1,5-диамина и их применения, фармацевтические композиции и фармацевтически приемлемые композиции, полученные из них
Иллюстрации
Показать всеИзобретение относится к новому производному 2,4-замещенного фенилен-1,5-диамина формулы (I) или его фармацевтически приемлемой соли, обладающим активностью ингибитора в отношении тирозинкиназы EGFR. Соединения могут найти применение для изготовления лекарственного средства для регулирования активности тирозинкиназы EGFR (рецептора эпидермального фактора роста) или лечения EGFR-зависимых заболеваний. Таким заболеванием являются рак, диабет, заболевания иммунной системы, нейродегенеративные заболевания, сердечно-сосудистые заболевания или заболевание с приобретенной резистентностью в ходе лечения с использованием модуляторов EGFR. При этом заболевание с приобретенной резистентностью обусловлено мутациями Т790, кодируемыми 20-м экзоном EGFR, или содержанием мутаций Т790, кодируемых 20-м экзоном EGFR. В соединении формулы (I)
А является любым, выбранным из или
где Z2 представляет собой CR5 или N; R5 представляет собой водород; Z21 представляет собой N; каждый из R4, R42, R43 независимо представляет собой водород или C1-6 алкил, 6-членный гетероциклоалкил, содержащий группу -NH в кольце или C1-6 галогеналкил; R41 представляет собой водород или галоген; R0 представляет собой водород; Z1 представляет собой CR6, где R6 представляет собой водород, галоген, трифторметил, метокси или -СО2С1-10 алкил; R1 представляет собой водород или является любым, выбранным из группы, состоящей из:
каждый из R2 и R3 независимо представляет собой водород; R12 представляет собой С1-6 алкокси. 3 н. и 6 з.п. ф-лы, 9 табл., 127 пр.
Реферат
Область техники
Настоящее изобретение относится к области медицинской техники, в частности к производным 2,4-дизамещенного бензол-1,5-диамина и их применениям в качестве ингибиторов тирозинкиназы рецептора эпидермального фактора роста (EGFR), а также к полученным из них фармацевтическим композициям и лекарственным композициям.
Предшествующий уровень техники
Рак легкого является самым распространенным заболеванием в мире. В Китае заболеваемость раком легких занимает первое место среди всех раковых заболеваний, и заболеваемость и смертность от рака также являются самыми высокими в Китае. В Китае 30% пациентов с раком легких имеют мутации EGFR, более 90% которых представляют собой мутацию L858R и делецию в 19-м экзоне, и эти пациенты являются более чувствительными к ингибиторам EGFR. Имеющееся в продаже первое поколение ингибиторов EGFR, таких как эрлотиниб, гефитиниб, оказывает положительное воздействие на этих пациентов, опухоль у более чем 60% пациентов уменьшается в размере, значительно продлевая выживаемость без прогрессирования заболевания. Однако у большинства пациентов формируется резистентность в течение 6-12 месяцев, первое поколение ингибиторов EGFR более не оказывает воздействия, и в настоящее время не существует никаких лекарств для таких пациентов. У 50% пациентов, демонстрирующих резистентность к первому поколению ингибиторов EGFR, клинически обнаруживается мутация EGFR Т790М. В клеточной линии Н1975, несущей мутацию Т790М, активность первого поколения ингибиторов EGFR, таких как гефитиниб и эрлотиниб, была больше чем 3 мкм, что означает практически отсутствие активности.
У пациентов, страдающих раком легких, с мутациями EGFR терапевтический эффект второго поколения необратимых ингибиторов пан-EGFR (Афатиниб (BIBW2992)), запущенных в производство в настоящее время, был значительно лучше, чем терапевтический эффект первого поколения ингибиторов EGFR. Однако второе поколение ингибиторов EGFR обладает также сильной ингибирующей активностью в отношении EGFR дикого типа, причем ингибирующая активность в отношении EGFR дикого типа была значительно выше, чем ингибирующая активность в отношении резистентной мутации Т790М, и у пациентов наблюдались серьезные побочные эффекты, такие как сыпь на коже, и воздействие второго поколения ингибиторов на пациентов с лекарственной резистентностью было слабым, только небольшая часть пациентов с резистентностью к первому поколению ингибиторов EGFR отвечала на лечение этими лекарствами.
Для повышения ингибирующей активности в отношении резистентной мутации Т790М с одновременным снижением ингибирующей активности в отношении EGFR дикого типа большое значение имеет разработка третьего поколения селективных ингибиторов для мутантов EGFR с более высокой активностью, лучшей селективностью и более низкой токсичностью.
Краткое описание изобретения
Целью настоящего изобретения является обеспечение производных 2,4-дизамещенного бензол-1,5-диамина или их фармацевтически приемлемой соли, стереоизомера, сольвата или пролекарства; а также фармацевтической композиции, включающей вышеупомянутое производное.
Второй целью настоящего изобретения является обеспечение применения вышеуказанного производного или композиции для получения лекарственного средства для регулирования активности тирозинкиназы EGFR или лечения EGFR-зависимых заболеваний.
В первом аспекте настоящего изобретения предложено соединение формулы (I) или его фармацевтически приемлемая соль, стереоизомер, сольват или пролекарство:
где А является любым, выбранным из:
или ;
где Z2 представляет собой CR5 или N; R5 представляет собой водород, галоген, трифторметил или С1-10 алкокси; Z21 представляет собой N или СН; каждый из R4, R42, R43 независимо представляет собой водород или С1-10 алкил, С3-10 циклоалкил, С3-10 гетероциклоалкил (например пиперидинил) или С1-10 галогеналкил; R41 представляет собой водород, галоген, трифторметил, С1-10 алкил или С1-10 алкокси; (предпочтительно, каждый из R4, R42, R43 независимо представляет собой водород, метил или этил; R41 представляет собой водород, хлор, фтор, трифторметил, метил или метокси); каждый из R1', R2' и R5' независимо представляет собой водород, С1-10 алкил; (предпочтительно, каждый из R1', R2' и R5' независимо представляет собой водород, метил или этил); каждый из R3', R4' независимо представляет собой водород, С1-10, или R3' и R4' образуют мостиковую кольцевую структуру; (предпочтительно, каждый из R3', R4' независимо представляет собой водород, метил или этил; или R3' и R4' образуют -СН2-); Y представляет собой О, СН2, NRa'; где Ra' представляет собой водород, метил, трет-бутокси карбон ил, ацетил, метилсульфонил; и n равно 0 или 1;
R0 представляет собой водород, галоген, С1-10 алкил, -NRaRb или -CO-NRaRb, где каждый из Ra, Rb независимо представляет собой С1-10 алкил;
Z1 представляет собой CR6 или N; где R6 представляет собой водород, галоген, трифторметил, метокси или -CO2C1-10 алкил;
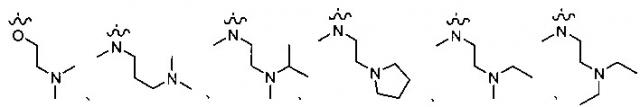
R1 представляет собой водород, или является любым, выбранным из группы, состоящей из:
,
или
;
каждый или R2 и R3 независимо представляет собой водород или -CH2NR7R8; где (1) каждый из R7, R8 независимо представляет собой водород или метил; или (2) R7 и R8 вместе с атомом азота, к которому они присоединены, образуют 5-6-членное азотсодержащее насыщенное гетероциклическое кольцо;
R12 представляет собой водород, галоген, С1-10 алкил или С1-10 алкокси (предпочтительно метокси).
В другом предпочтительном варианте осуществления А формулы (I) является любым, выбранным из группы, состоящей из:
;
где n, R4, R41, R42, R43, R1', R2', R3', R4', R5', Ra' являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления R4 формулы (I) представляет собой водород, метил, этил, изопропил, циклопропил, дифторметил или пиперидинил; R41 представляет собой водород, хлор, фтор, трифторметил, метил или метокси; R42 представляет собой водород, метил или этил; R43 представляет собой водород, метил или этил.
В другом предпочтительном варианте осуществления каждый из R2 и R3 формулы (I) независимо представляет собой водород; и R12 представляет собой метокси.
В другом предпочтительном варианте осуществления Z1 формулы (I) представляет собой CR6 or N; где R6 представляет собой водород, фтор, хлор, трифторметил, метокси или -СО2С1-10 алкил;
В другом предпочтительном варианте осуществления Z1 формулы (I) представляет собой CR6, где R6 представляет собой водород, фтор, хлор, трифторметил, метокси или -СО2СН3,
В другом предпочтительном варианте осуществления R0 формулы (I) представляет собой водород.
В другом предпочтительном варианте осуществления А формулы (I) является любым, выбранным из группы, состоящей из:
,
,
и
; при этом и могут быть и соответственно.
В другом предпочтительном варианте осуществления каждый из R2 and R3 формулы (I) независимо представляет собой водород.
В другом предпочтительном варианте осуществления каждый из R2 and R3 формулы (I) независимо представляет собой водород или -CH2NR7R8, и каждый из R7 и R8 независимо представляет собой водород или метил.
В другом предпочтительном варианте осуществления каждый из R2 и R3 формулы (I) независимо представляет собой водород, или -CH2NR7R8, и R7 и R8 вместе с атомом азота, к которому они присоединены, образуют 5-6-членное насыщенное азотсодержащее гетероциклическое кольцо.
В другом предпочтительном варианте осуществления каждый из R2 и R3 формулы (I) независимо представляет собой водород или -CH2NR7R8, и R7 и R8 вместе с соседним атомом азота образуют 5-6-членное азотсодержащее насыщенное гетероциклическое кольцо, и структура 5-6-членного азотсодержащего насыщенного гетероциклического кольца представлена формулой (III):
где X представляет собой О, S, NR9 или CR10R11; где каждый из R9, R10, R11 независимо представляет собой водород, С1-10 алкокси или -СО-С1-10 алкил.
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (IV-1):
где A, R0, R1, R2, R3 и R6 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (IV-2):
где A, R0, R1, R2 и R3 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (V-1):
где R1, R2, R3, R4, R41 и R6 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (V-2):
где R1, R2, R3, R4 и R41 являются такими как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (VI-1):
где R1, R2, R3, R4, R41 и R6 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (VI-2):
где R1, R2, R3, R4 и R41 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (VII-1):
где R1, R2, R3 и R6 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) показано в формуле (VII-2):
где R1, R2 и R3 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение, представленное формулой (VIII-1):
где R1', R2', R3', R4', R5', R1, R2, R3, R6 и Y являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение, представленное формулой (VIII-2):
где R1', R2', R3', R4', R5', R1, R2, R3 и Y являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (IX-1):
где R1', R2', R4', R5', R1, R2, R3 и R6 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (IX-2):
где R1', R2', R4', R5', R1, R2 и R3 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (Х-1):
где R1', R5', R1, R2, R3 и R6 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (Х-2):
где R1', R5', R1, R2 и R3 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (XI-1):
где R1, R2, R3, R4, R42, R43 и R6 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (XI-2):
где R1, R2, R3, R4, R42 и R43 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления, соединение формулы (I) представляет собой соединение формулы (XII-1):
где R1, R2, R3, R4, R41 и R6 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления соединение формулы (I) представляет собой соединение формулы (XII-2):
где R1, R2, R3, R4 и R41 являются такими, как определено в формуле (I).
В другом предпочтительном варианте осуществления в соединении формулы (XI-1) R6 представляет собой водород, фтор, хлор или трифторметил.
В другом предпочтительном варианте осуществления в соединении формулы (XI-1) или формулы (XI-2) каждый из R2 и R3 независимо представляет собой водород.
В другом предпочтительном варианте осуществления в соединении формулы (XI-1) или формулы (XI-2) R1 выбирают из:
или .
В другом предпочтительном варианте осуществления в соединении формулы (XI-1) или формулы (XI-2) каждый из R4, R42, R43 независимо представляет собой водород, С1-10 алкил, С1-10 галогеналкил или пиперидинил;
В другом предпочтительном варианте осуществления в соединении формулы (XI-1) или формулы (XI-2) каждый из R4, R42 и R43 независимо представляет собой водород, метил, этил, дифторметил или пиперидинил.
В другом предпочтительном варианте осуществления в соединении формулы (XI-1) или формулы (XI-2) R4 представляет собой водород, метил, дифторметил или пиперидинил и каждый из R42, R43 независимо представляет собой водород или метил.
В другом предпочтительном варианте осуществления в соединении формулы (V-1), формулы (V-2), формулы (VI-1), формулы (VI-2), формулы (XII-1) или формулы (XII-2) R4 представляет собой водород, С1-10 алкил, С3-10 циклоалкил или С1-10 галогеналкил.
В другом предпочтительном варианте осуществления в соединении формулы (V-1), формулы (V-2), формулы (VI-1), формулы (VI-2), формулы (XII-1) или формулы (XII-2) R4 представляет собой водород, метил, этил, изопропил, циклопропил или дифторметил.
В другом предпочтительном варианте осуществления в соединении формулы (V-1), формулы (V-2), формулы (VI-1), формулы (VI-2), формулы (XII-1) или формулы (XII-2) R41 представляет собой водород, хлор, фтор, трифторметил, метил или метокси.
В другом предпочтительном варианте осуществления в соединении формулы (V-1), формулы (V-2), формулы (VI-1), формулы (VI-2), формулы (XII-1) или формулы (XII-2) каждый из R2 и R3 независимо представляет собой водород.
В другом предпочтительном варианте осуществления в соединении формулы (V-1), формулы (VI-1) или формулы (XI1-1) R6 представляет собой водород, фтор, хлор, трифторметил, метокси или -CO2CH3,
В другом предпочтительном варианте осуществления в соединении формулы (V-1), формулы (V-2), формулы (VI-1), формулы (VI-2), формулы (XII-1) или формулы (XII-2) R1 выбирают из:
,
или .
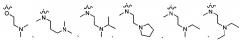
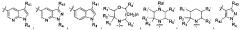
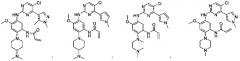
В другом предпочтительном варианте осуществления соединение выбирают из:
,
,
,
,
,
,
,
,
,
,
,
,
,
,
,
,
,
,
,
,
или ,
,
или .
Во втором аспекте настоящего изобретения предложена фармацевтическая композиция, включающая соединение по первому аспекту настоящего изобретения или его фармацевтически приемлемую соль, стереоизомер, сольват или пролекарство, и фармацевтически приемлемый носитель.
В другом предпочтительном варианте осуществления фармацевтическая композиция включает терапевтически эффективное количество соединения по первому аспекту настоящего изобретения, такого как соединения формулы (I), соединения формулы (IV-1), соединения формулы (IV-2), соединения формулы (V-1), соединения формулы (V-2), соединения формулы (VI-1), соединения формулы (VI-2), соединения формулы (VII-1), соединения формулы (VII-2), соединения формулы (VIII-1), соединение формулы (VIII-2), соединения формулы (IX-1), соединения формулы (IX-2), соединения формулы (Х-1), соединения формулы (Х-2), соединения формулы (XI-1), соединения формулы (XI-2) или указанных выше иллюстративных соединений, или их фармацевтически приемлемых солей, стереоизомеров, сольватов или пролекарств, и фармацевтически приемлемые носители.
Как правило, соединение по настоящему изобретению или его фармацевтически приемлемая соль может образовывать подходящую лекарственную форму для введения с одним или несколькими фармацевтически приемлемыми носителями. Эти лекарственные формы пригодны для перорального, ректального, местного, интраорального введения и другого парентерального введения (например подкожного, внутримышечного, внутривенного введения и т.д.). Например, лекарственные формы, пригодные для перорального введения, включают капсулы, таблетки, гранулы и сиропы. Соединения по настоящему изобретению, содержащиеся в этих лекарственных формах, могут представлять собой твердые порошки или гранулы; водные или неводные жидкие растворы или суспензии; эмульсии вода-в-масле или масло-в-воде. Такие лекарственные формы могут быть получены с активными соединениями и одним или несколькими носителями или эксципиентами с помощью обычных фармацевтических способов. Вышеупомянутые носители должны быть совместимы с активными веществами или другими наполнителями. В твердых лекарственных формах обычные нетоксичные носители включают в себя, но не ограничиваются ими, маннит, лактозу, крахмал, стеарат магния, целлюлозу, глюкозу, сахарозу и тому подобное. Носители, используемые для жидких препаратов, включают воду, физиологический раствор, водную декстрозу, этиленгликоль и полиэтиленгликоль. Активные соединения могут образовывать раствор или суспензию с вышеупомянутыми носителями.
Композиции по настоящему изобретению составляют, количественно измеряют и вводят способом в соответствии с медицинской практикой. "Эффективное количество" вводимого соединения зависит от таких факторов, как конкретное подлежащее лечению заболевание, индивидуум, который подвергается лечению, причина заболевания, мишень лекарственного средства и способ введения и т.д.
В третьем аспекте настоящего изобретения предложено применение соединения по первому аспекту настоящего изобретения или его фармацевтически приемлемой соли, стереоизомера, сольвата или пролекарства для получения лекарственного средства для регулирования активности тирозинкиназы EGFR или лечения EGFR-зависимых заболеваний.
Предпочтительно, EGFR-зависимое заболевание представляет собой рак, диабет, заболевания иммунной системы, нейродегенеративные заболевания или сердечно-сосудистые заболевания.
Предпочтительно, рак представляет собой немелкоклеточный рак легкого, рак головы и шеи, рак молочной железы, рак почки, рак поджелудочной железы, рак шейки матки, рак пищевода, рак поджелудочной железы, рак предстательной железы, рак мочевого пузыря, рак толстой и прямой кишки, рак яичника, рак желудка, злокачественные опухоли мозга, в том числе глиобластому и т.д., или любую их комбинацию.
Предпочтительно, немелкоклеточный рак легкого обусловлен мутациями EGFR, в том числе чувствительными мутациями (такими как мутация L858R или делеции в 19-м экзоне) и резистентными мутациями (такими как мутация EGFR Т790М).
Предпочтительно, соединение или его фармацевтически приемлемая соль, стереоизомер, сольват или пролекарство могут также быть применены для получения лекарственного средства для лечения заболевания с аномальной экспрессией EGFR, или заболевания, которое приобрело резистентность в ходе лечения с использованием модуляторов EGFR.
Предпочтительно, приобретенная резистентность представляет собой резистентность, обусловленную мутациями Т790, кодированными 20-м экзоном EGFR, или содержанием мутаций Т790, кодированных 20-м экзоном EGFR, таких как Т790М.
В настоящем изобретении термин модулятор EGFR относится к низкомолекулярному ингибитору тирозинкиназы, нацеленному на EGFR, такому как гефитиниб, эрлотиниб, икотиниб, лапатиниб или афатиниб.
В четвертом аспекте настоящего изобретения предложена фармацевтическая композиция, включающая терапевтически эффективное количество соединения по первому аспекту настоящего изобретения или его фармацевтически приемлемой соли, стереоизомера, сольвата или пролекарства, а также одно или более других лекарственных средств, выбранных из группы, состоящей из гефитиниба, эрлотиниба, икотиниба, лапатиниба, XL647, NVP-AEE-788, ARRY-334543, EKB-569, BIBW2992, HKI272, ВМС-690514, CI-1033, вандетаниба, PF00299804, WZ4002, цетуксимаба, трастузумаба, панитумумаба, матузумаба, нимотузумаба, залутумумаба, пертузумаба, MDX-214, CDX-110, IMC-11F8, Zemab, вакцины Her2 РХ 1041, ингибиторов HSP90, CNF2024, танеспимицина, алвеспимицина, IPI-504, SNX-5422, NVP-AUY922 или их комбинаций.
В дополнение к соединению по настоящему изобретению или его фармацевтически приемлемой соли, стереоизомеру, сольвату или пролекарству, другие лекарственные средства в фармацевтической композиции, описанной выше, представляют собой противоопухолевые средства, хорошо известные специалистам в данной области техники.
В настоящей заявке термин "терапевтически эффективное количество" относится к количеству, обеспечивающему функцию или активность в отношении людей и/или животных, и переносимому людьми и/или животными.
Терапевтически эффективное количество соединения по настоящему изобретению или его фармацевтически приемлемой соли, стереоизомера, сольвата или пролекарства, содержащееся в фармацевтической композиции или лекарственной композиции по настоящему изобретению, составляет предпочтительно от 0,1 мг - 5 г/кг (масса).
Фармацевтические композиции по настоящему изобретению могут быть использованы для лечения EGFR-зависимых заболеваний, таких как рак, диабет, нарушения иммунной системы, нейродегенеративные заболевания или сердечно-сосудистые заболевания, или для лечения заболевания с приобретенной резистентностью в ходе лечения с помощью модулятора EGFR.
Заболевание с приобретенной резистентностью обусловлено мутациями Т790, кодированными 20-м экзоном EGFR, или содержанием мутаций Т790, кодированных 20-м экзоном EGFR.
В другом предпочтительном варианте осуществления мутация Т790, кодированная 20-м экзоном EGFR, представляет собой Т790М.
При определенных заболеваниях для достижения желаемого терапевтического эффекта соединения по настоящему изобретению могут быть использованы в комбинации с другими лекарствами. Примером такого заболевания является немелкоклеточный рак легких (NSCLC). Например, терапевтически эффективное количество соединения формулы I по настоящему изобретению используют в комбинации с ингибиторами mTOR (мишени рапамицина млекопитающих) (например рапамицином); или ингибиторами Met (включая Met антитела MetMAb (моноклональные антитела) и низкомолекулярные ингибиторы Met PF02341066) MS; или ингибиторами IGF1R (рецептора инсулиноподобного фактора роста 1) (например OSI-906); или ингибиторами белков теплового шока и тому подобное.
Следует понимать, что каждый из указанных выше технических признаков изобретения и каждый технический признак, в частности описанный ниже (например в Примерах), может быть скомбинирован с другим в пределах объема настоящего изобретения для создавать новых или предпочтительных технических решений.
Подробное описание изобретения
В ходе долгого и интенсивного исследования изобретатели неожиданно обнаружили класс селективных ингибиторов мутаций EGFR. Анализы in vitro показали, что селективные ингибиторы в наномолярных концентрациях могут ингибировать двойной мутантный фермент EGFR T790M/L858R и пролиферацию клеточной линии Н1975, а также демонстрируют высокую ингибирующую активность в отношении EGFR чувствительной мутантной клеточной линии НСС827 (делеция в 19-м экзоне), но имеют относительно слабую ингибирующую активность в отношении фермента EGFR дикого типа и клеточной линии А431, Таким образом, соединения с такими структурами могут быть использованы не только для лечения EGFR чувствительного мутантного рака, но и для лечения случаев вторичной резистентности, генерируемых в ходе проводимой в настоящее время терапии EGFR-TKI (EGFR-ингибитор тирозинкиназы); в то же время, побочные эффекты, вызванные ингибированием EGFR дикого типа, значительно снижаются вследствие мутантной селективности соединений. Кроме того, эти соединения проявляют низкую цитотоксичность в нормальных клетках (таких как клетки 3Т3), тем самым значительно уменьшая неспецифические побочные эффекты, и являются идеальными заменителями второго поколения EGFR-TKI.
Значения терминов
В настоящей заявке термин "С1-10 алкил" относится к прямой или разветвленной насыщенной алифатической углеводородной группе, имеющей от 1 до 10 атомов углерода, например метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, гептил, октил, нонил, децил и тому подобное.
В настоящей заявке термин "С1-10 алкокси" относится к С1-10 алкил -О-, например метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси и тому подобное.
В настоящей заявке термин "галоген" обозначает фтор, хлор, бром или йод.
В настоящей заявке термин "С3-10 циклоалкил" относится к насыщенному или частично ненасыщенному моноциклическому или полициклическому циклическому углеводородному заместителю, содержащему от 3 до 10 атомов углерода, предпочтительно циклоалкилу, содержащему от 3 до 8 атомов углерода (С3-8 циклоалкил), наиболее предпочтительно к циклоалкилу, содержащему от 3 до 6 атомов углерода (С3-6 циклоалкил). Неограничивающие примеры моноциклического циклоалкила включают циклопропил, циклобутил, циклопентил, циклопентенил, циклогексил, циклогексенил, циклогексадиенил, циклогептил, циклогептатриенил и циклооктил, предпочтительно циклопропил, циклопентил, циклогексенил. Полициклический циклоалкил включает спиро-кольцо, конденсированное кольцо и мостиковое кольцо.
В настоящей заявке термин "С3-10 гетероциклоалкил" относится к насыщенному или частично ненасыщенному моноциклическому или полициклическому циклическому углеводородному заместителю, содержащему от 3 до 10 кольцевых атомов, где один или несколько кольцевых атомов представляют собой гетероатомы, выбранные из азота, кислорода или S(O)t (где t представляет собой целое число от 0 до 2), и другие кольцевые атомы представляют собой углерод, но С3-10 гетероциклоалкил не включает в себя кольцевой фрагмент, такой, как -О-О-, -O-S- или -S-S-. Предпочтительно, гетероциклоалкил включает от 3 до 8 кольцевых атомов, где от 1 до 3 кольцевых атомов представляют собой гетероатомы, предпочтительно, гетероциклоалкил, содержащий от 3 до 6 кольцевых атомов, и, более предпочтительно, гетероциклоалкил, включающий от 5 до 6 кольцевых атомов. Неограничивающие примеры моноциклических гетероциклических групп включают пирролидинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, гомопиперазинил, пиранил, тетрагидрофуранил и тому подобное. Полициклический гетероциклоалкил включает в себя спиро-кольцо, конденсированное кольцо и мостиковое кольцо.
В настоящей заявке термин "С1-10 галогеналкил" относится к алкилу, замещенному 1, 2, 3, 4 или 5 атомами галогена, где алкил является таким, как определено выше, предпочтительно представляет собой С1-10 галогеналкил, более предпочтительно С1-6 галогеналкил и наиболее предпочтительно С1-3 галогеналкил, в том числе (но не ограничиваясь этим) хлорэтил, дихлорметил, 1,2-дихлорэтил, бромэтил, фторэтил, фторметил, дифторметил, трифторметил и тому подобное.
Активные ингредиенты
Термин "активный материал по настоящему изобретению" или "активное соединение по настоящему изобретению" относится к соединению формулы (I) по настоящему изобретению или его фармацевтически приемлемой соли, или его сольвату, или его стереоизомеру, или его пролекарству, обладающему значительной ингибирующей активностью в отношении резистентности к мутации EGFR Т790М (в частности двойной мутации EGFR T790M/L858R).
В настоящей заявке термин "фармацевтически приемлемая(ые) соль(и)" включает в себя фармацевтически приемлемую(ые) соль(и) присоединения кислоты и соль(и) присоединения основания. "Фармацевтически приемлемые соли присоединения кислоты" относятся к солям, которые способны сохранять биологическую эффективность свободного основания без других побочных эффектов и образованы с неорганическими или органическими кислотами. Соли неорганических кислот включают, но не ограничиваются ими, гидрохлорид, гидробромид, сульфат, фосфат и тому подобное; соли органических кислот включают в себя, но не ограничиваются ими, формиат, ацетат, пропионат, гликолят, глюконат, лактат, оксалат, малеат, сукцинат, фумарат, тартрат, цитрат, глутамат, аспартат, бензоат, метансульфонат, п-толуолсульфонат, салицилат и т.п. Эти соли могут быть получены способами, известными в данной области техники. "Фармацевтически приемлемые соли присоединения основания" включают в себя, но не ограничиваются ими, соли неорганических оснований, такие как соли натрия, калия, кальция и магния, или включают в себя, но не ограничиваются ими, соли органических оснований, таких как соль аммония, соль триэтиламина, соль лизина, соль аргинина и тому подобное. Эти соли могут быть получены способами, известными в данной области техники.
В настоящей заявке соединения формулы (I) могут быть получены в одной или нескольких кристаллических формах, активные соединения по настоящему изобретению включают различные полиморфы и их смеси.
В настоящей заявке термин "сольват" относится к комплексу, образованному соединением по настоящему изобретению с растворителем. Сольват может быть образован либо путем реакции в растворителе, или осажден, или кристаллизован из растворителя. Например, комплекс, образованный с водой, называется "гидрат". Сольваты соединений формулы (I) находятся в пределах объема настоящего изобретения.
Соединения формулы (I) по настоящему изобретению могут содержать один или несколько хиральных центров и могут существовать в различных оптически активных формах. Когда соединение содержит хиральный центр, соединение включает энантиомеры. Настоящее изобретение включает в себя оба изомера и их смесь, такие как рацемические смеси. Энантиомеры могут быть разделены с использованием способов, известных в данной области техники, таких как кристаллизация и хиральная хроматография и тому подобное. Когда соединение формулы (I) содержит больше одного хирального центра, соединения могут включать диастереомеры. Настоящее изобретение включает конкретные изомеры, разделенные на оптически чистые изомеры, а также смеси диастереомерных изомеров. Диастереомерные изомеры могут быть разделены с использованием способов, известных в данной области техники, таких как кристаллизация и препаративная хроматография.
Настоящее изобретение включает пролекарства вышеуказанных соединений. Пролекарства включают известные аминозащитные группы и карбоксилзащитные группы, которые гидролизуются в физиологических условиях или высвобождаются в ходе ферментативной реакции с получением исходных соединений. Конкретные способы получения пролекарств можно найти в (Saulnier, MG; Frennesson, DB; Deshpande, MC; Hansel, SB and Vysa, DMBioorg. Med. Chem Lett. 1994, 4, 1985-1990; and Greenwald, RB; Choe, YH; Conover, CD; Shum, K.; Wu, D.; Royzen, M.J. Med. Chem. 2000, 43, 475).
Способ получения
Настоящее изобретение предлагает способ получения соединений формулы (I), соединения по настоящему изобретению могут быть легко получены с помощью различных синтетических операций, эти операции известны специалистам в данной области техники. Примеры получения этих соединений могут включать в себя (но не ограничиваются ими) способы, описанные ниже.
Предпочтительно, соединения формулы (I) могут быть получены с помощью следующих схем и иллюстративных способов, описанных в варианте осуществления, а также связанных публикациях, доступных для специалистов в данной области техники.
На практике, процедуры способа могут быть по желанию расширены или скомбинированы.
Схема 1:
Стадия 1: Реакция по хлору в 4 положении пиримидина с боратом или борной кислотой, или с соответствующим амином может быть проведена в присутствии подходящего катализатора и подходящего растворителя при определенной температуре. Палладиевым катализатором, используемым в реакции Сузук