Комплексное металл-саленовое соединение, обладающее собственным магнетизмом
Иллюстрации
Показать всеИзобретение относится к противоопухолевому лекарственному препарату. Препарат содержит магнитный лекарственный препарат, включающий новое металл-саленовое комплексное соединение, обладающее собственным магнетизмом, представленное формулой (I). Формула (I) отражает структуру соединения (II), представленную ниже
где М представляет собой Fe, и каждый из a-f представляет собой водород или каждый из a-f представляет собой метильную группу, или каждый из b и е представляет собой водород и каждый из а, с, d и f представляет собой метильную группу. Также предложены варианты противоопухолевых лекарственных препаратов и система направления магнитного лекарственного препарата. Изобретение позволяет предоставить противоопухолевый лекарственный препарат на основе нового металл-саленового комплексного соединения и его производных, обладающего собственным магнетизмом. 7 н. и 3 з.п. ф-лы, 7 ил., 6 пр.
Реферат
Область техники
Настоящее изобретение относится к новому металл-саленовому комплексному соединению, обладающему свойствами собственного магнетизма.
Уровень техники
В целом, когда лекарственное вещество вводится в живой организм, оно достигает места действия и проявляет свои фармакологические эффекты в этом месте действия, обеспечивая, таким образом, свои терапевтические эффекты. С другой стороны, если лекарственное вещество достигает другой ткани, иной, чем место его действия (например, нормальной ткани), то его действие не будет терапевтическим.
В этой связи является важным, как именно доставить лекарственный препарат к месту его действия. Методика направления лекарственного препарата к месту его действия, называемая доставкой лекарственного вещества, в последнее время тщательно изучалась и исследовалась. У такой доставки лекарственного вещества имеется по меньшей мере два преимущества. Одно преимущество состоит в том, что может быть получена достаточно высокая концентрация лекарственного вещества в ткани, относящейся к месту действия вещества. Фармакологические эффекты не будут значимыми, если концентрация лекарственного вещества в месте его действия не достигнет определенной постоянной величины или не будет превышать ее. Если концентрация лекарственного вещества будет низкой, то нельзя ожидать достаточных терапевтических эффектов.
Второе преимущество состоит в том, что лекарственное вещество направляется только в ткань, относящуюся к месту действия вещества, и, поэтому, побочные реакции в отношении нормальной ткани могут быть подавлены.
Такая доставка лекарственного вещества является самой эффективной в случае лечения рака с помощью противоопухолевых средств. Большинство противоопухолевых средств ингибируют рост раковых клеток, которые активно делятся, но при этом противоопухолевые средства также ингибируют рост клеток нормальной ткани, где клетки также активно делятся, такой как костный мозг, волосяные корни или слизистая оболочка пищеварительного тракта.
В этой связи больные раком, которым вводят противоопухолевые средства, страдают от побочных реакций, таких как анемия, потеря волос и рвота. Поскольку такие побочные реакции являются тяжелыми нагрузками для пациентов, то это приводит к тому, что дозировки необходимо ограничивать и фармакологические эффекты от противоопухолевых средств не могут быть достигнуты в достаточной степени.
Среди таких противоопухолевых лекарственных препаратов известны алкилирующие противоопухолевые лекарственные вещества, обозначающие в целом противоопухолевые средства, которые способны связываться с алкильными группами (-CH2-CH2-), например, нуклеиновой кислоты, кодирующей белок, и обеспечивать эффекты по алкилированию ДНК и ингибированию репликации ДНК, вызывая, тем самым, некроз клеток. Эти эффекты имеют действие независимо от циклов клеток, воздействуя также на клетки в периоде G0, сильно влияя на активно растущие клетки, и имеют тенденцию к повреждению, например, костного мозга, слизистой оболочки пищеварительного тракта, зародышевых клеток или волосяных корней.
Кроме того, среди противоопухолевых лекарственных препаратов известны антиметаболические лекарственные вещества, которые имеют структуры, схожие со структурой нуклеиновых кислот или метаболитов, возникающих в процессе синтеза белка, и которые ослабляют клетки, например, за счет ингибирования синтеза нуклеиновых кислот, и специфично действуют на клетки в период митоза.
Помимо этого, известны противоопухолевые антибиотики, представляющие собой химические вещества, полученные из микроорганизмов, и эти противоопухолевые антибиотики действуют как ингибиторы синтеза ДНК, а также они разрывают цепи ДНК, проявляя за счет этого свою противоопухолевую активность.
Также известны ингибиторы микроканальцев, имеющие противоопухолевые эффекты за счет непосредственного действия на микроканальцы, которые играют важную роль в обеспечении нормальных функций клеток, например, при формировании веретена во время клеточного деления, при локализации клеточных органелл и при транспорте веществ. Ингибиторы микроканальцев действуют на клетки, которые активно делятся, и на нервные клетки.
Кроме того, известны препараты платины, которые ингибируют синтез ДНК путем образовании цепей ДНК, блокированием их связей или связей белка с ДНК. Цисплатин представляет собой типичный лекарственный препарат, но он вызывает тяжелую нефропатию и требует использования большого количества замещающей жидкости.
Кроме того, также известны парагормональные противоопухолевые лекарственные препараты, которые эффективны против зависимых от гормонов опухолей. Женские гормоны или антиандрогенные лекарственные вещества применяют при зависимом от андрогенов раке предстательной железы.
Также известны молекулярно-нацеленные лекарственные препараты, используемые для целевого воздействия на молекулы, которые ответственны за молекулярные биологические процессы, характерные для соответствующих злокачественных опухолей.
Кроме того, известны ингибиторы топоизомеразы, которые представляют собой ферменты, образующие временные разрывы ДНК, и изменяющие количество точек сцепления цепей ДНК. Ингибитор топоизомеразы I представляет собой фермент, который генерирует разрывы в одной цепи кольцевой ДНК, обеспечивая встраивание другой цепи, а затем соединяет созданные разрывы; ингибитор топоизомеразы II временно разрывает обе цепи кольцевой ДНК, обеспечивая встраивание двух других цепей ДНК между двумя первоначальным цепями, и затем соединяет нарушенные цепи.
Также известны неспецифические иммуностимуляторы, которые ингибируют рост числа раковых клеток за счет активизирования иммунной системы.
Сейчас, как отмечено выше, больные раком, которым вводят противоопухолевые средства, страдают от побочных реакций, таких как анемия, потеря волос и рвота. Принимая во внимание такие побочные реакции, приводящие к тяжелым нагрузкам у пациентов, необходимые дозировки снижают, и фармакологические эффекты от противоопухолевых средств могут быть достигнуты в недостаточной степени. Из-за побочных реакций, при худшем варианте развития событий, имеется опасность смерти пациентов.
Таким образом ожидается, что лечение рака может быть осуществлено эффективно в случае подавления побочных реакций путем доставки лекарственного вещества, за счет направления противоопухолевого средства к раковым клеткам, и получения фармакологических эффектов, направленных на раковые клетки, непосредственно в раковых клетках. В отношении местно-анестезирующих средств имеются аналогичные проблемы. Местно-анестезирующие средства используются путем локального применения для лечения зуда и боли, например, на слизистой оболочке или коже, которые вызваны геморроидальным заболеванием, при стоматите, воспалении десен, кавернах, при удалении зубов или при операциях. Лидокаин (торговое название продукта: ксилокаин) известен как типичное местно-анестезирующее средство; однако лидокаин, являясь быстродействующим веществом, имеет антиаритмическое действие.
Кроме того, когда лидокаин, который является анестезирующим средством, вводят в спиннно-мозговую жидкость, обеспечивая анестезию спины, то лидокаин будет распространяться по спинно-мозговой жидкости; и в худшем варианте развития событий имеется опасность, что лидокаин может достичь цервикальной части спинного мозга, и, таким образом, это может привести к остановке дыхательной функции и вызывать критические негативные побочные эффекты.
Ожидается, что лечение рака может быть выполнено эффективно, в случае подавления побочных реакций путем доставки лекарственного вещества, за счет направления противоопухолевого средства к раковым клеткам, и получения фармакологических эффектов, направленных на раковые клетки, непосредственно в раковых клетках
Также ожидается, что доставка лекарственного вещества может предотвратить диффузию местно-анестезирующих средств, поддержать фармакологические эффекты, и снизить побочные реакции.
Пример конкретного способа доставки лекарственного вещества представляет собой применение носителя. Способ состоит в том, что носитель, который имеет тенденцию к концентрированию в районе места действия, нагружают лекарственным веществом, и этот носитель доставляет лекарственное вещество к месту его действия.
Перспективный носитель-кандидат представляет собой магнитное вещество, и предлагаемый способ состоит в присоединении носителя, который является магнитными веществами, к лекарственному веществу, и обеспечение доставки носителя с использованием магнитного поля для аккумулирования в месте действия (см., например, Патентный документ 1).
Однако, в случае использования магнитного вещества в качестве носителя, определенные трудности представляет пероральное введение такого магнитного носителя; кроме того, поскольку молекулы носителя в целом имеют большие размеры, то имеют место технические проблемы, связанные с силой связывания и аффинности между носителем и молекулами лекарственного вещества; и поэтому из-за вышеописанных причин практическое применение магнитного носителя для лекарственных веществ, было затруднено.
Поэтому было предложено местно-анестезирующее средство, в котором боковые цепи с положительной или отрицательной плотностью спинового заряда связаны со структурной основой органического соединения, и которое в целом имеет способность действовать в качестве местно-анестезирующего средства, и обладает способностью направляться с помощью внешнего магнитного поля; и если местно-анестезирующее средство применяется местно в отношении человека или животного, то оно сохраняется в области, где на тело локально воздействует внешнее магнитное поле, и лекарственные эффекты, которые изначально обеспечивает местно-анестезирующее средство, проявляются в этой области. В вышеуказанном способе, в качестве примера такого лекарственного препарата, используют железное-саленовое комплексное соединение (см. Патентный документ 2).
Кроме того, была опубликована обзорная статья относительно органического магнитного вещества, которое обладает магнитными свойствами, из высокомолекулярных полимерных материалов посредством синтеза "высокоспиновых молекул", имеющих большее количество параллельных спинов, чем обычные металлические магнитные вещества (см., например, непатентный документ 1).
Более того, также была опубликована работа, где описан способ, в котором активное соединение, содержащееся в цисплатине, было заменено другим элементом (см., например, непатентный документ 2).
Список цитируемых документов
Патентные документы
Патентный документ 1: выложенная публикация (kokai) японской патентной заявки № 2001-10978
Патентный документ 2: WO2008/001851
Непатентный документ 1: Hiizu Iwamura, "Molecular Design Aimed at Organic Ferromagnetic Substances", Feb. 1989 issue, p.p. 76-88
Непатентный документ 2: Kristy Cochran et al., Structural Chemistry, 13(2002), p.p. 133-140
Сущность изобретения
Техническая проблема
Непатентные документы 1 и 2, тем не менее, не раскрывают, что сам лекарственный препарат является магнитным веществом.
Цель настоящего изобретения состоит в предоставлении нового металл-саленового комплексного соединения и его производных, обладающих собственным магнетизмом.
Решение проблемы
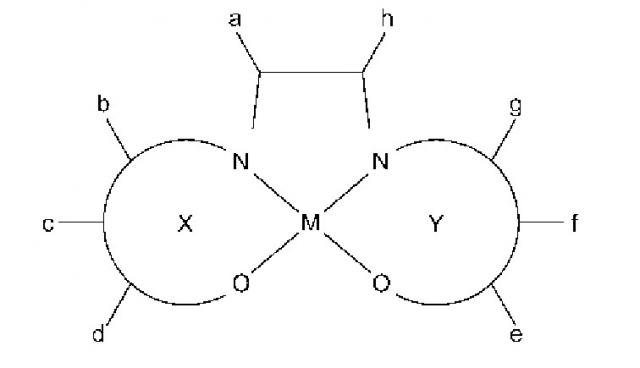
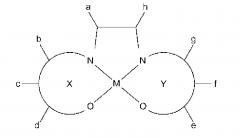
Для достижения вышеуказанной цели, настоящее изобретение характеризуется тем, что оно предоставляет новое металл-саленовое комплексное соединение, обладающее собственным магнетизмом, представленное следующей формулой (I).
Каждый из X и Y представляет собой пятичленную кольцевую структуру, содержащую координационную связь между N и М, или шестичленную кольцевую структуру, где М представляет собой двухвалентный металл, выбранный из Fe (железо), Cr (хром), Mn (марганец), Co (кобальт), Ni (никель), Мо (молибден), Ru (рубидий), Rh (родий), Pd (палладий), W (вольфрам), Re (рений), Os (осмий), Ir (иридий), Pt (платина), Nd (ниобий), Sm (самарий), Eu (европий) или Gd (гадолиний). Если оба X и Y представляют собой пятичленную кольцевую структуру, b и g отсутствуют, то формула (I) представляет собой любую из структур (i)-(iv).
(i) Каждый из a-h представляет собой водород или любую из указанных ниже групп (A)-(G) и -C(=O)m, (где m представляет собой водород или любую из указанных ниже групп (A)-(G));
(ii) каждый из (c, d) и (f, e) образует часть гетероциклической структуры и образует конденсированную структуру, представленную формулой (I) и гетероциклической структурой,
каждый из a, b, g и h представляет собой водород или любую из указанных ниже групп (A)-(G) и -C(=O)m, (где m представляет собой водород или любую из указанных ниже групп (A)-(G)),
гетероциклическая структура представляет собой любую из от трех- до семи-членных кольцевых структур, включающих фуран, тиофен, пиррол, пирролидин, пиразол, пиразолон, имидазол, 2-изоимидазол, оксазол, изоксазол, тиазол, имидазол, имидазолидин, оксазолин, оксазолидин, 1,2-пиран, тиазин, пиридин, пиридазин, пиримидин, пиразин, ортоксадин, оксазин, пиперидин, пиперазин, триазин, диоксан или морфолин, и
боковая цепь гетероциклической структуры представляет собой галоген, -R, -O-R (где R представляет собой одну функциональную группу, выбранную из углеводородной группы, включающей метильную группу), или водород;
(iii) каждый из (c, d) и (f, e) образует часть одной из конденсированных кольцевых структур, включающих бензол или нафталин и антрацен, и образует конденсированную структуру, представленную формулой (I) и конденсированной кольцевой структурой,
каждый из a, b, g и h представляет собой водород или любую из указанных ниже групп (A)-(G), и
боковая цепь для конденсированной кольцевой структуры представляет собой галоген, R-O-: (где R представляет собой одну функциональную группу, выбранную из углеводородной группы, включающей метильную группу), или водород;
(iv) каждый из a и h является частью циклической углеводородной структуры, включающей соединение, указанное ниже, и образует конденсированную структуру, представленную формулой (I) и циклической углеводородной структурой
или
каждый из b-g, и боковая цепь для циклической углеводородной структуры представляет собой водород или любую из указанных ниже групп (A)-(G).
(A) представляет собой -CO2R, -C(=O)R (где R представляет собой водород, или углеводород с цепочечной или циклической структурой, имеющий насыщенную структуру с числом углеродных атомов 1-6, или ненасыщенную структуру (алкан или алкин));
(B) представляет собой -CO(OCH2CH2)2OCH3;
(C) представляет собой
(D) представляет собой
(где R2 представляет одну из нуклеиновых кислот, которые образованы из аденина, гуанина, тимина, цитозина или урацила, или множество нуклеиновых кислот, которые объединены вместе);
(E) представляет собой -NHCOH или -NR1R2 (где R1 и R2 представляют собой водород или углеводород с цепочечной или циклической структурой, с одинаковой или разной насыщенной структурой с числом углеродных атомов 1-6, или ненасыщенной структурой (алкан или алкин));
(F) представляет собой -NHR3-,-NHCOR3, -CO2-R3, -S-S-R3 или -R3 (где R3 представляет собой водород или замещенное соединение, образованное в результате удаления уходящей группы, такой как гидроксильная группа; и замещенное соединение представляет собой функциональные молекулы, включающие по меньшей мере одно из ферментов, антител, антигенов, пептидов, аминокислот, олигонуклеотидов, белков, нуклеиновых кислот и медицинских молекул); и
(G) представляет собой атом галогена, такой как хлор, бром, или фтор.
Металл-саленовое комплексное соединение, представленное формулой (I), представляет собой органическое соединение, обладающее собственным магнетизмом, которое не содержит магнитного носителя. Поэтому другое представленное изобретение характеризуется тем, что оно предоставляет магнитное лекарственное средство, содержащее указанное металл-саленовое комплексное соединение в качестве активного ингредиента, и которое вводят в организм человека или животного, а затем направляют к ткани-мишени за счет воздействия внешнего магнитного поля на организм человека или животного.
Кроме того, металл-саленовое комплексное соединение, представленное формулой (I), эффективно для лечения опухолей, таких как рак. Поэтому другое представленное изобретение характеризуется тем, что оно предоставляет противоопухолевое лекарственное средство, содержащее магнитный лекарственный препарат в качестве активного ингредиента.
Система для направления металл-саленового комплексного соединения к месту действия выполнена так, что она обеспечивает магнитное поле для металл-саленового комплексного соединения снаружи организма, и она использует магнитные свойства металл-саленового комплексного соединения. Поэтому другое представленное изобретение характеризуется тем, что оно предоставляет способ направления магнитного лекарственного средства, такого как противораковое средство, содержащего металл-саленовое комплексное соединение в качестве активного ингредиента, к месту его действия, путем введения магнитного лекарственного средства в организм, с последующим воздействием на организм внешним магнитным полем. Кроме того, другое представленное изобретение характеризуется тем, что оно предоставляет систему магнитного направления лекарственного средства, включающую средство для введения магнитного лекарственного средства в организм, средство для воздействия магнитного поля на лекарственное средство, введенного в организм, и средство для перемещения магнитного поля к месту действия лекарственного средства.
Полезные эффекты изобретения
Согласно настоящему изобретению, предоставлены новое металл-саленовое комплексное соединение, обладающее собственным магнетизмом, магнитные лекарственные препараты, противоопухолевые лекарственные препараты, а также способ и система для направления магнитных лекарственных препаратов и противоопухолевых лекарственных препаратов, где используются это новое металл-саленовое комплексное соединение.
Краткое описание фигур
На фиг.1 представлена схематическая иллюстрация состояния, где стержневой магнит приведен в контакт с прямоугольной колбой, содержащей питательную среду клеток крысы L6.
На фиг.2 представлен график, показывающий результаты подсчета количества клеток, полученных путем фотографирования дна прямоугольной колбы в направлении от ее одного конца к другому концу.
На фиг.3 представлен перспективный вид устройства для магнитного направления.
На фиг.4 представлен график, показывающий результаты измерения ЯМР почки мыши, которая была подвергнута действию магнитного поля после внутривенного инъецирования металл-саленового комплексного соединения.
На фиг.5 представлены фотографии тканей сухожилия хвоста мыши, где показано действие саленового комплексного соединения на рост меланомы у мышей.
На фиг.6 представлен график, показывающий действие саленового комплексного соединения на рост меланомы у мышей.
На фиг.7 представлены микрофотографии, показывающие результаты гистологического исследования, где показаны эффекты действия саленового комплексного соединения на рост меланомы у мышей.
Описание вариантов выполнения изобретения
Предпочтительные варианты выполнения металл-саленового комплексного соединения формулы (I), обладающего собственным магнетизмом, представлены соединениями, имеющими структуры, показанные формулами (II)-(XI).
(II)
X, Y: шестичленная кольцевая структура,
(а-h) = H
(III)
X, Y: шестичленная кольцевая структура,
(c, f) = C(O)Н
(a, b, d, e, g, h) = H
(IV)
X, Y: пятичленная кольцевая структура,
(a, c, d, e, f, h) = H
(V)
X, Y: шестичленная кольцевая структура,
(a, b, g, h): H
(e, f), (g, h): составляют часть фурана, и фуран представляет конденсированную систему с главным скелетом молекулы.
M: Fe
(VI)
X, Y: шестичленная кольцевая структура,
(a, h): составляют часть циклогексана, и циклогексан представляет конденсированную систему с главным скелетом молекулы.
(c, d), (e, f): образуют бензол,
(b, g): Н
M: Fe
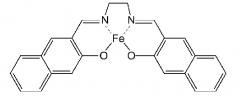
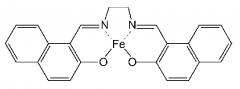
(VII)
X, Y: шестичленная кольцевая структура,
(a, h): составляют часть бензола,
(c, d), (e, f): образуют бензол,
(b, g): Н,
M: Fe
(VIII)
X, Y: шестичленная кольцевая структура,
(c, d), (e, f): образуют антрацен,
(a, b, g, h): H
M: Fe
(IX)
X, Y: шестичленная кольцевая структура,
(c, d), (e, f): образуют антрацен
(a, b, g, h) = H
Изомер (V)
M: Fe
(X)
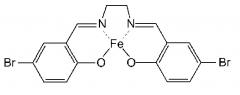
X, Y: шестичленная кольцевая структура,
(c, d), (e, f): образуют бензол,
боковые цепи в мета-положениях бензола представляют собой галогены (бром),
(a, b, g, h): H,
M: Fe
(XI)
X, Y: шестичленная кольцевая структура,
(c, d), (e, f): образуют бензол,
боковые цепи в мета-положениях бензола представляют собой метоксильные группы,
(a, b, g, h): H,
M: Fe
Поскольку металл-саленовое комплексное соединение формулы (I) обладает магнитными свойствами, и оно может направляться за счет действия внешнего магнитного поля, то абсолютное значение величины переноса заряда его боковой цепи должно быть предпочтительно менее 0,5 электронов (e). Замещенное соединение, описанное, например, в WO 2010/058280, может быть использовано в качестве указанного выше R3, который составляет указанную боковую цепь. Содержание вышеуказанной публикации входит в описание настоящей заявки.
Поскольку металл-саленовое комплексное соединение, представленное формулой (I), вводят внутрь организма, а затем направляют к ткани-мишени, подвергая организм воздействию внешнего магнитного поля, то величина магнитной силы металл-саленового комплексного соединения и сила намагничивания лекарственного препарата, содержащего это металл-саленового комплексного соединения, в качестве активного ингредиента, соответственно находится в пределах диапазона от 0,5 до 1,5 эме/г (электромагнитных единиц на грамм). Магнитные лекарственные препараты предназначены, главным образом, для введения в виде инъекции или с помощью трансфузии, или они могут быть представлены в форме порошкообразных лекарственных препаратов. В качестве растворителя препаратов для инъекций или трансфузий может быть использован, предпочтительно, физиологический раствор. Магнитный лекарственный препарат содержит в качестве активного ингредиента металл-саленовое комплексное соединение в количестве, равном, например, 50% по массе или более; и кроме того, магнитный лекарственный препарат может содержать разбавители, стабилизаторы, и дополнительные активные фармацевтические ингредиенты, которые не имеют никакого влияния или имеют небольшое влияние на эффективность, физические свойства или химические свойства металл-саленового комплексного соединения. Вышеуказанное металл-саленовое комплексное соединение может быть использовано как противораковое средство.
Примерами средств для воздействия магнитного поля на магнитный лекарственный препарат после введения магнитного лекарственного препарата в организм человека или животного, являются постоянные магниты или индукционные магнитные поля, такие как при ЯМР. Сила внешнего магнитного поля должна, предпочтительно, находиться в пределах диапазона от 0,5 до 1,0 T, или, более предпочтительно, от 0,8 до 1,0 Т. Примеры средств для направления магнитного поля к месту действия лекарственного средства включают средства ЯМР, а также X-Y координатные столы для перемещения постоянного магнита. Примеры средств воздействия магнитного поля на ткани места действия лекарственного средства включают средства для воздействия магнитного поля на поверхности тела и средства создания магнитного поля в кровеносных сосудах около тканей места действия лекарственного средства. С целью воздействия магнитного поля на поверхность организма, существуют средства для воздействия магнитного поля на переднюю часть организма и/или со стороны спины.
Примеры
Настоящее изобретение будет пояснено далее с помощью примеров.
Пример 1
Синтез металл-саленового комплексного соединения (II)
Первый пример синтеза
Металл-саленовое комплексное соединение (II) синтезировали в соответствии со следующей схемой реакции.
Синтез соединения 1
К раствору этилформиата (60 мл), содержащего моногидрохлорид сложного метилового эфира аминоуксусной кислоты (10,0 г, 0,079 моля) добавляли P-TsOH (10 мг), и полученный раствор нагревали до кипения. В раствор, при кипячении, добавляли несколько капель триэтиламина; полученный раствор кипятили с обратным холодильником в течение 24 часов и затем охлаждали до комнатной температуры. Затем отфильтровывали белый осадок гидрохлорида триэтиламина и остаток концентрировали до объема 20 мл. Полученный раствор охлаждали до температуры -5°С и затем фильтровали. Полученный остаток красно-коричневого цвета представлял собой концентрированный раствор соединения 1.
Синтез соединения 2
В растворе соединения 1 растворяли CH2Cl2 (20 мл). Затем к полученному раствору добавляли этан-1,2-диамин (1,2 г) и уксусную кислоту (HOAc) (20 мкл); и этот реакционный смешанный раствор подвергали кипячению с обратным холодильником в течение 6 часов. Затем раствор смеси реагентов охлаждали до комнатной температуры, получая, таким образом, 4 г маслянистого концентрата желтого цвета (соединение 2). Чистота полученного соединения 2 была увеличена за счет проведения флэш-хроматографии на колонке с силикагелем.
Синтез соединения 0
Соединение 2 и триэтиламин в метаноле (50 мл) и раствор хлорида металла (FeCl3(4H2O), для синтеза железо-саленового комплексного соединения) смешивали в метаноле (10 мл) в атмосфере азота. Смесь перемешивали в течение одного часа в атмосфере азота, получая, таким образом, соединение коричневого цвета. Затем это соединение сушили в вакууме, полученное соединение разбавляли дихлорметаном (400 мл), дважды промывали солевым раствором, сушили над Na2SO4 и затем подвергали сушке в вакууме, получая, таким образом, соединение 0 (металл-саленовое комплексное соединение (II)).
Второй пример синтеза
Металл-саленовое комплексное соединение (II) синтезировали в соответствии со следующей схемой реакции.
Соединение 5 синтезировали путем введения 3,4 г 3-метилацетилацетона (соединение 4) и 0,9 г этилендиамина (соединение 3) в безводный метанол (50 мл), поддерживая pH до 6 путем использования уксусной кислоты на льду. Полученный раствор кипятили с обратным холодильником в течении 15 минут и затем выпаривали до половины первоначального объема. После добавления воды до исходного объема раствора из него выпадал осадок, что привело, таким образом, к получению 1,4 г вещества белого цвета (соединение 5).
После этого соединение 5 (1,2 г, 5 мМ) растворяли в метаноле (50 мл), и к полученному раствору добавляли FeSO4⋅7H2O (1,4 г, 5 мМ), получая, таким образом, светлый синевато-зеленый раствор. Этот раствор перемешивали в течение 8 часов при комнатной температуре в атмосфере азота, и его цвет постепенно изменялся до коричневого. Раствор выпаривали до половины его объема и затем к полученному раствору добавляли такой же объем воды. Затем раствор подвергали действию вакуума для испарения метанола, получая, таким образом, коричневую массу. Эту массу собирали и промывали водой, затем сушили под вакуумом, получая, таким образом, 360 мг целевого соединения (металл-саленовое комплексное соединение (II)).
Третий пример синтеза
Металл-саленовое комплексное соединение (II) синтезировали в соответствии со следующей схемой реакции.
В реакционный сосуд с атмосферой азота помещали ацетат железа (II) (0,83 г, 4,8 мМ) и дегазированный метанол (48 мл), и к полученному раствору добавляли ацетилацетон (0,95 г, 9,5 мМ). Раствор перемешивали при кипячении с обратным холодильником в течение 15 минут и затем охлаждали. Выпавшие в осадок кристаллы отфильтровывали и полученный раствор промывали охлажденным метанолом (10 мл). Затем раствор высушивали под пониженным давлением, получая, таким образом, 1,07 г промежуточного продукта.
В реакционный сосуд с атмосферой азота помещали промежуточный продукт (1,07 г, 3,4 мМ), лиганд (0,70 г, 3,4 мМ), и дегазированный декалин (30 мл), и полученный раствор перемешивали при кипячении с обратным холодильником в течение 1 часа. После охлаждения раствора и отфильтровывания выпавшего в осадок твердого вещества, полученное твердое вещество промывали дегазированным циклогексаном (10 мл). Затем раствор высушивали под пониженным давлением, получая, таким образом, 0,17 г продукта (металл-саленовое комплексное соединение (II)).
Пример 2
Синтез металл-саленового комплексного соединения (III)
Металл-саленовое комплексное соединение (III) синтезировали в соответствии со следующей схемой реакции.
В реакционный сосуд с атмосферой азота помещали ацетат железа (II) (0,78 г, 4,5 мМ) и дегазированный метанол (20 мл) и к полученному раствору добавляли ацетилацетон (0,91 г, 9,9 мМ). Раствор перемешивали при кипячении с обратным холодильником в течение 15 минут и затем охлаждали. Выпавшие в осадок кристаллы отфильтровывали и полученный раствор промывали охлажденным метанолом (10 мл). Затем раствор высушивали под пониженным давлением, получая, таким образом, 0,58 г промежуточного продукта (выход 67%).
В реакционный сосуд с атмосферой азота помещали промежуточный продукт (240 мг, 0,75 мМ), лиганд (210 мг, 0,75 мМ) и дегазированный декалин (10 мл) и полученный раствор перемешивали при кипячении с обратным холодильником в течение 30 минут. После охлаждения раствора отфильтровывали осадок твердого вещества и полученное твердое вещество промывали дегазированным циклогексаном (3 мл). Затем раствор высушивали под пониженным давлением, получая, таким образом, 101 мг продукта (металл-саленовое комплексное соединение (III)).
Пример 3
Синтез металл-саленового комплексного соединения (IV)
Металл-саленовое комплексное соединение (IV) синтезировали в соответствии со следующей схемой реакции.
В реакционный сосуд с атмосферой азота помещали ацетат железа (II) (0,83 г, 4,8 мМ) и дегазированный метанол (48 мл) и к полученному раствору добавляли ацетилацетон (0,95 г, 9,5 мМ). Раствор перемешивали при кипячении с обратным холодильником в течение 15 минут и затем охлаждали. После этого к раствору соединения 6 (60 мг, 1,0 мМ) в CH2Cl2 (10 мл) добавляли соединение 7 (120 мг, 2,0 мМ) и SiO2 (1 г); и полученный раствор перемешивали в течение ночи при комнатной температуре для протекания реакции, синтезируя, таким образом, соединение 8. Затем в реакционный сосуд с атмосферой азота помещали полученное соединение 8 вместе с ацетатом железа (II) (0,83 г, 4,8 мМ) и дегазированным метанолом (48 мл) и к полученному раствору добавляли ацетилацетон (0,95 г, 9,5 мМ). Раствор перемешивали в течение 15 минут при кипячении с обратным холодильником и осажденные кристаллы отфильтровали, получая, таким образом, целевое соединение коричневого цвета (металл-саленовое комплексное соединение (IV)).
Пример 4
Соединения (V)-(XI) синтезировали способом, описанным на стр. 43-47 описания заявки WO2010/058280. Бром или метоксильную группу, которая представляет собой боковую цепь, присоединяли к главной структуре соединения для образовании комплексной связи металла с саленом путем замены защитной группы (NHBoc), которая связана с бензольным кольцом в пара положении с ОН группой бензольного кольца, бромом или метоксильной группой. В случае соединений (VIII) и (IX), где (c, d) и (e, f) образуют антрацен, в качестве исходного материала, вместо паранитрофенола, использовали следующее соединение.
Для синтеза металл-саленового комплексного соединения (VI), в котором (a, h) образуют циклогексан, и металл-саленового комплексного соединения (VII), в котором (a, h) образуют бензол, целевой сален, до образования координационной связи с металлом, был получен способом, описанным в Journal of Thermal Analysis and Calorimetry, Vol. 75 (2004) 599-606: см. экспериментальную часть на стр. 600.
Пример 5
Для определения того, может ли водный раствор каждого из металл-саленовых комплексных соединений (II)-(XI) быть захвачен постоянным магнитом или нет, было выполнено исследование протекания водных растворов в стеклянной трубке при их прокачивании с помощью насоса. Скорость протекания водного раствора металл-саленового комплексного соединения составляла 100 мм/с, диаметр стеклянной трубки составлял 1,3 мм, расстояние от поверхности стеклянной трубки до постоянного магнита составляло 1,35 мм, и концентрация соединения составляла 10 мг/мл. Используемый магнит представлял собой коммерчески доступный стержневой магнит круглого сечения (диаметр 20 мм; длина 150 мм; модель номер N50 от Shin-Etsu Chemical Co., Ltd.; максимальная магнитная индукция 0,8 T). Было проверено каждое комплексное соединение в отношении того, может ли оно быть захвачено в области, где действует магнит.
Пример 6
В культуральную среду (PBS), в которой находились крысиные клетки L6 в состоянии 30%-ой конфлюентности, было введено каждое из металл(железо)-саленовых комплексных соединений (II)-(XI), полученных вышеуказанными способами, порошок железо-саленового комплексного соединения (10 мг), на уровне, обеспечивающим визуальный контроль магнитного притяжения; и через 48 часов состояние культуральной среды было сфотографировано. На Фиг.1 представлена схематическая иллюстрация состояния, в котором стержневой магнит находится в контакте с прямоугольной колбой, содержащей культуральную среду с крысиными клетками L6. Через 48 часов вид со стороны дна прямоугольной колбы был сфотографирован в направлении от одного до другого конца, и было вычислено количество клеток; результаты показаны на фиг.2. На фиг.2 указана проксимальная область относительно магнита, которая находится в пределах проекции области торца магнита на дне прямоугольной колбы, и дистальная область относительно магнита, которая находится на противоположной стороне дна прямоугольной колбы относительно торца магнита.
На фиг.2 показано, что концентрация каждого металл-саленового комплекса увеличивается, когда металл-саленовый комплекс находится в проксимальном положении по отношению к магниту; и можно заметить, что количество клеток становится чрезвычайно низким, чем это имеет место в дистальном положении, из-за ингибирующего действия комплекса на рост ДНК. В результате лекарственный препарат может быть сконцентрирован в целевом месте его действия или в тканях человека за счет применения металл-саленового комплекса и системы, которая включает средство создания магнитного поля.
Далее будет пояснен пример направления, где используется направляющее устройство. В этом направляющем устройстве, как показано на фиг.3, пара магнитов 230 и 232, торцы которых обращены друг к другу по направлению силы тяжести, удерживаются стой